
病毒感染宿主细胞需要与其表面的受体结合。受体是影响宿主范围和种间传播的重要因素。2019年12月在湖北武汉暴发流行的不明原因肺炎,其病原体为一种新型冠状病毒,WHO将其命名为2019新型冠状病毒(2019-nCoV),研究发现血管紧张素转换酶2(ACE2)为2019-nCoV的受体。本文对已知人类冠状病毒受体及其应用作简要综述,以期为2019-nCoV的溯源、跨物种传播、流行病学分析以及抗病毒药物和疫苗的研究提供参考。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
冠状病毒(Coronavirus,CoV)是一类在自然界中广泛存在,对人、哺乳动物及家禽具有重大潜在威胁的病原体。由于病毒包膜表面有形如日冕或冠状的突起而得名冠状病毒[1,2]。病毒包膜表面含有3种主要结构蛋白:刺突蛋白(Spike,S)、包膜蛋白(Envelope,E)、膜蛋白(Membrane,M)[2]。E蛋白和M蛋白主要参与病毒的组装过程。S蛋白含有受体结合区域(receptor binding domain,RBD),能特异性结合宿主细胞表面的受体,介导病毒进入宿主细胞。
冠状病毒属于巢病毒目(Nidovirales)冠状病毒科(Coronaviridae)正冠状病毒亚科(Orthocoronavirinae)。冠状病毒基因组为单股正链RNA,大小27 000~32 000 bp,是所有RNA病毒基因组中最大的。基因组的5′端有帽子结构,其后包含多个开放阅读框(open reading frames,ORFs),3′末端有200~500个核苷酸的非翻译区(untranslated region,UTR)和典型的pola A尾。国际病毒学分类委员会根据基因组的结构特点将冠状病毒分为四个属,即α、β、γ和δ属。α属冠状病毒包括人冠状病毒229E(humancoroanvirus 229E,HCoV-229E)和人冠状病毒NL63(human coroanvirus NL63, HCoV-NL63)等8种。β属冠状病毒包括严重急性呼吸综合征冠状病毒(severe acute respiratory syndromes coronavirus,SARS-CoV)和中东呼吸综合征冠状病毒(Middle East respiratory syndrome coronavirus,MERS-CoV)等7种[2]。最新发现的2019新型冠状病毒(2019 novel coronavirus,2019-nCoV)目前归属于β属[3]。γ属冠状病毒包括鸡传染性支气管炎病毒(avian infectious bronchitis coronavirus,IBV);δ属冠状病毒包括猪δ冠状病毒(porcine deltacoronavirus,PDCoV)等[2]。
2019年12月,在湖北武汉暴发的2019-nCoV感染的肺炎是继2002年严重急性呼吸综合征和2012年中东呼吸综合征后,又一次冠状病毒跨物种传播、导致人类呼吸系统急性损伤的传染病。通过病毒核酸序列比对分析,推测2019-nCoV的自然宿主可能为蝙蝠,由某一中间宿主传染给人类[3]。这使人们再次意识到,一旦冠状病毒跨越种间屏障,将导致严重的人群感染。
病毒跨种间的传播与受体有重要关系。通常,病毒通过结合宿主细胞表面的受体,产生膜融合反应,进入宿主细胞。受体决定了宿主范围和组织嗜性。目前,已发现的人类冠状病毒受体有3种,即氨基肽酶N(aminopeptidase,APN,又名CD13)[4]、二肽基肽酶4(dipeptidyl peptidase 4,DPP4,又名CD26)[5]以及血管紧张素转换酶2(angiotensin-converting enzyme 2,ACE2)[6],见表1。本文将简要综述3种人类冠状病毒受体及其应用,以期为2019-nCoV的溯源、传播和治疗提供参考。
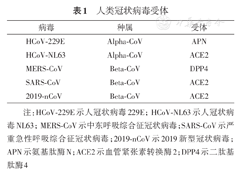
人类冠状病毒受体
人类冠状病毒受体
| 病毒 | 种属 | 受体 |
|---|---|---|
| HCoV-229E | Alpha-CoV | APN |
| HCoV-NL63 | Alpha-CoV | ACE2 |
| MERS-CoV | Beta-CoV | DPP4 |
| SARS-CoV | Beta-CoV | ACE2 |
| 2019-nCoV | Beta-CoV | ACE2 |
注:HCoV-229E示人冠状病毒229E;HCoV-NL63示人冠状病毒NL63;MERS-CoV示中东呼吸综合征冠状病毒;SARS-CoV示严重急性呼吸综合征冠状病毒;2019-nCoV示2019新型冠状病毒;APN示氨基肽酶N;ACE2示血管紧张素转换酶2;DPP4示二肽基肽酶4
APN又称CD13,是一种相对分子质量为150 000的Ⅱ型跨膜糖蛋白[4]。主要分布在肠道、呼吸道和肾脏上皮细胞表面[4]。α属冠状病毒中的HCoV-229E,猪传染性胃肠炎病毒(transmissible gastroenteritis virus,TGEV)、猪流行性腹泻病毒(porcine epidemic diarrhea virus,PEDV)和猫冠状病毒(feline coronavirus,FCoV)都能结合不同宿主的APN[7]。APN作为冠状病毒的受体具有种属特异性,如HCoV-229E能与人APN结合而不与猪APN结合;TGEV能与猪APN结合而不与人APN结合。但有研究发现PEDV能利用人APN和猪APN进入宿主细胞,提示PEDV可能对人类构成潜在威胁[7]。HCoV-229E致病性较弱,常引起人类的普通感冒[4]。TGEV与猪APN结合后会引起高致病性的猪群传染性腹泻。Liu等[8]用纯化的猪APN免疫家兔,获得高滴度的抗猪APN特异性抗体。该抗体能与天然猪APN发生中和反应,且能阻断TGEV的感染,为开发抗病毒药物提供了重要价值。
2013年,Raj等[5]研究证实MERS-CoV的受体为一种新的蛋白质,即DPP4,见表1。DPP4是Ⅱ型跨膜糖蛋白,在细胞表面以同源二聚体形式呈现,是继ACE2和APN之后发现的第三种人类冠状病毒的酶蛋白类受体[5]。DPP4在不同物种之间高度保守,主要在支气管上皮细胞和肺组织细胞中表达。DPP4可以促进肠降血糖素的降解,与T细胞的活化、趋化、细胞黏附、细胞凋亡以及致癌性等有关[9,10]。
MERS-CoV利用表面S蛋白作为黏附分子识别宿主细胞的CD26,介导病毒包膜与细胞质膜融合,进入宿主细胞。成功入侵的MERS-CoV可以抑制患者的免疫功能,促进病毒在体内的复制和传播[10]。
MERS-CoV受体的发现对其流行病学监测和物种传播提供重要依据。如比较MERS-CoV和不同物种的DPP4结合程度发现,人类、骆驼、马和蝙蝠的DPP4可以作为MERS-CoV的受体,小鼠、仓鼠和雪貂的DPP4则不能作为该病毒的受体[1]。在疫苗研制方面,针对DPP4的人源化单克隆抗体,能够有效阻断MERS-CoV的感染[10]。进一步通过生物学信息手段,分析获得MERS-CoV的RBD复合结构。以此区域为靶点开发疫苗,大量研究发现不仅能有效阻断MERS-CoV与受体的结合,并使免疫小鼠产生高滴度的中和抗体,被认为是安全、有效的MERS-CoV疫苗开发策略之一[10]。因此,MERS-CoV受体的研究为流行病学分析和疫苗研制奠定了重要基础。
ACE2是金属蛋白酶,属于Ⅰ型跨膜糖蛋白[6,11],广泛分布于人体的肾脏、心脏、小肠及肺组织中[6,11]。ACE2通过平衡血管紧张素活性来调节肾素血管紧张素系统,控制机体血压,对急性肺损伤、肺动脉高压具有保护作用;同时该酶在肠道中性氨基酸转运蛋白的表达中起重要作用[11]。
2003年,Li等[6]在Nature上报道ACE2是SARS-CoV的受体,见表1。SARS-CoV包膜上的三聚体刺突蛋白先与ACE2的胞外催化结构域的"疏水口袋"结合,促进细胞发挥内吞作用,形成内吞小体,继而病毒包膜与内体膜融合,使SARS-CoV进入宿主细胞[12,13]。在病毒入侵过程中,宿主组织蛋白酶、胰蛋白酶和跨膜丝氨酸蛋白酶2可以激活SARS-CoV的S蛋白,增强病毒的感染力[13]。
病毒结合宿主细胞受体后导致肺内ACE2水平下降,引起急性肺损伤,这也是SARS患者的死因之一。Kuba等[14]研究发现ACE2敲除小鼠对SARS-CoV具有抵抗性,肺部损伤较轻。Imai等[15]将重组ACE2用于急性肺损伤的小鼠,可明显降低小鼠急性肺损伤的程度。这些结果表明重组ACE2不仅可以阻断SARS-CoV的入侵,也能改善患者的急性肺损伤[11,14,15]。其次,利用SARS-CoV的不同毒株与人ACE2的结合程度,可以推测该毒株在人群中的流行程度[1]。Liang等[16]通过此方法发现SARS-CoV流行株hcGd03对人ACE2具有中等亲和力,会感染人类,但不会在人际间传播。比较SARS-CoV与不同物种的ACE2结合程度,也能推测SARS-CoV的潜在动物宿主,对其流行病学分析起到重要作用[1]。
HCoV-NL63感染多见于儿童,主要引起轻度或中度呼吸系统疾病,大多数成年人血清中含有中和抗体[17,18]。Hofmann等[18]研究表明HCoV-NL63利用与SARS-CoV相同的受体(ACE2)感染宿主细胞,但两者的致病性却完全不同。说明受体决定了宿主范围,但疾病类型却与之无关。进一步研究发现SARS-CoV与人ACE2结合能力比HCoV-NL63强[18],这提示冠状病毒的S蛋白可能与其致病性有关[17,18]。
2019年12月以来,在湖北武汉暴发流行不明原因肺炎,通过对患者标本的病原学检查分离出一种新型冠状病毒,世界卫生组织将其命名为2019-nCoV[19]。该病传染性强,传播途径主要为经呼吸道的飞沫传播和接触传播,气溶胶传播待确定,人群普遍易感染。Zhou等[3]通过病毒基因组的测序发现2019-nCoV与SARS-CoV有75%~80%的序列相同,与蝙蝠冠状病毒在全基因组水平上相似度高达96%。体外培养发现,该病毒在人气道原代上皮细胞内复制能力比SARS-CoV强[20]。
进一步研究发现,2019-nCoV的RBD与SARS-CoV较相似[21]。基于对SARS-CoV受体的理解认识,Xu等[21]通过对2019-nCoV的S蛋白结构模拟计算,发现2019-nCoV可以利用人ACE2作为受体,但结合能力可能比SARS-CoV要弱。Letko和Munster[22]合成SARS的S蛋白和2019-nCoV的RBD,与已知人类冠状病毒受体反应,发现2019-nCoV的RBD与SARS的S蛋白一样,都能利用ACE2进入宿主细胞。同时,Zhou等[3]发现2019-nCoV能结合来自人类、蝙蝠、果子狸和猪的ACE2入侵宿主细胞,但不能使用已知受体APN和DPP4。这些结果说明2019-nCoV通过S蛋白与人ACE2相互作用,来感染人的呼吸道上皮细胞,见表1[3,21,22]。最新研究发现,通过将人ACE2的胞外结构域和人免疫球蛋白IgG1的Fc区连接,构建一种新型重组蛋白(ACE2-Ig),能与2019-nCoV结合,并有效抑制病毒活性,为2019-nCoV抗病毒药物的研制提供重要参考[23]。另外,有研究指出消化道可能是2019-nCoV的潜在感染途径[24],部分患者初期存在腹泻症状可能与此有关[25]。该研究指出ACE2不仅在Ⅱ型肺泡上皮细胞、食道上皮细胞中高表达,在回肠和结肠中也高表达[24]。
截至2020年2月6日24时,共确诊31 161例,死亡636例,推测2019-nCoV的传染性比SARS-CoV和MERS-CoV要强。这是否与其他未知的受体相互作用有关?2019-nCoV是否会在人际传播中产生适应性突变?受体结合区域与SARS-CoV和MERS-CoV的RBD有何不同之处?这些问题仍然值得深入研究。
新型冠状病毒肺炎的暴发,促使人们进一步研究冠状病毒的进化与传播。大量研究表明,对病毒受体的认识不仅可以了解病毒的溯源、跨物种传播、入侵机制,同时可以针对受体及受体结合区域特点研究疫苗及抗病毒药物。目前,关于2019-nCoV受体的研究仍处于起步阶段。进一步研究2019-nCoV识别受体的分子机制,对病毒的溯源、中间宿主、流行病学分析和抗病毒药物的开发具有重要意义。
所有作者均声明不存在利益冲突



























