
对腔内热灌注化疗联合贝伐单抗治疗恶性胸腹腔积液的有效性进行Meta分析,为其进一步应用和研究提供依据。
计算机检索维普数据库、万方数据库、PubMed、中国知网数据库,收集腔内热灌注化疗联合贝伐单抗与单纯腔内热灌注化疗治疗恶性胸腹腔积液的临床对照试验,检索时限从各数据库建立到2018年1月。在严格依照纳入与排除标准下,两位研究者独立进行文献筛选、资料提取和质量评价工作,采用RevMan 5.3软件进行Meta分析。
共纳入4个临床对照试验,226例患者。Meta分析显示,贝伐单抗联合热灌注化疗组的临床有效率(OR=4.82,95 % CI 2.45~9.49,P<0.000 01)、恶性胸腹腔积液控制率(OR=4.06,95 % CI 1.09~15.11,P<0.05)、患者生命质量改善率(OR=6.79,95 % CI 3.53~13.08,P<0.000 01)均优于单纯热灌注化疗组,差异均有统计学意义。
热灌注化疗联合贝伐单抗可以提高恶性胸腹腔积液患者的临床有效率、积液控制率和生命质量改善率。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
恶性胸腹腔积液是恶性肿瘤晚期常见的并发症,可作为恶性肿瘤侵袭及转移的预测信息,临床多见于肺癌、卵巢癌、大肠癌等恶性肿瘤,淋巴回流抑制、低蛋白血症、血管通透性增加、血管内皮生长因子(VEGF)过度表达等因素可导致恶性胸腹腔积液产生。恶性腹腔积液患者的平均生存期不超过6个月,其对患者的生命健康构成严重威胁[1]。恶性胸腹腔积液患者虽经多次穿刺放液,但胸腹腔积液很快再次产生,选择最佳治疗方案是治疗恶性胸腹腔积液急需解决的问题。通过抑制VEGF减少肿瘤新生血管和降低血管通透性,抑制恶性胸腹腔积液产生,是临床治疗恶性积液的新思路。腔内热灌注化疗可提高病灶局部药物浓度以促进药物吸收,降低全身化疗药物剂量,不良反应较小。贝伐单抗以VEGF受体为靶点,可特异性抑制肿瘤血管新生从而控制肿瘤生长及侵袭,多用于大肠癌、肺癌、乳腺癌等肿瘤治疗[2]。靶向药物联合腔内热灌注化疗治疗方案的研究报道相对较少,目前已有腔内热灌注化疗联合贝伐单抗治疗恶性胸腹腔积液的文献报道,却鲜见系统评价。本研究对腔内热灌注化疗联合贝伐单抗治疗恶性胸腹腔积液的疗效进行Meta分析,以促进临床治疗并获得循证医学支持。
对照试验,无论是否采用随机隐藏或盲法,限制语种为中文。
确诊为恶性胸腹腔积液患者。纳入标准:(1)经病理组织学或细胞学诊断为恶性肿瘤的患者,B型超声或CT等检测方法明确有胸腔或腹腔积液;(2)患者均未经过放疗或化疗及生物治疗;(3)预计生存期在3个月以上。排除标准:(1)18岁以下恶性胸腹腔积液患者;(2)非癌性胸腹腔积液患者;(3)同时进行其他相关治疗。
试验组:腔内热灌注化疗联合贝伐单抗;对照组:单纯腔内热灌注化疗。
(1)有效率;(2)恶性积液控制率;(3)生命质量改善率。
利用计算机检索维普数据库、万方数据库、中国知网和PubMed,收集腔内热灌注化疗联合贝伐单抗与腔内热灌注化疗比较治疗恶性胸腹腔积液的对照研究文献,检索时限从各数据库建立至2018年1月,并利用互联网搜索引擎查找相关文献。检索词包括目标疾病和干预措施,根据不同数据库做相应调整。以"恶性腹腔积液""恶性胸腔积液"作为主检索词,以"热灌注化疗""贝伐单抗""治疗"作为副检索词,将主题词与关键词相互结合在上述文献数据库中检索相关文献。
依据纳入、排除标准筛选文献,依次阅读文献题目、摘要和全文,剔除不符合纳入标准的文献,对最终纳入的文献提取有效资料。在文献和资料提取过程中出现的疑点若两名研究员无法解决,则提请第三方解决。提取信息:(1)文献作者、发表日期和来源;(2)研究对象的基本特征和干预措施;(3)研究的随机方法,盲法,失访人数;(4)测量指标为有效率、控制率、生命质量改善率。以完全缓解(CR)+部分缓解(PR)计算有效率,以CR+PR+疾病稳定(SD)计算控制率,其中CR为胸腹腔积液完全消失并持续4周以上;PR为胸腹腔积液消失50 %以上,且相关症状明显缓解超过4周;SD为胸腹腔积液减少不足50 %,或增加不足25 %;疾病进展(PD)为胸腹腔积液增加明显并恶化;生命质量以Karnofsky评分为评价标准,改善为治疗后Karnofsky评分增加≥10分,稳定为Karnofsky评分变化<10分,下降为Karnofsky评分减少≥10分。
由2位研究者独立按照Cochrane系统评级员手册5.3版RCT的偏倚风险评估工具评价文献偏倚风险:(1)随机分配方法;(2)是否选择盲法;(3)结果资料是否完整;(4)分配方案的选择;(5)其他偏倚。
以Cochrane协作网提供的RevMan 5.3软件进行Meta分析。计数资料采用比值比(OR),计量资料采用均数差(MD)或标准均数差(SMD),取95 % CI作为疗效分析统计量。以χ2检验研究结果的异质性。若异质性检验结果为P>0.1且I2<50 %时,则各研究Meta分析采用固定效应模型;若异质性检验结果为P<0.1且I2>50 %,则进一步研究其异质性来源,并对相关因素进行亚组分析。当各研究结果间存在统计学异质性而无临床异质性或差异无统计学意义时,则Meta分析采取随机效应模型分析;当研究间异质性过大,则进行描述性分析。
初检出2 483篇文献,经过多层筛选,最终纳入4篇定性合成文献。
热灌注化疗联合贝伐单抗治疗恶性胸腹腔积液有效性Meta分析纳入研究的基本特征和方法学质量评价见表1。
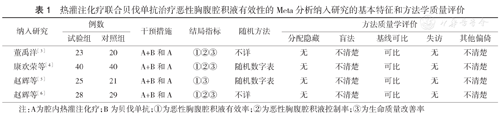
热灌注化疗联合贝伐单抗治疗恶性胸腹腔积液有效性的Meta分析纳入研究的基本特征和方法学质量评价
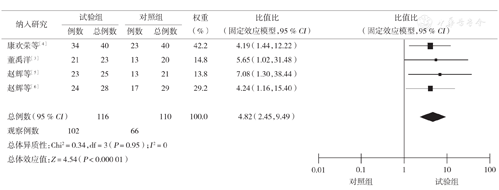
4个研究[3,4,5,6]均报道了恶性胸腹腔积液有效率,各研究结果间无统计学异质性(P=0.95,I 2=0),采用固定效应模型进行Meta分析。结果显示,两组有效率差异有统计学意义(OR=4.82,95 % CI 2.45~ 9.49,P<0.000 01),该结果支持试验组的疗效优于对照组(图1)。

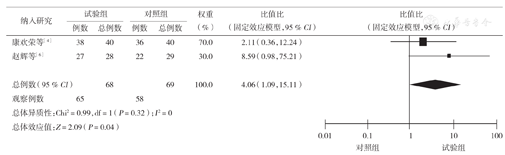
2个研究[4,6]均报道了恶性胸腹腔积液控制率,各研究结果间无统计学异质性(P=0.32,I 2=0),采用固定效应模型进行Meta分析。结果显示,两组控制率差异有统计学意义(OR=4.06,95 % CI 1.09~15.11,P<0.05),该结果支持试验组恶性积液控制优于对照组(图2)。

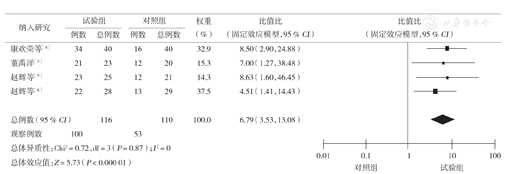
4个RCT均报道了患者生命质量改善率,各研究结果间无统计学异质性(P=0.87,I 2=0),采用固定效应模型进行Meta分析。结果显示,两组生命质量改善率差异有统计学意义(OR=6.79,95 % CI 3.53~13.08,P<0.000 01),该结果支持试验组的生命质量改善率优于对照组(图3)。

以恶性胸腹腔积液有效率为指标分析纳入研究的漏斗图对称性较好,提示纳入研究的4篇文献发表偏倚较小。
恶性积液主要包括恶性胸腔积液、恶性心包腔积液、恶性腹腔积液。临床晚期恶性肿瘤患者中恶性胸腹腔积液较为常见,患者生存期较短,当恶性腹腔积液患者缺乏有效治疗时,其平均生存期仅3.3个月[7],而恶性胸腔积液患者的3个月病死率高达65 %[8]。晚期淋巴瘤、肺癌、乳腺癌患者多有恶性胸腔积液。因淋巴分布特点,淋巴瘤患者恶性积液发病隐匿、症状复杂,容易引起误诊,不仅发生频率较高,甚至成为影响患者预后的因素[9]。临床中常通过检测癌胚抗原、糖类抗原(CA125、CA153、CA199)、基质金属蛋白酶2(MMP-2)、骨桥蛋白(OPN)等生化指标水平确诊恶性积液[10]。目前医疗界仍未确定统一或标准的针对恶性胸腹腔积液的治疗措施,众多学者尝试多种治疗方法联合应用以提高患者综合临床受益。恶性胸腹腔积液与中医"悬饮"病症表现相似,中医药联合胸腹腔灌注化疗受到关注[11]。罗银星等[12]将中药穴位敷贴(甘遂、大戟、白芥子)与顺铂胸腔灌注作为治疗组合,在24例恶性胸腔积液患者的治疗中其穴位选用双阴陵泉、双三阴交、患侧大包穴,20例对照组患者仅进行单一顺铂胸腔灌注,3周后经统计,两种治疗方法均能提高总体治疗有效率,且治疗组更能改善患者胸腔积液程度。热灌注化疗是治疗恶性胸腹腔积液有效方法,有利于热疗、化疗、腔内灌注三者协同治疗作用的发挥。针对恶性胸腹腔积液患者的治疗,热灌注化疗相对单纯的全身静脉化疗有许多优点:降低化疗药物用量,减轻不良反应,增加腔内局部的化疗药物浓度,并增强化疗药物对胸腹腔肿瘤组织的渗透性[13]。其热效应不仅可通过破坏癌细胞的染色体和溶酶体直接杀伤部分肿瘤细胞,还能使肿瘤组织血管痉挛进而破坏局部转移灶[14]。抑制VEGF成为治疗恶性胸腹积液措施中关键治疗靶点[15]。贝伐单抗通过与VEGF特异性结合,阻断其与受体结合而发挥抑制性作用,使肿瘤组织血管生长和再生得到抑制[16,17]。李凤玲[18]在一项针对非小细胞肺癌引起恶性胸腔积液的临床研究中,将贝伐单抗与顺铂联合应用,与单独采用顺铂治疗组相比,联合组近期有效率提高,生命质量改善更为显著,此外还将不良反应发生率由36.7 %降低至13.33 %。将热灌注化疗和贝伐单抗有机结合,理论上应该能发挥抑制肿瘤生长,控制胸腹腔积液生成的协同效应,临床上亦有研究支持[19]。
该Meta分析提示,热灌注化疗联合贝伐单抗与单纯热灌注化疗相比,能够提高患者的临床有效率、积液控制率和生命质量改善率。
(1)由于纳入研究的对照试验样本量较小,质量不高,故本系统评价证据强度不够;(2)纳入文献的腔内热灌注化疗在药物种类和剂量以及执行次数包括时间间隔、热灌注的温度参数等方面存在差异,不能完全消除临床异质性,故结果可能会受一定影响;(3)本研究局限于中文文献,未纳入外文相关研究CCT,故其适用性有一定局限;(4)纳入的研究缺少经济学参数,不能进一步评估热灌注联合贝伐单抗的经济学价值和患者经济承受度;(5)在安全性方面,由于所纳入文献仅有一篇明确记录了不良反应的种类和例数,故无法进行安全性分析,在临床中需要根据患者的具体情况考虑是否适合热灌注化疗联合贝伐单抗治疗,且应做好对可能发生不良反应的防范。
本系统评价进行的总结对今后深入研究和规范相关课题有一定帮助:在设计RCT时,尽可能按照循证医学思想严格控制各种偏倚,统一CCT诊断和治疗标准,提高CCT质量级别;在安全性评估方面,应详细记录胃肠道、骨髓抑制、发热等不良反应,以利于全面评价其安全性,有利于临床医师判断贝伐单抗联合腔内热灌注化疗对不同患者的适用性;贝伐单抗是针对VEGF的特性抗体,VEGF水平可以作为判断病情进展和治疗效果的一项指标,在CCT中对VEGF水平的检测可以客观判断治疗效果和提高该项研究的循证质量;应该加强研究近期、远期疗效和生存报告,以利于全面评价该治疗措施的临床价值。
无



























