
观察小细胞肺癌(SCLC)患者同步放化疗过程中血清胃泌素释放肽前体(Pro-GRP)与神经元特异性烯醇化酶(NSE)水平的变化情况及其意义。
回顾性分析2018年6月至2019年12月山西省肿瘤医院收治的80例SCLC患者资料,分为同步放化疗组(26例)与单纯化疗组(54例),采用酶联免疫吸附试验(ELISA)及电化学发光法检测患者治疗前后血清ProGRP和NSE水平,分析其与患者病情、治疗方法、治疗阶段及疗效的关系。
80例SCLC患者中,局限期患者Pro-GRP水平[127.43 pg/ml(17.61~1 547.30 pg/ml)]低于广泛期患者[547.87 pg/ml(20.20~2 111.00 pg/ml)],差异有统计学意义(U=312.65,P<0.01);局限期患者NSE水平[25.02 μg/L(4.72~64.64 μg/L)]亦低于广泛期患者[88.08 μg/L(5.52~104.64 μg/L)],差异有统计学意义(U=203.14,P<0.01)。同步放化疗组与单纯化疗组患者2、4个周期化疗后Pro-GRP及NSE水平均较治疗前下降,差异均有统计学意义(均P<0.01);同步放化疗组较单纯化疗组下降幅度大,但两组差异均无统计学意义(均P>0.05)。同步放化疗组客观缓解率为96.15%(25/26),高于单纯化疗组的70.37%(38/54),差异有统计学意义(χ2=6.972,P=0.008)。
SCLC患者同步放化疗过程中血清Pro-GRP和NSE水平可反映SCLC患者的病情变化。同步放化疗治疗SCLC的效果优于单纯化疗。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
目前,肺癌发病率及病死率居恶性肿瘤之首[1]。肺癌分为非小细胞肺癌(NSCLC)和小细胞肺癌(SCLC),其中SCLC恶性度高,疾病进展快,远处转移率高,自然病程短,对放疗和化疗高度敏感[2,3]。化疗联合胸部放疗是SCLC的主要治疗手段,手术切除只在极少数局限期患者中实施。同步放化疗在国外已被广泛应用,而在国内仍常采用序贯化放疗。胃泌素释放肽前体(Pro-GRP)与神经元特异性烯醇化酶(NSE)是SCLC敏感和特异的肿瘤标志物,它们在SCLC的诊断、评效、监测复发转移以及预测预后方面各有优势。本研究探讨血清Pro-GRP和NSE水平在SCLC患者同步放化疗过程中的变化及作用,并评估了SCLC同步放化疗相较于单纯化疗的疗效。
回顾性分析2018年6月至2019年12月在山西省肿瘤医院住院治疗的80例初诊SCLC患者资料,其中男性64例,女性16例,中位年龄55岁(31~75岁),Karnofsky评分≥70分。经纤维支气管镜或经皮肺穿刺或痰细胞学检测确诊为SCLC。治疗前完善胸部CT、颈部及腹部CT或彩色超声、头颅磁共振成像(MRI)、全身骨扫描等检查,根据VALG分期标准分为局限期(59例)及广泛期(21例)。所有患者无其他威胁生命的疾病,至少有一个可测量病灶。本研究经山西省肿瘤医院伦理委员会审核批准,所有患者均对本研究知情同意并签署知情同意书。
所有患者均完成4个周期EP(依托泊苷100 mg/d,第1天至第5天;顺铂75 mg/m2,分3~4 d给予)方案化疗。根据是否联合同步放疗,将所有患者分为同步放化疗组(26例)和单纯化疗组(54例)。放疗方式均为累积野方式照射,照射野范围为原发灶和阳性淋巴结区域,使用三维适形调强放射治疗(IMRT),6 MV X线外照射,处方剂量为95%计划靶区(PTV)DT 56~60 Gy/28~30次。采用头颈肩膜或体膜固定,CT模拟机进行定位扫描,层厚5 mm,扫描所得图像上传至Pinnacle三维治疗计划系统,逐层勾画靶区。危及器官受量:双肺V20%<25%,双肺平均剂量<15 Gy,食管V50%<50%且无热点,脊髓Dmax<45 Gy。
所有患者于治疗前、化疗2个周期及4个周期后采集清晨空腹肘静脉血3 ml,离心半径13.5 cm,3 000 r/min离心10~15 min,分离血清,采用酶联免疫吸附试验(ELISA)检测Pro-GRP水平,电化学发光法检测NSE水平,操作方法严格按照试剂盒说明书进行。试剂盒均购自瑞典CanAg诊断试剂公司。酶标仪为奥地利Tecan公司Sunrise酶标仪。
根据实体肿瘤疗效评价标准(RECIST)分为完全缓解、部分缓解、疾病稳定和疾病进展。
采用SPSS 24.0统计软件进行数据分析。计量资料不符合正态分布,采用中位数(范围)表示,采用Mann-WhitneyU检验对各组治疗前后数值进行比较,采用Wilcoxon秩和检验对同一指标下降幅度进行配对样本的检验。计数资料比较采用χ2检验。以P<0.05为差异有统计学意义。
80例SCLC患者中,局限期患者Pro-GRP水平[127.43 pg/ml(17.61~1 547.30 pg/ml)]低于广泛期患者[547.87 pg/ml(20.20~2 111.00 pg/ml)],差异有统计学意义(U=312.65,P<0.01);局限期患者NSE水平[25.02 μg/L(4.72~64.64 μg/L)]亦低于广泛期患者[88.08 μg/L(5.52~104.64 μg/L)],差异有统计学意义(U=203.14,P<0.01)。
两组患者2、4个周期化疗后血清Pro-GRP与NSE水平均较治疗前降低,差异均有统计学意义(均P<0.01)(表1)。同步放化疗组2、4个周期化疗后血清Pro-GRP与NSE下降幅度较单纯化疗组大,但两组差异均无统计学意义(均P>0.05)(表2)。
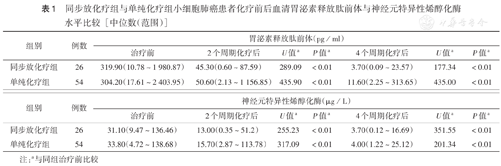
同步放化疗组与单纯化疗组小细胞肺癌患者化疗前后血清胃泌素释放肽前体与神经元特异性烯醇化酶水平比较[中位数(范围)]
同步放化疗组与单纯化疗组小细胞肺癌患者化疗前后血清胃泌素释放肽前体与神经元特异性烯醇化酶水平比较[中位数(范围)]
| 组别 | 例数 | 胃泌素释放肽前体(pg/ml) | ||||||
|---|---|---|---|---|---|---|---|---|
| 治疗前 | 2个周期化疗后 | U值a | P值a | 4个周期化疗后 | U值a | P值a | ||
| 同步放化疗组 | 26 | 319.90(10.78~1 980.87) | 45.30(0.60~87.59) | 289.09 | <0.01 | 3.70(0.09~23.57) | 177.34 | <0.01 |
| 单纯化疗组 | 54 | 304.20(17.61~2 403.95) | 50.60(2.13~1 156.85) | 435.90 | <0.01 | 11.60(2.25~313.65) | 435.00 | <0.01 |
| 组别 | 例数 | 神经元特异性烯醇化酶(μg/L) | ||||||
|---|---|---|---|---|---|---|---|---|
| 治疗前 | 2个周期化疗后 | U值a | P值a | 4个周期化疗后 | U值a | P值a | ||
| 同步放化疗组 | 26 | 31.10(9.47~136.46) | 13.00(0.35~51.2) | 255.23 | <0.01 | 3.70(0.12~16.69) | 351.55 | <0.01 |
| 单纯化疗组 | 54 | 33.80(4.72~138.68) | 15.70(2.87~113.78) | 317.09 | <0.01 | 4.00(1.22~25.12) | 201.34 | <0.01 |
注:a与同组治疗前比较
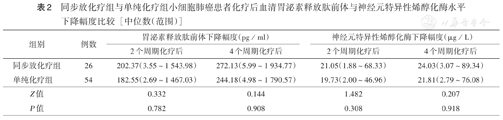
同步放化疗组与单纯化疗组小细胞肺癌患者化疗后血清胃泌素释放肽前体与神经元特异性烯醇化酶水平下降幅度比较[中位数(范围)]
同步放化疗组与单纯化疗组小细胞肺癌患者化疗后血清胃泌素释放肽前体与神经元特异性烯醇化酶水平下降幅度比较[中位数(范围)]
| 组别 | 例数 | 胃泌素释放肽前体下降幅度(pg/ml) | 神经元特异性烯醇化酶下降幅度(μg/L) | ||
|---|---|---|---|---|---|
| 2个周期化疗后 | 4个周期化疗后 | 2个周期化疗后 | 4个周期化疗后 | ||
| 同步放化疗组 | 26 | 202.37(3.55~1 543.98) | 272.13(5.99~1 934.77) | 21.05(1.88~68.33) | 24.03(3.07~89.34) |
| 单纯化疗组 | 54 | 182.55(2.69~1 467.03) | 244.18(4.98~1 790.57) | 19.73(2.00~46.96) | 21.81(2.79~76.08) |
| Z值 | 0.332 | 0.144 | 1.482 | 0.207 | |
| P值 | 0.782 | 0.908 | 0.308 | 0.918 | |
同步放化疗组完全缓解15例,部分缓解10例,客观缓解率为96.15%(25/26);单纯化疗组完全缓解16例,部分缓解22例,客观缓解率为70.37%(38/54);两组客观缓解率差异有统计学意义(χ2=6.972,P=0.008)。
SCLC因自身疾病特点被视作典型的全身性疾病,临床中往往采取全身性治疗手段[4]。随着现代医学的快速发展,放疗已逐步成为治疗局限期SCLC的首选方法,并取得了一系列治疗成果[5]。同步放化疗可使治疗时间缩短,减少肿瘤干细胞再增殖,优于单纯化疗及序贯化放疗。本研究结果亦显示对于SCLC,同步放化疗组疗效优于单纯化疗组。
NSE是一种参与糖酵解途径的关键酶,在SCLC中表达水平较高[6]。国内外研究认为初诊时NSE升高为SCLC患者的重要不良预后因素[7,8]。Pro-GRP是一种脑肠激素,在SCLC的诊断中有较高的特异性和可接受的敏感性[9,10,11,12,13],在一定程度上能更好地反映病情变化及预测预后。
段桦等[14]研究显示当SCLC患者病情变化时,NSE、Pro-GRP的水平变化有意义,但并非所有患者血清学变化均与影像学变化一致。张婷素等[15]研究显示,SCLC经过2个周期化疗后,有效组患者血清NSE及Pro-GRP水平降低,无效组患者血清NSE水平变化差异无统计学意义,Pro-GRP水平高于治疗前。提示Pro-GRP相较于NSE,在判定SCLC的病情变化中可能具有更高的应用价值,与其他研究结果相符[16,17]。本研究亦发现,血清Pro-GRP和NSE水平可以反映患者病情状况及变化,广泛期患者Pro-GRP和NSE水平高于局限期;2个周期化疗后,随着病情好转,Pro-GRP和NSE水平均下降,4个周期化疗后,Pro-GRP水平继续下降,但下降幅度不如前2个周期化疗后,NSE下降幅度较小或不变。其中同步放化疗组下降幅度大于单纯化疗组,侧面反映同步放化疗组治疗效果优于单纯化疗组,与两组近期疗效的评估结果相符。
综上所述,血清NSE和Pro-GRP水平可能作为SCLC分期的辅助依据。二者亦可作为监测SCLC病情变化、评估疗效等方面的参考指标,但由于本研究为回顾性研究,且病例数有限,结论尚需进一步研究证实。
所有作者均声明不存在利益冲突



























