
探讨右美托咪定和地塞米松抑制妇科肿瘤患者全身麻醉诱导时阿片类药物诱发呛咳(OIC)的有效性、安全性。
选取山西省肿瘤医院2019年3月至11月180例拟择期行全身麻醉下妇科肿瘤手术患者,按照随机数字表法分为空白对照组、右美托咪定组、地塞米松组,各60例。患者入室首先静息10 min(T0)。全身麻醉诱导前处理:右美托咪定组经电子输注泵泵入右美托咪定0.5 μg/kg(以0.9% NaCl注射液稀释至10 ml),地塞米松组静脉注射地塞米松10 mg,空白对照组泵入10 ml 0.9% NaCl注射液。5 min内泵完,泵注结束时间记为T1。泵注结束5 min后开始行麻醉诱导:首先静脉注射舒芬太尼0.3 μg/kg,5 s内注射完结(T2)。舒芬太尼注射2 min后(T3)依序注射苯磺顺阿曲库铵0.3 mg/kg,丙泊酚中长链注射液2 mg/kg,诱导后行去氮给氧、气管插管机械通气,插管后1 min记为T4。记录各组T2~T3期间OIC的发生率及严重性,以及T1~T4期间心动过速、心动过缓、高血压、低血压、呼吸抑制和肌强直的发生率。
右美托咪定组(10.0%,6/60)、地塞米松组(8.3%,5/60)患者OIC发生率均低于空白对照组(33.3%,20/60),三组差异有统计学意义(χ2=16.445,P<0.01),右美托咪定组与地塞米松组间OIC发生率差异无统计学意义(P>0.05)。右美托咪定组窦性心动过缓发生率(16.3%,10/60)高于空白对照组(0,0/60)与地塞米松组(8.4%,1/60),差异有统计学意义(P<0.05)。三组患者均未出现呼吸抑制、肌强直。
麻醉诱导前应用右美托咪定或静脉注射地塞米松预处理均可有效降低妇科肿瘤患者OIC发生率,两者作用效果无明显差异。输注右美托咪定后窦性心动过缓发生率升高。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
阿片类药物,如芬太尼、瑞芬太尼、舒芬太尼等常用于临床全身麻醉,可以起到镇痛、镇静、抑制心血管反应的作用[1]。其中舒芬太尼作为一种特异性μ阿片类受体激动剂,镇痛效价较高,且具有起效快、不产生免疫抑制、术中血流动力学影响小等优点,因而在全身麻醉诱导阶段应用更加广泛[2]。但静脉注射阿片类药物时常诱发患者不同程度的呛咳,其中舒芬太尼的阿片类药物诱发呛咳(OIC)发生率达40%[3]。OIC可在短时间内使全身麻醉患者空腔脏器内压、颅高压不同程度增高,从而导致脑疝、气胸;也可能导致上呼吸道一过性梗阻,引发反流误吸,造成吸入性肺炎等不良事件。虽然OIC具有自限性,持续时间很短[3],但对于伴有脑部疾患,如脑动脉瘤、高颅压、青光眼、眼部外伤以及急诊饱胃、气道过敏的患者,发生OIC尤其危险,是该类患者全身麻醉诱导过程中不可忽视的风险因素。发生OIC能采取迅速有效的干预措施对保证围术期安全和降低麻醉并发症发生率具有重要临床意义。已有临床试验应用不同药物如利多卡因、地塞米松、氯胺酮、右美托咪定以及弱阿片类药物如地佐辛等进行麻醉前预处理以抑制OIC的发生[4,5,6]。但临床指南尚未明确规定用于OIC预防的最适药物。相关文献报道右美托咪定与地塞米松均可有效降低OIC发生率,本研究对比右美托咪定与地塞米松预处理后妇科肿瘤患者OIC的发生率、严重程度以及不良反应,对OIC的预防提出建议。
纳入标准:美国麻醉医师协会(ASA)分级Ⅰ~Ⅱ级;心、肺、肝、肾功能正常;Mallampati分级Ⅰ~Ⅱ级;无长期吸烟史(吸烟≥1包/d,吸烟史≥5年),无哮喘、慢性支气管炎、慢性阻塞性肺疾病(COPD)病史;近1个月内无上呼吸道感染,术前2周胸部X线片显示无肺部炎症表现;未接受过呼吸专科治疗及使用过血管紧张素转换酶抑制剂、支气管扩张剂、皮质类固醇药物;无心动过缓病史;无阿片类药物滥用史。剔除气道评估为困难气道(Mallampati分级≥Ⅲ级)、麻醉过程中气管插管用时超过30 s的患者。
按照上述标准选取山西省肿瘤医院2019年3月至11月拟择期行全身麻醉下妇科手术患者187例。年龄18~50岁,体质量45~80 kg,体质量指数(BMI)18~24 kg/m2。按照随机数字表法将患者分为空白对照组、右美托咪定组、地塞米松组,三组患者临床资料差异均无统计学意义(均P>0.05)(表1)。本临床研究符合2013年修订的《赫尔辛基宣言》的要求,入组患者均已签署知情同意书。
全身麻醉诱导前使用不同药物处理的妇科肿瘤手术患者临床资料比较
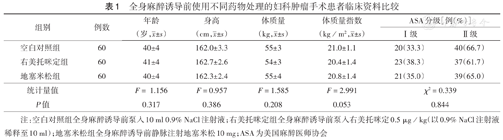
全身麻醉诱导前使用不同药物处理的妇科肿瘤手术患者临床资料比较
| 组别 | 例数 | 年龄(岁, ±s) ±s) | 身高(cm, ±s) ±s) | 体质量(kg, ±s) ±s) | 体质量指数(kg/m2, ±s) ±s) | ASA分级[例(%)] | |
|---|---|---|---|---|---|---|---|
| Ⅰ级 | Ⅱ级 | ||||||
| 空白对照组 | 60 | 40±4 | 162.0±3.3 | 55±3 | 21.0±1.1 | 20(33.3) | 40(66.7) |
| 右美托咪定组 | 60 | 41±4 | 162.7±2.6 | 54±3 | 20.4±1.4 | 23(38.3) | 37(61.7) |
| 地塞米松组 | 60 | 40±4 | 162.3±2.4 | 55±4 | 20.8±1.4 | 21(35.0) | 39(65.0) |
| 统计量值 | F= 1.156 | F=0.957 | F=1.585 | F=2.991 | χ2=0.339 | ||
| P值 | 0.317 | 0.386 | 0.208 | 0.053 | 0.844 | ||
注:空白对照组全身麻醉诱导前泵入10 ml 0.9% NaCl注射液;右美托咪定组全身麻醉诱导前泵入右美托咪定0.5 μg/kg(以0.9% NaCl注射液稀释至10 ml);地塞米松组全身麻醉诱导前静脉注射地塞米松10 mg;ASA为美国麻醉医师协会
所有患者术前均禁食8 h、禁水6 h,入手术室后建立液体通路(10 ml·kg-1·h-1),对患者进行常规心电图、脉搏血氧饱和度(SpO2)、血压、肌松监测及脑电双频谱指数(BIS)监测。所有患者不使用术前药。待患者静息10 min后进行局部麻醉下桡动脉穿刺置管有创动脉监测,给予患者面罩吸氧,氧流量2.5 L/min。右美托咪定组患者应用电子输注泵泵入右美托咪定0.5 μg/kg(右美托咪定以0.9% NaCl注射液稀释至10 ml),地塞米松组患者静脉注射地塞米松10 mg,空白对照组患者静脉注射10 ml 0.9% NaCl注射液。泵注结束5 min后行麻醉诱导:首先静脉注射舒芬太尼0.3 μg/kg,5 s内注射完毕,2 min后依序静脉注射苯磺顺阿曲库铵0.3 mg/kg,丙泊酚中长链注射液2 mg/kg,待BIS下降至50以下、肌松监测计数为0时行气管插管机械通气,维持患者呼气末二氧化碳分压(PETCO2)35~40 mmHg(1 mmHg=0.133 kPa)。麻醉维持:术中持续靶控输注丙泊酚4~8 mg·kg-1·h-1、瑞芬太尼0.25~4.00 µg·kg-1·h-1,每隔0.5 h间断追加肌松药,维持BIS为40~60。手术结束前10 min停用丙泊酚,手术结束时停用瑞芬太尼,待患者拔管清醒后送返麻醉后监测治疗室。
于入室后静息10 min(T0),药物泵注结束即刻(T1)、舒芬太尼注射后即刻(T2)、舒芬太尼注射后2 min(T3)、气管插管后1 min(T4)进行观察记录:T2~T3期间患者OIC发生率,并根据OIC发生次数进行严重程度分级,分级标准为Ⅰ级1~2次,Ⅱ级3~5次,Ⅲ级>5次;T1~T4期间患者心率、收缩压、舒张压、SpO2水平。记录心动过缓、心动过速、高血压、低血压、呼吸抑制和肌强直的发生情况。
T1~T4期间如果心率<50次/min,诊断为心动过缓,一旦发生予单次静脉注射阿托品0.5 mg;如果心率升高至基础值120%以上,诊断为心动过速[7,8],静脉注射艾司洛尔25 mg;平均动脉压(MAP)低于或高于基础值20%,分别诊断为高血压和低血压,分别采用乌拉地尔25 mg或去甲肾上腺素50 µg单次静脉注射调整血压;静脉注射舒芬太尼后SpO2<90%为呼吸抑制,立即给予面罩吸入100%纯氧[9,10]。
采用SPSS 22.0统计软件分析数据,计量资料符合正态分布,用均数±标准差( ±s)表示,多组间比较采用单因素方差分析,进一步两两比较采用LSD-t检验;多组间比较采用重复测量设计的方差分析;计数资料比较采用χ2检验或Fisher确切概率法。P<0.05为差异有统计学意义。
±s)表示,多组间比较采用单因素方差分析,进一步两两比较采用LSD-t检验;多组间比较采用重复测量设计的方差分析;计数资料比较采用χ2检验或Fisher确切概率法。P<0.05为差异有统计学意义。
空白对照组、右美托咪定组、地塞米松组患者OIC发生率分别为33.3%(20/60)、10.0%(6/60)、8.3%(5/60),三组OIC发生率差异有统计学意义(χ2=16.445,P<0.01)。空白对照组、右美托咪定组、地塞米松组发生Ⅰ级OIC分别为13例(65.0%)、5例(83.3%)、4例(80.0%),Ⅱ级OIC分别为6例(30.0%)、1例(16.7%)、1例(20.0%),Ⅲ级OIC分别为1例(5.0%)、0例、0例。右美托咪定组、地塞米松组患者OIC发生率及严重程度分级均低于空白对照组,差异均有统计学意义(均P<0.05);右美托咪定组与地塞米松组间差异无统计学意义(P>0.05)。
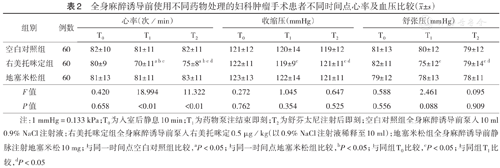
T1、T2时,右美托咪定组患者心率低于地塞米松组与空白对照组,差异均有统计学意义(均P<0.05),收缩压、舒张压差异均无统计学意义(均P>0.05);地塞米松组与空白对照组患者心率、收缩压、舒张压比较,差异均无统计学意义(均P>0.05)(表2)。
全身麻醉诱导前使用不同药物处理的妇科肿瘤手术患者不同时间点心率及血压比较( ±s)
±s)
全身麻醉诱导前使用不同药物处理的妇科肿瘤手术患者不同时间点心率及血压比较( ±s)
±s)
| 组别 | 例数 | 心率(次/min) | 收缩压(mmHg) | 舒张压(mmHg) | ||||||
|---|---|---|---|---|---|---|---|---|---|---|
| T0 | T1 | T2 | T0 | T1 | T2 | T0 | T1 | T2 | ||
| 空白对照组 | 60 | 82±10 | 81±11 | 82±11 | 121±12 | 120±14 | 119±12 | 81±13 | 80±12 | 79±12 |
| 右美托咪定组 | 60 | 80±9 | 70±11a b c | 75±8a b c d | 122±11 | 119±9c | 121±11c d | 82±11 | 75±12c | 79±14c d |
| 地塞米松组 | 60 | 81±13 | 81±11 | 83±11 | 123±13 | 122±14 | 121±11 | 79±12 | 78±13 | 78±11 |
| F值 | 0.420 | 18.994 | 11.322 | 0.272 | 1.045 | 0.647 | 0.588 | 2.461 | 0.095 | |
| P值 | 0.658 | <0.01 | <0.01 | 0.762 | 0.354 | 0.525 | 0.556 | 0.088 | 0.909 | |
注:1 mmHg=0.133 kPa;T0为入室后静息10 min;T1为药物泵注结束即刻;T2为舒芬太尼注射后即刻;空白对照组全身麻醉诱导前泵入10 ml 0.9% NaCl注射液;右美托咪定组全身麻醉诱导前泵入右美托咪定0.5 μg/kg(以0.9% NaCl注射液稀释至10 ml);地塞米松组全身麻醉诱导前静脉注射地塞米松10 mg;与同一时间点空白对照组比较,aP<0.05;与同一时间点地塞米松组比较,bP<0.05;与同组T0比较,cP<0.05;与同组T1比较,dP<0.05
空白对照组发生高血压2例(3.3%),心动过速1例(1.7%);右美托咪定组发生高血压1例(1.7%),低血压1例(1.7%),心动过速2例(3.3%),心动过缓10例(16.7%);地塞米松组发生高血压1例(1.7%),心动过缓1例(1.7%)。右美托咪定组心动过缓发生率高于空白对照组、地塞米松组(P<0.01)。所有患者均未出现呼吸抑制、肌强直。
OIC可造成脑疝、气胸、吸入性肺炎等严重后果,对患者预后造成不良影响。OIC的发生机制目前尚不明确,存在以下可能性:阿片类药物抑制中枢交感神经、兴奋迷走神经,这种效应可能会诱发咳嗽和支气管痉挛;静脉注射阿片类药物诱发肌肉突发强直,声带附近软组织收缩,也会引起呛咳;阿片类药物诱发的肺部巨细胞分泌组胺也是OIC发生的可能机制[11]。
已有多个临床试验采用多种不同药物预处理以降低OIC发生率。地塞米松是一种临床常用的皮质类固醇激素,它可有效稳定巨细胞,减缓组胺的释放。地塞米松可缓解豚鼠体内速激肽介导的支气管收缩。速激肽释放于气道C纤维活化后,可以直接导致气道平滑肌的收缩,同时速激肽也可间接引起气道内巨细胞释放组胺,进而激活组胺受体引发一系列反应。另有研究显示,地塞米松可提升中性内肽酶(neutral endopeptidase)活性,而这种中性内肽酶可以逆转气道上皮细胞的高反应性。此外,临床应用皮质类固醇也被认为可以增加肺泡细胞β肾上腺素受体数量[12]。以上均为地塞米松降低OIC发生率的可能机制。
相关研究显示麻醉前地塞米松预处理可预防术后恶心呕吐,也可减轻术后疼痛、水肿[13],这可能与皮质类固醇可抑制炎症因子有关[14]。地塞米松的应用同样可能引发一系列不良反应,作为一种皮质类固醇,它的超剂量使用会引起一定程度的免疫抑制,对于肿瘤患者手术而言,这将会增加肿瘤细胞扩散的风险,同时这种免疫抑制也会增加患者术后发生感染的可能性,不利于患者预后[15]。目前关于全身麻醉过程中地塞米松应用不良反应的报道还较少,尚需要进一步研究。
关于右美托咪定抑制OIC的相关研究已有不少。有研究表明,右美托咪定麻醉前预处理可将OIC发生率从26.7%降至6.7%[16]。右美托咪定作为一种选择性α2受体激动剂,具有镇静、镇痛、抑制交感神经兴奋的作用,应用于全身麻醉可以有效减少麻醉药物使用量。本研究中麻醉诱导前5 min应用0.5 µg/kg右美托咪定进行预处理,可降低OIC发生率,但关于右美托咪定的药理学研究认为,其镇静起效时间往往超过10 min,可以认为右美托咪定抑制OIC的效应与镇静作用无关[14]。已有大鼠实验证实右美托咪定可通过激动α2肾上腺受体逆转阿片类药物引起的肌强直[17],这可能是右美托咪定抑制OIC的可能机制,同时右美托咪定也可通过阻断组胺释放诱发的气管平滑肌收缩减少OIC的发生。
右美托咪定产生镇静、镇痛作用的同时常引起血流动力学不稳定。本研究中右美托咪定组心动过缓发生率高于空白对照组与地塞米松组。但收缩压、舒张压并未受到明显影响,不良反应发生率差异也无统计学意义。右美托咪定诱发的窦性心动过缓并未对患者产生器质性损害或对患者预后产生影响。
本研究局限性:(1)样本量较小,可能存在统计偏倚;(2)参加临床试验患者均为女性,但已有研究显示OIC发生与性别并无相关性,因此对试验结果影响有限[2];(3)本研究未进行不同剂量右美托咪定预处理与地塞米松对OIC预防效果比较。
总之,本研究结果表明地塞米松(10 mg)或右美托咪定(0.5 µg/kg)均可降低妇科肿瘤患者全身麻醉诱导时舒芬太尼引发的呛咳发生率,且效果接近,均可有效应用于OIC的预防。
所有作者均声明不存在利益冲突



























