
评价HyperCVAD/HDMTX-L方案作为弥漫大B细胞淋巴瘤挽救方案的疗效及安全性。
回顾性分析采用HyperCVAD/HDMTX-L方案挽救治疗54例弥漫大B细胞淋巴瘤患者的疗效及不良反应,分为CHOP或类CHOP方案治疗无效组27例和治疗后复发组24例,分别以HyperCVAD/MA方案治疗无效组22例和治疗后复发组26例为对照,比较两个方案治疗4个周期的疗效、不良反应和3年无进展生存(PFS)率。
HyperCVAD/HDMTX-L在CHOP或类CHOP方案无效组有效率59.3 %(16/27),3年PFS率73.3 %,HyperCVAD/MA组有效率61.9 %(13/21),3年PFS率61.5%,两组有效率、PFS率差异均无统计学意义(均P>0.05);HyperCVAD/HDMTX-L在CHOP或类CHOP方案治疗后复发组有效率47.8 %(11/23),3年PFS率54.5 % ,HyperCVAD/MA组有效率45.5 %(10/22),3年PFS率50.0 %,两组有效率、PFS率差异均无统计学意义(均P>0.05)。HyperCVAD/HDMTX-L组化疗相关的恶心、呕吐、白细胞减少、血小板减少、出血的发生率均低于对照组(均P<0.001)。
HyperCVAD/HDMTX-L方案可替代HyperCVAD/MA方案作为弥漫大B细胞淋巴瘤的挽救方案。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
弥漫大B细胞淋巴瘤(DLBCL)的标准一线治疗方案为R-CHOP方案,但有部分患者无法接受抗CD20单抗治疗,在CHOP或类CHOP方案治疗无效以及CHOP或类CHOP方案治疗复发后往往采用HyperCVAD/MA方案进行挽救治疗。在临床工作中,我们发现HyperCVAD/MA方案治疗DLBCL患者不良反应多,以骨髓抑制为重,尤其MA周期,Ⅲ、Ⅳ度白细胞减少常见,因此,我们探讨选用HyperCVAD/HDMTX-L方案挽救治疗DLBCL。
回顾性分析我院2009年2月到2012年3月经CHOP或类CHOP方案化疗2个周期未达部分缓解(PR)或者经CHOP或类CHOP方案化疗后复发且拒绝抗CD20单抗治疗的DLBCL患者资料, Karnofsky评分均≥80分。
CHOP或类CHOP方案治疗无效病例: HyperCVAD/HDMTX-L方案治疗27例(治疗组),中位年龄50岁(18~61岁),其中Ⅳ期7例、Ⅲ期12例、Ⅱ期7例、Ⅰ期1例;HyperCVAD/MA方案治疗22例(对照组),中位年龄49岁(15~60岁),其中Ⅳ期5例、Ⅲ期11例、Ⅱ期5例、Ⅰ期1例。两组一般资料差异无统计学意义(P>0.05)。
CHOP或类CHOP方案化疗后复发病例:治疗组24例,中位年龄51岁(17~63岁),其中Ⅳ期8例、Ⅲ期11例、Ⅱ期5例、Ⅰ期0例;对照组26例,中位年龄49岁(18~61岁),其中Ⅳ期8例、Ⅲ期13例、Ⅱ期4例、Ⅰ期1例。两组一般资料差异无统计学意义(P> 0.05)。
HyperCVAD/HDMTX-L方案:A方案为环磷酰胺300 mg/m2 1次/12 h第1天至第3天,地塞米松40 mg第1天至第4天、第11天至第14天,长春新碱2 mg第4、11天,多柔比星50 mg/m2第4天;B方案为甲氨蝶呤2 g/m2第1天,左旋门冬酰胺酶10 000 U第2天至第11天;A、B方案每个周期21 d,交替应用,4个周期达有效者继续4个周期化疗。
HyperCVAD/MA方案:A方案为环磷酰胺300 mg/m2 1次/12 h第1天至第3天,地塞米松40 mg第1天至第4天、第11天至第14天,长春新碱2 mg第4、11天,多柔比星50 mg/m2第4天;B方案为甲氨蝶呤1 g/m2第1天,阿糖胞苷3 g/m2 1次/12 h第2天至第3天;A、B方案每个周期21 d,交替应用,4个周期达有效者继续4个周期化疗。
疗效及常见不良反应的评价参照世界卫生组织(WHO)标准。有效为完全缓解(CR)+PR。治疗4个周期后比较两组的有效率;有效者每3个月随访1次,比较两组3年的无进展生存(PFS)情况。不良反应以每个周期为单位进行评价,因治疗组和对照组化疗方案中的A方案相同,不良反应只比较B方案相应的化疗周期。此外,对门冬酰胺酶相关的急性胰腺炎、出血与血栓等不良反应进行观察。
采用SPSS 19.0统计软件对数据进行分析,计数资料比较采用χ2检验,P<0.05为差异有统计学意义。
CHOP或类CHOP方案治疗无效的DLBCL患者中,治疗组可评价疗效27例,其中,CR 6例(22.2 %),PR 10例(37.0 %),稳定(SD)9例(33.3 %),进展(PD) 2例(7.4 % ),有效率59.3 %;对照组可评价疗效21例,其中CR 6例(28.6%),PR 7例(33.3 %),SD 5例(23.8 %),PD 3例(14.3 %),有效率61.9%;两组有效率差异无统计学意义(χ2= 0.035,P>0.05)。CHOP或类CHOP方案治疗后复发的DLBCL患者中,治疗组可评价疗效23例,其中, CR 3例(13.0 %),PR 8例(34.8 %),SD 7例(30.4 %),PD 5例(21.7%),有效率47.8 %;对照组可评价疗效22例,其中CR 5例(22.7 %),PR 5例(22.7 %),SD 8例(36.4 %),PD 4例(18.2 %),有效率45.5 %;两组有效率差异无统计学意义(χ2= 0.025,P>0.05)。
治疗组共进行155个周期B方案化疗,无死亡病例,对照组共进行137个周期B方案化疗,死亡2例。治疗组化疗相关的恶心、呕吐、白细胞减少、血小板减少、出血的发生率均低于对照组(均P<0.05 ),其他常见不良反应两组间差异均无统计学意义(均P> 0.05)(表1),未发现门冬酰胺酶相关的急性胰腺炎、出血与血栓。
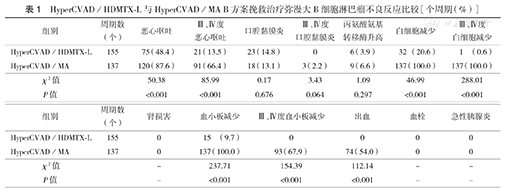
HyperCVAD/HDMTX-L与HyperCVAD/MA B方案挽救治疗弥漫大B细胞淋巴瘤不良反应比较[个周期(%)]
HyperCVAD/HDMTX-L与HyperCVAD/MA B方案挽救治疗弥漫大B细胞淋巴瘤不良反应比较[个周期(%)]
| 组别 | 周期数(个) | 恶心呕吐 | Ⅲ、Ⅳ度恶心呕吐 | 口腔黏膜炎 | Ⅲ、Ⅳ度口腔黏膜炎 | 丙氨酸氨基转移酶升高 | 白细胞减少 | Ⅲ、Ⅳ度白细胞减少 |
|---|---|---|---|---|---|---|---|---|
| HyperCVAD/HDMTX⁃L | 155 | 75(48.4) | 21(13.5) | 23(14.8) | 0 | 6(3.9) | 32(20.6) | 1(0.6) |
| HyperCVAD/MA | 137 | 120(87.6) | 91(66.4) | 18(13.1) | 3(2.2) | 9(6.6) | 137(100.0) | 137(100.0) |
| χ2值 | 50.38 | 85.99 | 0.17 | 3.43 | 1.09 | 46.99 | 288.01 | |
| P值 | <0.001 | <0.001 | 0.676 | 0.064 | 0.297 | <0.001 | <0.001 |
| 组别 | 周期数(个) | 肾损害 | 血小板减少 | Ⅲ、Ⅳ度血小板减少 | 出血 | 血栓 | 急性胰腺炎 |
|---|---|---|---|---|---|---|---|
| HyperCVAD/HDMTX⁃L | 155 | 0 | 15(9.7) | 0 | 0 | 0 | 0 |
| HyperCVAD/MA | 137 | 0 | 137(100.0) | 93(67.9) | 74(54.0) | 0 | 0 |
| χ2值 | - | 237.71 | 154.39 | 112.14 | - | - | |
| P值 | - | <0.001 | <0.001 | <0.001 | - | - |
CHOP或类CHOP方案治疗无效的DLBCL患者HyperCVAD/HDMTX-L方案化疗4个周期后有效的病例,在完成8个周期化疗后中位随访47个月(36~69个月),治疗组16例有效患者中,3年内失访1例(失访前仍CR),4例PD, 3年PFS率为73.3 %;对照组13例有效患者中,3年内PD 5例,3年PFS率为61.5%;两组3年PFS率差异无统计学意义(P= 0.505)。CHOP或类CHOP方案治疗后复发的DLBCL患者4个周期有效的病例在完成8个周期化疗后中位随访39个月(36~51个月),治疗组11例有效患者中,5例PD, 3年PFS率为54.5 %;对照组10例有效患者中,3年内PD 5例,3年PFS率为50.0 %;两组3年PFS率差异无统计学意义(P= 0.835)。
R-CHOP方案是目前国内外公认的治疗DLBCL的一线方案,其疗效及预期的风险受益得到国际上的认可,尤其是抗CD20单抗的应用使得DLBCL的无病生存期得到显著的延长。尽管如此,临床上仍有部分DLBCL患者因种种原因未能使用抗CD20单抗,以CHOP或类CHOP方案作为一线治疗。因此,探讨在没有抗CD20单抗参与下的DLBCL挽救治疗方案仍然具有一定的现实意义。
HyperCVAD/MA方案常用于高度侵袭性非霍奇金淋巴瘤的治疗,并取得了较好的临床疗效[1],也被用于DLBCL的挽救治疗。然而,HyperCVAD/MA方案的不良反应多,尤其是B方案中的中大剂量阿糖胞苷常常导致严重的骨髓抑制,进而导致严重感染及出血风险的增加,常常限制了其临床使用,因此,国内多家医疗机构尝试了一些改良方案,主要是降低B方案中阿糖胞苷的剂量以减少其骨髓抑制的程度,但是骨髓抑制,尤其是Ⅲ、Ⅳ度白细胞减少及血小板减少仍是最主要、最突出的不良反应[2,3,4]。
为了在保持挽救治疗效果的同时进一步减少化疗相关Ⅲ、Ⅳ度白细胞减少及血小板减少,从2009年起,我们开始尝试在HyperCVAD/MA方案的基础上,以左旋门冬酰胺酶替代中剂量阿糖胞苷,并提高甲氨蝶呤的化疗剂量,即以HyperCVAD/HDMTX-L方案替代HyperCVAD/MA方案作为DLBCL的挽救治疗方案。甲氨蝶呤主要通过抑制肿瘤细胞的二氢叶酸还原酶,使得肿瘤细胞生长所必需的四氢叶酸减少,从而抑制肿瘤细胞的生长。其作用的强弱与还原性叶酸载体功能有关,而B淋巴细胞系中还原性叶酸载体功能较其他细胞系强,这决定了B系肿瘤细胞对甲氨蝶呤更为敏感。因此,甲氨蝶呤是治疗B细胞肿瘤的一种非常重要的药物,尤其对中枢神经系统淋巴瘤/白血病具有很好的疗效[5,6]。甲氨蝶呤是浓度依赖性化疗药,其使用剂量0.5~6.0 g/m2不等,提高甲氨蝶呤的剂量亦有助于对"生理庇护所"肿瘤细胞的清除,减少其复发。甲氨蝶呤的骨髓抑制作用相对较轻,其最突出的不良反应是黏膜损害,严重的可致死亡,但经预防性应用甲酰四氢叶酸钙后绝大多数反应较为轻微[7],因此,将甲氨蝶呤从1 g/m2提高到2 g/m2将有助于提高疗效,且不良反应可控。左旋门冬酰胺酶通过水解门冬酰胺而干扰肿瘤细胞的能量代谢,在急性淋巴细胞白血病化疗中应用普遍。王婧等[8]研究发现,诱导中加入左旋门冬酰胺酶可改善成年人Ph-急性淋巴细胞白血病的预后,具有独立预后意义。左旋门冬酰胺酶与其他化疗药物联合治疗复发、难治性淋巴瘤也取得了较好的临床疗效[9,10]。大剂量甲氨蝶呤与门冬酰胺酶的联用使淋巴瘤细胞无法摄取其赖以生存的四氢叶酸及门冬酰胺,使淋巴瘤细胞受到双重打击,从而可抑制其生长。
从2009年至2012年,我们使用HyperCVAD/HDMTX-L方案挽救治疗CHOP或类CHOP方案治疗失败的DLBCL 27例、CHOP或类CHOP方案治疗后复发的DLBCL 24例。其中,CHOP或类CHOP方案治疗失败的患者HyperCVAD/HDMTX-L 4个周期后的有效率与HyperCVAD/MA方案相当(59.3%比61.9%, P>0.05),16例评价为有效的患者,中位随访47个月(36~69个月),PFS率与HyperCVAD/MA方案相当(73.3%比61.5 %,P=0.505);CHOP或类CHOP方案治疗后复发的DLBCL患者HyperCVAD/HDMTX-L治疗4个周期后的有效率与HyperCVAD/MA方案相当(47.8%比45.5 %,P>0.05),11例评价为有效的患者,中位随访39个月(36~51个月),PFS率为与HyperCVAD/MA方案相当(54.5%比50.0 %,P= 0.835)。本组共评价HyperCVAD/HDMTX-L方案中155个B方案化疗周期的不良反应,其恶心呕吐、白细胞减少、血小板减少、出血的发生率低于HyperCVAD/MA方案(均P<0.001),Ⅲ、Ⅳ度骨髓抑制少见,黏膜损害等其他常见不良反应均与HyperCVAD/MA方案相当(均P>0.05 ),治疗中未出现左旋门冬酰胺酶相关的出血、血栓、急性胰腺炎等。鉴于HyperCVAD/HDMTX-L方案与HyperCVAD/MA方案疗效无差异,但HyperCVAD/HDMTX-L方案Ⅲ、Ⅳ度骨髓抑制等严重不良反应明显降低,我们认为,作为DLBCL的挽救治疗方案, HyperCVAD/HDMTX-L疗效与HyperCVAD/MA相当,且安全性高,HyperCVAD/HDMTX-L方案可替代HyperCVAD/MA方案。
无



























