
版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
美国当地时间2019年3月17日上午,美国心脏病学院(American College of Cardiology,ACC)2019年会最新临床研究ACC/NEJM联合专场,吸引了无数人的目光,备受瞩目的PARTNER 3研究和EVOLUT研究结果正式发布。PARTNER 3研究发现,与接受外科手术的患者相比,经导管主动脉瓣置换术(transcatheter aortic valve replacement,TAVR)治疗低风险的严重主动脉瓣狭窄(aortic stenosis,AS)的患者术后1年的死亡率、卒中率或再住院率明显较低;EVOLUT研究也同样表明,在低危主动脉瓣重度狭窄的患者中,应用自膨胀环上生物瓣进行TAVR治疗的患者24个月时任何原因的死亡或致残性卒中发生率均较低,1年内因心力衰竭住院率也较低。作为点评专家,现代心脏病学"教父"马萨诸塞州波士顿布莱根妇女医院的Eugene Braunwald说,"我们所有人都应该记住,这是一个历史性的时刻""我们在AS的诊疗方面的进步令人难以置信"。
先前的SURTAVI、Sapien 3 Intermediate Risk、PARTNER 2A及NOTION研究逐渐将TAVR适应证扩展到低危患者(STS-PROM ≤ 3%),PARTNER 3研究和EVOLUT研究结果的发布证实了在外科手术风险低危的重度AS患者中,TAVR治疗方式优于外科手术治疗,为TAVR的临床应用和指南的更新提供了有力的证据(图1)。
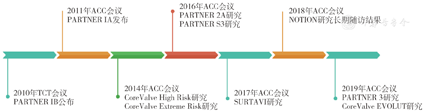

注:TCT会议为美国经导管心血管治疗学术会议;ACC为美国心脏病学院
过去半个世纪,外科经胸主动脉瓣置换术(transthoracic aortic valve replacement,SAVR)一直是严重AS患者的标准治疗方案。临床实践中有相当一部分患者由于各种原因不能接受这种创伤较大的手术,例如年龄较大、对手术的耐受性差、既往接受过开胸手术等,据统计,至少1 /3严重AS患者无法进行SAVR,医学界一直在探索创伤更小的经导管治疗技术。2002年,法国的Alain G. Cribier教授开展了首例人类TAVR,至今全球已有超过65个国家开展TAVR ,年手术量达8万例。预计到2025年,这一数字还将增长4倍,达到每年30万例以上,由此产生的花费达到近百亿美元。在过去的10年间,随着技术的进步,严重AS患者的治疗已经发生了显著改变。自2012年欧洲心脏病学会(European Society of Cardiology,ESC)和欧洲心胸外科协会(European Association of Cardio-Thoracic Surgery,EACTS)制定瓣膜疾病治疗指南后,积累了大量新的数据资料。
中国TAVR的发展明显滞后于西方,但随着TAVR技术不断进步、并发症不断减少、住院时间缩短,我国与西方国家的差距也逐渐缩小。2010年由复旦大学附属中山医院葛均波院士及中国医学科学院阜外医院高润霖院士带队,率先开展了中国前3例TAVR,截止到目前,全国约近百家心脏中心成功开展TAV R,完成超过2 000例TAVR病例。据估计,未来约有40万例中国AS患者可从中获益。
PARTNER系列研究开始于2007年5月,12年来共进行了4项重量级的研究。有里程碑意义的PARTNER研究是全球首个关于TAVR的大型、多中心、随机对照研究,旨在评估第一代球囊扩张型瓣膜(Edwards Sapien)的效果。研究分为两个队列,其中A队列入选了外科手术高危的、重度AS患者,而B队列入选了外科手术禁忌的AS患者。
PARTNER IB研究公布于2010年美国经导管心血管治疗(Transcatheter Cardiovascular Therapeutics,TCT)学术会议,研究入选了21个中心共358例患者,随机分为传统治疗组(包括球囊扩张成形术)及TAVR组,首要终点为全因死亡率。结果显示,1年随访时,TAVR组死亡率(30.7% vs. 50.7%,P<0.001 ),复合终点(死亡+再住院)发生率(42.5% vs. 71.6%,P<0.001 ),明显低于传统治疗组。30 d随访结果,TAVR组的卒中(5.0% vs. 1.1%,P=0.006)及主要血管并发症发生率较传统治疗组高(16.2% vs. 1.1%,P<0.001)。1年随访时超声心动图显示无人工瓣膜发生狭窄或反流,无瓣膜发生功能性退化。PARTNER IB研究证实,对于外科手术禁忌的重度AS患者,TAVR优于传统保守治疗,显著降低全因死亡率及全因死亡与再住院死亡复合的终点,改善患者症状[1]。
PARTNER IA研究公布于2011年ACC大会,该研究入选了35个中心共699例外科手术高危AS患者,随机分至TAVR组(n=348)或SAVR组(n=351 )。研究主要终点是1年全因死亡率。研究结果显示,1年随访结果,TAVR组的全因死亡率优于SAVR组(24.2% vs. 26.8 % ,P=0.44);30 d随访结果,TAVR组和SAVR组的全因死亡率分别是3.4%和6.5 % (P=0.07),TAVR组和SAVR组卒中发生率差异无统计学意义(3.8% vs. 2.1% ,P=0.20),TAVR组主要血管并发症的发生率较SAVR组高(11.0% vs. 3.2% ,P<0.001 ),而SAVR组的其他不良事件发生率,包括大出血(9.3% vs. 19.5% ,P<0.001)和新发心房颤动(8.6% vs. 16.0%,P=0.006)较TAVR组高。同PARTNER IB研究一样,1年随访时超声心动图提示瓣膜功能良好,跨瓣压差无明显提高,瓣周漏无增加。其研究结果显示,对于外科手术高危的重度AS患者,TAVR不劣于外科手术效果(1年死亡率24.2% vs. 26.8%,P=0.44),但是两者有各自不同的围手术期风险[2]。
另外,PARTNER Ⅰ研究5年随访结果在2014年TCT会议上公布,研究者入选术后第1年及第5年行超声心动图检查的86例TAVR患者及48例SAVR患者,两组患者基线特征相似。与标准治疗组相比,TAVR组的全因死亡率显著降低(93.6% vs. 71.8% );中位生存时间显著延长(11.1个月vs. 29.7个月);5年内再次入院率显著减少(87.3% vs. 47.6% )。随访期间,TAVR组术后的瓣口面积无明显变化(P=0.35 ),主动脉平均跨瓣压一直保持稳定状态(P=0.41 )。此外,在接受TAVR治疗的患者中,随访期间总体主动脉瓣反流、跨瓣主动脉瓣反流及瓣周主动脉瓣反流情况无明显变化,TAVR组卒中风险较标准治疗组并未增加。对SAVR患者的纵向评估结果显现出类似趋势。研究结果表明,对于不能外科手术的严重AS患者,与标准治疗相比,TAVR依然持续发挥优势,包括改善生存质量,提高心功能,降低再次入院率等[3]。
CoreValve临床研究是大型、多中心、前瞻性、对照研究,旨在评估第一代自膨胀式瓣膜的效果。其中CoreValve Extreme Risk研究入选外科手术禁忌的患者(同PARTNER B研究,入选标准为症状性重度AS患者,预计术后30 d内死亡或不可逆的致残发生风险≥ 50%)。CoreValve High Risk研究入选外科手术高危的患者。
CoreValve Extreme Risk是一项前瞻性、多中心、非随机、单组目标值对照研究,该研究入选了来自美国41个中心506例患者(489例患者最终接受TAVR ),主要终点为1年的全因死亡或大卒中的复合终点。研究结果显示,1年随访时,全因死亡率和大卒中发生率分别为24.3%和4.3%,低于预计的目标值(26.0% vs. 43.0%,P<0.000 1);30 d随访,全因死亡率和大卒中发生率分别为8.4%和2.3%;30 d内危及生命或致残性的出血发生率为12.7%,主要血管并发症为8.2%,永久性心脏起搏器安置发生率21.6%。中、重度主动脉瓣瓣周漏发生率,12个月时较出院时降低(4.2% vs. 9.7%,P=0.004 )。该研究结果表明,对于外科手术禁忌的AS患者,使用CoreValve自膨胀式瓣膜行TAVR手术是安全有效的[4]。
CoreValve High Risk研究是一项前瞻性、多中心、随机、对照研究,在2014年ACC上发布。该研究入选来自美国48个中心795例外科手术高危患者,随机分为TAVR组(n=394)及SAVR组(n=401 ),主要终点为1年的全因死亡率。使用接受治疗分析时,TAVR组1年的全因死亡率较SAVR组明显降低(14.2% vs. 19.1%,非劣势检验P<0.001,优势检验P=0.04 )。使用意向治疗分析得出相似结论。在超声心动图评估的瓣膜功能指标、心功能状态及生活质量方面,TAVR组不劣于SAVR组。进一步分析还发现1年时TAVR组主要心血管事件和脑血管事件低于SAVR组。研究结论是,对于外科手术高危的AS患者,使用CoreValve行TAVR治疗的1年生存率高于SAVR,该研究结果首次证实外科手术高危患者行TAVR优于SAVR[5]。
并且,2016年ACC会议上报道了CoreValve试验的3年结果,数据显示,TAVR与患者全因死亡率或卒中发生率明显降低有关(37.3% vs. 46.7%,P= 0.006 ),且TAVR组主动脉瓣血流动力学优于外科手术组[6]。2018年JACC发表了CoreValve High Risk研究的5年随访结果,TAVR组患者的全因死亡率为55.3%,SAVR组为55.4%,差异无统计学意义。TAVR组患者的主要卒中发生率为12.3%,SAVR组为13.2%,TAVR组患者的平均主动脉压差为(7.1±3.6)mmHg(1 mmHg=0.133 kPa),SAVR组为(10.9±5.7 ) mmHg,无明显的瓣膜血栓事件发生。另外,TAVR组患者的永久起搏器植入率为33%,SAVR组为19.8%。研究结果显示,在外科高风险患者中,TAVR和SAVR的5年全因死亡率和卒中发生率差异无统计学意义,而严重血流动力学结构瓣膜恶化发生率不尽相同[7]。
2016年ACC会议上报道了PARTNER 2A和PARTNER S3i的研究结果,该研究旨在比较外科手术中危的AS患者进行TAVR与SAVR的安全性和有效性。
PARTNER 2A研究旨在评估第二代球囊扩张型瓣膜(SapienXT)的效果,研究入选了来自美国和加拿大57个中心的2 032例具有严重症状的中危AS患者,随机分成应用SAPIEN XT进行TAVR治疗组(n=1 011)和SAVR治疗组(n=1 021),两组间的基线资料数据差异均无明显统计学意义。TAVR组中,76.3%为经股动脉途径,23.7%为经心尖或经主动脉途径。主要终点事件为2年全因死亡及致残性卒中。结果显示,TAVR组与SAVR组在随访2年主要终点事件发生率方面差异无明显统计学意义(19.3% vs. 21.1%,P=0.253 );而在经股动脉途径亚组分析中,TAVR组的2年主要终点事件发生率低于SAVR组且具有统计学意义(16.8% vs. 20.4%,HR=0.79 ,P=0.05)。30 d随访的主要血管并发症TAVR组更高,但在危及生命的出血事件、急性肾损伤和新发心房颤动则优于SAVR组。超声心动图提示TAVR术后瓣膜面积和压差的改善优于SAVR,但是中重度瓣周漏的发生率多于SAVR。PARTNER 2A研究表明,对于中危且具有严重症状的AS患者用SAPIEN XT进行TAVR治疗,与外科手术相比具有相似的2年主要终点事件发生率,且经股动脉途径进行TAVR治疗还可显著降低全因死亡和致残性卒中发生率[8]。
PARTNER S3i研究是应用第三代球囊扩张型瓣膜(Sapien3)的观察性研究,共入选1 077例外科手术中危的患者。研究发现,对于AS中危患者,应用SAPIEN 3进行TAVR治疗组相比SAVR组可使1年全因死亡率下降7.4%,所有卒中风险下降4.6%,同时使中度或重度主动脉瓣反流风险下降1.5%。对PARTNER S3i研究中SAPIEN 3 TAVR患者和PARTNER 2A研究中SAVR中危患者的倾向性分析提示,SAPIEN 3 TAVR在降低全因死亡和所有卒中方面均优于SAVR,而在减少中度或重度主动脉瓣反流方面劣于SAVR;就主要复合终点而言,二者差异无统计学意义。而且,生存分析提示,SAPIEN 3 TAVR获益在术后几个月内即显现,这在一定程度上反映了器械和操作的优越性[9]。
2017年ACC公布的SURTAVI研究和2016年公布的PARTNER 2A研究可称为姊妹研究,该研究在外科手术中危患者中对使用自膨胀式瓣膜的TAVR与外科SAVR的效果和安全性进行了比较。该研究入选1 746例外科手术中危的AS患者,美国胸外科医师协会(Society of Thoracic Surgeons,STS)评分3%~8%(评分分值由0至100%,分值越高,提示治疗后30 d内死亡风险越高),随机分为SAVR组及TAVR组(试验应用了美敦力的第一代Core Valve以及新的Evolut R生物瓣膜),主要终点为2年全因死亡或者致残性卒中。研究结果表明,2年随访时,TAVR和SAVR组终点事件发生率分别为12.6%和14% ,两组间差异无统计学意义,另外SAVR组肾功能衰竭、心房颤动、输血的发生率更高,TAVR组起搏器置入率及瓣周漏发生率更高。2年随访时,与SAVR相比,TAVR组瓣膜平均跨瓣压差更低,瓣口面积更大。该研究结果表明,在中危AS患者中,TAVR在安全性和有效性方面至少与SAVR相当[10]。
既往研究已证实,TAVR在高手术风险及不适合行外科手术治疗患者中均具有良好的疗效,而对于中低危患者是否适用的问题仍然亟待解决。PARTNER 2A等一系列研究结果的公布无疑为这片未知之地燃起了希望之火。
NOTION研究是一项前瞻性、多中心、非盲法、优效性随机对照临床试验,旨在比较心脏超声提示严重AS患者人群中TAVR和SAVR的获益与风险。该研究共纳入280例患者(其中81.8%为低危患者),将其按1:1随机分入TAVR组(使用自扩张假体)和SAVR组,主要终点事件由全因死亡、卒中和心肌梗死共同组成,次要终点事件为安全性、有效性以及心脏超声结局。对所有患者随访5年,并在随访1年时对患者的主要终点事件进行评估。
2015年,NOTION研究公布了1年随访结果,意向治疗人群中,TAVR组和SAVR组的主要终点事件发生率差异无统计学意义(13.1% vs. 16.3%,有效性P=0.43 ),实际治疗人群中结果也未发生变化;两组心血管源性死亡率和假体再植入率无差别;与SAVR组患者相比,TAVR组患者传导异常发生率较高,需植入起搏器,主动脉瓣总反流率较高,纽约心脏病协会(New York Heart Association,NYHA)心功能分级较高,但瓣孔面积改善较为明显;SAVR组患者主要或危及生命的出血事件、心源性卒中、急性肾损伤(Ⅱ期或Ⅲ期)和30 d时新发心房颤动或心房颤动加重的发生率较高[11]。
2018年ACC会议上,公布了NOTION研究的5年随访结果,其结果显示在外科低危AS患者中,主要终点事件发生率TAVR组与SAVR组差异无统计学意义(39.2% vs.35.8%,P=0.86 ),其中全因死亡率、卒中率和心肌梗死的发生率两组间差异无统计学意义;随访5年中,TAVR组瓣膜反流(8.2% vs. 0 ,P<0.001 )和起搏器植入率高于SAVR组(43.7% vs. 8.7%,P<0.001),但TAVR组瓣口面积(1.7 cm2vs.1.2 cm2,P<0.001)和平均跨瓣压差(8.2 mmHg vs.13.7 mmHg,P<0.001)明显优于SAVR组。该研究表明,NOTION研究是首个报道STS评分≤ 4%的低危人群中行TAVR或SAVR后的5年随访结果的研究。该研究5年随访结果显示,对于外科手术低危患者,TAVR组与SAVR组全因死亡率、卒中、心肌梗死或以上事件复合发生率差异无统计学意义[12]。
2018年EuroPCR期间,Lars Sondergaard分享了NOTION研究6年数据的结果,其结果显示,与SAVR相比,行TAVR后患者的血流动力学改善持续优于SAVR;TAVR组瓣膜结构退化率明显低于SAVR。此外,TAVR组与SAVR组均无瓣膜血栓形成,心内膜炎发生率也相似。两组的生物瓣失效率相当,发生率均较低。但该研究中主动脉瓣口尺寸基于超声心动图而非CT评估,且无核心超声心动图专家审核影像结果,存在一定局限性。
2019年ACC会议发布PARTNER 3的研究结果,该研究是针对低危AS患者的前瞻性、多中心、非盲法、随机对照临床试验,外科手术风险低危的重度AS患者按1:1比例随机分配至TAVR组和外科手术组,主要终点是1年内的死亡、卒中或再入院的复合终点。该研究纳入来自71个中心的1 000例患者,患者的平均年龄为73岁,STS评分平均为1.9%。研究结果显示TAVR组患者的主要终点事件率显著低于手术组(8.5% vs. 15.1%)。TAVR组患者的30 d卒中率(0.6% vs. 2.4% )、卒中或死亡事件率(1.0% vs. 3.3%)、新发心房颤动率(5.0% vs. 39.5%)均显著低于手术组。此外,TAVR组患者平均住院时间更短(3 d vs. 7 d),30 d不良预后结局[死亡或堪萨斯城心肌病患者生活质量量表(the Kansas city cardiomyopathy questionnaire,KCCQ)评分低]风险也更低(3.9% vs. 30.6% )。主要血管并发症、永久性起搏器植入、中或重度瓣周漏发生率两组之间无差异。该研究结果表明,接受TAVR的低危AS患者1年的死亡、卒中、再住院的复合终点事件发生率显著低于SAVR组;次要终点分析表明,与外科手术组相比,TAVR治疗组30 d新发心房颤动率更低,住院时间更短,治疗效果更好。另外,接受TAVR的患者在NYHA心功能分级、6 min步行距离和KCCQ评分方面比接受外科手术的患者改善的更快[13]。
2019年ACC会议同样公布了CoreValve Evolut研究,该研究旨在比较低手术死亡风险患者接受自膨胀式瓣膜经TAVR和SAVR治疗的死亡率。研究共纳入1 468例患者,其中有1 403例患者接受了TAVR或SAVR手术,所有患者的平均年龄为74岁,主要研究终点为24个月的死亡或卒中致残的复合时间发生率。TAVR组的24个月的主要终点事件率为5.3%,外科手术组则为6.7%。TAVR组患者的30 d卒中致残率(0.5% vs. 1.7% )、出血并发症(2.4% vs. 7.5% )、急性肾损伤(0.9% vs. 2.8% )、心房颤动(7.7% vs. 35.4%)发生率均显著低于外科手术组,但中或重度瓣周漏(3.5% vs. 0.5% )、永久起搏器植入率(17.4% vs. 6.1%)则高于外科手术组。此外,TAVR组患者在12个月时,跨主动脉瓣压差较低(8.6 mmHg vs. 11.2 mmHg ),有效瓣膜口面积较大(2.3 cm2vs. 2.0 cm2)。其研究结果表明对于外科手术死亡风险低的严重AS患者,TAVR就24个月死亡和卒中致残的复合终点事件率而言,不劣于外科手术[14]。
TAVR已经改变了我们对AS患者的治疗方式,目前包括PARTNER、CoreValve等多项临床研究也逐步证实其在高危、中危、低危患者中具有良好的效果。相信随着操作技术的进步和治疗器械的不断完善,TAVR治疗必将改写AS的传统治疗方案,结构性心脏病治疗也会进入一个以TAVR为代表的导管介入时代。
FRANCE-2注册研究是高危人群中TAVR治疗最大的长期数据集,研究结果支持了在这一人群中进行TAVR治疗的长期有效性。该研究不仅连续纳入了接受TAVR治疗的最大队列患者,而且459例患者在随访的第5年还接受了超声心动图评估,提供了瓣膜耐久性的信息。
2018年ESC会议报告了FRANCE-2注册研究数据,该研究共纳入4 201例接受CoreV-alve或Edwards TAVR治疗的高危连续患者。5年随访结果显示,全因死亡率为60.8%,大部分心血管事件发生在瓣膜置换的1个月内,此后发生率较低(每年<2% )。但心力衰竭是个例外,在1年时发生率为14.3%,之后下降到每年<5%。在瓣膜方面,随着时间的推移,平均梯度、瓣膜面积和主动脉瓣反流保持稳定状态。Martine Gilard教授表示,中度及重度结构性瓣膜退化(structural valve deterioration,SVD)从1年的6.9%增加到5年的13.3%,但其中分别只有1.4%和2.5%的病例是重度SVD。低的严重血流动力学SVD发生率和良好的NYHA功能状态维持至5年,也支持了这2种瓣膜用于高危患者的长期有效性[15]。
沿用2014年ACC/美国心脏协会(American Heart Association,AHA)瓣膜病管理指南中提到的瓣膜病患者危险分层,将STS <4%定义为外科手术低危,4%~8%为中危,>8%为高危。针对高危及有外科禁忌的症状性重度AS的患者行TAVR治疗已被国内外普遍接受并实施。PARTNER Ⅱ研究以及SURTAVI等多项研究结果均显示,针对中危患者行TAVR手术,在安全性及有效性方面与SAVR相当。2017年ACC/AHA瓣膜病指南进行了更新,将TAVR手术的适应人群扩大到了中危患者(Ⅱ a, B)。2017年ESC瓣膜病指南更是将中危重度AS患者行经股动脉路径TAVR的推荐级别升为Ⅰ类推荐。
随着2019年PARTNER 3和EVOLUT等研究的发布,证实在外科手术风险低危的重度AS患者中,TAVR治疗方式优于外科手术治疗,将为TAVR的临床应用和指南的更新提供有力的证据。
在2018年第四届"中国瓣膜(杭州)"会议上,葛均波院士进行了"TAVR 2018:机遇与挑战"的学术报告并对TAVR未来发展趋势进行预测,他指出TAVR的终极目标是all comers TAVR(全患群TAVR ),就是无论何种危险程度,无论什么样解剖,甚至是无论什么年龄,只要是需要干预的主动脉瓣病变,都可以做TAVR[16]。随着TAVR技术和器械的不断进展,我们有理由相信全患群TAVR的时代终将会到来,然而这其中也面临诸多问题和挑战。第一,中国患者的二叶式主动脉瓣的发生率远远高于欧美,其手术难度和风险均高于三叶式主动脉瓣,有更高的瓣中瓣发生率,二瓣化AS进行TAVR治疗仍存在挑战;第二,随着TAVR手术逐渐向低危人群、全患群发展,瓣膜的耐久性将成为一个巨大的挑战;第三,目前TAVR手术的费用远高于外科手术,如果能进一步降低器械的费用以及能够纳入医疗保险,将极大地推动TAVR在我国的发展;第四,TAVR患者多数是老年患者,TAVR术后治疗除了改善症状、防治并发症外,更重要的是提高患者的生活质量,TAVR术后的心脏康复就尤其重要。
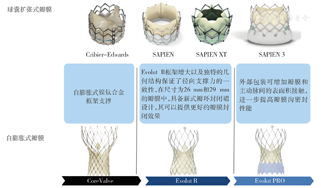
TAVR的安全性和有效性已得到认可,并被广泛应用于临床,为提高成功率、减少并发症,近几年来新型瓣膜不断涌现,目前的瓣膜主要有球囊扩张式、自膨胀式以及其他形式(图2),其中球囊扩张式瓣膜以Edwards SAPIEN瓣膜为代表,自膨胀式瓣膜以美敦力CoreValve瓣膜为代表,目前均已推出第三代瓣膜并进入市场。SAPIEN瓣膜以牛心包为材料,具有可扩展的钴铬框架,SAPIEN 3在SAPIEN XT基础上,对瓣膜定位进行了优化升级,尺寸范围为20、23、25、29 mm,外部有一个由聚对苯二甲酸乙二醇酯组成的"围裙",可遮盖约1/3框架末端部分,这种设计可有效降低瓣周漏,术后30 d中重度瓣周漏由12.2%降到0.8%,并且使用了更加细化的结构支撑模式以及更简化的输送系统,鞘管尺寸进一步缩小,23、26 mm的瓣膜经由14 F鞘管传输,29 mm瓣膜可经由16 F鞘管传输。CoreValve瓣膜以猪心包为材料,具有自膨胀镍钛诺框架的密闭心包裙样结构,第三代Evolut PRO瓣膜基于先前的Evolut R模型,尺寸范围为23、26、29 mm,外部包装可增加瓣膜和主动脉瓣间的表面积接触,进一步提高瓣膜的密封性能,专门设计用于减少瓣周漏的发生,术后30 d中重度瓣周漏从9.0%降到3.5%,同时适用于血管径狭小的患者。

我国的TAVR虽然起步较晚,但发展十分迅速。目前,全国可行TAVR手术的中心有20个省市逾80家医院,总共完成手术2 000余例,其中,经外周血管入路约1 600例。自2010年10月3日上海复旦大学附属中山医院心内科葛均波教授成功完成了国内首例TAVR,近10年以来有多种国外瓣膜以及中国自主研发的瓣膜不断进入临床研究并正式进入市场(图3)。
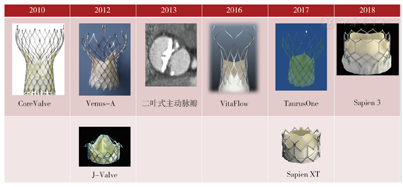

在此期间,第一个国内自主设计、具有完全自主知识产权的瓣膜Venus A于2017年5月上市。同样具有我国自主知识产权第二代介入瓣膜J-Valve也于2017年5月宣布上市,可同时治疗AS和主动脉瓣关闭不全(图4)。VitaFlow、TaurusOne、Sapien XT及Sapien 3瓣膜均已完成入组并进入随访阶段。2019年中国介入心脏病学大会(China Interventional Therapeutics, CIT )上中国医学科学院阜外医院吴永健教授代表研究组报告了TaurusOne经导管主动脉瓣膜系统安全性和有效性临床试验术后30 d的结果,以及预试验术后30 d和12个月的结果,显示TaurusOne瓣膜系统治疗我国重度AS患者安全有效,患者心功能得到明显改善,同时不良反应较少发生。
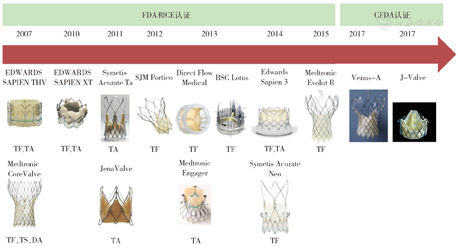

注:TF:经股动脉;TA:经心尖;TS:经锁骨下动脉;DA:经主动脉
在影像评估方面,结合中国人群个体化特点,由中国医学科学院阜外医院吴永健教授团队提出的多平面瓣环测量技术、复旦大学附属中山医院葛均波院士团队提出的小球囊测量方法、浙江大学附属第二医院王建安教授团队提出的序贯球囊测量策略以及四川大学华西医院陈茂教授团队提出的Optimal Reshaping(华西医院命名)优化测量技术均为我国TAVR技术的发展做出了实质性贡献。
国家十二五项目中由中国医学科学院阜外医院牵头的我国首个瓣膜性心脏病全国前瞻性队列研究"中国老年瓣膜性心脏病住院患者队列研究"(CHINA-DVD)已经结束,并于2018年在ESC年会上由吴永健教授报告了初步数据。
与欧美不同的是,我国二叶式主动脉瓣患者居多,钙化程度更重。而且目前我国各中心TAVR经验及团队构建差异明显,多数中心处于学习曲线阶段,机遇与挑战并存。而随着新一代瓣膜进入临床,手术成功率将不断提高,并发症也将不断降低。如世界首个预装瓣膜Venibri Valve,使得瓣膜可以在导管室随取随用,Venus A+可回收系统、Vitaflow可回收系统以及经股动脉途径的J-Valve将会给我们的手术自主创新带来越来越多的思路。
此外,经多中心合作,中华医学会心血管病学分会结构学组和中国医师协会心血管病分会结构专家委员会于今年发布了《中国经导管主动脉瓣置入术临床路径专家共识》[17],旨在为中国TAVR技术的发展铺垫可靠基石,为更多的临床医生提供帮助,为更多的患者解决病痛。
TAVR经过短短十几年的发展,已有面向低危、低龄、重度AS患者的趋势,为患者带来了福音。但是,TAVR的发展尚需更多的技术革新和器械的研发改良,期待TAVR可以在我国进行规范化的推广和普及。


























