
长期以来,人们一直认为2型糖尿病(T2DM)是一种终身性疾病。近年的临床实践显示,一些T2DM患者在采取某些干预措施后可停用降糖药而血糖仍处于正常或接近正常水平,目前多数学者用“缓解”来描述T2DM患者这种代谢持续改善至接近正常的状态。该文对T2DM缓解的概念和判断标准、实现T2DM缓解的策略、T2DM缓解的影响和预测因素进行介绍,并阐述诱导T2DM缓解的可能机制。T2DM缓解具有重要的临床意义,不仅使患者在一段时间内免于药物治疗,而且可降低患者并发症的发生风险,针对缓解机制的研究还有望衍生出新的干预靶点,但该领域仍存在若干需要解决的问题。临床上对已经缓解的T2DM患者仍不能放松管理,需要定期复查,如患者血糖超过控制标准应按照指南及时启动相应的治疗。

长期以来,人们一直认为2型糖尿病(type 2 diabetes mellitus,T2DM)是一种终身性疾病。尤其是著名的英国前瞻性糖尿病研究(United Kingdom Prospective Diabetes Study,UKPDS)结果显示,不论采用何种治疗方法,T2DM患者的血糖都呈进行性升高,而不得不加大治疗强度[1]。这更加强化了T2DM是“进展性”疾病的认识[2],患者一旦使用了降糖药,药物剂量只会逐渐增大、种类只会逐渐增多,而永无停药的可能。但是,近年的临床实践显示,一些T2DM患者在采取某些干预措施后可停用降糖药而血糖仍处于正常或接近正常水平。目前多数学者用“缓解(remission)”一词来描述糖尿病患者这种代谢持续改善至接近正常的状态。这一概念引起了国内外学者的广泛关注。我们通过文献复习,对糖尿病缓解的概念和判断标准、实现T2DM缓解的策略、T2DM缓解的影响和预测因素进行介绍,并阐述诱导T2DM缓解的可能机制。
关于T2DM缓解的标准(有些文献称为“定义”),目前尚不统一。2009年,美国糖尿病学会(American Diabetes Association,ADA)发布的共识声明建议,参考肿瘤学术语将糖尿病免于药物治疗的状态称为“缓解(remission)”,并进一步分为部分缓解(partial remission)、完全缓解(complete remission)和长期缓解(prolonged remission)[3]。部分缓解指的是在停用降糖药的情况下,糖化血红蛋白(glycated hemoglobin A1c,HbA1c)<6.5%(48 mmol/mol)、空腹血糖(fasting plasma glucose,FPG)达到5.6~6.9 mmol/L(100~125 mg/dl)且维持1年以上。完全缓解指在停用降糖药的情况下血糖正常(HbA1c正常、FPG<5.6 mmol/L)至少1年。长期缓解指完全缓解持续5年或5年以上[3]。
Lean等[4]在著名的糖尿病缓解临床试验(Diabetes Remission Clinical Trial,DiRECT)中使用的标准为停用降糖药的情况下HbA1c<6.5%至少2个月。2019年,英国临床糖尿病学家协会(Association of British Clinical Diabetologists,ABCD)和初级保健糖尿病协会(Primary Care Diabetes Society,PCDS)发布的T2DM缓解立场声明中,将糖尿病缓解定义为患者停用降糖药后血糖在糖尿病诊断标准以下至少6个月[5]。Kalra等[6]提出的标准为HbA1c<7.0%、持续至少6个月、不能用二甲双胍以外的降糖药。
最近ADA联合欧洲糖尿病研究协会(European Association for the Study of Diabetes,EASD)、美国内分泌学会和英国糖尿病协会发布了T2DM缓解共识报告[7],该共识报告甫一发布即引起广泛重视,报告文本于2021年8月30日同步在线发表于Diabetes Care、JCEM、Diabetologia和Diabetic Medicine。该共识报告认为,较之曾经使用的“消退(resolution)”“逆转(reversal)”“治愈(cure)”等词汇,“缓解(remission)”一词最适合描述糖尿病患者在停用降糖药的情况下代谢持续改善至接近正常的状态。“缓解”表明糖尿病并不总是“活动的(active)”和“进展的(progressive)”,同时也强调了上述代谢改善状态可能也不是永久的,“消退(resolution)”“逆转(reversal)”“治愈(cure)”都意味着已经建立正常的糖代谢状态并可持久甚至永远维持,而这些可能是人们期望的结局(hoped-for outcome),但显然目前尚不能做到这一点,而且有可能会让患者误认为“已经正常”而放松疾病管理。与2009年版ADA共识声明不同的是,2021年版共识报告建议不再区分部分缓解、完全缓解和长期缓解,所制定的缓解标准也不同于2009年版共识声明:在停用降糖药的情况下HbA1c<6.5%且持续至少3个月即可视为缓解。如果存在血红蛋白变异、贫血等影响HbA1c测定结果的因素,可以根据连续葡萄糖监测(continuous glucose monitoring,,CGM)测量的日平均血糖计算估测的HbA1c(estimated HbA1c,eA1c)或葡萄糖管理指标(glucose management indicator,GMI)[8],GMI<6.5%可作为替代标准。
一般认为,T2DM缓解的前提是停用降糖药。但晚近Kalra等[6]提出,既然二甲双胍和生活方式干预都是T2DM的一线治疗,T2DM的缓解也无需排斥二甲双胍治疗,即在单用二甲双胍(无其他降糖药)的基础上如果HbA1c<7.0%且持续6个月以上也可视为缓解,但这种观点目前只是一家之言。
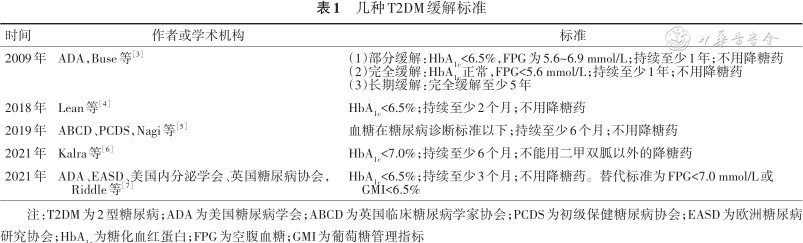
几种T2DM缓解标准见表1。
几种T2DM缓解标准
几种T2DM缓解标准
| 时间 | 作者或学术机构 | 标准 |
|---|---|---|
| 2009年 | ADA,Buse等[3] | (1)部分缓解:HbA1c<6.5%,FPG为5.6~6.9 mmol/L;持续至少1年;不用降糖药 (2)完全缓解:HbA1c正常,FPG<5.6 mmol/L;持续至少1年;不用降糖药 (3)长期缓解:完全缓解至少5年 |
| 2018年 | Lean等[4] | HbA1c<6.5%;持续至少2个月;不用降糖药 |
| 2019年 | ABCD、PCDS,Nagi等[5] | 血糖在糖尿病诊断标准以下;持续至少6个月;不用降糖药 |
| 2021年 | Kalra等[6] | HbA1c<7.0%;持续至少6个月;不能用二甲双胍以外的降糖药 |
| 2021年 | ADA、EASD、美国内分泌学会、英国糖尿病协会,Riddle等[7] | HbA1c<6.5%;持续至少3个月;不用降糖药。替代标准为FPG<7.0 mmol/L或GMI<6.5% |
注:T2DM为2型糖尿病;ADA为美国糖尿病学会;ABCD为英国临床糖尿病学家协会;PCDS为初级保健糖尿病协会;EASD为欧洲糖尿病研究协会;HbA1c为糖化血红蛋白;FPG为空腹血糖;GMI为葡萄糖管理指标
规范T2DM缓解的血糖标准、持续时间具有重要的意义。从逻辑上说,糖尿病缓解应该指的是在停用降糖药的情况下血糖仍控制在诊断标准以下,即HbA1c<6.5%。如存在影响HbA1c测定结果的因素(如血红蛋白变异等),则可以FPG作为替代指标。考虑到FPG存在一定的变异性,建议将2次非同日FPG<7.0 mmol/L作为T2DM缓解的替代标准。餐后血糖(postprandial plasma glucose,PPG)变异较大,易受膳食、运动等因素影响,不是良好的缓解判断标准。关于血糖控制持续的时间,DiRECT研究[4]及ADA等制订的共识报告[7]建议的时间标准都较短,建议以>6个月或12个月为宜。
目前用于诱导T2DM缓解的方法主要有3类,即代谢手术、强化生活方式干预和药物干预。减重代谢手术是最早使用的方法,实际上,正是减重手术对糖尿病患者血糖具有显著改善作用这一临床现象促进了人们对糖尿病缓解问题的关注和研究。代谢手术是最有效的诱导T2DM缓解的方法,不仅缓解率高,而且持续时间长[9, 10, 11]。Mingrone等[11]的随机对照试验结果显示,Roux-en-Y胃旁路术(Roux-en-Y gastric bypass,RYGB)10年缓解率为25.5%,胆胰转流术(biliopancrtic diversion,BPD)10年缓解率为50.0%,而常规药物治疗组随访10年仅1例患者在转为手术治疗后获得缓解。不过,代谢手术为有创治疗,且有一定的并发症风险,依从性低,只适合少数患者。
强化生活方式干预也是有效的诱导T2DM缓解的方法,英国学者Taylor等在这一方面做了诸多卓有成效的工作。众所周知,糖尿病患者减重代谢手术后数日,在体重明显下降之前,血糖即已显著改善甚至恢复正常,Taylor推测代谢手术后血糖的快速改善源于突然的能量负平衡,此种能量负平衡使得肝内和胰内脂肪快速减少,改善了肝脏的胰岛素抵抗并解除了β细胞的抑制。基于这一思路,他们先后设计并实施了Counterpoint研究[12]、通过长期热量摄入正常化行动对抗β细胞衰竭(counteracting beta cell failure by long term action to normalize calorie intake,Counterbalance)研究[13]及DiRECT研究[4],其中以DiRECT研究最为著名。在DiRECT研究之前,糖尿病患者健康行动(Action for Health in Diabetes,Look AHEAD)研究[14]也探讨了强化生活方式干预对T2DM缓解的影响,但效果并不理想,强化生活方式干预组1、2、3、4年糖尿病缓解率仅分别为11.5%、9.2%、6.4%和3.5%,对照组1、2、3、4年糖尿病缓解率分别为2.0%、1.7%、1.3%和0.5%。DiRECT研究用低热卡(825~853 kcal/d)的全代餐(total diet replacement)使超重或肥胖的糖尿病患者体重快速下降,1年糖尿病缓解率为46%(对照组缓解率为4%),体重降低<5、5~10、11~15、>15 kg组的缓解率分别为7%、34%、57%和86%[4];强化膳食干预组2年糖尿病缓解率仍达36%(对照组缓解率为3%),体重降低>10 kg的患者2年缓解率达64%[15]。强化膳食和增加代谢糖尿病干预(diabetes intervention accentuating diet and enhancing metabolism,DIADEM-I)试验[16]是另一项著名的强化生活方式诱导T2DM缓解的研究,该研究以居住在卡塔尔的中东和北非T2DM患者为研究对象,结果显示强化生活方式干预组1年糖尿病缓解率达61%(对照组为12%,P<0.000 1)。
药物干预是另一种常用的诱导T2DM缓解方法,我国学者在这方面作出了很多工作[17, 18, 19]。Weng等[19]的研究显示,于新诊断的T2DM患者,早期胰岛素泵强化治疗组1年糖尿病缓解率为51.1%,多次胰岛素注射强化治疗组1年缓解率为44.9%,口服降糖药强化治疗组1年缓解率为26.7%。一些新型降糖药如胰高糖素样肽1受体激动剂(glucagon-like peptide-1 receptor agonist,GLP-1RA)、钠-葡萄糖共转运蛋白2(sodium-glucose cotransporter-2,SGLT2)抑制剂等可能也有类似的作用,但目前尚缺乏相关的以糖尿病缓解作为主要终点的临床研究。
探讨T2DM缓解的影响或预测因素有助于识别出合适的患者,具有重要的临床意义。目前已有10余种积分系统用以预测代谢手术缓解T2DM[20],较常用的有ABCD和IMS积分系统[9]。ABCD积分系统包括年龄(age)、体重指数(body mass index,BMI)、C肽和病程(duration)4个指标;IMS积分系统包括降糖药数目、胰岛素使用与否、糖尿病病程和HbA1c水平4个指标。研究显示,年龄较轻、病程轻短、胰岛功能较好预示患者有较大的机会通过代谢手术获得糖尿病的缓解[9,20]。
强化生活方式干预缓解T2DM与体重降低程度、年龄、糖尿病病程有关。DiRECT研究显示,体重降低程度(无论是降低的绝对重量还是相对重量)是最强的预测因素,体重多降低1 kg,1年缓解率增加24%(P<0.000 1),2年缓解率增加23%(P<0.000 1)[21]。还有一些因素(如基线甘油三酯和γ-氨基转移酶水平)也影响缓解率[21]。但是,令人意外的是,基线BMI、空腹胰岛素、空腹C肽和糖尿病病程却不影响DiRECT研究的糖尿病缓解率[21]。Look AHEAD研究中强化生活方式干预组的缓解率较低可能与其体重降低幅度较小(1年体重降低7.9%,4年体重降低3.9%)、年龄较大(基线平均年龄58.6岁)、病程较长(基线平均病程5年)有关。DIADEM-I研究强化生活方式干预组的缓解率较高可能与其体重降低幅度较大、年龄较低、病程较短有关,DIADEM-I研究强化生活方式干预组1年体重平均降低11.98 kg,基线平均年龄41.9岁,基线平均病程21.9个月;而DiRECT研究强化生活方式干预组1年体重平均降低10.00 kg,基线平均年龄52.9岁,平均基线病程3.0年。
关于胰岛素强化治疗诱导的T2DM缓解,较低的基线FPG、较高的BMI、较好的早相胰岛素分泌、较低的外源性胰岛素需要量、较短的病程预示患者有较大的机会获得缓解[22]。
关于T2DM缓解的机制,目前尚未完全阐明。β细胞再分化(redifferentiation)可能是重要机制之一。高血糖等代谢应激使T2DM患者胰岛β细胞发生去分化(dedifferentiation),这些去分化的β细胞失去分泌胰岛素的能力,但并没有死亡。降糖药物强化治疗迅速改善了高血糖,去分化的β细胞可发生再分化,胰岛素分泌能力遂恢复[22, 23]。代谢手术诱导的T2DM缓解还与胃肠道激素的变化及胆酸的变化等因素有关[24]。
强化生活方式干预及代谢手术诱导的T2DM缓解都与急剧的能量负平衡有关,Taylor等[25, 26]对其中的机制作了较深入的探讨。基于Counterpoint研究、Counterbalance研究和DiRECT研究,Taylor等[25, 26]提出孪生循环假说(twin cycle hypothesis)来解释T2DM的发生发展及缓解机制[25, 26],这一假说具有重要的意义,但也存在一些不足,如对膳食脂肪的作用重视不够;忽视了肌肉脂肪沉积的作用,而动物实验和临床研究结果都显示肌肉脂肪沉积在T2DM的发生、发展中具有重要的作用。
如果在Taylor等[25, 26]学说的基础上,引入一个新的循环(肌肉循环),形成三循环假说(图1),用以解释能量摄入及限制在T2DM发生、发展及缓解中的作用可能更为合理。简述如下:(1)膳食碳水化合物摄入过多,使进入肝细胞内的葡萄糖增加,超过肝细胞能量代谢需要,多余的葡萄糖在肝细胞内合成甘油三酯(如果存在肌肉胰岛素抵抗,则甘油三酯合成更多,因肌肉胰岛素抵抗致肌肉摄取葡萄糖减少势必使进入肝细胞内葡萄糖增多),造成肝脏脂肪增加,从而诱发肝脏通路选择性胰岛素抵抗,即胰岛素抑制肝糖产生的能力降低,但其促进肝脏脂质合成的作用不受影响。肝脏选择性胰岛素抵抗一方面使FPG升高,另一方面使基础胰岛素分泌增加(以抑制肝糖产生),形成空腹高胰岛素血症,而高胰岛素血症反过来又刺激肝脏甘油三酯合成增加,形成恶性循环(肝循环)。(2)肝脏甘油三酯合成增加使输出的极低密度脂蛋白(very low density lipoprotein,VLDL)增多,膳食脂肪(尤其是饱和脂肪)摄入过多使血液中乳糜微粒(chylomicron,CM)增加。VLDL和CM均富含甘油三酯,这些甘油三酯在脂肪等组织经脂蛋白脂酶作用产生游离脂肪酸(free fatty acid,FFA),FFA被脂肪细胞摄取在胞内代谢产生能量或重新合成甘油三酯储存起来。如果VLDL和CM过多,产生的FFA超过脂肪组织的储脂能力,则导致肌肉、胰岛等组织脂肪异位沉积。(3)胰岛脂肪异位沉积使葡萄糖刺激的胰岛素分泌(glucose-stimulated insulin secretion,GSIS)减少,GSIS减少可引起PPG和FPG升高,而FPG和PPG的持续升高反过来又通过葡萄糖毒性引起GSIS的下降,形成恶性的胰岛循环。(4)肌肉脂肪异位沉积可引起肌肉胰岛素抵抗。由于肠道吸收的膳食葡萄糖进入机体后主要由肌肉组织摄取,这一过程受胰岛素的调控,故肌肉胰岛素抵抗可引起PPG升高。PPG升高使餐后胰岛素分泌增加,引起餐后高胰岛素血症,反过来又刺激肌肉脂肪合成增加,产生恶性的肌肉循环。(5)三个循环不是彼此独立的,而是相互联系的,最后导致糖尿病。(6)急剧的能量负平衡可以阻断上述恶性循环,恢复肝脏及肌肉胰岛素敏感性、β细胞的胰岛素分泌能力,从而使血糖正常化。
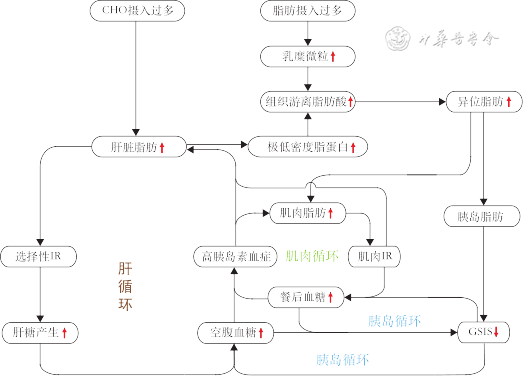

注:CHO为碳水化合物;IR为胰岛素抵抗;GSIS为葡萄糖刺激的胰岛素分泌
总之,T2DM患者的缓解已经是现实而非梦想!T2DM缓解具有重要的意义,不仅使患者在一段时间免于药物治疗,而且可降低患者并发症风险,针对缓解机制的研究还有望衍生出新的干预靶点。但该领域仍存在若干需要解决的问题,如缓解标准尚不统一、对非肥胖及病程较长的T2DM患者仍缺乏有效的缓解措施、缓解后复发(relapse)等。我们要加强T2DM缓解的相关研究,积极探索新的缓解方法,如生活方式干预联合GLP-1RA、SGLT2抑制剂、GLP-1受体和葡萄糖依赖性促胰岛素多肽受体双激动剂、GLP-1受体和胰高糖素受体双激动剂等新型降糖药,识别出各缓解方法的最佳人群,努力提高缓解率及依从性,降低复发率。我们也应该认识到,T2DM一些病理生理学缺陷并不因缓解而完全消失,这意味着已经缓解的T2DM患者仍不能放松管理,需要定期复查,如患者血糖超过控制标准应按照指南及时启动相应的治疗。
所有作者均声明不存在利益冲突



























