2017年,中华医学会感染病学分会艾滋病学组和中华医学会热带病与寄生虫学分会艾滋病学组共同制订并发布了第1版《HIV合并结核分枝杆菌感染诊治专家共识》。2021年,中国性病艾滋病防治协会HIV合并结核病专业委员会组织相关专家对第1版共识进行了修订和更新。新版共识更新了人类免疫缺陷病毒感染/艾滋病患者的结核病预防性治疗、结核病的分子诊断、耐药结核病的治疗、抗反转录病毒治疗启动时机与方案、结核相关免疫重建炎症综合征的诊断及处理、不良反应等方面的进展。本共识将根据最新临床研究证据定期进行更新。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
人体感染结核分枝杆菌(Mycobacterium tuberculosis, MTB)后可表现为结核潜伏感染(latent tuberculosis infection,LTBI)和结核病(tuberculosis)2种情况[1]。HIV感染是结核病发病的独立危险因素,HIV感染者LTBI进展为结核病的风险较HIV阴性者显著增加[2,3]。结核病是HIV感染/AIDS患者常见的机会性感染之一和疾病进展的重要影响因素[4],也是HIV感染/AIDS患者死亡的主要原因之一[5]。2021年WHO发布的全球结核病报告显示,2020年全球估计有990万人罹患结核病,其中8.0%的患者为HIV阳性,2020年约21.4万例HIV阳性结核病患者死亡[6]。2013年发表的一项荟萃分析显示,MTB/HIV合并感染率为23.51%,非洲、亚洲、欧洲、拉丁美洲和美国MTB/HIV合并感染率分别为31.25%、17.21%、20.11%、25.06%和14.84%[7]。2016年发表的一项基于我国10个省市的调查研究显示,新确诊的住院HIV感染/AIDS患者中有近1/3合并有结核病[8];2020年发布的一项基于2015年至2019年数据的研究报告显示,我国HIV感染/AIDS患者中结核病的患病率为0.7%(范围为0.2%~5.2%)[9]。HIV/MTB合并感染是影响公众健康的重要公共卫生问题。
在HIV/MTB合并感染者中,HIV与MTB之间存在复杂的相互作用,二者相互促进各自疾病进展,HIV/MTB合并感染者往往表现出更高的HIV载量、更大的病毒储存库、更为明显的异常免疫激活,以及更多见的播散性结核病[10]。HIV感染/AIDS合并结核病的发病机制及其诊治均有其相对特异性。HIV/MTB合并感染的诊断相对更为困难[11]:临床表现不典型,合并多种其他机会性感染使病情更复杂,肺外结核相对更为常见。一项基于尸检结果的研究显示,在资源受限地区,结核病占成人HIV相关疾病死亡的40%,其中近50%的结核病患者在死亡前没有得到确诊[12]。HIV/MTB合并感染的治疗有其特殊性,涉及抗结核和抗反转录病毒治疗(anti-retroviral therapy,ART)2个方面,药物不良反应、服药依从性、药物间相互作用等均会影响疗效,HIV感染/AIDS患者结核病治疗成功率也相对较低,2021年WHO全球结核病报告显示2019年新发结核病患者的治疗成功率为86%,而HIV阳性结核病患者治疗成功率只有77%[6]。此外,HIV/MTB合并感染增加了患者罹患耐多药结核病(multidrug resistant tuberculosis,MDR-TB)/广泛耐药结核病(extensive drug resistant tuberculosis,XDR-TB)的风险[13,14,15]。
为了进一步规范成人HIV/MTB合并感染的诊治,中华医学会感染病学分会艾滋病学组和中华医学会热带病与寄生虫学分会艾滋病学组于2017年共同制订并发布了第1版《HIV合并结核分枝杆菌感染诊治专家共识》[16],该共识是基于我国HIV/MTB合并感染的流行现状、临床实践和研究进展编写的,同时参考了国内外HIV/MTB合并感染诊疗相关指南。近年来,HIV/MTB合并感染领域的研究取得了重大进展,尤其是在ART、耐药结核病治疗、结核病诊断技术等方面;此外,在国家传染病重大科技专项的支持下,我国在HIV感染/AIDS合并结核病的ART时机、抗结核治疗方案和疗程等研究方面也取得了新进展。基于以上情况,2021年中国性病艾滋病防治协会HIV合并结核病专业委员会组织相关专家对第1版共识进行了修订和更新。本共识也将随着HIV/MTB合并感染流行病学的变迁及临床与基础研究的进步而定期更新。
LTBI指的是机体对MTB抗原刺激产生持续的免疫应答但无明显活动性结核病的一种状态,也称为MTB感染[17]。感染者没有结核病的症状和体征,痰等各种标本抗酸染色涂片和培养均为阴性,影像学检查正常。LTBI不具有传染性,但机体免疫状态发生改变后可进展为活动性结核病,在某些情况下,MTB可以一直呈潜伏感染而不发病,是否进展为活动性结核病与机体的免疫状态密切相关。HIV阴性健康人群中,LTBI终身进展为活动性结核病的风险为5%~10%,且多发生在感染后的前5年内[17];在HIV感染者中,LTBI进展为活动性结核病的风险显著高于HIV阴性者,其风险为每年3%~16%[1]。
目前,尚无用于LTBI检测的"金标准"。临床上用于LTBI检测的方法主要有结核菌素皮肤试验(tuberculin skin test,TST)、γ干扰素释放试验(interferon-γ release assay,IGRA)。TST简单易操作,但无法区分MTB感染和卡介苗接种,在免疫缺陷人群中的灵敏性较低。IGRA检测LTBI的特异性高于TST,且不受卡介苗接种和非结核分枝杆菌(nontuberculous mycobacteria,NTM)感染的影响[1]。相对于TST而言,IGRA的灵敏性受免疫缺陷的影响较小[1]。WHO结核病预防性治疗(tuberculosis preventive treatment,TPT)指南推荐TST和IGRA均可用于LTBI的检测,并对二者做了同等程度的推荐[17]。需要注意的是:阳性检测结果并非是LTBI进展为活动性结核病风险的可靠预测指标,也无足够的研究证据显示何者在预测LTBI进展为活动性结核病风险方面更优。
WHO TPT指南推荐TST和IGRA均可用于HIV阳性人群LTBI的检测[17]。鉴于我国卡介苗接种较为普遍及结核病的流行状况,推荐IGRA作为LTBI筛查的主要方法。基层医院由于检测条件有限,难以开展IGRA,也可考虑使用TST筛查LTBI。考虑到HIV感染/AIDS患者LTBI进展为活动性结核病的风险高这一事实,IGRA和TST检测阳性均应看作是MTB感染的有力证据,并注意排除活动性结核病的可能。
我国为结核病高负担国家,为了降低HIV感染/AIDS患者中活动性结核病的发病率,对HIV感染/AIDS患者进行LTBI筛查极为重要。建议所有HIV感染/AIDS患者,无论是否已接受ART均应常规接受LTBI筛查。进行LTBI筛查前应询问患者是否有结核病相关临床表现(发热、咳嗽、咯血、盗汗、体质量减轻、胸痛、乏力、呼吸困难),如患者具有相关临床表现则进行痰涂片、痰培养、影像学检查,以及MTB快速分子检测技术等来排除活动性结核病的可能。如无特殊不适,则进一步筛查是否为LTBI,推荐使用IGRA(首选)和TST(IGRA不可获得或无法进行时可选择)进行检测,阳性者考虑为LTBI。
HIV感染/AIDS患者中LTBI筛查的重点人群推荐如下:所有新确诊的HIV感染/AIDS患者均应进行LTBI筛查;严重免疫抑制的AIDS患者(CD4+T淋巴细胞计数<200/μL),如LTBI筛查阴性而又没有接受TPT,应在启动ART后免疫功能得到重建,即CD4+T淋巴细胞计数≥200/μL后再次进行LTBI筛查;对于反复或正暴露于活动性结核病的HIV感染/AIDS患者,建议每年接受LTBI筛查[1]。
TPT是指对具有出现活动性结核病可能的患者给予治疗措施以减少进展为结核病的风险,也指MTB感染的治疗或LTBI预防性治疗[17]。依据WHO指南,HIV感染/AIDS患者(包括已接受ART的患者、孕妇和曾经接受过抗结核治疗者)如排除了活动性结核病的可能,无论免疫抑制的程度或即使未进行LTBI检测的情况下,均应接受TPT[17]。HIV感染/AIDS患者中,LTBI检测阳性者比LTBI检测阴性者从TPT中获益更多,可使用TST或IGRA筛查LTBI以帮助识别出现活动性结核病的高风险人群。然而,LTBI筛查不应成为HIV感染/AIDS患者启动TPT的先决条件,对于HIV感染/AIDS患者而言,LTBI检测对实施TPT并非必需。但在LTBI检测阴性的HIV感染/AIDS患者中,应注意评估实施TPT的利弊。HIV感染/AIDS患者如果与活动性结核病患者有密切接触,不论TST和IGRA检测结果如何,均推荐接受TPT[1]。在实施TPT之前,需排除活动性结核病的可能,还需评估有无实施TPT的禁忌证。
WHO指南推荐的TPT方案[17]如下:①异烟肼方案,剂量为5 mg/(kg·d),每日口服1次,疗程为6个月或9个月,可同时联用维生素B6(25 mg/d)以减少周围神经炎的发生;②异烟肼[剂量为5 mg/(kg·d)]联合利福平[剂量为10 mg/(kg·d)]方案,每日口服1次,疗程为3个月;③利福喷丁(剂量为每周900 mg)+异烟肼(剂量为每周900 mg),每周口服1次,疗程为12周。亦可选用以下方案:④利福平[10 mg/(kg·d)]方案,每日口服1次,疗程为4个月;⑤利福喷丁(600 mg/d)+异烟肼(300 mg/d),每日口服1次,疗程为1个月。
HIV感染/AIDS患者(包括孕妇)合并LTBI者推荐接受TPT和ART。合并LTBI的HIV感染/AIDS患者建议尽早接受ART,ART方案与普通HIV感染/AIDS患者相同,但需考虑到药物不良反应增加的可能。目前,我国常用的免费ART方案为:替诺福韦+拉米夫定+依非韦伦,齐多夫定+拉米夫定+依非韦伦。不选择含奈韦拉平的方案,可根据情况选择替诺福韦/恩曲他滨、丙酚替诺福韦(tenofovir alafenamide,TAF)/恩曲他滨、整合酶抑制剂、利匹韦林、多拉韦林等尚未列入免费目录的抗病毒药物。
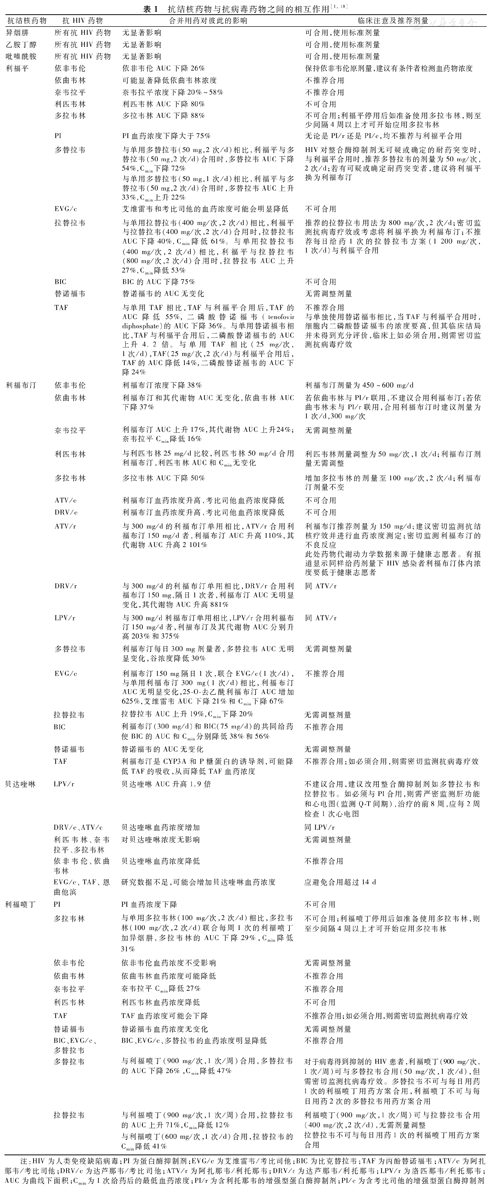
需要注意抗病毒药物和抗结核药物之间的相互作用(表1)[1,18]。使用上述方案③(利福喷丁+异烟肼,每周口服1次,疗程为12周)进行TPT时,ART可选择含依非韦伦或拉替拉韦(拉替拉韦的剂量为400 mg,每日2次)的方案;近年来有研究表明上述方案③与多替拉韦合用没有>3级的不良反应发生,方案③与多替拉韦合用时无需调整多替拉韦的剂量[19],因此,此时ART也可使用含多替拉韦(剂量为50 mg,每日口服1次)的方案。使用上述方案⑤(利福喷丁+异烟肼,每日口服1次,疗程为1个月)进行TPT时,ART应选择含依非韦伦的方案而不选择含拉替拉韦或多替拉韦的方案。
| 抗结核药物 | 抗HIV药物 | 合并用药对彼此的影响 | 临床注意及推荐剂量 |
|---|---|---|---|
| 异烟肼 | 所有抗HIV药物 | 无显著影响 | 可合用,使用标准剂量 |
| 乙胺丁醇 | 所有抗HIV药物 | 无显著影响 | 可合用,使用标准剂量 |
| 吡嗪酰胺 | 所有抗HIV药物 | 无显著影响 | 可合用,使用标准剂量 |
| 利福平 | 依非韦伦 | 依非韦伦AUC下降26% | 保持依非韦伦原剂量,建议有条件者检测血药物浓度 |
| 依曲韦林 | 可能显著降低依曲韦林浓度 | 不推荐合用 | |
| 奈韦拉平 | 奈韦拉平浓度下降20%~58% | 不推荐合用 | |
| 利匹韦林 | 利匹韦林AUC下降80% | 不可合用 | |
| 多拉韦林 | 多拉韦林AUC下降88% | 不可合用;利福平停用后如准备使用多拉韦林,则至少间隔4周以上才可开始应用多拉韦林 | |
| PI | PI血药浓度下降大于75% | 无论是PI/r还是PI/c,均不推荐与利福平合用 | |
| 多替拉韦 | 与单用多替拉韦(50 mg,2次/d)相比,利福平与多替拉韦(50 mg,2次/d)合用时,多替拉韦AUC下降54%,Cmin下降72% | HIV对整合酶抑制剂无可疑或确定的耐药突变时,与利福平合用时,推荐多替拉韦的剂量为50 mg/次,2次/d;若有可疑或确定耐药突变者,建议将利福平换为利福布汀 | |
| 与单用多替拉韦(50 mg,1次/d)相比,利福平与多替拉韦(50 mg,2次/d)合用时,多替拉韦AUC上升33%,Cmin上升22% | |||
| EVG/c | 艾维雷韦和考比司他的血药浓度可能会明显降低 | 不可合用 | |
| 拉替拉韦 | 与单用拉替拉韦(400 mg/次,2次/d)相比,利福平与拉替拉韦(400 mg/次,2次/d)合用时,拉替拉韦AUC下降40%,Cmin降低61%。与单用拉替拉韦(400 mg/次,2次/d)相比,利福平与拉替拉韦(800 mg/次,2次/d)合用时,拉替拉韦AUC上升27%,Cmin降低53% | 推荐的拉替拉韦用法为800 mg/次,2次/d;密切监测抗病毒疗效或考虑将利福平换为利福布汀;不推荐每日给药1次的拉替拉韦方案(1 200 mg/次,1次/d)与利福平合用 | |
| BIC | BIC的AUC下降75% | 不可合用 | |
| 替诺福韦 | 替诺福韦的AUC无变化 | 无需调整剂量 | |
| TAF | 与单用TAF相比,TAF与利福平合用后,TAF的AUC降低55%,二磷酸替诺福韦(tenofovir diphosphate)的AUC下降36%。与单用替诺福韦相比,TAF与利福平合用后,二磷酸替诺福韦的AUC上升4.2倍。与单用TAF相比(25 mg/次,1次/d),TAF(25 mg/次,2次/d)与利福平合用后,TAF的AUC降低14%,二磷酸替诺福韦的AUC下降24% | 不推荐合用 | |
| 与单独使用替诺福韦相比,当TAF与利福平合用时,细胞内二磷酸替诺福韦的浓度要高,但其临床结局并未得到充分评价,临床上如必须合用,则需密切监测抗病毒疗效 | |||
| 利福布汀 | 依非韦伦 | 利福布汀浓度下降38% | 利福布汀剂量为450~600 mg/d |
| 依曲韦林 | 利福布汀和其代谢物AUC无变化,依曲韦林AUC下降37% | 若依曲韦林与PI/r联用,不建议合用利福布汀;若依曲韦林未与PI/r联用,合用利福布汀时建议剂量为1次/d,300 mg/次 | |
| 奈韦拉平 | 利福布汀AUC上升17%,其代谢物AUC上升24%;奈韦拉平Cmin降低16% | 无需调整剂量 | |
| 利匹韦林 | 与利匹韦林25 mg/d比较,利匹韦林50 mg/d合用利福布汀,利匹韦林AUC和Cmin无变化 | 利匹韦林剂量调整为50 mg/次,1次/d;利福布汀剂量无需调整 | |
| 多拉韦林 | 多拉韦林AUC下降50% | 增加多拉韦林的剂量至100 mg/次,2次/d;利福布汀剂量不变 | |
| ATV/c | 利福布汀血药浓度升高,考比司他血药浓度降低 | 不可合用 | |
| DRV/c | 利福布汀血药浓度升高,考比司他血药浓度降低 | 不可合用 | |
| ATV/r | 与300 mg/d的利福布汀单用相比,ATV/r合用利福布汀150 mg/d者,利福布汀AUC升高110%,其代谢物AUC升高2 101% | 利福布汀推荐剂量为150 mg/d;建议密切监测抗结核疗效并进行血药浓度测定;密切监测利福布汀的不良反应 | |
| 此处药物代谢动力学数据来源于健康志愿者。有报道显示同样给药剂量下HIV感染者利福布汀体内浓度要低于健康志愿者 | |||
| DRV/r | 与300 mg/d的利福布汀单用相比,DRV/r合用利福布汀150 mg,隔日1次者,利福布汀AUC无明显变化,其代谢物AUC升高881% | 同ATV/r | |
| LPV/r | 与300 mg/d利福布汀单用相比,LPV/r合用利福布汀150 mg/d者,利福布汀及其代谢物AUC分别升高203%和375% | 同ATV/r | |
| 多替拉韦 | 利福布汀每日300 mg剂量者,多替拉韦AUC无明显变化,谷浓度降低30% | 无需调整剂量 | |
| EVG/c | 利福布汀150 mg隔日1次,联合EVG/c(1次/d),与单用利福布汀300 mg(1次/d)相比,利福布汀AUC无明显变化,25-O-去乙酰利福布汀AUC增加625%,艾维雷韦AUC下降21%和Cmin下降67% | 不推荐合用 | |
| 拉替拉韦 | 拉替拉韦AUC上升19%,Cmin下降20% | 无需调整剂量 | |
| BIC | 利福布汀(300 mg/d)和BIC(75 mg/d)的共同给药使BIC的AUC和Cmin分别降低38%和56% | 不推荐合用 | |
| 替诺福韦 | 替诺福韦的AUC无变化 | 无需调整剂量 | |
| TAF | 利福布汀是CYP3A和P糖蛋白的诱导剂,可能降低TAF的吸收,从而降低TAF血药浓度 | 不推荐合用;如必须合用,则需密切监测抗病毒疗效 | |
| 贝达喹啉 | LPV/r | 贝达喹啉AUC升高1.9倍 | 不建议合用,建议改用整合酶抑制剂如多替拉韦和拉替拉韦。如必须与PI合用,则需严密监测肝功能和心电图(监测Q-T间期),治疗的前8周,应每2周检查1次心电图 |
| DRV/c、ATV/c | 贝达喹啉血药浓度增加 | 同LPV/r | |
| 利匹韦林、奈韦拉平、多拉韦林 | 对贝达喹啉浓度无影响 | 无需调整剂量 | |
| 依非韦伦、依曲韦林 | 贝达喹啉血药浓度降低 | 不推荐合用 | |
| EVG/c、TAF、恩曲他滨 | 研究数据不足,可能会增加贝达喹啉血药浓度 | 应避免合用超过14 d | |
| 利福喷丁 | PI | PI血药浓度下降 | 不可合用 |
| 多拉韦林 | 与单用多拉韦林(100 mg/次,2次/d)相比,多拉韦林(100 mg/次,2次/d)联合每周1次的利福喷丁加异烟肼,多拉韦林的AUC下降29%,Cmin降低31% | 不可合用;利福喷丁停用后如准备使用多拉韦林,则至少间隔4周以上才可开始应用多拉韦林 | |
| 依非韦伦 | 依非韦伦血药浓度不受影响 | 无需调整剂量 | |
| 依曲韦林 | 依曲韦林血药浓度可能降低 | 不推荐合用 | |
| 奈韦拉平 | 奈韦拉平Cmin降低27% | 不推荐合用 | |
| 利匹韦林 | 利匹韦林血药浓度降低 | 不可合用 | |
| TAF | TAF血药浓度可能会下降 | 不推荐合用;如必须合用,则需密切监测抗病毒疗效 | |
| 替诺福韦 | 替诺福韦血药浓度无变化 | 无需调整剂量 | |
| BIC、EVG/c、多替拉韦 | BIC、EVG/c、多替拉韦的血药浓度明显降低 | 不推荐合用 | |
| 多替拉韦 | 与利福喷丁(900 mg/次,1次/周)合用,多替拉韦的AUC下降26%,Cmin降低47% | 对于病毒得到抑制的HIV患者,利福喷丁(900 mg/次,1次/周)可与多替拉韦合用(50 mg/次,1次/d),但需密切监测抗病毒疗效。多替拉韦不可与每日用药1次的利福喷丁用药方案合用,利福喷丁不可与每日用药2次的多替拉韦用药方案合用 | |
| 拉替拉韦 | 与利福喷丁(900 mg/次,1次/周)合用,拉替拉韦的AUC上升71%,Cmin降低12% | 利福喷丁(900 mg/次,1次/周)可与拉替拉韦合用(400 mg/次,2次/d),无需剂量调整 | |
| 与利福喷丁(600 mg/次,1次/d)合用,拉替拉韦的Cmin降低41% | 拉替拉韦不可与每日用药1次的利福喷丁用药方案合用 |
注:HIV为人类免疫缺陷病毒;PI为蛋白酶抑制剂;EVG/c为艾维雷韦/考比司他;BIC为比克替拉韦;TAF为丙酚替诺福韦;ATV/c为阿扎那韦/考比司他;DRV/c为达芦那韦/考比司他;ATV/r为阿扎那韦/利托那韦;DRV/r为达芦那韦/利托那韦;LPV/r为洛匹那韦/利托那韦;AUC为曲线下面积;Cmin为1次给药后的最低血药浓度;PI/r为含利托那韦的增强型蛋白酶抑制剂;PI/c为含考比司他的增强型蛋白酶抑制剂
临床实施TPT时,应综合考虑药物的可及性和安全性,以及药物间相互作用和患者服药依从性等因素来选择TPT方案和ART方案。TPT实施中应密切监测药物的不良反应及服药依从性。如出现肝脏损伤,应按照肝损伤后的处理方案进行处理,待肝功能恢复后可重启干预治疗,可在密切观察下使用原方案治疗,也可更换为其他方案。
HIV感染/AIDS患者结核病的诊断需要结合临床表现、辅助检查、影像学和病理检查结果来进行综合判断,尤其要注意HIV感染/AIDS患者结核病的临床表现及诊断有其自身特殊性,不能将用于普通人群结核病的诊断方法和思路简单地套用于HIV感染/AIDS患者结核病的诊断中。在进行诊断时,应注意患者的免疫功能状态,因为免疫缺陷程度对患者的临床表现及结核病诊断技术的灵敏性与特异性均可能产生一定影响,HIV感染/AIDS患者无论CD4+T淋巴细胞计数的水平均可出现结核病,随着免疫抑制程度的加重,肺外结核或播散性疾病变得常见。
HIV感染/AIDS患者每次随访均应系统筛查是否存在结核病[20]。尽管单纯的临床症状(发热、咳嗽、盗汗和体质量减轻)筛查对结核病诊断的灵敏性低,但临床实践中仍需注意询问患者有无结核病典型表现,需要注意的是HIV感染/AIDS患者的结核病可以无临床症状。有研究显示,是否接受ART、CD4+T淋巴细胞计数、体重指数和1种以上肺结核症状组成的评分标准可提高肺结核诊断的特异性,同时保持了一定的灵敏性[21]。胸部影像学检查对于HIV感染/AIDS患者结核病的筛查具有较好的灵敏性,但对确诊结核病而言缺乏特异性。需要注意的是胸部X线或CT检查正常的患者也不能完全排除肺结核的可能。CRP是一种炎症标志物,对于HIV感染/AIDS患者结核病筛查的灵敏性与症状筛查相当,但特异性不低于症状筛查[20]。MTB快速分子检测技术如结核分枝杆菌/利福平耐药实时荧光定量核酸扩增检测(Xpert Mycobacterium tuberculosis/rifampin,Xpert MTB/RIF)、Xpert MTB/RIF Ultra、Truenat MTB、Truenat MTB Plus及环介导等温扩增检测(loop mediated isothermal amplification,LAMP)可应用于HIV感染/AIDS患者结核病的筛查[20]。
病原学检测和病理检查仍是目前确诊结核病的主要依据。病原学检查方法主要有涂片镜检、培养和核酸检测。涂片和培养是目前临床诊断结核病的基本检测方法,是目前临床实践中确诊结核病的主要手段,也是评价抗结核疗效的主要方法。然而,由于涂片镜检的灵敏性低,WHO推荐用快速分子检测取代涂片镜检作为疑似结核病的初始诊断检测方法[22];培养技术是目前临床实践中结核病病原学确诊的金标准,然而,阳性结果常需1~3周而常不能及时满足临床需要[22]。核酸检测方法主要分为DNA检测和RNA检测两大类,核酸检测有助于快速诊断,其灵敏性高于痰涂片,建议对疑似结核病患者至少进行1次相关临床标本的MTB核酸检测[1]。
HIV感染/AIDS患者结核病的诊断需要灵敏性更高的检测技术。目前,用于结核病快速诊断的技术主要有Xpert MTB/RIF、Xpert MTB/RIF Ultra、基于芯片的分子检测技术(Truenat MTB、MTB Plus和MTB-RIF Dx)、线性探针技术、LAMP,以及用于HIV感染/AIDS人群的尿脂阿拉伯甘露聚糖抗原侧流免疫检测(lateral flow urine lipoarabinomannan assay,LF-LAM)技术[22]。WHO推荐上述快速检测技术作为肺结核和肺外结核诊断的初始诊断检测方法,但不推荐用于抗结核疗效的评价[22]。然而,Xpert MTB/RIF、Xpert MTB/RIF Ultra和Truenat尚未在HIV感染/AIDS人群中进行充分的评价,但根据其在涂片阴性结核病诊断中的重要作用,推测其在HIV感染/AIDS患者结核病诊断中具有重要价值。
Xpert MTB/RIF检测是一种实时荧光定量PCR技术,可以用于结核病的分子诊断和利福平相关耐药基因(rpoB基因)的检测,但其在涂片阴性的结核病和HIV相关结核病患者中的灵敏性相对较低[22]。研究显示,HIV感染/AIDS患者中Xpert MTB/RIF技术诊断肺结核的灵敏性和特异性均较高,且能快速区分MTB和NTM,具有较好的应用价值[23]。Xpert MTB/RIF Ultra是Xpert MTB/ RIF的更新设计版本,其检测的灵敏性进一步提高。WHO指南推荐痰Xpert MTB/RIF检测而不是传统的痰涂片镜检或培养作为疑似肺结核的初始诊断检测方法;对于近5年内无结核病病史,或曾有结核病病史且结束抗结核治疗的时间已超过5年的疑似肺结核患者,推荐使用痰Xpert MTB/RIF Ultra检测作为初始诊断检测方法;对于曾有结核病病史且结束抗结核治疗的时间不到5年的疑似肺结核患者,痰Xpert MTB/RIF Ultra检测可作为初始诊断检测方法[22]。对于疑似结核性脑膜炎患者,推荐脑脊液Xpert MTB/RIF或Xpert MTB/RIF Ultra检测作为初始诊断检测方法;对于其他疑似肺外结核患者,可选择相应的临床标本如淋巴结穿刺液、淋巴结活组织检查标本、胸腔积液、腹水、心包穿刺液、关节穿刺液和尿液进行Xpert MTB/RIF检测来作为初始诊断检测方法;对于疑似淋巴结结核,可选择淋巴结穿刺液或淋巴结活组织检查标本进行Xpert MTB/RIF Ultra检测来作为初始诊断检测方法;对于HIV相关性播散性结核疑似患者,血液Xpert MTB/RIF检测可作为初始诊断检测方法。Truenat是一种PCR技术,Truenat MTB或Truenat MTB Plus可作为疑似肺结核患者的初始诊断检测方法。
LAMP是一种MTB的快速检测技术,常在1 h内出结果,在紫外灯下可肉眼观察检测结果,在资源有限地区可代替涂片镜检作为结核病的诊断技术。目前,此技术主要针对痰标本的检测,用于其他临床标本尚未充分评价。WHO指南推荐LAMP作为痰涂片的替代方法用于疑似肺结核患者的诊断,同时也可作为具有肺结核症状和体征的成人痰涂片镜检的后续检测,尤其是痰涂片阴性的标本[22]。然而,LAMP不应替代Xpert MTB/RIF,后者可同时进行MTB鉴定和耐药检测,Xpert MTB/RIF技术不可及时则可以考虑选择LAMP。对于HIV感染/AIDS患者而言,LAMP对疑似结核病的诊断价值并不优于痰涂片镜检,也不推荐代替其他灵敏性高的分子诊断技术如Xpert MTB/RIF或Xpert MTB/RIF Ultra。
LF-LAM在普通人群结核病诊断中的灵敏性较差,但在HIV感染/AIDS患者中的灵敏性相对较高,尤其在CD4+T淋巴细胞计数低的患者中,因此,LF-LAM可用于HIV感染/AIDS患者结核病的辅助诊断:①有结核病症状和体征或CD4+T淋巴细胞计数<200/μL的住院HIV感染/AIDS患者均推荐使用LF-LAM来辅助结核病的诊断;②有结核病症状和体征或CD4+T淋巴细胞计数<100/μL的门诊就诊HIV感染/AIDS患者,均建议使用LF-LAM来辅助结核病的诊断[22]。有痰的HIV感染/AIDS患者仍应将痰Xpert MTB/RIF或Xpert MTB/RIF Ultra检测作为初始诊断检测方法。LF-LAM作为一种辅助诊断技术,常与其他检测技术联合应用,不能替代其他传统检测方法,也不能作为分诊检测技术。
线性探针技术可用于MTB的分子检测和耐药检测,尤其适合检测MTB对多种一线和二线药物的敏感性。近年来开发的新的核酸扩增检测技术可用于MTB的检测,还可检测其对利福平、异烟肼、吡嗪酰胺及二线抗结核药物的敏感性[24]。
依据WHO指南,对于结核病的诊断,推荐快速分子诊断方法作为初始诊断检测技术;对于HIV感染/AIDS患者结核病的诊断,推荐快速分子诊断技术联合LF-LAM进行诊断;当初始诊断检测结果阴性时,如仍不能排除结核病的,应结合其他检测如影像学及相关临床评价或培养等加以明确[22]。MTB检测后均推荐进行药物敏感检测以指导临床治疗。
HIV感染者结核病病理学改变与其免疫状态有关,随着免疫抑制程度的加重,典型结核性肉芽肿可表现为形成不良甚至完全缺乏[1]。
影像学检查对于AIDS患者结核病的筛查和诊断具有重要价值,但需注意晚期AIDS患者肺结核影像学表现与免疫功能尚可的AIDS患者存在明显不同:下叶、中叶、间质性和粟粒样渗出多见,而空洞性病变少见;胸内淋巴结病变多见,常表现为纵隔淋巴结肿大,而肺门淋巴结病变相对少见[1]。在免疫抑制的HIV感染/AIDS患者中(如CD4+T淋巴细胞计数<200/μL),有临床表现或痰培养阳性的患者,胸部影像学检查可正常。
HIV感染/AIDS患者结核病诊断的主要推荐意见如下。
1.所有HIV感染/AIDS患者随访时均应系统筛查是否存在结核病,可通过结核病典型症状、痰抗酸染色涂片镜检、痰分枝杆菌培养、CRP检测、胸部X线或CT检查,以及MTB快速分子检测来进行筛查。
2.对于具有结核病相关临床表现的患者,针对可能的结核病发生部位,如中枢神经系统、肺部及腹腔等进行筛查。由于肺结核最为常见,所以肺结核筛查推荐常规进行,应该包含在任何部位结核病的筛查中。
3.鉴于HIV感染/AIDS患者结核病诊断的复杂性,推荐联合应用多种技术来提高诊断的灵敏性和特异性,包括抗酸染色涂片镜检、分枝杆菌培养、影像学检查、病理检查、快速分子诊断技术和LF-LAM等。
4.对于肺结核的诊断,推荐进行痰抗酸染色涂片镜检和痰分枝杆菌培养及痰标本MTB快速分子检测。HIV感染的疾病晚期或免疫高度抑制及非空洞性病变时,痰涂片阴性肺结核较为多见,但痰培养的阳性率不受免疫缺陷的影响[25],临床标本应同时送检固体和液体培养基进行分枝杆菌培养。对于肺结核疑似患者,推荐留取3份痰标本进行涂片、培养和快速分子检测,痰标本的留取间隔时间为8~24 h[1,26]。
5.推荐尽可能留取标本以明确诊断:进行抗酸染色涂片、分枝杆菌培养和MTB快速分子检测,以及组织病理学检查来明确诊断,减少诊断性抗结核治疗。HIV感染/AIDS患者肺外结核多见,尤其是淋巴结结核、结核性胸膜炎、结核性脑膜炎、结核性心包炎和肠结核等。随着免疫抑制程度的加重,肺外结核的可能性增大,尽早留取相应标本进行检测对于明确诊断至关重要,尤其注意留取粪便、尿液、脑脊液及穿刺液进行抗酸染色涂片、培养和MTB快速分子检测。尽管血培养阳性率极低,临床上有条件也应尽可能进行,但对于血培养分枝杆菌阳性的患者,应注意排除NTM感染的可能。HIV相关性结核病患者淋巴结受累多见,淋巴结穿刺标本行病理学检查及涂片和培养对于结核病的诊断价值高[27]。对于免疫功能严重抑制的患者,尿液和血液分枝杆菌培养的阳性率相对较高[28,29]。组织病理学表现与患者免疫缺陷程度有关,免疫功能相对正常的患者,其结核病灶中可形成典型的肉芽肿病变,随着免疫缺陷程度的加重,病灶中肉芽肿病灶常缺乏。对于肺外结核,推荐同时尽早送检相应标本如支气管肺泡灌洗液(bronchoalveolar lavage fluid,BALF)、胸腔积液和脑脊液等进行MTB快速分子检测。
6.对于少数诊断困难的结核病尤其是肺外结核,可进行IGRA检测以协助诊断,但IGRA检测不能用于区分LTBI和活动性结核病。研究显示,T-SPOT.TB诊断HIV感染/AIDS合并活动性结核病的灵敏度和特异度分别为37.1%和88.7%[30],提示在免疫功能高度抑制的AIDS患者中,不推荐T-SPOT.TB作为筛查活动性结核病的常规手段,但鉴于其高特异度,可作为辅助诊断工具。另一项研究显示,在HIV感染/AIDS合并活动性结核病患者中,T-SPOT.TB检测的阳性率并不受CD4+T淋巴细胞计数水平的影响[31]。这些研究说明,T-SPOT.TB在HIV感染/AIDS合并活动性结核病诊断中具有一定辅助诊断价值,但应注意的是阴性检测结果也不能完全排除结核病的诊断。
7.推荐进行分枝杆菌菌型鉴定,最好能鉴定至具体的菌种,如无法进行菌型鉴定,则至少区分MTB和NTM以指导治疗。需要注意的是,HIV感染/AIDS患者可存在MTB和NTM同时感染的情况,尽管这种情况并不多见。
8.对于临床上高度怀疑结核病的患者,在系统检查后仍无法明确诊断的,可考虑进行诊断性治疗,但需严格掌握指征并客观评估诊断性治疗的反应。
9.临床上对于不能完全排除结核病的肺部感染患者,可考虑先经验性抗普通感染治疗,抗菌治疗方案中不宜应用含有喹诺酮类、氨基糖苷类和利奈唑胺等具有抗MTB活性的抗感染药物,并客观评价治疗反应。
原则上,HIV感染/AIDS患者结核病的治疗与单纯结核病患者相同,但需注意抗结核药物和抗病毒药物间的相互作用。HIV感染/AIDS患者结核病治疗的主要推荐意见如下。
1.对于临床表现和相关检查尤其是影像学检查结果高度怀疑结核病的HIV感染/AIDS患者,可在采集相关标本进一步送检后尽快开始抗结核治疗。初始治疗方案中应该包含异烟肼、利福平(或利福布汀)、乙胺丁醇和吡嗪酰胺4种药物,可采用固定剂量的复合制剂(fixed-dose combination,FDC)来进行治疗。
2.对于抗酸染色涂片阳性的患者,建议先按照结核病进行治疗,而后根据菌型鉴定结果进行调整,不推荐对涂片阳性的患者常规同时进行抗MTB和NTM治疗,但对于高度怀疑存在NTM病的患者,可在抗结核治疗的同时加用抗NTM药物,再根据治疗反应及菌型鉴定结果进行调整。
3.对于所有新确诊的结核病患者,推荐常规检测MTB对一线抗结核药物的敏感性,对于治疗后4个月培养仍为阳性或一度转阴后再次转阳的患者,推荐再次进行一线药物的敏感性检测。如MTB对一线抗结核药物耐药,推荐检测MTB对二线药物的敏感性。曾接受过抗结核治疗或暴露于耐药结核病的患者,推荐进行MTB耐药检测[26,32]。MTB耐药检测技术包括表型耐药检测和基因型耐药检测,目前应用于临床的主要是表型耐药检测。WHO推荐的利福平耐药检测的分子诊断技术有Xpert MTB/RIF、Xpert MTB/RIF Ultra和线性探针技术,推荐在抗结核治疗前使用快速药物敏感检测技术来检测MTB对抗结核药物的敏感性[22,33]。
4.如果MTB对一线抗结核药物敏感,则使用异烟肼+利福平(或利福布汀)+乙胺丁醇+吡嗪酰胺进行2个月的强化期治疗,然后使用异烟肼+利福平(或利福布汀)进行4个月的继续期治疗[1,26]。一项针对敏感肺结核短程治疗方案的研究显示,4个月短程治疗方案(先使用异烟肼+利福喷丁+莫西沙星+吡嗪酰胺进行2个月的强化期治疗,然后使用异烟肼+利福喷丁+莫西沙星进行2个月的继续期治疗)的抗结核疗效非劣效于传统的标准6个月治疗方案[34]。基于这一研究结果,WHO推荐此短程治疗方案可作为敏感肺结核(包括HIV感染/AIDS人群)治疗的选择方案[35,36]。然而,这一短程方案尚未在HIV感染/AIDS患者中进行充分评价,临床上需对此问题进行进一步研究。
5.对于HIV感染/AIDS合并结核病,抗结核治疗的强化期和继续期建议采用每日服药的直接面视下督导化疗(directly observed treatment,DOT)治疗策略,而不主张采取间歇治疗;建议采用个案管理的模式进行治疗管理[26]。
6.异烟肼耐药结核病的治疗:对异烟肼耐药而对利福平敏感的结核病,推荐使用利福平+乙胺丁醇+吡嗪酰胺+左氧氟沙星治疗6个月,不推荐在治疗方案中添加链霉素或其他注射抗结核药物[33]。
7.利福平耐药结核病(rifampicin resistant tuberculosis,RR-TB)治疗的失败率高,治疗后易复发。WHO指南建议RR-TB按照MDR-TB来进行治疗[33]。
8.结核病复发(relapse)后的治疗[26]:复发是指结核病完成治疗疗程(培养已经转阴)后的某个时间(通常在完成治疗后的6~12个月)出现涂片或培养转阳或临床上出现活动性结核病的表现。对于复发的患者,建议在治疗之前采集标本进行MTB培养和药物敏感检测,药物敏感检测至少要检测MTB对利福平和异烟肼的敏感性,推荐使用快速药物敏感检测技术进行检测,但需注意药物敏感检测结果呈现假阳性的可能。复发患者可重新使用利福平+吡嗪酰胺+异烟肼+乙胺丁醇;如患者既往用药不规则,MTB耐药的风险高,可根据病情经验性给予扩展的强化治疗:利福平+吡嗪酰胺+异烟肼+乙胺丁醇+注射用抗结核药物+喹诺酮类药物,再根据药物敏感检测结果调整治疗方案。患者再次出现结核病还需注意排除再感染MTB的可能。
9.结核病中断治疗(treatment interruptions)后的处理[26]:对于中断抗结核治疗的经治者,需根据中断治疗之前的病情及服药情况来决定继续治疗还是重新开始治疗;建议在重启治疗之前均应采集标本进行MTB培养和药物敏感检测,药物敏感检测至少要检测MTB对利福平和异烟肼的敏感性,推荐使用快速药物敏感检测技术进行检测。根据药物敏感检测结果来制订抗结核方案,并进行依从性指导。
10.结核病治疗失败(failure)后的处理[26]:治疗失败指的是抗结核治疗4个月(我国、欧洲和WHO定义为5个月)后培养仍为阳性的情况。对于药物敏感的肺结核,通常在标准治疗后3个月内痰培养转阴,3个月后仍呈阳性的患者需仔细评估治疗应答延迟的原因。治疗失败的可能原因:MTB原发耐药或获得性耐药、服药依从性差、服药错误、治疗药物的血药浓度不足等。临床出现疑似治疗失败时,应回顾治疗史、完善体格检查并进行胸部影像学检查。此外,初始病原体培养结果、耐药检测、治疗方案及用药依从性等情况均应仔细评估,必要时进行抗结核药物血药浓度检测。所有可获取的培养标本都应再次进行病原体培养及MTB耐药检测,推荐使用直接基于临床标本或培养出的MTB的快速分子检测技术来进行耐药检测。在检测结果出来之前,可先经验性使用二线抗结核药物进行抗结核治疗,而后根据耐药检测结果调整二线抗结核方案,不可在治疗失败的抗结核治疗方案基础上单个加用新的抗结核药物来进行治疗。
11.MDR-TB和XDR-TB及准广泛耐药结核病(pre-extensive drug resistance tuberculosis,Pre-XDR-TB)治疗应该个体化,应结合MTB的耐药性、能够获得的抗结核药物种类、病情的严重程度及合并感染的情况加以综合考虑。推荐参照WHO耐药结核病治疗指南、中国防痨协会和中华医学会结核病分会制订的相关指南和共识来制订抗结核治疗方案[33,37,38]。WHO把治疗耐药结核病的药物分为:A组(左氧氟沙星或莫西沙星、贝达喹啉、利奈唑胺)、B组(氯法齐明、环丝氨酸或特立齐酮)和C组[乙胺丁醇、德拉马尼、吡嗪酰胺、亚胺培南/西司他丁或美罗培南、阿米卡星(或链霉素)、乙硫异烟胺或丙硫异烟胺、对氨基水杨酸]。WHO 2020年结核病整合指南对MDR-TB/RR-TB患者治疗的推荐意见:方案中应包括所有3种A组药物和至少1种B组药物,以保证抗结核治疗开始时至少有4种可能有效的药物,且确保贝达喹啉疗程结束后仍至少有3种可能有效的药物维持治疗[33]。若方案中只能包括1~2种A组药物,则2种B组药物均应该纳入方案;若A组和B组药物不足以组成有效方案,则应选择C组药物来组成治疗方案。总疗程通常为18~20个月,培养转阴后常需继续15~17个月,总疗程及培养转阴后的疗程可根据治疗应答来做相应调整。对于未接受过二线药物治疗或二线药物暴露不足1个月且MTB对氟喹诺酮类药物敏感的MDR-TB/RR-TB患者,WHO指南推荐可使用9~12个月含贝达喹啉全口服的短程治疗方案。
12.对于HIV感染/AIDS患者敏感肺结核的治疗,WHO指南推荐标准的6个月疗程[39]。研究显示,对绝大多数患者而言,6个月的疗程是足够的,对抗结核治疗的反应延迟(即在抗结核治疗2个月后仍有结核病相关临床表现或者MTB培养仍为阳性)或胸部X线片上出现空洞的结核病或播散性肺外结核或强化期未能使用吡嗪酰胺的患者,抗结核疗程均应延长至9个月[1]。对于HIV感染/AIDS合并结核病患者,均建议在抗结核治疗期间启动ART,如果在抗结核治疗期间未启动ART,可将抗结核疗程延长至9个月[26]。中枢神经系统结核疗程应该延长至9~12个月,骨、关节及脊柱结核疗程通常为6~9个月,其他部位的肺外结核疗程通常为6个月[26]。
13.结核病孕妇患者的治疗与一般成人患者相同,但应注意以下情况:①异烟肼对人虽无致畸作用,但在妊娠及产后使用异烟肼更易引起肝功能损伤,因此,应注意监测肝功能。②利福平对人无致畸作用;利福布汀可用于孕妇;利福喷丁在动物中可致畸形,不建议用于孕妇。③动物实验显示吡嗪酰胺无致畸作用,但吡嗪酰胺在孕妇中应用的经验极为有限[1,26]。WHO指南建议结核病孕妇患者应使用吡嗪酰胺,如在化学治疗方案中不包含吡嗪酰胺,抗结核疗程需延长至9个月。④尚无证据表明乙胺丁醇对人具有致畸作用,成人服用乙胺丁醇后可引起视力损伤,但接受乙胺丁醇治疗的孕妇所生产的婴儿尚未出现视力损伤的报道。⑤耐药结核病孕妇的治疗尚缺乏足够的经验,很多药物不宜用于孕妇。链霉素和卡那霉素可引起新生儿听神经损伤,故孕妇不应使用,如必须使用氨基糖苷类药物,则可考虑使用阿米卡星或卷曲霉素。喹诺酮类药物通常不宜用于孕妇,但对于耐药结核病,可根据耐药检测结果选用喹诺酮类药物。对氨基水杨酸可考虑用于耐药结核病孕妇的治疗。乙硫异烟胺不推荐用于孕妇。环丝氨酸在孕妇中尚无应用的经验。一项南非回顾性研究结果显示,孕妇使用贝达喹啉后的治疗转归与非妊娠成人相当,妊娠期使用贝达喹啉可能与婴儿出生低体质量(<2 500 g)相关,但超过80%的婴儿在出生后1年体质量增加且发育正常[40]。
14.研究显示糖皮质激素有助于提高结核性脑膜炎的生存率[41]。美国感染病学会(Infectious Diseases Society of America,IDSA)和WHO敏感结核病治疗指南均推荐结核性脑膜炎患者接受6~8周的糖皮质激素治疗(泼尼松或地塞米松)[26,39]。结核性脑膜炎临床研究中糖皮质激素的使用方法如下[41]:地塞米松前2~4周剂量为0.3~0.4 mg/(kg·d),后每周减量0.1 mg/(kg·d),直至0.1 mg/(kg·d),之后改为4 mg/d,再每周减量1 mg/d,总疗程为12周。HIV感染/AIDS患者合并结核性脑膜炎治疗中建议应用糖皮质激素,但目前尚无研究比较不同剂量和疗程的糖皮质激素使用的疗效和不良反应的差异,因此,糖皮质激素使用的最佳剂量和疗程尚待研究。WHO敏感结核病治疗指南指出,结核性心包炎患者可使用糖皮质激素[39];但近年来研究显示,糖皮质激素并不能改善预后,因此,在IDSA指南中结核性心包炎患者不推荐常规使用糖皮质激素,但IDSA指南建议在一些情况下如大量心包积液及心包穿刺液中炎症标志物或炎症细胞升高明显时,可酌情考虑使用糖皮质激素[26]。
15.对于HIV感染/AIDS合并结核病患者,尤其具有高龄、肾功能衰竭、营养不良或糖尿病等情况,使用异烟肼时建议同时使用维生素B6以降低发生神经病变方面不良反应的风险[26]。
16.抗结核治疗后的疗效评估和随访与非HIV感染者相同,由于患者同时接受ART,建议进行更为密切的随访和观察。每月应对患者服用抗结核药物的耐受性、依从性、疗效及不良反应进行评价,应采取措施提高患者服药的依从性。必要时可借助治疗药物浓度监测技术来指导和调整治疗方案。耐药结核病的治疗效果的评价强调抗酸染色涂片镜检和MTB培养的重要性。
所有合并结核病的HIV感染/AIDS患者无论CD4+T淋巴细胞计数水平的高低均应接受ART [1,18,26,36]。目前,主张合并结核病的HIV感染/AIDS患者尽早启动ART [1,18,36],推荐在抗结核治疗后2周内尽早启动ART [36]。对于HIV感染孕妇合并活动性结核病,为了母亲健康和阻断HIV母婴传播,ART也应尽早进行。如合并耐药结核病(MDR-TB或XDR-TB),也应尽早启动ART,在确定MTB耐药使用二线抗结核药物后8周内开始ART[33,36]。中枢神经系统结核患者启动ART的最佳时机尚未明确,通常建议在抗结核治疗后的4~8周启动ART[36]。临床上一时难以明确或排除结核病的HIV感染者,不应因此而推迟启动ART。
利福霉素是短程抗结核治疗方案中的基本药物,但是利福霉素与常用抗HIV药物,即蛋白酶抑制剂(protease inhibitor,PI)、非核苷类反转录酶抑制剂(non-nucleoside reverse transcriptase inhibitor,NNRTI)、整合酶抑制剂之间存在相互作用(表1)。在目前临床应用的利福霉素中,利福平是最强的肝脏P450酶诱导剂,利福布汀对肝脏P450酶的诱导作用明显低于利福平,尽管利福霉素与抗病毒药物之间存在相互作用,但利福霉素仍应尽可能用在HIV感染/AIDS合并结核病患者中。
利福平或利福布汀均可与核苷类反转录酶抑制剂(nucleotide reverse transcriptase inhibitor,NRTI)合用;利福平和利福喷丁不推荐与多拉韦林、利匹韦林或依曲韦林合用;利福布汀可与PI或NNRTI(除地拉韦定)合用,但在某些合用方案中利福布汀和抗病毒药物的剂量需要调整(表1)。依非韦伦能降低利福布汀的血药浓度,当二者联用时,利福布汀的剂量应该增加至0.45~0.60 g/d;奈韦拉平不影响利福布汀的血药浓度,因此,当二者合用时,不用调整利福布汀的剂量。利福平对奈韦拉平的血药浓度影响较大,二者合用有增加肝脏损伤的危险,二者合用对HIV感染/AIDS合并结核病患者的抗病毒疗效欠佳且容易导致停药,故奈韦拉平不推荐用于HIV感染/AIDS合并结核病的患者。利福平不能与奈非那韦、沙奎那韦、茚地那韦、阿扎那韦及增强型PI合用。
合并结核病的HIV感染/AIDS患者ART方案和治疗原则与单纯HIV感染/AIDS患者相同,但需考虑药物间相互作用、药物不良反应等问题。使用含利福平的抗结核治疗方案与含依非韦伦的ART方案具有良好的疗效和较低的不良反应。使用含利福平抗结核治疗方案的患者推荐的首选ART方案为:替诺福韦+拉米夫定+依非韦伦,不能耐受替诺福韦的可选择齐多夫定(或阿巴卡韦)+拉米夫定+依非韦伦。在体质量超过60 kg的患者中,依非韦伦与利福平合用时需要将依非韦伦增加至800 mg/d,但目前认为利福平对依非韦伦的影响不大。基于以上情况,目前推荐与利福平合用时依非韦伦仍使用标准剂量(600 mg/d)[1]。WHO指南推荐替诺福韦+拉米夫定+低剂量依非韦伦(400 mg/d)的ART方案也可用于HIV感染/AIDS患者的抗病毒治疗,有研究显示合并结核病的患者,利福平与低剂量依非韦伦(400 mg/d)合用对依非韦伦血药浓度影响小而不影响其抗病毒疗效,WHO指南认为低剂量依非韦伦方案也可用于合并结核病的HIV感染/AIDS患者中[36],而IDSA指南认为这方面的研究数据少,但仍推荐使用标准剂量的依非韦伦方案[1]。鉴于研究证据尚有限,MTB/HIV合并感染者如仍使用含依非韦伦的ART方案,目前仍推荐依非韦伦标准剂量。
合并结核病的HIV感染/AIDS患者也可选择替诺福韦+拉米夫定+整合酶抑制剂的ART方案[42]。研究显示,含多替拉韦的ART方案在合并结核病的HIV感染/AIDS患者中的抗病毒疗效非劣效于含依非韦伦的ART方案[43],含多替拉韦的ART方案已被推荐用于合并结核病的HIV感染/AIDS患者中[1,18,36];而含标准剂量拉替拉韦(400 mg,2次/d)的ART方案在合并结核病的HIV感染/AIDS患者中未显示其抗病毒疗效非劣效于含依非韦伦的ART方案,因此,含标准剂量拉替拉韦的ART方案仅被推荐用于特定部分的合并结核病的HIV感染/AIDS患者中[44]。需要注意的是,多替拉韦与利福平合用时,需要增加多替拉韦的剂量(50 mg,2次/d);基于目前的研究结果,拉替拉韦合并使用利福平时,建议增加拉替拉韦剂量(800 mg,2次/d)[44]。利福布汀对氨基转移酶的诱导作用较弱,使用多替拉韦或拉替拉韦治疗的HIV感染/AIDS合并结核病患者可以考虑使用利福布汀替代利福平,无需调整剂量。艾维雷韦/考比司他(elvitegravir/cobicistat,EVG/c)和新一代的整合酶抑制剂比克替拉韦(bictegravir, BIC)均不推荐与利福霉素类药物合用。
如抗结核使用的是利福布汀,则ART方案可使用PI,但需注意调整相关药物的剂量,与PI合用时利福布汀的推荐剂量为0.15 g/d[1]。一旦患者停止使用PI而改用其他抗病毒药物时,则应相应调整利福布汀的剂量,有条件的建议进行血药浓度监测以指导相关药物的剂量调整。如结核病是在启动ART后确诊的,则应根据抗结核方案对ART方案进行调整。
TB-IRIS是HIV感染/AIDS合并MTB感染者接受ART后较早出现的并发症,以局部或全身性过度炎症反应为特征,主要有2种类型:治疗矛盾型免疫重建炎症综合征(immune reconstruction inflamatory syndrome,IRIS)和暴露型IRIS[1]。治疗矛盾型IRIS在临床上相对多见,通常发生在ART后的1~4周,是指合并结核病的HIV感染/AIDS患者接受抗结核治疗后临床症状改善,接受ART后,由于免疫系统对炎症反应能力的增强,结核病症状可能再加重,除发热外,患者可有胸膜浸润或者出现新结核病灶,同时纵隔淋巴结或外周淋巴结肿大,皮肤或内脏出现结核脓肿、结核性关节炎或骨髓炎等。对于播散性结核患者而言,出现TB-IRIS时,肝脏相关性TB-IRIS较多见,表现为恶心、呕吐,肝大,胆汁淤积性肝功能异常,以及偶有黄疸,肝活体组织检查提示肉芽肿性肝炎[1]。治疗矛盾型TB-IRIS通常持续2~3个月,但部分患者的症状可持续数月甚至更长时间,持续时间长的患者通常表现有化脓性淋巴结炎和脓肿形成。一项荟萃分析显示,HIV感染/AIDS合并结核病患者中IRIS发生率为18%,TB-IRIS导致的死亡并不常见,TB-IRIS相关死亡病例占比为2%[45]。治疗矛盾型IRIS发生的风险因素包括:基线CD4+T淋巴细胞计数低,尤其<100/μL;基线病毒载量高;播散性结核或肺外结核;抗结核治疗与启动ART之间的时间间隔短,尤其是在抗结核治疗的前2个月内启动ART[1]。暴露型IRIS是指亚临床未识别的结核感染在启动ART后新出现结核病表现,临床症状出现快且类似于细菌性肺炎,局部也可出现淋巴结炎和脓肿,暴露型IRIS在临床上相对少见。
治疗矛盾型TB-IRIS诊断的参考标准[1]:① HIV感染/AIDS合并结核病患者接受抗结核治疗后临床状况改善,接受ART后,结核病的临床症状出现恶化。在患者对ART产生应答的同时,伴随过度炎症反应,结核病病情加重及病灶扩大或新出现病灶。②这种临床症状加重与新的机会性感染、HIV相关性肿瘤、药物不良反应、耐药或治疗失败无关。③ ART后HIV载量下降和(或)CD4+T淋巴细胞计数增加。
治疗矛盾型TB-IRIS通常具有自限性,对于轻度的IRIS可使用非甾体类解热镇痛药物如布洛芬进行治疗,无需调整抗病毒和抗结核治疗方案,对于出现化脓性淋巴结炎或脓肿的患者可能需要穿刺排脓。对症状明显的TB-IRIS,可使用糖皮质激素进行治疗[1]:①使用含利福平的抗结核治疗方案者,可使用泼尼松1.5 mg/(kg·d)治疗2周,后0.75 mg/(kg·d)治疗2周;②使用含利福布汀和增强型PI的治疗方案者,可使用泼尼松1.0 mg/(kg·d)治疗2周,后0.5 mg/(kg·d)治疗2周。对于暴露型TB-IRIS应进行标准的抗结核治疗,症状严重危及生命者,可考虑加用糖皮质激素治疗。
HIV感染/AIDS患者出现TB-IRIS可使病情加重甚至死亡,尽管抗结核治疗与启动ART之间的时间间隔是发生TB-IRIS的影响因素,但近年来研究表明,早期ART有助于降低病死率,因此,除结核性脑膜炎外,对于HIV感染/AIDS合并结核病患者均主张尽早接受ART[1]。研究显示,对于出现治疗矛盾型TB-IRIS风险高的患者(CD4+T淋巴细胞计数低尤其<100/μL、抗结核治疗后30 d内启动ART、对抗结核治疗应答良好、对利福平敏感、无卡波西肉瘤、无活动性乙型肝炎),在启动ART的同时使用糖皮质激素(泼尼松40 mg/d治疗2周后改用20 mg/d治疗2周)有助于降低TB-IRIS的发生率[46]。基于这项研究,对于出现治疗矛盾型TB-IRIS风险高的患者,可考虑预防性使用糖皮质激素[1]。然而,这方面尚需积累更多证据,临床实践中不建议常规实施。
合并感染人群的治疗涉及抗结核和抗HIV治疗,药物的不良反应可能会叠加,尤其是在治疗耐药结核病时,药物的不良反应相对多见;药物之间的相互作用可能会导致合用时某些药物的血药浓度增加而致使药物不良反应增加。治疗过程中要密切监测药物的不良反应。抗结核治疗过程中不良反应常见,由于同时服用抗HIV药物及其他治疗/预防机会性感染的药物,通常很难明确引起不良反应的具体药物,一线抗结核药物不可随意停用或换成二线药物,而应首先对症处理后密切观察,再根据情况调整。
胃肠道反应在抗结核和抗病毒药物中最为常见。如果出现胃肠道反应,应检测肝功能,注意氨基转移酶及胆红素变化。如果胃肠道反应并非由肝损伤所致,则通常无需调整治疗,继续观察和支持对症处理,必要时可给予抗酸制剂治疗,或改变服药时间及随餐服用。
利福平和吡嗪酰胺的胃肠道反应比较多见,部分患者反应较重,但不可随意停用;一旦停用,抗结核疗效会受到很大影响。给予对症处理后,大部分患者胃肠道反应能逐渐缓解。
皮疹在抗结核药物中也较为常见。如果皮疹轻微,可继续抗结核并予以抗过敏等对症治疗。如果皮疹严重,所有抗结核药物均需暂时停用,直至皮疹明显缓解。重新加用抗结核药物时应遵循一定的策略:逐一添加,且彼此间间隔2~3 d。首先加用利福平或利福布汀,依次加用异烟肼、乙胺丁醇或吡嗪酰胺;如果皮疹再发,最后加用的药物应立即停用。如果瘀点、瘀斑性皮疹考虑是由血小板减少所致,则应永久性停用利福平或利福布汀。如果皮疹伴有发热或黏膜受累,所有药物需要立即中止,患者原抗结核方案更换为替代用药组合。
HIV感染/AIDS合并结核病患者接受数周抗结核治疗后仍有发热时,原因可能为:药物热、合并其他病原体感染及IRIS。抗结核药物致发热时,患者尽管高热,但仍可感觉良好;患者发热常无特殊规律,也不一定存在嗜酸性粒细胞升高。如果能够排除其他病原体感染和结核加重或IRIS可能,则应停用所有抗结核药物。发热缓解后,应重启抗结核治疗,重启的策略与抗结核药物致皮疹后重启抗结核治疗策略相同。
抗结核治疗过程中出现的肝损伤多数是由抗结核药物所致,利福平、吡嗪酰胺和异烟肼均可引起肝损伤,但需注意抗病毒药物和磺胺类药物也可致肝损伤,并排除合并病毒性肝炎、脂肪肝等基础性肝病,以及存在饮酒或服用其他可致肝损伤的药物等引起肝损伤的情况。在启动抗结核治疗之前应常规检测肝功能和病毒性肝炎相关标志物。
如ALT水平<3倍正常值上限(upper limit of normal,ULN),可继续严密观察而不更改抗结核方案。发生以下情况应停用可致肝损伤的药物,并严密评估患者状况:ALT>5×ULN,ALT≥3×ULN并伴随肝损伤的临床表现,胆红素>2×ULN。停用致肝损伤的抗结核药物后,应在密切观察下改用3种以上无肝损伤的抗结核药物进行治疗。ALT恢复至<2×ULN时,应逐一重启因肝损伤而停用的抗结核药物,先试用利福平,1周后肝损伤若无加重,加用异烟肼,1周后肝损伤仍无加重,再加用吡嗪酰胺。若出现肝损伤的临床表现或ALT升高,则停用最后加用的药物。在重启抗结核药物的过程中,利福平、异烟肼和吡嗪酰胺可从小剂量逐渐增加至治疗剂量。
NRTI类抗HIV药物如齐多夫定,以及抗结核药物如利奈唑胺、异烟肼、环丝氨酸、链霉素、卷曲霉素、阿米卡星、乙(丙)硫异烟胺和氟喹诺酮类药物均可引起周围神经病变,合用后不良反应增加[47]。周围神经病变多发生在下肢,以四肢末梢特别是双足为重。处理建议:①如有可能,避免上述药物的同时联合使用,必须应用时选择毒性较小的药物;②在使用上述药物时,联合使用维生素B6;③对于麻痛等感觉症状明显者,可应用三环类抗抑郁药物或抗惊厥药物如阿米替林、卡马西平或加巴喷丁;④与利奈唑胺相关的神经炎常发生在后续使用阶段,且症状常持久,一旦发生可减量至300 mg/d,如症状无改善或进一步加重应考虑停用利奈唑胺[37,47]。
抗HIV药物如依非韦伦,以及抗结核药物如环丝氨酸、异烟肼、乙(丙)硫异烟胺和氟喹诺酮类药物均可导致头痛、癫痫、抑郁、失眠、异梦等神经精神症状。处理建议如下:①症状轻者可给予对症处理。②对于环丝氨酸相关不良反应而言,轻度精神症状可减少环丝氨酸用量或停药,起始使用低剂量环丝氨酸(250~500 mg/d)可减轻治疗初期的头痛症状,剂量在1~2周内逐渐增加至足量或适量;推荐每服用250 mg环丝氨酸予以50 mg维生素B6口服以预防其神经不良反应。③心理支持治疗,抑郁症状明显时尽早给予抗抑郁治疗,精神症状明显的给予抗精神病治疗。④降低可疑药物的用量或停用/更换可疑药物[38]。
抗HIV药物如依非韦伦和洛匹那韦/利托那韦、氟喹诺酮类抗结核药物、贝达喹啉、德拉马尼及氯法齐明均可导致Q-T间期延长,Q-T间期超过500 ms的患者发生室性心律失常的风险明显增加[48]。处理建议:①使用氟喹诺酮类药物时应尽可能避免同时使用可能延长Q-T间期的药物,有Q-T间期延长病史的患者通常应避免使用这类药物;②密切监测心电图变化,经反复心电图检查确认Q-T间期超过500 ms或延长超过60 ms时应停用贝达喹啉及其他相关药物;③监测血钾、血钙和血镁水平,建议保持血钾水平高于4 mmol/L,血镁水平高于0.74 mmol/L[38,48]。
执笔专家:沈银忠[上海市(复旦大学附属)公共卫生临床中心感染与免疫科]、卢洪洲[南方科技大学第二附属医院(深圳市第三人民医院)]、陈耀凯(重庆市公共卫生医疗救治中心感染科)、王辉[南方科技大学第二附属医院(深圳市第三人民医院)感染一科]、戈宝学(同济大学附属上海市肺科医院结核病实验室)、马萍[天津市(南开大学附属)第二人民医院感染二科]、刘莉[上海市(复旦大学附属)公共卫生临床中心感染与免疫科]、陈雅红(福建医科大学孟超肝胆医院感染科)、代丽丽(首都医科大学附属北京佑安医院性病艾滋病门诊)、邓爱花(江西省胸科医院内五科)、高勇(中国科学技术大学附属第一医院暨安徽省立医院感染病院)、韩宁(首都医科大学附属北京地坛医院感染一科)、何浩岚(广州医科大学附属市八医院感染科)、蒙志好(广西壮族自治区胸科医院感染科)、阮连国(武汉市金银潭医院感染科)、孙燕(郑州市第六人民医院感染科)、汪习成(云南省传染病医院艾滋病关爱中心)、王晖(上海市交通大学医学院附属瑞金医院感染科)、谢志满(南宁市第四人民医院感染科)、辛晓丽(沈阳市第六人民医院感染三科)、袁子清(阜阳市第二人民医院感染一科)、张仁芳[上海市(复旦大学附属)公共卫生临床中心感染与免疫科]、周锐峰(成都市公共卫生临床医疗中心感染科)、周泱[南方科技大学第二附属医院(深圳市第三人民医院)感染一科]、冯萍(四川大学华西医院感染性疾病中心)、陈晓红(哈尔滨医科大学附属第四医院感染三病房)、沙巍(同济大学附属上海市肺科医院结核病临床研究中心)、岳建军(山西医科大学附属肺科医院太原市第四人民医院感染科)、张云桂(云南省传染病医院结核科)
参与共识制订的专家(按姓氏笔画排序):丁海波(中国医科大学附属第一医院国家卫健委艾滋病免疫学重点实验室)、王立静(石家庄市第五医院感染十科)、王汝刚(大连市公共卫生临床中心感染科)、王其亮(安徽省濉溪县医院感染科)、王福祥[南方科技大学第二附属医院(深圳市第三人民医院)感染三科]、龙海(贵阳市公共卫生救治中心感染科)、叶珺(安徽医科大学第二附属医院感染病科)、叶富秀(伊宁市第二人民医院关爱中心)、地里下提·阿不力孜(新疆医科大学第八附属医院骨科)、成娟(盐城市第二人民医院感染科)、师金川(杭州市西溪医院感染二科)、吕建楠(广西壮族自治区胸科医院艾防中心)、朱大庆(赣州市第五人民医院感染科)、乔英(呼和浩特市第二医院感染科)、刘波(鞍山市传染病医院感染科)、刘曦(中山大学附属第五医院感染病防治中心)、刘凤君(川北医学院附属医院感染科)、刘春礼(郑州市第六人民医院感染科)、安晓渊(遵义市第四人民医院感染科)、苏菲菲(温州市中心医院感染科)、李鑫(首都医科大学附属北京地坛医院感染科)、李重熙(昆明市第三人民医院感染一科)、李雪梅(大庆市第二医院感染科)、杨涤(首都医科大学附属北京地坛医院感染一科)、杨正贵(宁夏回族自治区第四人民医院行政办公室)、杨学刚(保定市人民医院感染科)、杨宗兴(杭州市西溪医院感染二科)、邹美银(南通市第三人民医院感染科)、汪美华(南通市第三人民医院感染科)、宋波(哈尔滨医科大学附属第四医院感染科)、张瑛(辽宁省朝阳市第四医院胸外科)、张强(首都医科大学附属北京地坛医院骨科)、张凤池(徐州市传染病医院感染科)、张玉林(首都医科大学附属北京佑安医院呼吸与重症医学科)、张海晴(徐州市传染病医院结核二科)、张培泽[南方科技大学第二附属医院(深圳市第三人民医院)肺二科]、陈仁芳(无锡市第五人民医院感染与免疫科)、陈礼运(芜湖市第三人民医院感染科)、陈国春(常州市第三人民医院感染一科)、陈绛青(南昌市第九医院感染二科)、欧勤芳(无锡市第五人民医院结核科)、周宇(温州医科大学附属第三医院感染科)、周华英(中南大学湘雅二医院感染科)、周国强(长沙市第一医院感染与免疫科)、秦大为(黔东南州人民医院传染病院)、钱峰(苏州市第五人民医院感染科)、侯明杰(郑州市第六人民医院感染一科)、徐玉敏(上海交通大学医学院附属瑞金医院院感科)、曹晓英(郴州市第二人民医院感染科)、曹婉娴(中国科学技术大学附属第一医院暨安徽省立医院感染病院七病区)、韩军(无锡市第五人民医院感染与免疫科)、谢敬东(上海交通大学医学院附属瑞金医院感染科)、靳娟(西安市第八医院抗病毒门诊)、蓝珂(广西壮族自治区胸科医院感染科二病区)、窦艳云(广西壮族自治区胸科医院感染科二病区)、蔡琳(成都市公共卫生临床医疗中心感染二科)、熊玉红(江西省胸科医院内五科)、潘松南(黑龙江省传染病防治院感染科)、薛秀兰(厦门大学附属第一医院感染科)
参与讨论专家:肖和平(同济大学附属上海市肺科医院)、初乃惠(首都医科大学附属北京胸科医院)、邓国防[南方科技大学第二附属医院(深圳市第三人民医院)肺病二科]、周琳[广东省人民医院(广东省医学科学院)]、陈亮(广东省结核病控制中心)、赵清霞(河南省传染病医院感染科)、刘水青(贵阳市公共卫生临床中心感染一科)、王敏(长沙市第一医院感染病中心)、朱彪(浙江大学医学院附属第一医院感染科)、陈军[上海市(复旦大学附属)公共卫生临床中心感染与免疫科]、何盛华(成都市公共卫生临床医疗中心感染一科)
所有作者均声明不存在利益冲突