
本文报道1例重症溃疡性结肠炎(SUC)患者,在除外机会性感染的基础上,激素治疗无效并发肠穿孔,最终行外科急诊手术治疗。术后经多学科团队(MDT)讨论,以肠内营养支持治疗为主,辅助直肠抗炎治疗,择期行回肠储袋肛管吻合术,患者获得较好的生活质量。通过病例分析结合文献学习,探讨SUC的MDT诊治策略。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
患者男性,47岁,教师,因"腹胀1个月,腹泻伴黏液脓血便20 d,口腔溃疡2周"入院。患者于2020年3月无明显诱因(追问病史有进食海鲜史)出现腹胀,无腹痛、腹泻、恶心、呕吐、纳差等症状,自行口服中成药1周后出现腹泻,伴黏液脓血便,3 ~ 5次/d,2周前出现反复的多发口腔溃疡。4 d前就诊于当地医院,体温最高达38.5℃,肠镜检查示结直肠黏膜弥漫性出血,表面坏死,附着黏液,诊断为溃疡性结肠炎(ulcerative colitis,UC),对症治疗后症状无明显变化,为求进一步治疗入我院。发病以来,患者体质量下降2 kg。患者既往体健,否认过敏史、传染病史、慢性病史和手术史。
体格检查:体温36.5℃,心率88次/min,呼吸19次/min,血压114/76 mmHg(1 mmHg = 0.133 kPa),患者体质量指数为26.1 kg/m2。腹软,全腹无压痛、反跳痛,肝脾肋下未触及,无移动性浊音,肠鸣音正常,双下肢无水肿。
实验室检查:白细胞计数12.9 × 109/L,中性粒细胞百分比85.7%,血红蛋白105 g/L,血小板计数560 × 109/L。大便含大量红细胞、白细胞,潜血阳性。白蛋白35.8 g/L。红细胞沉降率(erythrocyte sedimentation rate,ESR)40 mm/1 h。白细胞介素(interleukin,IL)-6为59.66 pg/ml,降钙素原0.156 ng/ml,C-反应蛋白(C-reactive protein,CRP)23.3 mg/L。EB病毒含量2.86×103拷贝/ml,血清人类巨细胞病毒(cytomegalovirus,CMV)<1.0 × 103拷贝/ml。肿瘤指标均为阴性。多次便培养、血培养、结核杆菌T淋巴细胞酶联免疫斑点试验(T-spot.TB)均为阴性。
肠镜:回盲部及升结肠未见明显异常,横结肠肝曲至直肠可见黏膜血管纹理消失,呈颗粒样改变,散在点片状红斑及糜烂,降结肠为重,黏膜凹凸不平。内镜诊断为UC(E3广泛结肠型),内镜下Mayo评分2分(图1)。
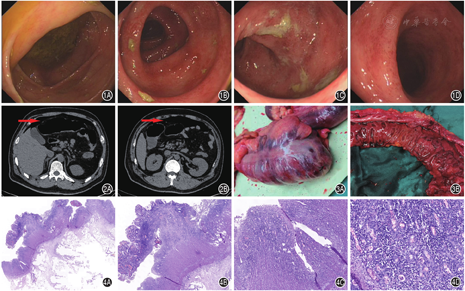

病理提示黏膜伴糜烂,间质内大量急慢性粒细胞浸润,可见隐窝小脓肿形成。
腹盆腔CT:左半结肠肠壁弥漫性增厚,伴周围少量渗出,邻近肠系膜区小血管增多并多发小淋巴结,考虑炎症性肠病。
入院后患者持续排黏液脓血便,6 ~ 10次/d,总量约500 ml/d,血占比约30%;每天热峰为38.5 ~ 39℃。参照改良Truelove和Witts评分,考虑中至重度UC。治疗上,给予美沙拉嗪肠溶片(4 g/d)口服和美沙拉嗪灌肠液(4 g/d),嘱患者少渣饮食,给予肠内营养乳剂(1000 ml/d)支持对症治疗。治疗7 d后,患者症状及实验室指标未见明显变化,而腹痛进行性加重,经专科讨论后升阶梯治疗,给予静脉输注甲强龙(60 mg/d)治疗。
患者在静脉激素治疗期间,症状及实验室指标等依然无改善,腹痛呈进行性加重,最高体温隔日波动于正常及高热之间。第7天查腹部X线立位平片:双膈下未见游离气体影。继续治疗第8天,考虑患者病情反复,腹痛逐渐加重,拟给予环孢素3 mg/(kg·d)或英夫利西单克隆抗体(简称单抗)转化治疗,但患者当天出现剧烈腹痛。查体:腹肌紧张,全腹压痛及反跳痛,肠鸣音弱。急诊腹部CT:考虑肠道穿孔,并腹腔积气,腹盆腔积液,回盲部结构显示不清,右半结肠扩张积气、积液,结肠扩张直径5 ~ 6 cm,未提示中毒性巨结肠(图2)。胃肠外科专科讨论后,立即行剖腹探查术+全结肠切除术+部分回肠切除术+回肠造瘘术。
术后大体病理提示回盲部穿孔,全结肠呈穿凿样改变,黏膜大片脱落,部分区域残存黏膜孤岛(图3);镜下病理结果提示结肠部分区域黏膜糜烂、缺失,伴炎性渗出、坏死,大部分区域黏膜及黏膜下层血管高度充血、水肿,伴大量中性粒细胞、淋巴细胞、浆细胞浸润,伴隐窝脓肿形成,局灶炎细胞浸润至固有肌层及浆膜层,残存黏膜局灶腺上皮伴轻度非典型增生(图4)。结合临床及病理,考虑诊断为重症溃疡性结肠炎(severe ulcerative colitis,SUC)。术后患者以营养支持为主,激素逐渐减量,生命体征、血便及腹痛症状逐渐好转。
普通外科:患者以腹胀、腹泻伴黏液脓血便起病,内科保守治疗无效,因腹腔穿孔行手术治疗。目前患者考虑为SUC,术前系全结肠病变,降结肠及乙状结肠病变较重,由于入院前后患者采用药物灌肠治疗,直肠病变相对较轻,术前讨论保留直肠。术后患者残留10 cm直肠,可能出现残留直肠的持续性炎症、残端开裂、术后肠系膜纤维化挛缩等严重并发症,建议暂不考虑行进一步手术治疗。待患者病情稳定后可考虑行直肠切除+回肠储袋肛管吻合(ileal pouch-anal anastomosis,IPAA),但也要重视术后储袋炎、储袋吻合口瘘等并发症。
病理科:结合内镜检查及手术切除后获取的肠道组织进行分析,患者术后结肠组织病理提示大部分黏膜缺损,形成深达固有肌层的溃疡,溃疡面可见大量炎性渗出,炎性肉芽组织形成,可见幼稚的新生毛细血管,纤维结缔组织增生,大量中性粒细胞及淋巴细胞、浆细胞浸润,部分区域淋巴组织增生,淋巴滤泡形成,无瘢痕及肉芽肿,可除外克罗恩病,同时提示病程较短,疾病进展迅速。患者抗酸染色阴性,镜下未见巨细胞、核内包涵体、"猫头鹰眼"等改变,暂无感染证据,上述结果大致符合UC的病理表现。
感染病科:从患者的病史、实验室检查、病理分析,仅有血EB病毒拷贝数的轻度增高,无特殊临床意义,没有发现全身播散性感染及肠道感染的证据,但感染作为发病的始动因素,目前无法确定。患者目前诊断SUC。SUC患者常常合并机会性感染,由于受病原学检出条件的限制,临床诊断存在难度。因此,患者术后需密切监测原发病活动,警惕机会性感染的发生。
消化内科:这是1例比较少见且进展迅速的SUC并发穿孔行外科手术的病例。其复杂性首先在于诊断方面,患者病史短,不是典型的UC,病理提示病变并不局限在黏膜层,但综合临床表现、影像及术后病理考虑UC可能性大,反复的口腔溃疡可能对诊断有一定的帮助。其次在合并感染方面,患者是否合并机会性感染,目前无任何有价值临床证据。在转换治疗方面,患者激素使用时间超过1周可考虑转换治疗,《炎症性肠病诊断与治疗的共识意见》指出视病情严重程度和恶化倾向,足量激素使用可适当延迟,但应注意,不恰当的拖延势必大大增加手术的风险。该患者在激素治疗期间,体温隔天正常,隔天高热,提示激素治疗部分有效,但不能完全控制疾病进展。在疾病进展方面,UC的病变大部分局限在黏膜层及黏膜下层,很少发生穿孔,但SUC进展迅速,可能会出现穿孔,患者的穿孔部位和肠镜检查的严重病变部位不一致,考虑患者疾病进展,穿孔可能发生在肠道薄弱或者肝曲、脾曲、回盲部等特殊解剖部位。在是否再次手术方面,考虑目前直肠病变较重,如果进一步手术治疗,溃疡性直肠炎还存在,建议密切随访之后再请胃肠外科会诊。治疗上给予美沙拉嗪栓剂、肠内营养乳剂,择期复查肠镜并随访。
患者术后外院肠道病理会诊结果回报:全结肠+末端回肠病理表现符合UC,结核杆菌抗酸染色阴性,弱抗酸染色阴性,CMV原位杂交(-),EB病毒编码RNA的原位杂交(-)。治疗上继续给予对症治疗,以肠内营养乳剂为主,逐步过度饮食,美沙拉嗪栓剂(0.5 g bid)抗炎治疗,血常规及炎症指标如CRP、IL-6、降钙素原等均恢复正常,患者症状体征较前无明显变化,最终诊断为急性SUC。患者分别于术后3、6个月复查肠镜结果均提示为溃疡性直肠炎。2020年11月,于外院行腹腔镜辅助直肠切除+IPAA+回肠保护性造口术。2021年3月,于外院行小肠袢式造口还纳术。术后各项生命体征平稳,伤口愈合良好,肠内营养联合半流质饮食耐受情况较好。2021年7月行肠镜检查提示:IPAA术后封套炎。目前患者以少渣饮食为主,间断辅助肠内营养乳剂,病情稳定。
UC的诊断及治疗是复杂的临床问题,往往需要具有丰富经验的临床医师和多学科团队(multidisciplinary team,MDT)共同探讨,最终做出正确的判断和处理[1]。特别是急性SUC,属于临床急危重症,常常合并消化道出血、中毒性巨结肠或结肠穿孔,临床抉择棘手,一旦延误治疗良机,疾病可能危及患者生命,因此,审慎及时正确的处理可使患者获益。
UC因缺乏诊断金标准,需要结合病史、实验室检查、内镜、影像学及病理结果后综合判断[2]。特别是进展迅速的SUC,更需要充分利用MDT诊治模式来提高临床诊治能力。该患者急性病程,病情极其凶险,从病程上看,不太符合UC诊断,但从患者的实验室检查、内镜、影像学及病理检查结果拟诊为SUC。根据体温、血红蛋白、ESR等指标,患者结肠切除风险可高达48%[3]。从发病之初就预示着患者存在较高的病残率和病死率。从术后的病史、病理检查及随访来看,患者的诊断最终考虑为急性SUC。
SUC常常合并严重感染,常见的机会性感染包括CMV、艰难梭菌感染等。研究表明,在重症UC患者中,活动性炎症结肠组织CMV阳性率约为30%[4,5]。因住院、抗菌药物或免疫抑制剂的使用以及合并并发症等,UC患者合并艰难梭菌感染的风险较高[6]。特别是SUC合并感染后病情加重,加速疾病进展,因此,对SUC患者应尽快行感染筛查并积极治疗。该患者入院后持续高热,多次便培养、血培养为阴性,从实验室检查、病理及内镜下综合判断,结核、肝炎病毒、CMV、细菌等均无感染依据。从患者术后肠道大体病理提示全结肠布满穿凿样溃疡,提示可能存在特殊感染,但外院病理检测显示无结核、CMV及EB病毒感染证据,考虑到患者病情进展迅速,不能除外因检测手段有限而尚未发现的感染证据。本病例提示我们,UC合并机会性感染难以辨识,特别是病情进展迅速的SUC,更需要警惕机会性感染的可能性。
SUC的治疗需要全面评估病情,根据病情轻重、病变累及范围及患者对药物的反应情况选择个体化、综合性的治疗方案。静脉使用糖皮质激素是SUC的一线治疗方案,但超过30%的患者对激素抵抗,面临药物拯救治疗或外科手术治疗[7]。从该患者的诊治中,我们认识到,对激素治疗有效的评价,不仅仅观察体温、排便频率和血便量,还需参考全身状况、体格检查及血清学指标综合判断。当然,对于激素及各种抗感染治疗后仍然处于高热、病情无任何好转、提示病情可能在进展的这类特殊病例,有必要在短期内增加结肠镜复查。可根据患者情况选择,例如直乙状结肠镜检查的风险相对较低,这样有助于动态判断疾病进展情况。治疗共识提出,如拯救治疗4 ~ 7 d无效,应及时转手术治疗;或在足量激素治疗3 d无效后立即手术治疗[8]。全结直肠切除术是一种根治手段,可去除病变肠段,彻底消除复发和癌变风险。1978年Parks和Nicholls[9]报道了全结直肠切除+IPAA,已成为UC外科治疗的标准手术方式。SUC患者的分期手术策略可采用IPAA三期手术方案(一期结肠次全切除术+回肠造口,二期残余结直肠切除+IPAA+预防性回肠造口,三期造口还纳),通过第一期手术解除患者的主要矛盾和危重状态,再通过后续的两期手术达到根治性切除病变、保持消化道连续性、避免肠造口的治疗目标[7,10]。需要注意的是,首次手术可保留直肠至直肠乙状结肠交界处,甚至保留部分乙状结肠,以利后续手术。该患者经静脉足量使用激素,但病情不断反复,提示激素部分抵抗,症状逐渐加重,出现急性腹膜炎体征,提示肠道穿孔,立即行全结肠+部分回肠切除术+回肠造瘘术,病情平稳后行IPAA两期手术,效果良好。
从该患者的治疗过程,临床医生要深刻认识SUC疾病进展迅猛及复杂多变的特点,严格把握手术指征。应发挥消化内科、感染科、影像科、营养科、胃肠外科等多学科协作优势,结合患者的病史、症状、体征、实验室、影像、内镜及病理等检查,综合判断手术时机,在制定个性化治疗方案时要以关切患者生活质量为导向,审慎进行临床决策[11,12]。
所有作者均声明不存在利益冲突



























