
评价利妥昔单抗(RTX)在难治性肾病综合征患儿中维持缓解的有效性。
回顾性研究。将2018年11月至2020年11月华中科技大学同济医学院附属武汉儿童医院肾内科诊断为难治性肾病综合征的22例患儿纳入研究,予RTX治疗。外周血中CD19+B淋巴细胞≥1%总淋巴细胞者追加1剂RTX(375 mg/m2),每例患儿使用3~4剂,早期停用钙调神经磷酸酶抑制剂(CNI),后续使用霉酚酸酯治疗。采用Kaplan-Meier法对RTX治疗后患儿的蛋白尿无复发率和无频复发肾病综合征或激素依赖肾病综合征发生率进行分析,采用Wilcoxon秩和检验对使用RTX前后的复发次数进行分析。采用秩和检验对RTX治疗前后患儿的体质量指数(BMI)及身高进行比较。
22例患儿中,20例患儿完成治疗方案,1年和2年的蛋白尿无复发生存率分别为85%和40%,CNI停用后复发频率降低。所有患儿BMI及身高在使用RTX治疗前与使用RTX 1年后、2年后比较,差异均有统计学意义(均P<0.05),使用RTX后1、2年比较,差异均无统计学意义(均P>0.05)。
使用RTX在停用激素和其他免疫抑制剂情况下也可有效降低难治性肾病综合征的复发率,同时可使患儿BMI及身高得到明显改善。RTX治疗难治性肾病综合征患儿安全有效。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
原发性肾病综合征(primary nephritic syndrome,PNS)是儿童最常见的肾小球疾病。虽然初始糖皮质激素治疗后,80%~90%的患儿可获完全缓解,但80%~90%的患儿在起病1年内由于激素减量和/或停药后复发,至少20%的儿童表现为频复发肾病综合征(frequently relapse nephritic syndrome,FRNS)和激素依赖肾病综合征(steroid-dependent nephrotic syndrome,SDNS),这些儿童有很高的终末期肾衰竭风险[1]。
对儿童FRNS/SDNS的标准治疗方法为免疫抑制剂治疗,包括环磷酰胺、钙调神经磷酸酶抑制剂(calcineurin inhibitor,CNI)(环孢素、他克莫司)和霉酚酸酯(Mycophenolate mofetil,MMF)[2]。尽管这些治疗有效,但这些治疗需长期使用激素及免疫抑制剂,且存在治疗时和治疗后蛋白尿反复复发的患儿症状,称为难治性肾病综合征[3]。因此,迫切需要一种不含类固醇或免疫抑制剂的新疗法。
利妥昔单抗(Rituximab,RTX)被证实在难治性肾病综合征患儿中可取得疗效[4,5],且2021年肾脏疾病:改善全球预后(Kidney Disease:Improving Global Outcomes,KDIGO)指南[6]指出,在儿童难治性肾病综合征患儿中使用RTX可作为一种治疗选择。然而,RTX的有效性、安全性及治疗周期目前尚不明确。因此,本研究对RTX治疗儿童难治性肾病综合征的疗效和安全性进行分析,以期为临床治疗提供参考。
回顾性队列研究。选取2018年11月至2020年11月华中科技大学同济医学院附属武汉儿童医院儿科诊断为复杂性FRNS/SDNS的22例难治性肾病综合征患儿,其中男20例,女2例;年龄(4.02±2.96)岁。22例患儿中,1例患儿监护人拒绝接受随访,1例患儿使用1次RTX后1周内出现复发,监护人要求停用RTX治疗,认为该患儿治疗失败。余20例患儿纳入最终研究。入选标准:(1)患儿在使用RTX前完善肾活检检查(表1);(2)首次使用RTX治疗;(3)RTX治疗前监测CD19+B淋巴细胞>10%;(4)CD4+ T、CD8+ T淋巴细胞计数>200个/μL;(5)RTX治疗后随访至少24个月。本研究已通过医院医学伦理委员会批准(批准文号:2021R138-F01),患儿监护人均知情同意并签署知情同意书。
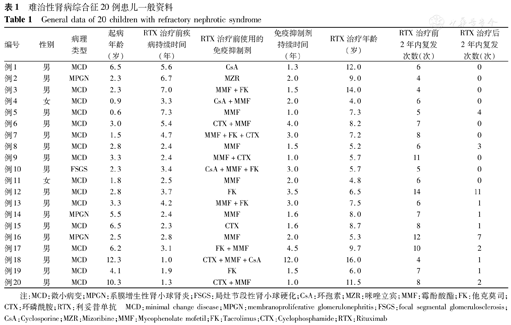
难治性肾病综合征20例患儿一般资料
General data of 20 children with refractory nephrotic syndrome
难治性肾病综合征20例患儿一般资料
General data of 20 children with refractory nephrotic syndrome
| 编号 | 性别 | 病理类型 | 起病年龄(岁) | RTX治疗前疾病持续时间(年) | RTX治疗前使用的免疫抑制剂 | 免疫抑制剂持续时间(年) | RTX治疗年龄(岁) | RTX治疗前2年内复发次数(次) | RTX治疗后2年内复发次数(次) |
|---|---|---|---|---|---|---|---|---|---|
| 例1 | 男 | MCD | 6.5 | 5.6 | CsA | 1.3 | 12.0 | 6 | 0 |
| 例2 | 男 | MPGN | 2.3 | 6.7 | MZR | 2.0 | 9.0 | 4 | 0 |
| 例3 | 男 | MCD | 2.3 | 7.0 | MMF+FK | 1.5 | 14.0 | 4 | 0 |
| 例4 | 女 | MCD | 0.9 | 3.3 | CsA+MMF | 2.0 | 4.0 | 6 | 0 |
| 例5 | 男 | MCD | 0.6 | 7.3 | MMF | 1.0 | 7.3 | 5 | 4 |
| 例6 | 男 | MCD | 3.0 | 5.4 | CTX+MMF | 4.0 | 8.2 | 7 | 0 |
| 例7 | 男 | MCD | 1.5 | 4.7 | MMF+FK+CTX | 3.0 | 7.2 | 8 | 0 |
| 例8 | 男 | MCD | 2.8 | 2.4 | MMF | 1.5 | 5.2 | 6 | 3 |
| 例9 | 男 | MCD | 3.3 | 2.4 | MMF+CTX | 1.0 | 5.7 | 11 | 0 |
| 例10 | 男 | FSGS | 2.3 | 3.4 | CsA+MMF+FK | 3.0 | 5.7 | 5 | 0 |
| 例11 | 女 | MCD | 1.8 | 2.5 | MMF | 2.0 | 4.8 | 6 | 0 |
| 例12 | 男 | MCD | 2.8 | 3.7 | FK | 3.5 | 6.5 | 14 | 11 |
| 例13 | 男 | MCD | 3.3 | 4.2 | MMF+FK | 3.0 | 7.5 | 6 | 1 |
| 例14 | 男 | MPGN | 5.5 | 2.4 | MMF | 1.6 | 8.0 | 7 | 1 |
| 例15 | 男 | MCD | 6.5 | 2.3 | CTX | 1.6 | 8.7 | 8 | 1 |
| 例16 | 男 | MPGN | 2.5 | 2.8 | MMF | 2.0 | 5.3 | 12 | 7 |
| 例17 | 男 | MCD | 6.2 | 3.1 | FK+MMF | 4.5 | 9.7 | 10 | 2 |
| 例18 | 男 | MCD | 12.3 | 1.0 | CTX+MMF+CsA | 12.0 | 16.0 | 4 | 1 |
| 例19 | 男 | MCD | 4.1 | 1.9 | FK | 1.5 | 6.0 | 7 | 1 |
| 例20 | 男 | MCD | 10.3 | 1.3 | CTX+MMF | 1.0 | 11.5 | 8 | 2 |
注:MCD:微小病变;MPGN:系膜增生性肾小球肾炎;FSGS:局灶节段性肾小球硬化;CsA:环孢素;MZR:咪唑立宾;MMF:霉酚酸酯;FK:他克莫司;CTX:环磷酰胺;RTX:利妥昔单抗 MCD:minimal change disease;MPGN:membranoproliferative glomerulonephritis;FSGS:focal segmental glomerulosclerosis;CsA:Cyclosporine;MZR:Mizoribine;MMF:Mycophenolate mofetil;FK:Tacrolimus;CTX:Cyclophosphamide;RTX:Rituximab
符合并满足以下4项标准中的2项及2项以上:(1)严重类固醇依赖,在使用RTX治疗前需大剂量泼尼松[>0.5 mg/(kg·d)]维持;(2)既往接受过2种或2种以上免疫抑制剂治疗;(3)使用CNI治疗超过3年以上;(4)出现类固醇不良反应,如高眼压、白内障和股骨头坏死。
20例患儿中,微小病变(minimal change disease,MCD)16例,系膜增生性肾小球肾炎(membranoproliferative glomerulonephritis,MPGN)3例,局灶节段性肾小球硬化(focal segmental glomerulosclerosis,FSGS)1例。因为只有1例FSGS,所以根据病理类型分为2组:MCD组和MPGN+ FSGS组。
患儿糖皮质激素和/或免疫抑制剂诱导尿蛋白转阴后,予RTX[美罗华(RTX注射液),生产批号:J20170034,生产公司:瑞士罗氏制药公司](每次375 mg/m2,最大剂量每次500 mg,前2剂每周1次,连续2次)治疗,治疗后直接停用MMF,3~6个月中逐渐减停激素及CNI,当外周血中CD19+B淋巴细胞≥1%时,追加1剂RTX,每例患儿使用3~4剂,使用时间及次数见表2,后续当CD19+B淋巴细胞≥1%时,加用MMF维持治疗[600~1 200 mg/(m2·d),分2次],选择使用MMF的时间见表2。
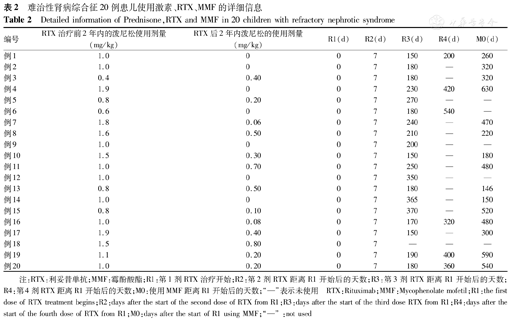
难治性肾病综合征20例患儿使用激素、RTX、MMF的详细信息
Detailed information of Prednisone,RTX and MMF in 20 children with refractory nephrotic syndrome
难治性肾病综合征20例患儿使用激素、RTX、MMF的详细信息
Detailed information of Prednisone,RTX and MMF in 20 children with refractory nephrotic syndrome
| 编号 | RTX治疗前2年内的泼尼松使用剂量(mg/kg) | RTX后2年内泼尼松的使用剂量(mg/kg) | R1(d) | R2(d) | R3(d) | R4(d) | M0(d) |
|---|---|---|---|---|---|---|---|
| 例1 | 1.0 | 0 | 0 | 7 | 150 | 200 | 260 |
| 例2 | 1.0 | 0 | 0 | 7 | 180 | — | 320 |
| 例3 | 0.4 | 0.40 | 0 | 7 | 180 | — | 320 |
| 例4 | 1.9 | 0 | 0 | 7 | 230 | 420 | 630 |
| 例5 | 0.8 | 0.20 | 0 | 7 | 270 | — | — |
| 例6 | 0.6 | 0 | 0 | 7 | 180 | 540 | — |
| 例7 | 1.8 | 0.06 | 0 | 7 | 240 | — | 470 |
| 例8 | 1.6 | 0.50 | 0 | 7 | 210 | — | 220 |
| 例9 | 1.0 | 0 | 0 | 7 | 200 | — | — |
| 例10 | 1.5 | 0.30 | 0 | 7 | 150 | — | 180 |
| 例11 | 1.0 | 0.70 | 0 | 7 | 250 | — | 480 |
| 例12 | 1.0 | 0 | 0 | 7 | 350 | — | — |
| 例13 | 0.8 | 0.50 | 0 | 7 | 180 | — | 146 |
| 例14 | 1.0 | 0 | 0 | 7 | 365 | — | 150 |
| 例15 | 0.8 | 0.10 | 0 | 7 | 370 | — | 520 |
| 例16 | 1.0 | 0.08 | 0 | 7 | 170 | 320 | 480 |
| 例17 | 1.9 | 0.40 | 0 | 7 | 150 | — | 300 |
| 例18 | 1.5 | 0.80 | 0 | 7 | — | — | — |
| 例19 | 1.1 | 0.20 | 0 | 7 | 190 | 400 | 590 |
| 例20 | 1.0 | 0.20 | 0 | 7 | 180 | 360 | 540 |
注:RTX:利妥昔单抗;MMF:霉酚酸酯;R1:第1剂RTX治疗开始;R2:第2剂RTX距离R1开始后的天数;R3:第3剂RTX距离R1开始后的天数;R4:第4剂RTX距离R1开始后的天数;M0:使用MMF距离R1开始后的天数;"—"表示未使用 RTX:Rituximab;MMF:Mycophenolate mofetil;R1:the first dose of RTX treatment begins;R2:days after the start of the second dose of RTX from R1;R3:days after the start of the third dose RTX from R1;R4:days after the start of the fourth dose of RTX from R1;M0:days after the start of R1 using MMF;"—":not used
观察期为第1次使用RTX起随访2年。在首次使用RTX后第1周、第2周、第4周及以后每个月监测1次CD19+细胞数、血分析及肝肾功能,随访期间每个月进行血压、身高、体质量测量。在整个观察期内,患儿自测尿蛋白试纸评估是否复发。若持续3 d尿蛋白3+则认为复发[7],予泼尼松2 mg/kg,最大剂量60 mg/d,继续原来剂量的MMF治疗,糖皮质激素剂量在6个月内逐渐减少,每隔2~4周递减剂量5~10 mg。
(1)使用RTX后蛋白尿无复发率,无FRNS或SDNS发生率;(2)开始使用RTX后2年内的复发次数。
(1)记录外周血CD19+B淋巴细胞耗竭后,首次检测其恢复比例>1%的时间;(2)记录使用RTX前及使用RTX后1年和2年后身高标准差及体质量指数(BMI)变化;(3)评估与RTX相关的不良反应。
应用SPSS 19.0软件进行统计分析。计量资料用 ±s表示。计量资料均行Shapiro-Wilk正态性检验,符合正态分布的使用t检验,否则采用秩和检验。Kaplan-Meier方法用于分析蛋白尿复发率和发生FRNS、SDNS所需的时间;Wilcoxon秩和检验用于开始使用RTX前2年内和开始给药后2年内的复发次数比较,以及用于使用RTX前后患儿的BMI及身高变化比较。P<0.05为差异有统计学意义。
±s表示。计量资料均行Shapiro-Wilk正态性检验,符合正态分布的使用t检验,否则采用秩和检验。Kaplan-Meier方法用于分析蛋白尿复发率和发生FRNS、SDNS所需的时间;Wilcoxon秩和检验用于开始使用RTX前2年内和开始给药后2年内的复发次数比较,以及用于使用RTX前后患儿的BMI及身高变化比较。P<0.05为差异有统计学意义。
患儿一般情况见表1。20例患儿中,RTX治疗前使用过环孢素4例,咪唑立宾1例,MMF 15例,他克莫司7例,环磷酰胺7例。MCD组和MPGN+ FSGS组进行比较,2组RTX治疗前2年内复发次数[(7.25±2.62)次比(7.00±3.56)次]和治疗后2年内复发次数[(1.62±2.78)次比(2.00±3.37)次]差异均无统计学意义(t=0.132、-0.206,均 P>0.05);2组发病年龄[(4.26±3.31)岁比(3.15±1.57)岁]、RTX首次治疗年龄[(8.39±3.43)岁比(7.00±1.79)岁]、治疗前疾病持续时间[(3.63±1.92)年比(3.83±1.96)年]、治疗前免疫抑制剂使用持续时间[(2.78±2.70)年比(2.15±0.60)年]差异均无统计学意义(t=0.975、1.126、-0.178、0.847,均 P>0.05)。
开始使用RTX后,患儿第1年和第2年的尿蛋白无复发率分别为85%和40%。在使用RTX 2年的观察期内,6例患儿诊断为FRNS/SDNS。第1年和第2年无FRNS/SDNS的发生率为85%和70%(图1)。复发率由用药前7.2次/(人·2年)降至用药后的1.7次/(人·2年),虽然随访期间患儿减停激素和/或免疫抑制剂,但复发率仍在降低(图2)。泼尼松的使用平均剂量由用药前的1.1 mg/(kg·人)减至RTX治疗后的0.2 mg/(kg·人)。
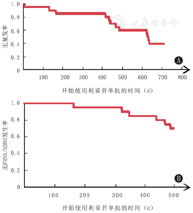

注:FRNS:频复发肾病综合征;SDNS:激素依赖肾病综合征;RTX:利妥昔单抗 FRNS:frequently relapse nephritic syndrome;SDNS:steroid-dependent nephrotic syndrome;RTX:Rituximab
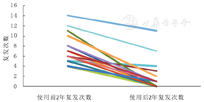

患儿在使用RTX前的外周血CD19的比例为7.08%~23.99%,第1次使用RTX后均有效抑制了B淋巴细胞功能(CD19比例<1%)。使用RTX后外周血CD19+ B淋巴细胞比例恢复≥1%的中位时间为180 d(图3)。
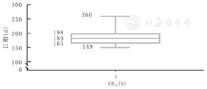

患儿的BMI及身高在使用RTX治疗前和使用RTX 1年后比较以及使用RTX治疗前和使用RTX 2年后比较,差异均有统计学意义(均 P<0.05)。患儿BMI及身高变化在RTX用药1年后和RTX用药2年后比较,可观察到改善趋势,但差异均无统计学意义(均 P>0.05)(图4)。


在使用RTX后有3例出现不良反应,其中2例系胃肠道反应,表现为恶心、呕吐;1例系过敏反应,表现为面部出现皮疹,及时对症处理后有效控制症状,不需要停药治疗。患儿均未出现严重不良反应。
目前有研究[8,9]报道,RTX治疗后、B细胞恢复时加用MMF进行维持治疗可有效改善尿蛋白复发次数、延长尿蛋白缓解时间,不但很少出现严重不良反应,且MMF治疗可长期耐受。
本研究方案所使用的治疗方案为予RTX(每次375 mg/m2,最大剂量每次500 mg,前2剂每周1次,连续2次)治疗,3~6个月逐渐减停激素及CNI,当外周血中CD19+B淋巴细胞≥1%时追加1剂RTX,每例患儿使用3~4剂,后续使用MMF抑制免疫反应,本研究发现,这种治疗方案可使尿蛋白的无复发率明显升高,即使停用激素和/或免疫抑制剂,复发率也明显下降。同时本研究显示,使用RTX后,由于激素的使用剂量下降,患儿身高及BMI得到明显改善。
Iijima等[10]的临床试验显示,每周使用RTX共4次,1年无复发存活率为29%。Tellier等[11]对18例SDNS患儿使用RTX,首次予1~4剂RTX,观察2年,患儿尿蛋白无复发率为22%。本研究治疗方案显示,患儿1年尿蛋白无复发率为85%,2年为40%,这提示本研究方案具有优势性。
Fujinaga和Hirano[12]对37例激素依赖型肾病综合征患儿进行单次RTX治疗后,患儿CD19+B淋巴细胞在5个月内开始回升。黄建萍等[13]研究发现,使用RTX后的CD19+B淋巴细胞持续低水平的时间为(6.10±0.92)个月。本研究显示RTX后CD19+B淋巴细胞维持<1%的中位时间为180 d。
免疫抑制剂可作为辅助治疗以维持难治性肾病综合征RTX治疗后蛋白尿的缓解。Basu等[14]研究表明,RTX对激素耐药型肾病综合征的疗效还取决于多种因素,即使充分免疫抑制后也可能对治疗结果产生不利影响,这取决于活跃的肾小球数量,B淋巴细胞耗竭或B淋巴细胞恢复并不是维持缓解或复发的唯一标准,MMF的免疫调节在B淋巴细胞恢复后仍有维持缓解的作用。MMF维持治疗可帮助避免重复使用RTX,并可能有助于其更安全的使用。在RTX后使用MMF将治疗失败的风险降低了80%,且耐受性良好[9]。张涛等[15]研究表明,MMF可显著延长尿蛋白持续缓解时间并减少尿蛋白复发次数,并减少严重的RTX相关不良事件。RTX重复给药5次及5次以上的安全性尚待评估,因此不推荐延长重复给药时间,可在B淋巴细胞恢复期间予MMF维持治疗。
本研究患儿均未出现严重不良反应,仅有轻度胃肠道异常及过敏反应,及时对症处理后有效控制了症状。虽然其他研究中发现RTX可直接导致IgG水平下降[16,17],但本研究中患儿在2年观察期内未见明显IgG下降,也未显著增加感染的概率。
本研究的潜在不足为予3~4次RTX治疗在某些患儿中可能过多。10%~20%的患儿使用1次或2次RTX治疗后,可维持多年的长期缓解[16,18]。Takahashi等[19]研究提示,1年内未复发的患儿可能无需额外使用RTX。然而本研究显示,1年无尿蛋白复发率高达85%,而在使用RTX 2年的观察期内,仅6例(30%)患儿诊断为FRNS/SDNS。因此具体的RTX治疗疗程需增加病例数和延长随访时间进行制定。此外,本研究病例数较少,病理类型FSGS仅1例,只能将FSGS合并到MPGN中与MCD进行比较,后续会增加样本量行进一步统计分析。
综上,使用RTX在停用激素和其他免疫抑制剂情况下也可有效降低疾病复发率,同时有效促进患儿更好地生长追赶,RTX治疗对复杂性FRNS/SDNS患儿治疗有效且安全。今后有待进一步扩大样本量,延长随访时间,进一步证实影响RTX治疗效果的相关因素。
所有作者均声明不存在利益冲突



























