
探讨新生儿小肠闭锁围手术期应用加速康复外科管理模式的安全性及有效性。
回顾性分析2016年9月至2020年12月在哈尔滨医科大学附属第二医院行手术治疗的27例小肠闭锁患儿的临床资料。2018年9月至2020年12月收治的13例患儿,围手术期采用加速康复外科管理模式为ERAS组,其中男3例,女10例;患儿手术日龄为2.00(1.00,3.00) d。2016年9月至2018年8月收治的14例患儿,采用传统围手术期处理方案为对照组,其中男7例,女7例;患儿手术日龄为3.00(1.75,3.25) d。比较两组患儿术后肠内营养开始时间、术后首次经口喂养时间、术后首次排气时间、术后首次排便时间、完全静脉营养时间、术后住院时间、术后并发症、非计划二次手术、需二次手术率等方面的差异。符合正态分布且方差齐的计量资料组间差异比较采用t检验,其余计量资料采用非参数Mann-Whitney检验;计数资料组间比较采用Fisher确切概率法。
ERAS组和对照组在术后开始肠内营养的时间[2.0(1.5,2.5) d比6.0(5.0,8.0) d,P<0.0001]、术后首次经口喂养时间[4.0(3.0,5.0) d比9.5(5.0,11.0) d,P=0.0006]、术后首次排气时间[2.0(1.0,2.0) d比2.5(2,3.25) d,P=0.048]、完全静脉营养时间[12.0(8.5,13.0) d比18.0(11.5,21.5) d,P=0.012]、术后住院时间[20.0(11.0,24.5) d比24.5(23.0,27.0) d,P=0.029]显著缩短或提前,差异均有统计学意义。ERAS组术后首次排便时间(3.15±1.63) d比对照组的(4.71±3.10) d有所缩短,但差异无统计学意义。两组患儿在术后相关并发症、非计划二次手术、需二次手术等指标差异无统计学意义。
新生儿小肠闭锁围手术期应用加速康复外科围手术期管理模式是安全可行的,能够有效加速患儿胃肠道功能恢复速度,缩短完全静脉营养时间,缩短患儿术后住院时间,且不增加并发症的发生率,加速患儿的康复进程。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
新生儿小肠闭锁是一种多因素作用导致的消化道连续性中断,是新生儿外科中较常见的消化道畸形,也是新生儿肠梗阻的常见原因[1]。外科手术恢复肠管连续性及保持吻合口肠管通畅是唯一的治疗方式。但患儿术后仍然面临多种并发症,如肠梗阻、吻合口瘘、营养不良和术后长期肠功能恢复不良等,严重影响患儿预后。加速康复外科(enhanced recovery after surgery,ERAS)是指在循证医学的证据基础上,以减少患者心理及生理创伤应激反应为目的,通过外科、麻醉、护理、营养等多学科合作,优化围手术期的处理,减少创伤应激和并发症,促进患者的康复[2]。近年来在成年患者领域的不断实践越来越显示出加速康复外科的优越性,但在小儿外科领域的研究尚处于起步阶段,尤其是在新生儿方面,本研究回顾性分析应用ERAS对先天性肠闭锁患儿围手术期进行管理的临床资料,报告如下。
回顾性分析2016年9月至2020年12月在哈尔滨医科大学附属第二医院行手术治疗的27例小肠闭锁患儿的临床资料。2018年9月至2020年12月收治的13例肠闭锁患儿,围手术期采用加速康复外科管理模式为ERAS组;2016年9月至2018年8月收治的14例患儿,围手术期均采用传统处理方案为对照组。两组患儿手术日龄、性别、孕龄、出生体重等一般资料比较,差异均无统计学意义(P均>0.05),具备可比性(表1)。根据Grosfeld分型标准对先天性小肠闭锁进行分型[3]。两组患儿在肠闭锁位置、肠闭锁病理分型之间相比,差异无统计学意义(P>0.05),具备可比性(表2)。
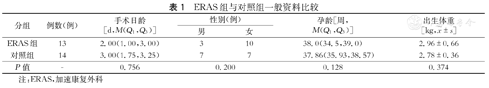
ERAS组与对照组一般资料比较
ERAS组与对照组一般资料比较
| 分组 | 例数(例) | 手术日龄[d,M(Q1,Q3)] | 性别(例) | 孕龄[周,M(Q1,Q3)] | 出生体重[kg, ±s] ±s] | |
|---|---|---|---|---|---|---|
| 男 | 女 | |||||
| ERAS组 | 13 | 2.00(1.00,3.00) | 3 | 10 | 38.0(34.5,39.0) | 2.96±0.66 |
| 对照组 | 14 | 3.00(1.75,3.25) | 7 | 7 | 37.86(35.93,38.57) | 2.78±0.36 |
| P值 | - | 0.756 | 0.200 | 0.128 | 0.374 | |
注:ERAS,加速康复外科
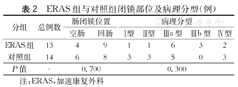
ERAS组与对照组闭锁部位及病理分型(例)
ERAS组与对照组闭锁部位及病理分型(例)
| 分组 | 总例数 | 肠闭锁位置 | 病理分型 | |||||
|---|---|---|---|---|---|---|---|---|
| 空肠 | 回肠 | Ⅰ型 | Ⅱ型 | Ⅲa型 | Ⅲb型 | Ⅳ型 | ||
| ERAS组 | 13 | 4 | 9 | 1 | 1 | 6 | 3 | 2 |
| 对照组 | 14 | 6 | 8 | 3 | 3 | 5 | 0 | 3 |
| P值 | - | 0.700 | 0.300 | |||||
注:ERAS,加速康复外科
患儿术前严重肺部感染、合并其他系统可危及生命的疾病、家属因个人原因中断治疗者均不在本研究范畴内。本研究获得哈尔滨医科大学附属第二医院伦理委员会审核通过(KY2020-255),患儿家长均知情同意。
27例患儿均行手术治疗,ERAS组采用加速康复外科理念进行围手术期的管理,对照组采用传统围手术期处理方式,具体措施见表3。

ERAS组与对照组患儿围手术期管理措施
ERAS组与对照组患儿围手术期管理措施
| 处理措施 | ERAS组 | 对照组 |
|---|---|---|
| 术前 | ||
| 术前宣教 | 术前进行ERAS相关宣教,详尽的告知家长患儿的病情及采用的治疗方案、并发症及预防措施,可能预后等,签订手术知情同意书 | 术前常规宣教,签订手术知情同意书 |
| 禁食及胃肠减压 | 入院后禁食,留置胃管 | 入院后禁食,留置胃管 |
| 预防应用抗菌药物 | 术前0.5~1 h给予预防性用药 | 术前0.5~1 h给予预防性用药 |
| 术中 | ||
| 麻醉方式 | 气管插管全身麻醉 | 气管插管全身麻醉 |
| 手术入路 | 首选经脐小切口 | 经脐小切口或开腹探查口 |
| 手术方式 | 首选一期吻合(肠切除肠端背吻合漏斗样成形) | 肠切除肠端背吻合 |
| 造瘘方式 | 首选悬吊造瘘次选其他造瘘方式 | 悬吊造瘘与其他造瘘(Santulli-blanc或bishop-koop) |
| 术中体温管理 | 加热毯、手术室温度控制等术中全程保温 | 随机室温保温 |
| 术中液体管理 | 控制输液量及速度,用心率、无创血压脉搏检测和尿量调整补液速度及补液量 | 不强调规定术中输液速度及输液量 |
| 术后 | ||
| 胃肠减压 | 引流液较少时尽早拔除 | 引流液较少时拔除 |
| 肠内营养时间 | 术后24~48 h开始肠内营养,经胃管或悬吊造瘘管进行微量喂养,肠管耐受性良好时逐渐增加奶量,并尽早开始经口喂养 | 全量肠外营养,胃肠减压内容物减少,性状为无色胃液后,开始肠内营养 |
| 镇静镇痛 | 术后安慰奶嘴蘸5%葡萄糖液吸吮、音乐疗法等 | 不采取特殊措施 |
| "早期活动" | 鼓励家长术后2~3 d抚摸按摩、逐步怀抱患儿活动 | 卧床休息 |
注:ERAS,加速康复外科
手术入路、手术方式、合并疾病、手术时间、术中出血量、术后肠内营养开始时间、术后首次经口喂养时间、术后首次排气时间、术后首次排便时间、完全静脉营养时间、术后住院时间、并发症发生情况、需二次手术率等临床数据。
患儿一般状态良好,切口愈合良好,无感染及发热;各器官功能良好;能经口喂养满足生理需要量,排便及排气正常;无任何引流管及导管;无其他需要处理的并发症;家属同意回家康复。
应用SPSS 25.0统计学软件处理分析。计量资料若服从正态分布用 ±s表示;若不服从正态分布,用M(Q1,Q3)表示。若两组数据符合正态分布且方差齐,两组间变量差异性检验方法用t检验;若数据不服从正态或者两组间方差不齐,组间比较用非参数Mann-Whitney检验。由于本研究两组总样本量小于40,因此计数资料组间比较所用方法为Fisher确切概率法。P<0.05为差异有统计学意义。
±s表示;若不服从正态分布,用M(Q1,Q3)表示。若两组数据符合正态分布且方差齐,两组间变量差异性检验方法用t检验;若数据不服从正态或者两组间方差不齐,组间比较用非参数Mann-Whitney检验。由于本研究两组总样本量小于40,因此计数资料组间比较所用方法为Fisher确切概率法。P<0.05为差异有统计学意义。
两组患儿在手术入路方面,ERAS组8例行经脐小切口进行手术,与对照组相比差异无统计学意义(P=0.050,表4)。两组患儿在手术方式方面,ERAS组7例选择一期吻合,与对照组相比差异无统计学意义(P=0.300,表4)。
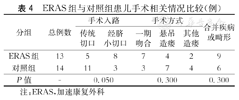
ERAS组与对照组患儿手术相关情况比较(例)
ERAS组与对照组患儿手术相关情况比较(例)
| 分组 | 总例数 | 手术入路 | 手术方式 | 合并疾病或畸形 | |||
|---|---|---|---|---|---|---|---|
| 传统切口 | 经脐小切口 | 一期吻合 | 悬吊造瘘 | 其他造瘘 | |||
| ERAS组 | 13 | 5 | 8 | 7 | 4 | 2 | 9 |
| 对照组 | 14 | 11 | 3 | 3 | 7 | 4 | 6 |
| P值 | - | 0.050 | 0.300 | 0.300 | |||
注:ERAS,加速康复外科
两组患儿在合并其他畸形或疾病方面,ERAS组中9例,对照组中6例合并其他畸形或疾病,主要包括胎粪性腹膜炎、肠扭转、空肠异位胰腺、脐肠瘘、先天性肠旋转不良、梅克尔憩室。两组合并疾病或畸形相比,差异无统计学意义(P=0.300,表4)。
两组患儿术后开始肠内营养时间、术后首次经口喂养时售后首次排气时间、完全静脉营养时间、术后住院时间,ERAS组优于对照组,差异均有统计学意义;两组患儿手术时间、术中出血量、术后首次排便时间相比,差异无统计学意义(表5)。
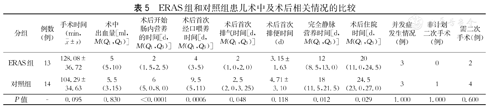
ERAS组和对照组患儿术中及术后相关情况的比较
ERAS组和对照组患儿术中及术后相关情况的比较
| 分组 | 例数(例) | 手术时间(min, ±s) ±s) | 术中出血量[ml,M(Q1,Q3)] | 术后开始肠内营养的时间[d,M(Q1,Q3)] | 术后首次经口喂养时间[d,M(Q1,Q3)] | 术后首次排气时间[d,M(Q1,Q3)] | 术后首次排便时间(d) | 完全静脉营养时间[d,M(Q1,Q3)] | 术后住院时间[d,M(Q1,Q3)] | 并发症发生情况(例) | 非计划二次手术(例) | 需二次手术(例) |
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ERAS组 | 13 | 128.08±36.72 | 5(5,10) | 2(1.5,2.5) | 4(3,5) | 2(1.0,2.0) | 3.15±1.63 | 12(8.5,13.0) | 20(11.0,24.5) | 3 | 0 | 2 |
| 对照组 | 14 | 104.29±34.63 | 5.5(3,15) | 6(5.0,8.0) | 9.5(5,11) | 2.5(2.0,3.25) | 4.71±3.10 | 18(11.5,21.5) | 24.5(23.0,27.0) | 3 | 1 | 4 |
| P值 | - | 0.095 | 0.830 | <0.0001 | 0.0006 | 0.048 | 0.118 | 0.012 | 0.029 | 1.000 | 1.000 | 0.600 |
两组患儿并发症发生情况、非计划二次手术、因造瘘需二次手术相比,差异均无统计学意义(表5)。ERAS组患儿有3例发生术后并发症,分别为切口感染(1例),术后肠梗阻(1例,经保守治疗后好转),新生儿坏死性小肠结肠炎(1例,经保守治疗后好转);对照组患儿有3例发生术后并发症,分别为切口裂开(1例),吻合口瘘(1例,经二次手术黎氏管引流后好转)和术后肠梗阻(1例,经保守治疗后好转)。对照组中1例患儿因并发症行二次手术治疗,预计ERAS组中2例、对照组中4例因造瘘手术需行二次闭瘘术。
术后康复是一个复杂过程,可受到手术创伤大小、应激与代谢反应强弱、各种导管的留置、术后疼痛和进食情况等多方面因素的影响。ERAS的最终目的正是在于减轻手术应激创伤、减轻术后并发症,促进患儿康复。ERAS理念在国内尚处于不断完善与发展过程中,中国ERAS相关专家组2018年发布《加速康复外科中国专家共识及路径管理指南》[4],并相继发布在结直肠、胃手术、肝胆手术、胰十二指肠等领域的专家共识,用于指导国内ERAS的相关临床研究和应用,使其更加规范、标准,但目前主要多应用于成人外科领域。
儿童尤其是婴幼儿及新生儿是一个特殊的群体,其往往面对更为复杂的围手术期应激,因此合理优化围手术期处理措施更加重要和迫切。重要的是,小儿ERAS研究不可完全搬用成人ERAS的成功经验,还需结合小儿自身特征和疾病的特殊性[5]。Reisman等[6]通过前瞻性研究初步证明了ERAS理念在小儿腹部、胸部、泌尿等常规手术中是安全有效的。近年来,国内在胆道闭锁、巨结肠、先天性肠旋转不良、胆总管囊肿手术的ERAS研究中发现ERAS可加快患儿术后康复时间,具有住院时间短、住院费用少的优点,且不增加术后并发症[7,8,9]。欧洲ERAS协会于2020年5月首次发布了《新生儿肠道手术围手术期监护共识指南》[10],该指南针对新生儿肠切除手术提供17条ERAS建议,内容包括术式选择、预防性应用抗生素、防止术中体温过低、围手术期液体管理、镇痛、最优血红蛋白阈值、围手术期沟通、家长的参与、术后早期营养护理和肠液回输10个方面。但是,其中某些支持建议的证据处于较低或中等的质量,如何应用于临床尚需进一步的探讨[11]。总之,目前小儿外科领域在ERAS方面的研究尚处于起步阶段,应该在结合患儿疾病特点,在优化围手术期处理措施的基础上,进行更多前瞻性、多中心、大样本的高质量临床研究,进一步推动ERAS在小儿外科领域的发展。本研究应用ERAS理念对新生儿肠闭锁患儿围手术期的处理模式进行优化,以期促进患儿胃肠功能恢复,加速患儿的康复过程。
相比于成人,新生儿有其独特的生理特点,新生儿先天性肠闭锁更有其特殊的疾病特点。肠闭锁手术的目的在于恢复肠管的连续性及保持吻合口的通畅,本团队应用ERAS围手术期处理模式,尽可能减轻手术创伤应激,促进患儿术后肠功能的恢复。本研究中ERAS组的父母通过术前宣教工作,对患儿术前及术后恢复的各阶段情况有更深的了解,有助于减轻家属焦虑情绪,使其更好地配合完成相关诊疗工作。Short等[12]的研究也发现在小儿的治疗过程中,父母具有重要作用,术前沟通有助于父母合理的参与治疗过程,促进患儿康复。缩短术前禁食时间也是ERAS的重要理念之一,但对于肠闭锁患儿,尚不存在此部分内容,对于可疑消化道畸形胎儿(如肠闭锁、食道闭锁等)出生后即需要禁食处理,无需确定术前进食时间。本研究中对于疑似肠闭锁患儿均入院后即予以禁食,并留置胃管进行胃肠减压,防止呕吐导致误吸或吞入空气后使梗阻肠道进一步充气扩张。
手术阶段是肠闭锁患儿整个治疗过程的重要部分。新生儿围手术期的气道管理相比于成人会面临更多困难,这也是麻醉过程重要因素之一[13]。成人ERAS方案中强调全身麻醉或联合硬膜外阻滞,但此方案并不适合于小儿尤其是新生儿,本研究中ERAS组与对照组均采用气管插管全身麻醉,具有便于气道管理、防止呕吐及反流误吸等优点,也是危急、重大手术患儿的首选麻醉方案。新生儿体温的管理可直接影响手术及麻醉复苏,影响患儿术后恢复进程,这是由于新生儿术中自身体温调节能力不足、麻醉药物对体温调节中枢的抑制、手术消毒过程带走较多热量、身体范围暴露过多等原因易发生低体温。术中低体温可增加切口感染及心脏不良事件发生率,还可导致儿童代谢紊乱、硬肿等并发症[14]。本研究中患儿手术中将其置于加热毯,四肢用柔软的棉花卷包裹,头部盖上小布块等方法全程术中保温,监测核心体温不低于36℃,同时腹部消毒采用温热碘伏溶液进行,并尽可能减少消毒时间。ERAS强调目标导向性液体治疗,肠闭锁患儿中部分为早产或低体重儿,液体管理应更加精准,精准的液体治疗能减少各种并发症。但是中心静脉压、心输出量等目标导向性液体监测指标有具有一定创伤性,小儿尤其新生患儿如何安全应用有待进一步研究[15]。因此,本研究ERAS组采用心率、无创血压脉搏检测和尿量来指导补液,在保证维持血流动力学稳定以保障器官及组织灌注的基础上,不进行盲目或常规补液。
精良的外科技术是ERAS实施的前提,而如何减少手术应激是ERAS理念中的重要问题。手术微创化是外科医生追求的目标之一,新生儿肠闭锁经右上腹部横切口传统开腹手术,不仅具有切口大、术后瘢痕明显的缺点,还常暴露过多小肠,对腹腔干扰重,导致术后肠功能恢复慢[16]。近年来,随着腹腔镜技术的迅速发展,肠闭锁手术逐渐由传统开腹手术转变为腹腔镜辅助治疗,但更多用于治疗十二指肠闭锁或狭窄。新生儿肠管纤细、肠壁薄,对腹腔镜下吻合技术要求高,而且新生儿腹腔空间小,操作困难。所以,腹腔镜下吻合肠管,不适合空回肠闭锁患儿。但是空回肠的系膜相对较长且不固定,加之新生儿腹壁薄而柔软,可向各方向延伸,因此空回肠易于提出腹腔外。经脐周或经脐手术入路可在对前腹壁破坏最小的情况下进入腹腔,将腹腔镜手术微创瘢痕美观的优点与开放暴露直视下手术便于操作的优点结合起来。由于本研究尚处于探索阶段,因此ERAS组及对照组中均存在开腹和经脐手术入路的患儿。ERAS组中患儿更倾向于选择经脐手术入路以减少手术创伤,对于术前怀疑空回肠闭锁的患儿进行经脐手术入路探查,经脐右缘半圆切口入路将肠管提出腹腔外进行手术操作。尤其是对于产前检查即考虑胎儿存消化道畸形,生后消化道造影也高度怀疑空回肠闭锁的患儿,产前产后的一体化治疗使术者更加了解患儿病程变化,更有信心选择经脐手术切口。但是,本研究出于安全性考虑对于胎儿期彩色超声可疑伴发畸形、胎粪性腹膜炎或术前肠闭锁诊断不明确的患儿,仍选择了传统切口。Alemayehu等[17]的研究将经脐手术入路与传统开腹探查比较,并发症并未增加,手术结果类似。经脐手术入路适用于多种疾病及腹部环境(如炎症、粘连、穿孔等),对于早产儿或低体重儿也是安全可行的[18]。需要注意的是,经脐手术入路面临操作困难,如因肠管扩张无法暴露全部肠管或腹部环境复杂时,应及时延长切口。仔细检查远端肠管是否通畅也肠闭锁手术过程是至关重要的步骤。
肠闭锁常见的手术方式分为肠切除一期吻合术或造口的分期手术,其选择常根据患儿的一般状态、肠闭锁位置及病理分型、腹腔内情况及术者的偏好等综合决定。本研究中ERAS组患儿对于非复杂性肠闭锁首选一期吻合术,仅对于复杂性肠闭锁(如Ⅲb型、Ⅳ型或合并复杂性胎粪性腹膜炎等)可选择造瘘术。Margot等[16]比较了肠切除一期吻合术和分期手术对新生儿肠闭锁的疗效,发现一期肠吻合手术的术后并发症发生率均低于分期手术,且住院时间更短。本研究中对于不适合一期吻合的空肠闭锁患儿首选一期肠端侧吻合加悬吊造瘘术,即隧道式造瘘术,使硅胶导管从近端肠管经吻合口插置远端肠管,导管沿纵轴埋入近端扩张的肠管肠壁内,并将造口导管引出腹壁。彭小旅和李权[19]研究发现悬吊造瘘可降低因发生吻合口瘘而导致的死亡率,从而显著提高新生儿肠闭锁的手术治愈率。经悬吊造瘘不仅能降低吻合口压力,还可比肠吻合患儿进行更早期的肠内营养(术后24 h),尤其是适合高位空肠闭锁、远端有足够肠管进行营养吸收的患儿。传统造瘘方式(如Santulli-blanc或bishop-koop造瘘)无法避免患儿需行第2次手术进行闭瘘,而悬吊造瘘一般于术后2周后拔除造瘘管即可,不仅减轻患儿家庭负担,还有利于患儿康复。虽然悬吊造瘘术在一定程度上具有明显优势,但当面临远端具有吸收能力的小肠较短时,不能进行早期肠内营养,这时可能影响肠道的通畅性,而且对于悬吊造瘘的远期并发症问题也有待进一步研究。因此,传统造瘘方式仍具有不可取代的意义。
早期肠内营养是ERAS的核心内容,肠内营养更符合人体生理,长期肠外营养可导致肠黏膜屏障破坏,肠道菌群移位等多种肠外营养相关并发症。2017年欧洲营养学协会关于外科营养指南建议胃肠道术后患儿应早期喂养[20]。早期喂养有利于肠道微生态,减少肠道菌群紊乱移位,促进胃肠道激素分泌,促进胃肠蠕动和功能恢复,还可减少术后腹腔粘连。ERAS理念认为排便不是进食的必然前提,术后早期进食不会增加吻合口瘘的风险,本研究中ERAS组采取术后24~48 h内进行早期喂养,患儿可经胃管鼻饲或经悬吊造瘘管开展早期肠内营养,先给予5%葡萄水1~2 ml/kg,2~3 h一次,并根据耐受情况逐渐加量,且逐渐改为母乳或深度水解奶粉。而对照组按照传统围手术期处理方案,根据肠功能恢复、胃肠减压的情况,一般于术后5~7 d,开始喂养并缓慢加量。张宁等[21]针对早产低体重十二指肠肠梗阻的患儿开展早期肠内营养的研究,结果显示其有助于肠道功能恢复,缩短术后首次排气时间,还可减少静脉营养使用的时间,缩短术后住院时间,且不增加并发症的发生。本研究中ERAS组中术后首次排便较对照组时间差异无统计学意义,可能与患儿早期进食量过少,术中远端肠管内容物已被完全清理或样本量过少有关。
对于术后疼痛管理,婴幼儿尤其是新生儿疼痛调节系统不如成人完善,新生儿感受到术后的疼痛,会限制新生儿的呼吸,从而诱发呼吸系统感染并发症的发生[22]。但目前新生儿镇痛药物如何应用尚无定论。本研究ERAS组中通过安抚奶嘴、抚触、蔗糖水口服、音乐疗法等非药物干预方法,来减少患儿的术后疼痛。术后有效的疼痛管理是早期活动的前提,提倡术后早期活动还可有利于胃肠道蠕动、呼吸系统等多种系统的功能恢复,但由于新生儿活动能力有限,常需外界辅助。本研究中鼓励患儿家属术后2~3 d即可抚摸或按摩患儿,并逐步怀抱患儿活动。
综上所述,ERAS可应用于新生儿小肠闭锁的围手术期管理中,可促进胃肠道功能恢复,促进患儿康复,缩短住院时间。本研究作为单中心研究,病例数较少,具有一定的局限性,推动ERAS在小儿外科甚至是新生儿外科方面的发展,仍需要更多前瞻性、多中心、大样本的高质量研究。但由于新生儿群体及疾病的特殊性,ERAS的实施仍面临多种挑战,建立多学科协作诊疗模式更有益于新生儿ERAS的发展[23]。
所有作者均声明不存在利益冲突



























