
儿童急性呼吸窘迫综合征(PARDS)在儿科重症监护室中较为常见,严重威胁儿童生命健康。PARDS的规范诊断和管理非常重要,临床医师对PARDS认识不足可能会延误诊治,进而疾病进展加重导致不可逆的肺损伤等严重后果。第2届儿童急性肺损伤共识会议(PALICC-2)更新了PARDS的诊断及管理指南。现围绕PALICC-2中有关PARDS的定义、诊断、管理策略等方面进行重点解读,供临床参考,以期提高儿科医师对PARDS的规范诊断及管理水平。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
急性呼吸窘迫综合征(acute respiratory distress syndrome,ARDS)是一种异质性临床综合征,可导致高死亡率和远期致残率[1,2]。2015年儿童急性肺损伤共识会议(Pediatric Acute Lung Injury Consensus Conference,PALICC)首次发布关于儿童急性呼吸窘迫综合征(pediatric acute respiratory distress syndrome,PARDS)的定义,并制定管理指南(以下简称PALICC-1)[3]。然而,各地区对PARDS的诊断和管理存在明显差异,研究发现PALICC-1在各儿童重症监护室(PICU)中的实施情况有所不同,间接导致PARDS更高的死亡率。近年来,随着研究的深入,特别是PARDS的病理生物学、肺保护观念[驱动压力、机械力、自主呼吸相关性肺损伤(patient self-inflicted lung injury,P-SILI)]的更新、新通气技术[经鼻高流量吸氧(high-flow nasal cannula,HFNC)]的临床应用[4,5,6],信息化和临床决策工具的实施;同时考虑到医疗资源受限地区(resource-limited settings,RLS)对指南修订的需求,第2届儿童急性肺损伤共识会议(PALICC-2)更新了PARDS的诊断及管理指南(以下简称PALICC-2)[7,8]。现对新指南的重要部分进行解读。
(1)对年龄做了明确界限,小于18岁的患儿除外围生期肺疾病均适用PALICC-2诊断标准;并声明新生儿同时适用PALICC-2定义或新生儿定义(蒙特勒定义[9]);青少年同时适用PALICC-2定义或成人定义(ARDS柏林定义[1])。
(2)新指南提出新的诊断概念"possible PARDS",暂译为"拟诊PARDS"。当诊断条件不能完全满足PARDS的所有标准但又存在PARDS的可能时,可作出"拟诊PARDS"的诊断,同时强调"拟诊PARDS"应当按照确诊PARDS进行规范化治疗。
(3)PALICC-1关于PARDS风险人群的判定条件:经鼻无创呼吸支持[持续气道正压通气(continuous positive airway pressure,CPAP)/双水平气道正压通气(bilevel positive airway pressure,BiPAP)]时吸入气中的氧体积分数(FiO2)≥ 40%,脉搏血氧饱和度(SpO2)达到88%~97%;PALICC-2关于PARDS风险人群的认定标准为:任何方式的氧气支持尚未达到"拟诊PARDS"或PARDS的标准时,即可认定为PARDS风险人群。氧气支持治疗的新定义:①有创机械通气(invasive mechanical ventilation,IMV)或无创机械通气(noninvasive ventilation,NIV)时满足FiO2>21%;②面罩或鼻导管吸氧时超过以下年龄段的氧流量阈值:<1岁时,氧流量≥2 L/min;1~5岁时,氧流量≥4 L/min;6~10岁时,氧流量≥6 L/min;>10岁时,氧流量≥8 L/min。氧流量计算公式:氧流量=吸氧流速×FiO2。
(4)PALICC-2对接受NIV的患儿诊断PARDS时提出明确要求:①全面罩式的NIV(CPAP/BiPAP),FiO2>21%;②持续气道正压或呼气末正压(positive end-expiratory pressure,PEEP)≥5 cmH2O(1 cmH2O=0.098 kPa),见表1。

PARDS的诊断标准
Diagnosis of PARDS
PARDS的诊断标准
Diagnosis of PARDS
| 年龄 | 0~18岁,除外围生期肺疾病患儿 | |
| 发病时间 | 已知临床损伤出现7 d内发生的低氧症状和胸部影像学改变 | |
| 肺水肿来源 | 不能完全用左心衰竭或液体过负荷解释 | |
| 胸部影像学 | 除外肺不张或胸腔积液导致的单侧或双侧新发的肺实质病变 | |
| FiO2>21%,氧合状态 | 有创机械通气:OI≥4或OSI≥5 | |
| 与疾病严重程度分级 | 无创机械通气(全面罩方式,压力≥5 cmH2O):PaO2/FiO2≤300或SpO2/FiO2≤250 | |
| 初诊PARDS≥4 h后启动严重程度分级 | ||
| 有创机械通气时 | 轻/中度OI<16或OSI<12 | 重度OI≥16或OSI≥12 |
| 无创机械通气时 | 轻/中度PaO2/FiO2>100或SpO2/FiO2>150 | 重度PaO2/ FiO2≤100或SpO2/FiO2≤150 |
| 特殊群体(不适用上述严重程度分级标准) | ||
| 发绀型先天性心脏病 | 符合以上标准,出现不能用心脏疾病解释的急性氧合恶化 | |
| 慢性肺部疾病 | 符合以上标准,出现氧合情况较基线水平急性恶化 | |
注:PARDS:儿童急性呼吸窘迫综合征;FiO2:吸入气中的氧体积分数;OI:氧合指数;OSI:氧饱和度指数;PaO2:动脉血氧分压;SpO2:脉搏血氧饱和度;OI=MAP(cmH2O)×FiO2/PaO2(mmHg);OSI=MAP(cmH2O)×FiO2/SpO2;MAP:平均气道压;1 cmH2O=0.098 kPa PARDS:pediatric acute respiratory distress syndrome;FiO2:fraction of inspiration oxygen;OI:oxygenation index;OSI:oxygenation saturation index;PaO2:partial pressure of oxygen;SpO2:pulse oximeter oxygen saturation;OI=MAP(cmH2O)×FiO2/PaO2(mmHg);OSI=MAP(cmH2O)×FiO2/SpO2;MAP:mean airway pressure;1 cmH2O=0.098 kPa
(5)PALICC-1对使用NIV的PARDS不进行严重程度分级。PALICC-2则指出使用NIV的PARDS也需进行严重程度分级,而且将PARDS的严重程度仅划分为轻/中度和重度两级,同时将分级阈值的界限设定为整数。PALICC-2提出在初诊PARDS至少4 h后启动疾病严重程度分级[10],拟诊PARDS及PARDS风险人群不适用该严重程度分级。部分初诊PARDS的患儿经临床处置后病情会得到改善,因此强调初诊4 h后进行分级能更真实体现疾病严重程度。接受IMV患儿的PARDS诊断和分级标准与PALICC-1区别不大,见表1。评估过程应当确保患儿相对稳定,不应将暂时性氧饱和度降低作为诊断标准;当使用SpO2进行评估时,应确保SpO2≤97%。
(6)PALICC-2新增:HFNC条件下判定"拟诊PARDS"的氧流量阈值为:1.5 L/(kg·min)或≥30 L/min,但HFNC与经鼻NIV模式不能作为诊断PARDS的充分条件,只能作为"拟诊PARDS"的条件。PALICC-2依然强调胸部影像学是诊断PARDS的必要条件,但RLS地区未能完成影像学检查时,只要满足时间、氧合障碍、高风险因素等条件,应被认定为"拟诊PARDS"[8]。
(7)PALICC-2指出当患儿的呼吸衰竭是由于气道阻塞导致时,不能诊断为拟诊PARDS或PARDS风险人群(例如严重的哮喘发作、病毒感染引起的支气管痉挛)。
根据指南原文整理出PALICC-2关于PARDS的诊断标准,见表1。
根据指南原文整理出"拟诊PARDS、PARDS风险人群"的诊断标准,见表2。

拟诊PARDS、PARDS风险人群的诊断标准
Diagnosis of possible PARDS and at-risk for PARDS
拟诊PARDS、PARDS风险人群的诊断标准
Diagnosis of possible PARDS and at-risk for PARDS
| 年龄 | 0~18岁,除外围生期肺疾病患儿 |
| 发病时间 | 已知临床损伤出现7 d内发生的低氧症状和胸部影像学改变 |
| 肺水肿来源 | 不能完全用左心衰竭或液体过负荷解释 |
| 胸部影像学 | 除外肺不张或胸腔积液导致的单侧或双侧新发的肺实质病变 |
| 拟诊PARDS时经鼻氧气支持治疗的阈值 | 经鼻接口的NIV(CPAP/BiPAP,FiO2>21%)或HFNC[≥1.5 L/(kg·min)或≥30 L/min]:PaO2/FiO2≤300或SpO2/FiO2≤250 |
| PARDS风险人群的氧气支持治疗阈值 | 任何方式的氧气支持确保SpO2≥88%,但又达不到确诊PARDS或拟诊PARDS的标准 |
| 特殊群体(不适用PARDS严重程度分级标准) | |
| 发绀型先天性心脏病 | 符合以上标准,出现不能用心脏疾病解释的急性氧合恶化 |
| 慢性肺部疾病 | 符合以上标准,出现氧合情况较基线水平急性恶化 |
注:PARDS:儿童急性呼吸窘迫综合征;NIV:无创机械通气;CPAP:持续气道正压通气;BiPAP:双水平气道正压通气;FiO2:吸入气中的氧体积分数;HFNC:经鼻高流量吸氧;PaO2:动脉血氧分压;SpO2:脉搏血氧饱和度 PARDS:pediatric acute respiratory distress syndrome;NIV:noninvasive ventilation;CPAP:continuous positive airway pressure;BiPAP:bilevel positive airway pressure;FiO2:fraction of inspiration oxygen;HFNC:high-flow nasal cannula;PaO2:partial pressure of oxygen;SpO2:pulse oximeter oxygen saturation
PALICC-2放宽了PARDS的诊断区间,目的是提高临床医师对PARDS的警惕,以便更早进行干预。为方便理清诊断思路,结合指南信息,绘制出PARDS诊断流程图供临床参考,见图1。特殊人群的诊断条件参照表1、表2。
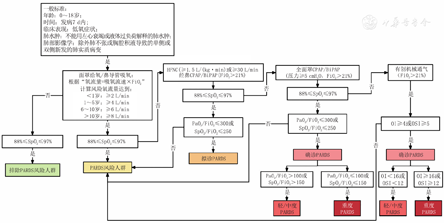

注:PARDS:儿童急性呼吸窘迫综合征;SpO2:脉搏血氧饱和度;HFNC:经鼻高流量吸氧;CPAP:持续气道正压通气;BiPAP:双水平气道正压通气;PaO2:动脉血氧分压;FiO2:吸入气中的氧体积分数;OI:氧合指数;OSI:氧饱和度指数;1 cmH2O=0.098 kPa PARDS:pediatric acute respiratory distress syndrome;SpO2:pulse oximeter oxygen saturation;HFNC:high-flow nasal cannula;CPAP:continuous positive airway pressure;BiPAP:bilevel positive airway pressure;PaO2:partial pressure of oxygen;FiO2:fraction of inspiration O2;OI:oxygenation index;OSI:oxygenation saturation index;1 cmH2O=0.098 kPa
PALICC-2仍建议对PARDS患儿采取肺保护性通气策略,并对潮气量、平台压、驱动压、最佳PEEP、肺复张技术推荐限制范围和操作建议。目的是降低机械通气相关的肺损伤及P-SILI。
(1)PARDS患儿仍建议使用带套囊的气管插管[12],以减少气道压力损失带来的非预计的PEEP降低。
(2)通气模式:PALICC-2仍未对首选的通气模式进行推荐,未来研究需继续评估控制通气与辅助通气模式对疾病预后的影响。PALICC-2对高频振荡通气(high-frequency oscillatory ventilation,HFOV)能否替代常规通气也未进行推荐,仅在常规通气无法达到肺保护性通气策略时可考虑使用。使用HFOV时,需持续监测氧和二氧化碳变化及血流动力学,滴定平均气道压以达到最佳肺容积。
(3)通气压力:PALICC-2指出应在安静状态下测量通气压力,并按照限制范围进行参数设置。建议设置平台压≤28 cmH2O,对于胸壁顺应性降低的患儿可将平台压提高至29~32 cmH2O;建议驱动压限制在15 cmH2O以内。
要求安静状态下根据氧合、氧供、血流动力学状态及呼吸系统顺应性滴定最佳PEEP,PEEP水平通常保持在或高于ARDS网络协作组发布的"低PEEP/高FiO2"表中的范围[13],见表3;这是新指南中唯一作出强推荐的临床建议。滴定最佳PEEP应注意不能超过平台压或驱动压的限制范围。
(4)潮气量:PALICC-2建议PARDS患儿应用6~8 mL/kg(标准体重)的生理潮气量,不建议>8 mL/kg的潮气量。如果为了满足平台压和驱动压限制,建议使用4~6 mL/kg的潮气量,低于4 mL/kg的潮气量应慎重。
(5)肺复张策略:PALICC-2对肺复张策略无明确建议,可尝试缓慢增加或降低PEEP行肺复张,但不建议持续肺膨胀。
拟诊PARDS和PARDS风险人群在使用常规氧疗或HFNC后表现出呼吸衰竭恶化的迹象,暂无明确的气管插管指征时,建议在限定的时间范围(6 h)内尝试NIV,并观察临床变化。应用NIV的患儿在6 h内没有临床改善或出现如呼吸频率增加或心率增快、呼吸做功增加、SpO2/FiO2恶化等征象时,建议进行气管插管。建议对NIV支持的重度PARDS或合并其他严重器官功能障碍的患儿更早进行气管插管。
PARDS患儿使用NIV时应使用压力支持以减少呼吸肌做功。对于年幼儿童,可在确保足够的通气驱动和气道保护反射的条件下,通过采用适当镇静提高全面罩NIV的耐受性。同时强调应在训练有素的工作人员进行密切监测的条件下使用NIV,及时识别病情恶化、处理并发症。
新指南建议轻/中度PARDS维持SpO2在92%~97%。重度PARDS在滴定最佳PEEP后,可以接受SpO2<92%,当SpO2<92%时,建议监测中心静脉血氧饱和度等反映氧供/氧耗的标志物,维持机体氧供氧耗平衡。患儿均应避免SpO2长期暴露于<88%或>97%的水平。
建议在保持推荐的通气压力和潮气量范围内,PARDS患儿可在pH≥7.20的条件下,出现允许性高碳酸血症。应注意允许性高碳酸血症禁忌条件:颅内高压、重度肺动脉高压、特定类型先天性心脏病、血流动力学不稳定和显著的心室功能不全等。
不建议常规使用碳酸氢盐,存在严重的代谢性酸中毒或肺动脉高压对心功能产生不利影响或血流动力学不稳定时,可以考虑补充碳酸氢盐。
不建议在PARDS患儿中常规使用iNO,重度PARDS患儿iNO治疗可作为抢救措施或桥接体外生命支持的桥梁。应用iNO时,应在使用最初4 h内持续进行效果评估,在没有确切效果时应停止iNO。
PALICC-2不建议常规使用肺表面活性物质,仅在特定人群中选择性使用,目前没有足够的证据来指导哪些人群可能获益。不建议常规使用皮质类固醇,对新型冠状病毒(SARS-CoV-2)引起的PARDS患儿使用皮质类固醇可能会获益。
PALICC-2对于其他干预措施无效的PARDS和低氧血症患儿,可考虑使用俯卧位,需评估俯卧位通气时的氧合改善情况,但俯卧位的持续时间并未做出推荐。
进行气管插管的PARDS患儿应保持气道通畅,重度PARDS可考虑应用气管内吸引技术,不建议吸引前常规滴注生理盐水,当为了清除顽固、黏稠的分泌物时,在吸引前可考虑滴注生理盐水。新指南目前尚无法对PARDS患儿进行特定的气道清理方法(如胸部物理治疗和黏液溶解剂)提出建议。对于儿科日益增多的软式支气管镜的应用并未给出相关建议和说明。
PALICC-2建议PARDS患儿应采取滴定最低有效剂量的药物进行镇静。使用有效可靠的疼痛、镇静、谵妄和戒断评分量表进行每日监测。对于镇静时间≥5 d的PARDS患儿,应当评估医源性戒断综合征的风险。
如果单独使用镇静剂无法达到有效的保护性通气目标,建议使用最低有效剂量的NMB联合镇静剂,并进行肌松水平监测。
PALICC-2推荐对所有PARDS患儿最低限度的监测要求包括持续的呼吸频率、心率、血氧饱和度和间歇性无创血压监测。
使用标准体重进行PARDS患儿肺容积(如潮气量、呼吸系统顺应性)估量,若实际体重低于标准体重,则使用较低的体重。推荐有创通气时持续监测潮气量,并进行呼吸回路补偿校准;建议在小婴儿中监测气管插管末端的呼出潮气量,并注意由于流量传感器造成的额外死腔。对于患儿呼吸努力的监测和评估是必要的,及时干预以减轻由跨肺压增大、呼吸钟摆、人机不同步、肺灌注增加等P-SILI。
PALICC-2推荐PARDS患儿接受IMV时,应持续监测二氧化碳,并使用呼气末时间-二氧化碳描记图或容积-二氧化碳描记图。如能获取动脉血二氧化碳分压(PaCO2)和呼气末二氧化碳分压(PETCO2)/混合呼出气二氧化碳分压时,应当计算并监测死腔量。
PALICC-2建议监测呼气末肺泡死腔分数(end tidal alveolar dead space fraction,AVDSF)协助床旁指导疾病的严重程度和风险分层[AVDSF=(PaCO2-PETCO2)/PaCO2][21,22,23,24]。
PALICC-2建议PARDS患儿均应接受血流动力学监测及液体平衡状态监测。建议重度PARDS患儿通过动脉置管持续监测有创动脉压和动脉血气。推荐对怀疑心功能不全或重度PARDS患儿,采用超声心动图检查,以评估左、右心室功能、前负荷状态及肺动脉压力情况。
胸部影像学对于诊断PARDS、发现并发症(如气漏、设备移位)、评估疾病严重程度都是必要的,检查频率应根据患儿的临床状况和可用条件来决定。目前无法对常规使用胸部CT、肺超声检查和电阻抗断层成像技术提出建议,未来需研究可能受益于常规使用这些检查的特定人群。
PALICC-2建议每日评估拔管撤机的可能性,对于符合拔管标准的患儿,应进行标准化自主呼吸试验来测试拔管准备情况。
PALICC-2建议对肺部病变可逆的重度PARDS患儿,当肺保护性通气策略导致气体交换不足时,评估ECMO治疗可能性,尚无证据支持严格的标准用来选择可能获益于ECMO治疗的群体。建立ECMO的决议应当基于一个成熟的专家团队对病史、临床状态进行连续的系统化评估。当使用最佳的非ECMO治疗失败时,应考虑将患儿转移至ECMO中心进行救治。
PALICC-2建议对于心功能稳定的重度PARDS患儿应优先选择静脉-静脉体外膜氧合(VV-ECMO)模式,但临床实际应根据患儿年龄、体重、血管内径、插管型号等因素综合考虑ECMO支持模式。
PALICC-2建议在ECMO支持下的PARDS患儿应当保持正常动脉血氧分压(PaO2),避免过高的PaO2;应缓慢降低PaCO2,避免PaCO2快速下降。对于ECMO支持下的PARDS患儿,建议机械通气的压力设置应符合肺保护性通气的压力限制。所有ECMO后的幸存儿童均应接受近期及远期的神经发育和身体功能评估。
新指南无法对PARDS患儿中应用ECCO2R技术的时机提出建议,未来需进一步研究。
基于PALICC-2的建议和声明,结合指南原文,将PARDS的关键治疗或管理策略的示意性总结进行整理,见图2。
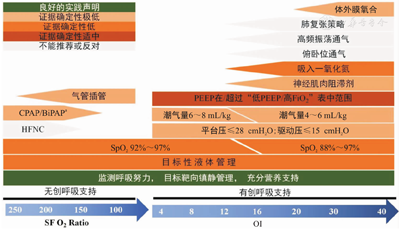

注:PALICC-2:第2届儿童急性肺损伤共识会议;PARDS:儿童急性呼吸窘迫综合征;CPAP:持续气道正压通气;BiPAP:双水平气道正压通气;HFNC:经鼻高流量吸氧;PEEP:呼气末正压;FiO2:吸入气中的氧浓度分数;SpO2:脉搏血氧饱和度;SF O2 Ratio:氧饱和度与吸入氧浓度比率;OI:氧合指数;aBiPAP模式不能耐受时应转为CPAP模式;1 cmH2O=0.098 kPa PALICC-2:the Second Pediatric Acute Lung Injury Consensus Conference;PARDS:pe-diatric acute respiratory distress syndrome;CPAP:continuous positive airway pressure;BiPAP:bilevel positive airway pressure;HFNC:high-flow nasal cannula;PEEP:positive end-expiratory pressure;FiO2:fraction of inspiration oxygen;SpO2:pulse oximeter oxygen saturation;SF O2 Ratio:oxygen saturation/FiO2 ratio;OI:oxyge-nation index;acontinuous positive airway pressure if unable to tolerate bilevel noninvasive ventilation;1 cmH2O=0.098 kPa
经历PICU后幸存的PARDS患儿应注意随访远期发病率并评估预后。应在出院后3个月内进行肺功能异常筛查,至少包括:呼吸症状问卷调查、呼吸系统查体、脉搏血氧仪检测。条件可行时建议完善肺功能仪检查,评估出院后前3个月的肺功能情况。发现肺功能异常后应转诊至专科医师(儿科医师或儿科肺科医师)处进一步评估、治疗并进行长期随访,应兼顾与健康相关的生活质量、身体状况、神经认知、情感、家庭和社会功能评估。
新指南建议临床医师使用自动信息化工具筛查危重患儿,并监测肺保护性通气策略的依从性。建议卫生管理部门提供人力和物质资源,以帮助临床医师研发、使用电子工具,建立协作网络共享临床数据和研究进展。未来,国内学者应积极寻求基于数据科学的网络化协作,以提升对PARDS的管理质量。
RLS中如果无法满足所有的PARDS标准,当患儿的病史、体格检查与已知的诱发因素和临床特征一致时,可使用"拟诊PARDS"这一诊断术语,并无需绝对依赖影像学检查。同时使用SpO2 /FiO2或OSI参数进行判定是更加可行的。建议RLS中PARDS风险人群需应用CPAP/HFNC,而不采用一般的氧疗;对于拟诊PARDS患儿优选CPAP,但条件受限时HFNC仍优于一般氧疗。RLS中选择肺部治疗和辅助治疗时,需综合考虑现有证据级别。临床医师需充分评估治疗措施的可用性和成本,权衡利弊后作出决策。未来纳入RLS中PARDS相关研究是有必要的,以提供适合RLS地区的最优建议。
综上所述,PALICC-2指南的制定是基于对现有证据的严格和系统评估,并使用GRADE证据分级和证据-决策框架的透明学方法作为支撑,对于早期规范化识别、诊断PARDS以及集束化管理此类患儿具有较高的指导意义。但是,该指南总体仍缺乏高质量的随机研究证据,除了1个强推荐意见外,其余的建议或声明都是有条件的,也限制了该指南的应用。其次,PALICC-2工作组考虑了所有建议的可行性、安全性、公平性和实施情况,提出了目前为止较有价值的推荐意见。PALICC-2为未来研究的主要内容作出了说明,期待在以后的研究中获取更多的信息,为进一步认识PARDS的特点和规范管理提供证据支持。
所有作者均声明不存在利益冲突




























