
新型冠状病毒感染疫情期间,为遏制新型冠状病毒传播所采取的一系列非药物干预措施对季节性流感(简称流感)的流行模式产生了影响,流感活动强度显著降低,未再检测出B/Yamagata谱系。全国流感哨点监测数据显示,2012—2019年度,流感呈现明显的季节性流行特征,年均流感病毒检测阳性率为14.57%。新型冠状病毒感染疫情暴发后,我国流感的常规季节性规律被打破,2020—2021年度呈极低流行水平(年均检测阳性率<1.0%),2021—2022年度冬季高峰复现。自2022年12月26日对新型冠状病毒感染实施“乙类乙管”后,社会活动逐步恢复,流感活动强度出现反弹,呈现反季节流行,并出现流感与新型冠状病毒、呼吸道合胞病毒和肺炎支原体感染等其他呼吸道传染病交互或共同流行。流感和其他呼吸道传染病防控强调多病共防,建议长期、持续监测流感病毒和新型冠状病毒等的流行趋势;注重促进重点人群的流感和新型冠状病毒疫苗接种;加强普及防控知识,提高公众自我防病意识等。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
自2020年新型冠状病毒感染(简称“新冠病毒感染”)疫情暴发以来,全球范围内季节性流感(简称“流感”)病毒活动呈现出明显变化。全球流感病原学监测数据(来源FluNet数据库)显示,新冠病毒感染大流行开始后,全球流感活动强度显著降低[1, 2];2021年秋季开始逐步回升[3];至2022年秋季,许多国家(美国、澳大利亚等)已恢复到2011—2019年的活动水平[4, 5]。
新冠病毒感染大流行期间,我国为遏制新冠病毒传播所采取的一系列非药物干预措施(non-pharmaceutical intervention,NPI)对降低流感病毒传播同样有效[6]。流感活动的大幅降低导致人群对流感病毒的免疫力下降,人群易感性增加。2022年12月26日,我国宣布将新型冠状病毒肺炎更名为新冠病毒感染,并实施“乙类乙管”[7],社会活动逐渐恢复到常规水平。本文旨在分析我国新冠病毒感染疫情暴发前后的流感流行特点,对未来流感的流行趋势进行分析,为今后流感防控工作提供参考。
流感病毒属于正黏病毒科,是单股、负链、分节段的RNA病毒,分为甲、乙、丙、丁(或A、B、C、D)四种型别[8]。甲、乙型流感病毒通过发生抗原漂移,感染先前已获得免疫的宿主,导致流感周而复始的季节性流行。另外,甲型流感病毒可发生抗原转变而导致流感大流行[9]。20世纪以来,甲型流感病毒多次[如1918年A(H1N1)、1957年A(H2N2)、1968年A(H3N2)、2009年A(H1N1)pdm09]引起大流行[10, 11]。大流行性甲型流感病毒可替换既往流行的流感病毒亚型,并演变为季节性流行毒株[12]。如,1957年大流行毒株A(H2N2)取代了既往的A(H1N1),并演变为季节性流行,直至1968年被大流行毒株A(H3N2)取代;2009年大流行毒株A(H1N1)pdm09取代了之前的A(H1N1),并演变为季节性流行至今[13]。
乙型流感病毒于1940年被发现[14],1983年依据抗原性和遗传特征的不同被分为B/Victoria和B/Yamagata两个系[15]。20世纪80年代,全球流行的乙型流感主要为B/Victoria系;90年代开始,B/Yamagata系成为主要流行系,B/Victoria系仅在亚洲地区少量检测到[16, 17, 18, 19];2000年后,B/Victoria和B/Yamagata系以不同的流行强度在每个流感季共同流行[20, 21];而从2020年3月以来,自然流行的B/Yamagata系基本消失[1]。
根据国家流感中心发布的ILI哨点监测数据显示[22],2012—2019年度(《全国流感监测技术指南》定义每年第14周至次年第13周为一个流感监测年度),我国ILI(体温≥38 ℃,有咳嗽或咽喉疼痛之一者)报告病例数在门急诊病例数中的占比(简称ILI报告占比,ILI%)具有明显的流行高峰。南方地区存在冬春季和夏季两个高峰,冬春季高峰一般发生在12月至次年3月,2012—2019年度ILI%峰值范围3.5%~8.0%,夏季高峰则在6—7月,2012—2019年度ILI%峰值范围3.5%~4.6%。北方地区仅有冬春高峰,高峰时间与南方地区相近,2012—2019年度ILI%峰值范围4.2%~8.5%。
新冠病毒感染疫情暴发后,全国的ILI%出现明显下降,2020—2021年度未出现明显的高峰。2022年7月左右,南方地区出现夏季高峰,第25周ILI%最高,为7.5%。2022年冬春季ILI%激增,为近10年来最高,南方地区2022年第51周ILI%最高(达到13%);北方地区2023年第10周ILI%最高(8.7%)。
2012—2019年度,全国流感监测网络实验室共检测ILI监测标本1 937 634例,年均流感病毒检测阳性率为14.57%。2017—2019年的年均检测阳性率较高,各年度依次为20.36%、14.34%和16.41%;2014年较低,仅12.14%[22]。甲型流感病毒为主要流行毒株,每年流行,A(H1N1)pdm09和A(H3N2)交替成为优势流行毒株;B/Victoria系在2015—2016年度和2019—2020年度与甲型流感共同流行,B/Yamagata系在2014—2015年度和2017—2018年度与甲型流感共同流行(图1)。
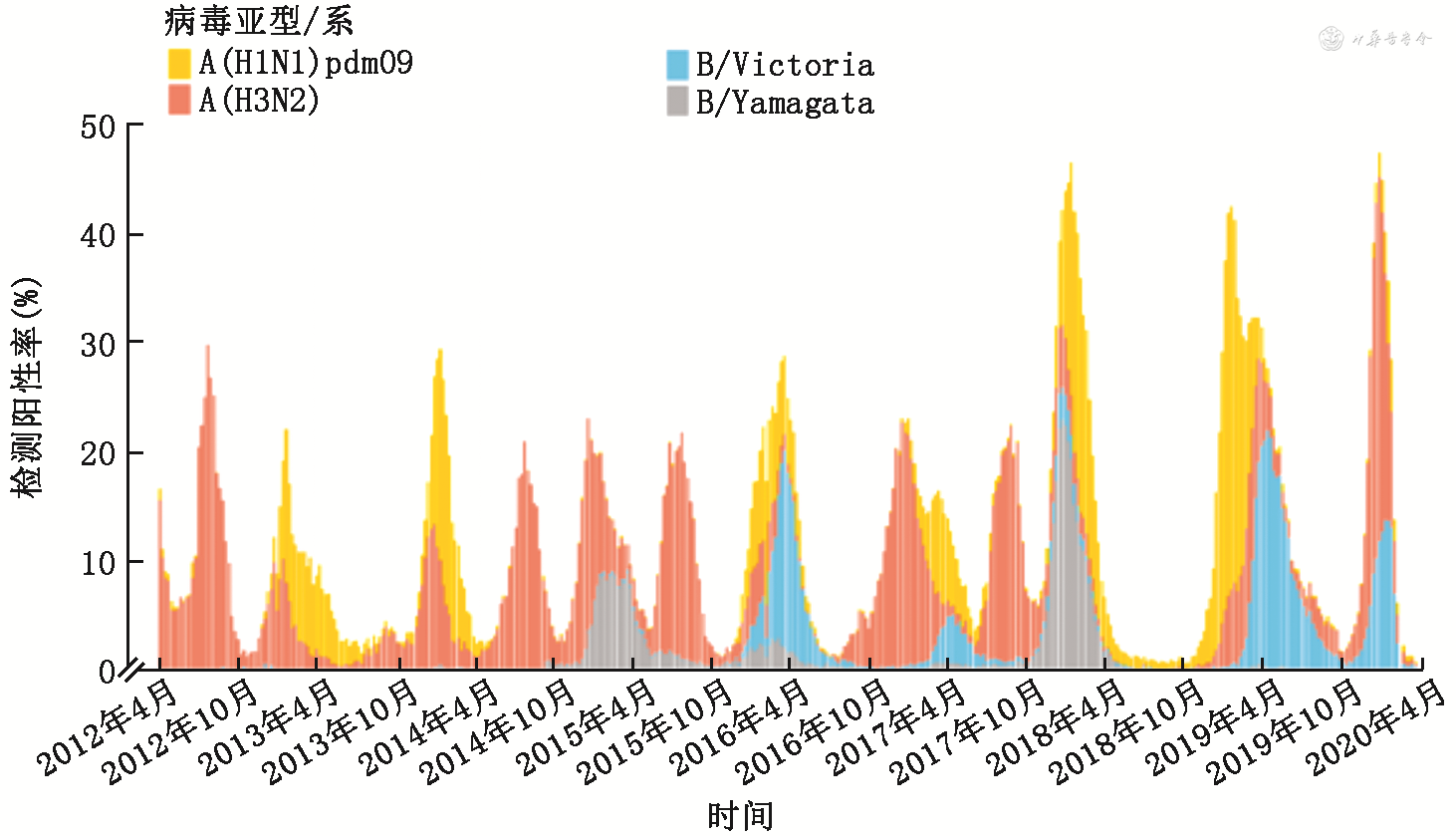

2020—2021年度,流感在我国呈极低流行水平(年均检测阳性率<1.0%),2020年底开始缓慢升高[23]。2021—2022年度,流感病毒检测阳性率在2022年初达到峰值(以周计,南方省份为25.7%,北方省份为31.8%),B/Victoria系为优势流行毒株[23]。2022—2023年度,南方个别省份自2022年5月开始进入夏季流感流行高峰,以A(H3N2)亚型为绝对优势株,流感活动强度达到近5年来同期最高水平;同期的北方省份流行活动保持低水平[22]。自12月26日对新冠病毒感染实施“乙类乙管”后[7],流感活动强度自2月开始显著上升,3月达到峰值后回落,A(H3N2)和A(H1N1)pdm09为主要流行毒株。2023—2024年度,南方省份尚未出现既往的夏季流行。从10月开始,我国流感病毒检测阳性率持续上升,南方高于北方[22,24](图2)。新冠病毒感染疫情暴发后,我国未检测到B/Yamagata毒株[22],与全球情况一致[1, 2]。
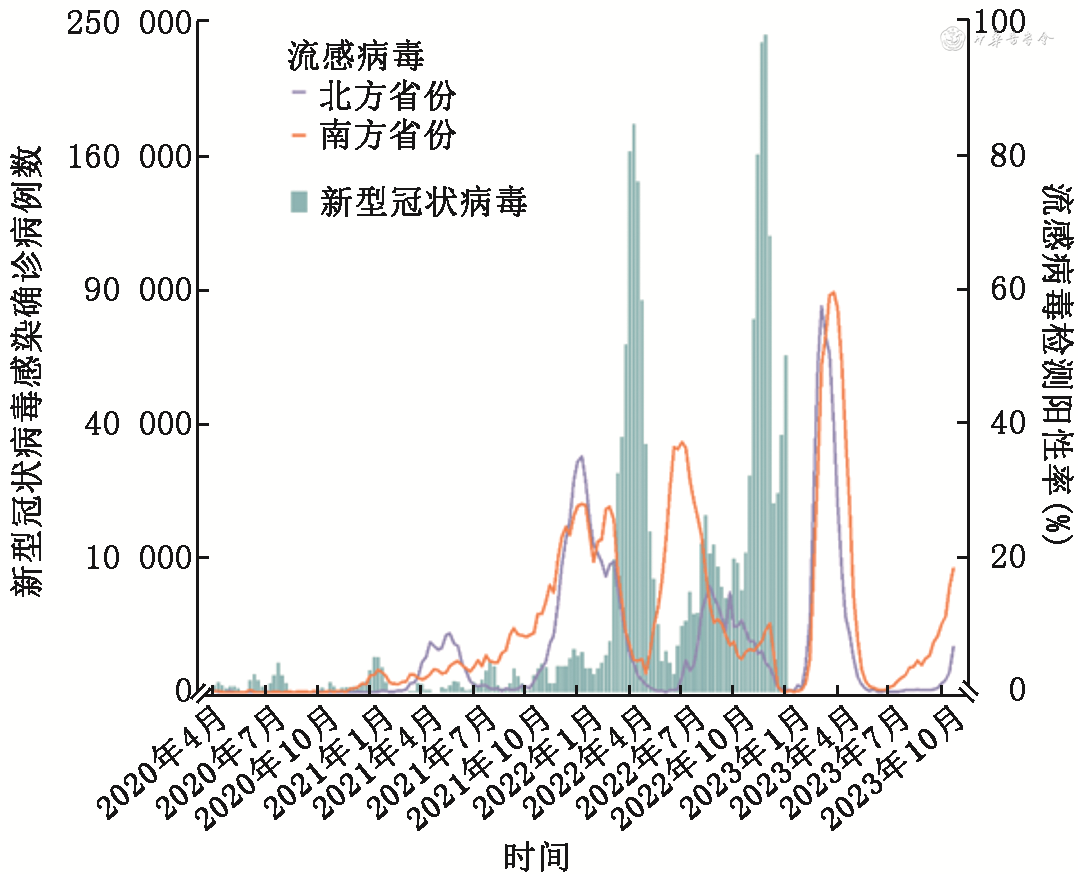

新冠病毒感染疫情暴发前,受到毒株变异、宿主易感性和环境等因素的影响,我国流感流行有明显季节性,并呈现出一定的地域差异。Yu等[26]从省级层面分析了我国2005—2011年流感的季节性。结果显示,甲型流感的年度周期性随纬度的增加而增强:纬度>33°N的北方省份呈冬季流行模式,每年1—2月出现单一年度高峰;纬度<27°N的南方省份在每年4—6月出现单一年度高峰;而两者之间的中纬度的地区呈现每年1—2月和6—8月的双周期高峰。乙型流感在我国大部分地区呈单一冬季高发,B/Victoria和B/Yamagata系交替流行,在个别年份两个谱系会共同流行[27]。Liao等[28]通过阈值法确定季节性指标,采用分层聚类的方法,按照“北方、中部、西南、东南”四个地理区对城市进行划分,描述了我国2010—2018年的流感季节性模式,相较于既往研究[26],发现我国北部、中部和西南地区冬春季流感活动时间更长(12月至次年3月),中部和西南地区夏季流感活动时间更短(7—8月)。东南地区流行期的分布因流行季节而异,缺乏规律性,高峰时间在第52周到次年的第31周之间。另一项模型研究也表明[29],在2009年A(H1N1)pdm09大流行后,我国A(H1N1)pdm09和乙型流感的流行高峰主要发生在冬春季;A(H3N2)在北部地区的流行高峰主要发生在冬春季,而在中部和南部地区流行高峰发生在夏秋季。。
流感病毒新毒株[如1918年A(H1N1)、2009年A(H1N1)pdm09]的出现和传播会改变流感的季节性流行模式,但这种影响通常仅限于大流行的第1年,随后便恢复到常规季节性流行模式[30, 31]。例如,2009年A(H1N1)pdm09大流行于北半球流感春季高峰期结束后开始,7月达到峰值,2010年秋季回归典型的季节性流行模式。
新冠病毒感染疫情暴发后,受为遏制新冠病毒传播所采取的NPI,以及人群行为模式等改变的影响,同全球其他国家一样,我国流感的常规季节性规律被打破,其影响比既往流感大流行对季节性的影响更显著。2020—2021流感季,我国流感呈高度散发,冬季高峰消失。2021—2022流感季,如同全球其他国家(如北半球的美国[32, 33]和南半球澳大利亚和智利等国[34]),冬季高峰复现,但仍低于往年峰值;南方地区出现夏季高峰,同期北方地区的流感活动处于低水平。2022—2023流感季,不同于全球多个国家(流感流行模式已与新冠大流行之前相似[35, 36, 37]),我国流感活动出现反季节流行,即冬春流感季较以往滞后约2个月,流感活动强度略高于新冠病毒感染疫情前的自然流行年份,但仍为季节性流行水平。
Lei等[38]使用2018—2022年我国流感监测数据,建立易感者-疫苗接种者-感染者-恢复者-易感者模型(susceptible-vaccinated-infected-recovered-susceptible,SVIRS),预测了2023—2025年我国的流感流行趋势。当NPI完全取消时,2022—2023流感季我国南方和北方流感活动高峰期的发病率将分别增加3.8倍和3.0倍,高峰期滞后,但达到峰值的速度更快。2024—2025流感季南方流感发病率将逐渐恢复到新冠病毒感染大流行前的水平;而北方地区NPI放宽的影响将一直持续至2024—2025流感季。另一项预测我国未来3年流感流行趋势的模型研究[35]结果显示,2023—2026年,A(H1N1)pdm09在南北方的流行高峰均在冬季(1—4月);A(H3N2)在南方的流行高峰出现在夏季(5—7月),北方出现在冬季(12月至次年2月)。
流感流行受病毒、宿主和环境等多因素共同影响,采用数学模型难以准确预测未来的流行模式,加上不同研究所使用的模型方法和情境假设等不同,不同研究得出的结论不完全一致。本文主要引用该领域目前高质量模型研究文章,及国内外专家评述,探讨流感未来流行趋势。受到所引用文献方法局限性等影响,对未来流感流行趋势的判断可能存在偏倚。为了更好地了解和应对未来的流感流行,需要长期系统地开展高质量的流感监测,并从方法学上提高流感流行趋势预测模型的准确性和可靠性,及时为制定有效的防控策略提供科学依据。
自2020年3月以来,WHO流感活动中心未检测到自然流行的B/Yamagata系毒株,认为B/Yamagata系感染风险较低。因此,可以合理推断该谱系已不在人群中传播,未来引起流行的可能性较小[39]。由于乙型流感病毒的不同系间存在交叉保护作用,B/Yamagata系的消失会增加人群对于乙型病毒的易感性,从而加快B/Victoria系的抗原进化[40, 41]。有研究发现,B/Victoria系病毒中血凝素抗原的某些位点氨基酸缺失会对其抗原性产生显著影响,形成抗原性差异较大的多个分支,可能导致未来出现一种或多种乙型流感病毒的共同流行[42]。目前,尚无法准确预测未来流感的流行毒株和流行强度。
气候因素会影响呼吸道病毒的传播,低温和干燥在增加病毒稳定性传播的同时可削弱宿主的免疫系统,因此呼吸道病毒一般都在冬季达到流行高峰[43]。另外,不同病毒之间存在宿主竞争效应[44],因此,尽管不同呼吸道病毒存在类似的季节性流行模式,但很少同时达到流行高峰。例如,呼吸道合胞病毒的流行高峰期一般比甲型流感病毒提前6周[45]。
对全球22个国家2019—2022年流感监测数据的分析表明,在新冠病毒感染大流行期间,新冠病毒和流感病毒呈交替流行[37,46]。Wang等[47]比较了2020年1月至2023年3月期间WHO 6个区域中新冠病毒和流感病毒的流行趋势,发现在新冠病毒感染疫情大流行早期1年多的时间里,流感病毒检测阳性率一直低于10%,随后随着德尔塔株活动减弱而逐渐上升;在奥密克戎株大流行前3个月,流感病毒检测阳性率出现下降,在奥密克戎株活动减弱时又显著增加;每次交替的持续时间约为3~4个月,呈现出“跷跷板效应”[48]。
新冠病毒感染疫情已不再构成国际关注的突发公共卫生事件[49],目前尚未观察到新冠病毒遵循典型的季节性流行模式。随着新变异株(尤其是传播能力和免疫逃避能力增强的)出现,以及人群通过自然感染和(或)疫苗接种获得的免疫保护随时间逐渐衰减,新冠病毒感染疫情呈现出小规模波浪式反复流行的新常态[50]。研究显示,尽管新冠病毒流行缺乏典型的季节性,但流行高峰期一般出现在每年11月至次年4月,与流感冬季流行高峰前后交替或同步[4,51, 52, 53]。自2023年10月以来,我国呼吸道疾病已进入高发季节,多种呼吸道传染病叠加流行,流行周期迁延,对公众健康造成严重影响的同时,使门急诊等医疗服务系统长时间处于高负荷状态。该现象可能归因于新冠病毒感染损害了人体免疫系统,导致人体对于其他病原体抵抗能力降低[54]。我国目前主要流行的呼吸道病原体为流感病毒,同时还有呼吸道合胞病毒、肺炎支原体等共同传播[55];另外,新冠病毒仍存在潜在流行风险,不容忽视。
由于流感病毒的快速变异以及人群普遍易感,防控工作面临很大挑战。接种流感疫苗是预防流感的最有效手段,WHO[56]和《中国流感疫苗预防接种技术指南(2023—2024)》[57]均建议尽早接种流感疫苗,三价和四价疫苗无优先推荐。为了提高每年流感疫苗推荐株与流感病毒流行株的匹配性,仍需要长期、持续的监测不同型/亚型/系流感病毒的流行趋势,加强流感病毒基因序列和流感流行模式的信息共享。此外,公共卫生部门应加强普及流感防控知识,及时发布流感流行预警与提示信息,提高公众自我防病意识。
冬春季呼吸道传染病防控强调多病共防。对于具有特异性疫苗的呼吸道传染病,应通过优化疫苗接种服务提升便利性、加强政策倡导和科普减少疫苗犹豫,以及促进同时接种等多途径提高人群接种率。尤其是注重提高医务人员、老年人、低龄儿童和慢病患者等重点人群的疫苗接种率。对于流感疫苗,鼓励有条件的地方对重点人群实施免费接种,提升接种率。对于新冠病毒疫苗和流感疫苗的同时接种,基于针对新冠病毒原型株的灭活疫苗和灭活流感疫苗同时接种的非劣效、四期随机对照临床试验[58, 59],《中国流感疫苗预防接种技术指南(2023—2024)》指出,经审慎考虑,认为≥18岁人群可以同时接种灭活流感疫苗和新冠病毒疫苗,其安全性和免疫原性是可以接受的,可以降低感染流感病毒或新冠病毒后出现严重疾病的风险,能够减少接种者前往接种门诊的次数,提高免疫接种效率[57]。然而,我国尚无关于其他类型的新冠病毒疫苗(如腺病毒载体疫苗、重组亚单位疫苗,针对XBB新冠病毒的疫苗)和流感疫苗(如减毒活疫苗)同时接种的安全性和免疫原性证据,还需继续评估[60]。此外,新冠和流感的联合疫苗正在加快研发中,目前已进入临床试验阶段[61]。由于病毒毒株不断变异进化,疫苗抗原与流行毒株不匹配的风险增加,疫苗有效性降低[62],故开发通用疫苗对于预防多种变异毒株至关重要[63]。为应对流感和新冠病毒感染等呼吸道传染病交互或共同流行,我国已将新冠病毒监测纳入流感哨点监测网络,同时监测两种病毒的流行趋势是实现同防同控的又一有效举措。
王铭韩, 胡泽鑫, 冯录召, 等. 新型冠状病毒感染疫情后我国季节性流感的流行趋势与防控建议[J]. 中华医学杂志, 2024, 104(8): 559-565. DOI: 10.3760/cma.j.cn112137-20231220-01430.
所有作者声明不存在利益冲突



























