器官移植是挽救终末期器官衰竭患者生命的重要手段,但是供器官短缺已经成为全世界器官移植界共同面临的难题,严重制约器官移植事业的发展。世界上多个国家已经建立较为成熟的器官捐献体系,在一定程度上为缓解供器官短缺创造了有利条件。本文分析总结了国外器官捐献工作的特点以及工作现状,探索促进中国器官捐献发展的途径,为进一步优化和完善我国器官捐献与移植体系提供理论参考。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
器官移植已经成为挽救终末期器官衰竭患者生命的重要手段。然而,随着医学技术的不断发展,器官移植数量的不断增长,供器官短缺的问题日益严重,"器官匮乏"成为器官移植领域的瓶颈,严重制约着器官移植事业的发展[1,2]。2010年,我国正式启动了公民逝世后器官捐献试点工作,并于2013年2月在全国范围内推开。从2015年1月1日起,公民自愿捐献成为我国移植器官唯一来源。经过十余年的改革发展,目前已经建立了器官捐献和移植事业的"中国模式"。本文将对国外器官捐献及器官获取组织(Organ Procurement Organization,OPO)工作的特点及现状进行探讨,以期为我国器官捐献与移植体系的优化和完善提供参考。
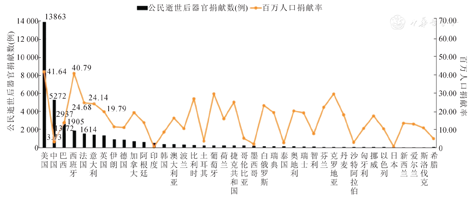
百万人口器官捐献率(per million population,PMP)是指每百万人口中器官捐献者的数量。2020年之前,全球器官捐献数量呈逐年上升的趋势,2019年全球共完成41 695例逝世后器官捐献,但仍仅能满足约10%的器官移植需求。西班牙(2 302例,PMP为49. 6)、美国(11 870例,PMP为36. 1)、葡萄牙(347例,PMP为33. 7)、克罗地亚(131例,PMP为32. 0)和法国(1 924例,PMP为29. 4)为全球PMP排名前5的国家,其中西班牙的PMP达到了全球历史最高值[3]。2020年新型冠状病毒的大流行给全人类的生活带来了重大影响,各国器官捐献工作也经受了重大考验,全球公民逝世后器官捐献例数下降到36 102例,例数同比下降13. 41%;西班牙公民逝世后器官捐献为1 777例,其PMP下降到37. 97,例数同比下降22. 81%;但可能得益于美国公民生前签署的捐献志愿书具有法律效力,非特殊情况家属无权推翻,美国公民逝世后器官捐献为12 588例,其PMP一举超越西班牙,达到了38. 03,例数同比上升6. 05%。根据全球捐献和移植观察站(Global Observatory on Donation and Transplantation,GODT)发布的《2021年器官捐献和移植国际数据》[4],2021年美国PMP居全球首位,达到41. 6;西班牙、冰岛、葡萄牙、克罗地亚、比利时等国家紧随其后,PMP分别为40. 8、36. 7、29. 6、29. 5、26. 9(图1)。
器官捐献来源主要分为活体捐献和死亡捐献2种。活体捐献是在不影响器官捐献者生命安全和不造成其健康损害的前提下,由健康成人个体自愿提供生理和技术上可以切取的部分器官移植给他人(如肾脏、部分肝脏和部分肺脏捐献等)的器官捐献,主要受限于亲属和配偶等家庭成员之间。死亡捐献是指在死亡后一定时限内获取具有活力的器官,移植给终末期器官衰竭患者,以挽救生命或改善生活质量。死亡捐献在中国也被称为公民逝世后器官捐献[5]。
世界卫生组织明确了2种死亡捐献形式,分别为神经学标准诊断死亡后的脑死亡器官捐献(donation after brain death,DBD)和使用心肺标准确认死亡后的心死亡器官捐献(donation after cardiac death,DCD)[6]。DBD和DCD也是国际医学界对死亡器官捐献常用的分类。
目前,亚洲国家中,印度、韩国、土耳其和日本等以活体捐献为移植器官主要来源,且活体肾移植或肝移植比例均大于50%;伊朗、泰国等以死亡捐献为移植器官的主要来源,且DBD比例高于全球平均水平(77. 4%)[6]。在大多数情况下,这2种形式的捐献在同一个国家或地区是同时实行的[7]。
在器官捐献同意政策方面,目前国外主要有2种模式,分别为知情同意和推定同意(表1)[8,9,10,11,12,13,14,15,16,17,18]。其中,知情同意是指捐献者和其直系亲属充分知悉器官捐献相关政策、法规、医疗技术及伦理等信息,由捐献者本人或其直系亲属共同做出接受或拒绝捐献器官的意愿。推定同意则是指如果公民在逝世前未明确表示拒绝器官捐献,则可以推定其同意捐献器官,人体器官获取组织可根据相关法律规定在其逝世后获取可供移植的器官和组织。在实行知情同意政策的国家,捐献者生前已表达捐献意愿或其家属同意在其逝世后进行器官捐献,捐献者才能完成器官捐献;相反,在实行推定同意政策的国家,任何人都是潜在的器官捐献者,如果逝者生前不愿意在逝世后捐献自己的遗体或器官,就必须生前在相关机构进行登记,表达不进行遗体或器官捐献的意愿。
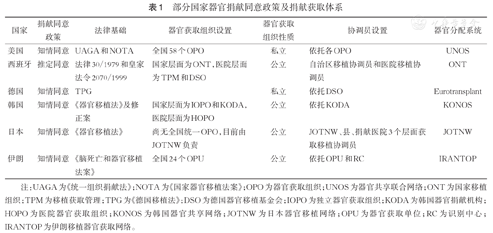
部分国家器官捐献同意政策及捐献获取体系
部分国家器官捐献同意政策及捐献获取体系
| 国家 | 捐献同意政策 | 法律基础 | 器官获取组织设置 | 器官获取组织性质 | 协调员设置 | 器官分配系统 |
|---|---|---|---|---|---|---|
| 美国 | 知情同意 | UAGA和NOTA | 全国58个OPO | 私立 | 依托各OPO | UNOS |
| 西班牙 | 推定同意 | 法律30/1979和皇家法令2070/1999 | 国家层面为ONT,医院层面为TPM和DSO | 公立 | 自治区移植协调员和医院移植协调员 | ONT |
| 德国 | 知情同意 | TPG | 私立 | 依托DSO | Eurotransplant | |
| 韩国 | 知情同意 | 《器官移植法》及修正案 | 国家层面为IOPO和KODA,医院层面为HOPO | 公立 | 依托KODA | KONOS |
| 日本 | 知情同意 | 《器官移植法》 | 尚无全国统一OPO,目前由JOTNW负责 | 公立 | JOTNW、县、捐献医院3个层面获取移植协调员 | JOTNW |
| 伊朗 | 知情同意 | 《脑死亡和器官移植法案》 | 全国24个OPU | 公立 | 依托OPU和RC | IRANTOP |
注:UAGA为《统一组织捐献法》;NOTA为《国家器官移植法案》;OPO为器官获取组织;UNOS为器官共享联合网络;ONT为国家移植组织;TPM为移植获取管理;TPG为《德国移植法》;DSO为德国器官移植基金会;IOPO为独立器官获取组织;KODA为韩国器官捐献机构;HOPO为医院器官获取组织;KONOS为韩国器官共享网络;JOTNW为日本器官移植网络;OPU为器官获取单位;RC为识别中心;IRANTOP为伊朗移植器官获取网络。
就器官捐献而言,推定同意被认为是最有利于器官捐献和移植事业发展的模式,但是在严格的推定同意模式下,逝者的个人权利可能会受到侵犯;而知情同意模式的优点则在于不会引起太大的社会争议,但是这种完全依赖民众自主行为的捐献模式受制于民众整体捐献意愿水平。需要指出的是,不同国家的器官捐献同意政策可受国际和其国内因素影响而改变。智利、芬兰、希腊、乌拉圭、威尔士等国家和地区近年来相继实施了推定同意政策,澳大利亚、丹麦、德国、以色列、罗马尼亚和美国部分州也一直在讨论是否将现行的器官捐献知情同意政策改为推定同意政策[19]。
关于实施何种器官捐献同意政策有助于提高器官捐献率,医学界一直有不同意见。有研究表明,实施推定同意政策有助于提高器官捐献率[20,21,22,23,24];然而,另一些研究则表明推定同意政策的实施对提高器官捐献率影响较小[19,25,26,27,28]。通过对不同国家实施推定同意政策取得的效果进行分析研究表明,器官捐献同意政策可能只是影响器官捐献率众多因素中的一个,国家层面器官捐献与移植制度的完善和民众器官捐献理念的改变,可能对器官捐献率的提升产生更明显的效果[29,30]。
为了规范器官捐献行为、保证器官捐献的合法性和公正性,部分国家制定了相关的法律和规定,形成了较完备善的器官捐献和移植制度。
西班牙实施的器官捐献和移植相关法律主要是1979年的第30号法律(法律30/1979)和1999年的皇家法令2070号(皇家法令2070/1999)[31]。法律30/1979主要规定了死亡的判定标准、器官的获取和移植程序等一般性的普遍规定,同时也提出了"西班牙模式"的重要特征:器官捐献的组织结构模式[32]。皇家法令2070/1999则主要规定了器官捐献与移植的组织架构,同时还详细规定了死亡的判定标准,强调宣传器官捐献与移植要常态化,突出器官捐献与移植中自愿、利他与无私的精神[9]。
作为世界上最早开展器官移植的国家,美国的器官捐献与移植实践规则建立在《统一组织捐献法》(Uniform Anatomical Gift Act,UAGA)与《国家器官移植法案》 (National Organ Transplants Act,NOTA)这2部法律的基础之上[33]。美国器官移植的法制化历程从1968年通过UAGA开始,规范了器官捐献与移植行为,至1973年,该法案已经在美国50个州及哥伦比亚特区统一实施。1984年,美国又通过了法律效力更高的NOTA,禁止器官与组织的非法交易,并提出要建立移植与获取网络[34]。在此基础上成立的美国器官共享联合网络(United Network for Organ Sharing,UNOS)成功形成了覆盖全美国的器官移植网络,建立了有效的机构运行机制,较好缓解了供体短缺的紧迫状况。
早在20世纪60年代,德国就成功开展了器官移植,但直到1997年《德国移植法》(Transplantation-sgesetz,TPG)才正式生效。TPG规范了公民逝世后及活体捐献器官的捐献、获取和转运。器官分配的责任由德国器官获取组织德国器官移植基金会(The Deutsche Stiftung Organtransplantation,DSO)承担,该组织也是协调德国器官捐献的主管机构。TPG要求德国医学协会为移植医学的特定领域制定指导方针,这些指导方针必须考虑到医学科学的现状,并定期更新以解决运行过程中出现的问题[11,35]。
韩国自2000年开始实施《器官移植法》,并建立了韩国器官共享网络(Korean Network for Organ Sharing,KONOS)。KONOS负责移植等待者名单管理、处理协调和政策执行问题,是执行器官分配等移植相关任务的国家机构,在器官移植活动的管理和评估中发挥重要作用[36,37]。2010年,韩国国民议会通过了《器官移植法》修正案,其中包括强制报告潜在脑死亡患者、建立国家独立器官获取组织(Independent Organ Procurement Organization,IOPO)以及韩国器官移植登记处(Korean Organ Transplantation Registry,KOTRY)。韩国器官捐献机构(Korea Organ Donor Agency,KODA)也于2010年成立,当地医院所有潜在的脑死亡患者都要向KODA报告,由KODA确定患者是否达到脑死亡标准,并与脑死亡患者家属进行沟通以征得其同意以进行器官捐献。通过以上努力,韩国死亡器官捐献者数量明显增加,器官移植旅游现象在一定程度上也得以改善[38]。
日本脑死亡器官捐献与移植开展比较晚,直到1997年10月《器官移植法》实施,日本才开始进行脑死亡器官捐献。《器官移植法》要求脑死亡器官捐献者在生前书面声明同意和家属同意其进行脑死亡器官捐献,并且不允许15岁以下儿童进行脑死亡器官捐献。由于该法律对器官捐献条件的严格限制,日本直到1999年2月才进行了第1例脑死亡器官捐献,且随后几年的脑死亡器官捐献数量依然极低[39]。为了增加脑死亡器官捐献供者数量,日本于2010年对《器官移植法》进行了修订,修订版本明确了以下几点:一是如果脑死亡患者生前没有拒绝器官捐献,仅征得家属同意就可以进行器官捐献;二是允许年龄小于15岁的儿童进行器官捐献;三是在特定条件下,器官捐献者家属可以优先使用捐献者的器官[40]。《器官移植法》修订后,脑死亡器官捐献者数量由2009年的7例增加到2011年的44例[41];死亡器官捐献的PMP持续在1以下,与其他发达国家相比,日本的PMP依然处于极低水平[15]。
由于缺乏死亡捐献供肾,1979年后伊朗在德黑兰启动了活体亲属和非亲属肾移植(living related and living unrelated kidney transplant,LUKT)计划[42]。1988年,伊朗实施了由政府进行监管和资助的LUKT计划,通常被称为"伊朗肾移植模式"[43]。该计划主要通过活体非亲属捐献为终末期肾病患者提供肾移植。在该模式下,年龄在18~35岁的肾脏捐献者被转介给伊朗肾脏基金会进行登记,再推介给移植团队,在肾脏捐献和移植完成后,活体非亲属捐献者将获得政府的奖励和健康保险,也能获得由肾移植受者或慈善组织提供的经济奖励(由伊朗肾脏基金会在移植前协助商定)[44,45,46]。为将脑死亡捐献器官移植合法化,伊朗议会在2000年通过了《脑死亡和器官移植法案》,但由于文化和宗教信仰以及公众对脑死亡概念缺乏认识,伊朗的脑死亡器官移植数量较少,到2000年底总共只进行了84例脑死亡捐献供肾移植手术[43]。在随后20年内,伊朗器官捐献和移植团队通过加大器官捐献理念公众宣传、扩大边缘供体、培训各地的协调员和医护人员、建立高效的器官分配网络等方式,促使死亡器官捐献数量持续上升,2003至2019年,伊朗的PMP由0. 75上升到14. 3[18]。
Mollaret等[47]在20世纪50年代首次提出脑死亡的概念,该概念一直受到各领域专家广泛讨论,直到1968年世界医学协会才承认脑死亡可以作为人类死亡的标志。同年,美国哈佛大学医学院首次提出了指导脑死亡判定的医学标准,即"哈佛脑死亡标准"[48]。目前,"脑死亡即为人类死亡"的说法已经被国际医学界广泛接受[49]。但尽管大约有70%的国家已对脑死亡进行立法或发布了脑死亡判定相关的指南,各国在脑死亡判定的实践中仍然存在差异。Othman等[50]汇总了部分国家关于脑死亡判定相关情况(表2)。2020年发表的《脑死亡判定国际专家共识》[51],是基于文献综述和多学科国际专家组的意见形式的,有助于指导专业协会和国家修订或制定脑死亡判定的操作和程序,从而提高各国判定标准的一致性。
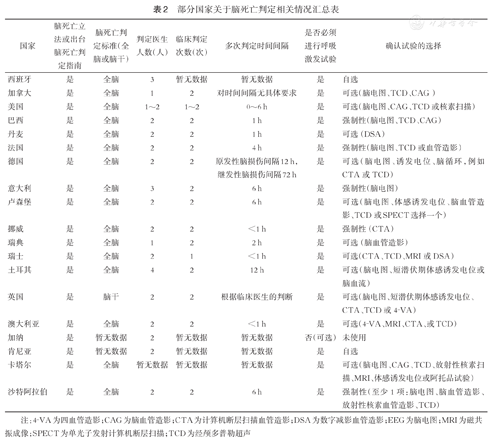
部分国家关于脑死亡判定相关情况汇总表
部分国家关于脑死亡判定相关情况汇总表
| 国家 | 脑死亡立法或出台脑死亡判定指南 | 脑死亡判定标准(全脑或脑干) | 判定医生人数(人) | 临床判定次数(次) | 多次判定时间间隔 | 是否必须进行呼吸激发试验 | 确认试验的选择 |
|---|---|---|---|---|---|---|---|
| 西班牙 | 是 | 全脑 | 3 | 暂无数据 | 暂无数据 | 是 | 自选 |
| 加拿大 | 是 | 全脑 | 1 | 2 | 对时间间隔无具体要求 | 是 | 可选(脑电图、TCD、CAG) |
| 美国 | 是 | 全脑 | 1~2 | 1~2 | 0~6 h | 是 | 可选(脑电图、CAG、TCD或核素扫描) |
| 巴西 | 是 | 全脑 | 2 | 2 | 1 h | 是 | 强制性(脑电图、TCD、CAG) |
| 丹麦 | 是 | 全脑 | 2 | 2 | 1 h | 是 | 可选(DSA) |
| 法国 | 是 | 全脑 | 2 | 2 | 4 h | 是 | 强制性(脑电图、TCD或血管造影) |
| 德国 | 是 | 全脑 | 2 | 2 | 原发性脑损伤间隔12 h,继发性脑损伤间隔72 h | 是 | 可选(脑电图、诱发电位、脑循环,例如CTA或TCD) |
| 意大利 | 是 | 全脑 | 3 | 2 | 6 h | 是 | 强制性(脑电图) |
| 卢森堡 | 是 | 全脑 | 2 | 2 | 6 h | 是 | 可选(脑电图、体感诱发电位、脑血管造影、TCD或SPECT选择一个) |
| 挪威 | 是 | 全脑 | 2 | 2 | <1 h | 是 | 强制性(CTA) |
| 瑞典 | 是 | 全脑 | 1 | 2 | 2 h | 是 | 可选(脑血管造影) |
| 瑞士 | 是 | 全脑 | 2 | 1 | <1 h | 是 | 可选(CTA、TCD、MRI或DSA) |
| 土耳其 | 是 | 全脑 | 4 | 2 | 12 h | 是 | 可选(脑电图、短潜伏期体感诱发电位或脑血流) |
| 英国 | 是 | 脑干 | 2 | 2 | 根据临床医生的判断 | 是 | 可选(脑电图、短潜伏期体感诱发电位、CTA、TCD或4-VA) |
| 澳大利亚 | 是 | 全脑 | 2 | 2 | <1 h | 是 | 可选(4-VA、MRI、CTA、或TCD) |
| 加纳 | 是 | 暂无数据 | 2 | 暂无数据 | 暂无数据 | 否(可选) | 未使用 |
| 肯尼亚 | 是 | 暂无数据 | 2 | 暂无数据 | 暂无数据 | 是 | 自选 |
| 卡塔尔 | 是 | 全脑 | 暂无数据 | 暂无数据 | 暂无数据 | 是 | 可选(脑电图、CAG、TCD、放射性核素扫描、MRI、体感诱发电位或阿托品试验) |
| 沙特阿拉伯 | 是 | 全脑 | 2 | 2 | 6 h | 是 | 强制性(至少1项:脑电图、脑血管造影、放射性核素血管造影、TCD) |
注:4-VA为四血管造影;CAG为脑血管造影;CTA为计算机断层扫描血管造影;DSA为数字减影血管造影;EEG为脑电图;MRI为磁共振成像;SPECT为单光子发射计算机断层扫描;TCD为经颅多普勒超声
OPO是国外器官捐献与移植工作的核心组织,主要负责器官捐献的宣传、登记、评估、获取和分配等工作,对器官捐献和移植成功率有着至关重要的影响。在器官捐献率方面取得较好成绩的国家,在器官捐献组织与网络建设方面都有独到的经验。
西班牙器官捐献和移植体系建设已有30多年的历史,在2015年以后,由于政策的变化及技术的再次突破,西班牙器官捐献和移植数量大幅增加,PMP从保持多年的35. 0上升至49. 6(2019年),居全球首位。
西班牙成功的关键在于实施了"西班牙模式",器官捐献的组织结构模式是其主要特征。
一是三层管理结构,即建立了国家、区域和地方(医院内)3个层面的器官获取与移植组织机构,不同层次的组织机构承担不同的责任[9,52]。在国家层面,建立由西班牙卫生与社会政策部管理的国家移植组织(National Transplant Organisation,ONT),主要负责提高器官捐献数量、协调获取和分配及移植全过程[9,10]。在区域层面,在每个自治区中设立1名移植协调员,主要负责自治区之间以及ONT与院内协调员之间的联系沟通。在地方医院层面,每个ICU病房都配备由专业医护担任的兼职移植协调员,主要承担发现潜在捐献者、征询家属捐献同意和管理器官捐献与获取全过程的责任。独立于移植团队的移植获取管理(the Transplant Procurement Management,TPM)团队也在器官捐献获取中发挥着重要作用。TPM团队位于医院内部,专注院内潜在捐献者的识别,这也是西班牙模式成功的重要因素。
二是实施了死亡捐献过程质量保障计划,邀请潜在捐献者所在医院的移植协调员和所在区域其他医院的专家和移植协调员,对潜在捐献者进行评估,从源头对捐献器官进行质量控制。
三是与媒体密切合作,通过不同方式,对移植协调员、ICU和急诊医生、护士等其他医疗卫生专业人员开展不同类型的课程培训。培训内容侧重于沟通技巧、家庭咨询和征询捐献同意,积极营造信任捐献体系和支持捐献的社会氛围。TPM联合西班牙捐献移植研究院(the Donation and Transplantation Institute,DTI)对医院层面参与器官捐献获取过程的医疗卫生专业人员进行培训,也为"西班牙模式"取得成功并且向其他国家进行推广发挥了重要作用。另外,相关主管部门还拿出单独预算用来支持这些推动器官捐献的活动,也为器官捐献相关工作的开展提供了保障[53]。
1984年NOTA通过后,美国就启动了国家器官共享系统的开发,成立了器官获取与移植网络(Organ Procurement and Transplantation Network,OPTN),用于收集器官移植的相关数据。NOTA规定OPTN应由非营利的独立组织通过竞标合同进行管理,在器官移植体系架构中,UNOS通过竞标获得了与政府合作的合同,负责OPTN的管理和运营,参与美国器官移植体系建设。
根据NOTA,由医疗保险和补助服务中心(Centers for Medicare & Medicaid Services,CMS)指定全美国58个OPO各自的服务区域,并每4年对OPO进行一次绩效评估,如不符合要求将会被取消器官获取资质[33]。OPO在指定的服务区域内开展工作,当发现潜在捐献者时,通过UNOS配对查询系统按照规定进行器官分配[8]。
根据TPG规定,潜在捐献医院和移植中心、协调单位德国器官获取组织DSO以及国际欧洲器官分配机构Eurotransplant三方必须积极参与死亡器官捐献工作。
潜在捐献医院的任务是根据德国医学会的指导方针对潜在捐献者进行脑死亡诊断,与患者家属进行沟通,并在征得器官捐献同意时通知最近的DSO手术中心,将潜在捐献者移交给DSO完成捐献器官获取。为保证随时为所有德国医院提供快速支持,DSO将德国划分为7个服务区,每个服务区包括一个或几个联邦州,每个地区的器官捐献由DSO执行医师领导的区域协调中心组织,并对DSO协调器官捐献过程中涉及的所有步骤提供一系列服务和支持。对潜在捐献者进行初步评估后,DSO会将所有相关数据发送给Eurotransplant,再由Eurotransplant通过分配系统匹配受者。一旦确定受者,Eurotransplant就会与DSO和捐献医院的协调员一起协助器官获取的准备工作,DSO也负责将获取的器官运送到接受器官的移植中心。捐献过程中产生的人员和耗材费用则由DSO负责报销[54]。
韩国的器官分配由KONOS负责,由KODA和医院器官获取组织(Hospital-based Organ Procurement Organization,HOPO)(指定为维护疑似脑死亡患者的特殊医疗机构)进行器官获取[55]。韩国有47家KODA签约医院和36家HOPO。在HOPO中,脑死亡器官捐献的流程在潜在捐献者诊断为脑死亡后就开始了,而KODA是签约医院向其报告发现脑死亡患者后才进入器官捐献流程,当KODA接到疑似脑死亡患者的报告时,会立即派遣协调员参与器官捐献事宜。协调员协助评估脑死亡、脑死亡捐献者的维护、器官和组织的获取以及相关善后事宜[14]。
日本目前尚未建立全国统一的OPO。器官获取、分配由日本器官移植网络(Japan Organ Transplant Network,JOTNW)负责[56],由于日本的国土面积相对较小,交通运输相对便利,一旦确定了捐献器官的接受者,JOTNW指定移植医院派出获取团队前往捐献医院进行获取[15,16]。
值得一提的是,日本设立了JOTNW、县、捐献医院3个层面的获取移植协调员(procurement transplant coordinators,PTC)。JOTNW-PTC需要完成在移植等待名单中选择合适受者、协调实验室完成配型、与移植中心保持沟通并安排运送获取团队和捐献器官等工作。县PTC主要负责公众教育和扩大潜在捐献医院的数量,保证捐献过程的合法性。大多数县会委托捐献医院的工作人员担任院内PTC,开展院内日常器官捐献与移植相关活动,协调完成器官获取,必要时协助JOTNW-PTC、县PTC征得家属的器官捐献同意。三个层面PTC在增加器官捐献和使获取过程顺利进行等方面发挥着重要作用[17]。
伊朗实施器官捐献和移植的部门是器官获取单位(Organ Procurement Unit,OPU)和识别中心(Recognition Center,RC),是由卫生部指定的在规定区域内提供器官捐献获取服务的部门,目前已覆盖了伊朗所有地区。OPU主要负责发现脑死亡患者、协调捐献者评估、捐献者管理、器官获取以及开展家属咨询。RC是OPU的组成部分,主要负责开展脑死亡判定、捐献者管理以及征询家属捐献同意。一旦征得捐献同意,RC会把捐献案例转介给OPU以完成器官捐献和获取。所有OPU和RC都有设置ICU的医院,用于潜在捐赠者管理,器官获取仅在OPU中进行。伊朗目前设立了114个国家器官捐献和移植单位,包括24个OPU、31个RC和59个移植单位[18]。
2001年,为完善器官获取体系,伊朗建立了伊朗移植器官获取网络(Iranian Network for Transplant Organ procurement,IRANTOP)。IRANTOP的主要工作包括器官移植登记、器官分配和财务管理等,共设立了7个团队,包括脑死亡识别团队、脑死亡判定团队、器官获取团队、重症监护室和善后团队、器官分配委员会、组织配型实验室团队以及统计和研究团队,各团队相互配合完成器官捐献分配相关工作[57]。
纵观世界上目前PMP较高的国家,器官捐献与移植事业的发展无不建立在坚实的捐献移植法律与制度的基础之上(表1),通过制定符合国情的捐献同意政策和建立有利于器官捐献与移植事业发展的相关组织机构,开展培训和宣传赢得民众对捐献体系和器官捐献事业的信任,同时配备较充裕的资金支持,形成较为完善的器官捐献与获取体系,推动器官捐献与移植事业的持续发展。但是也要看到体系的完善是逐步进行的,例如西班牙早在1979年就开始了器官捐献和移植计划,但是"西班牙模式"的核心包括器官捐献三个层面的管理、设立器官捐献协调员以及开展相关培训,都是在随后30年内逐步建立的[30,53,58]。因此,在不断优化体系的同时,相关政策的适时调整和持续实施,也是实现器官捐献与移植事业的可持续发展的重要保障。我国即将正式实施的《人体器官捐献和移植条例》,将全面促进我国器官捐献和移植制度体系化建设[59]。
西班牙在公民逝世后器官捐献领域所取得的巨大成功,被多个国家(地区)竞相效仿,部分国家(地区)通过引入"西班牙模式",在器官捐献方面也获得了长足的进步,例如意大利和韩国等[39,60]。这些国家在引入"西班牙模式"核心制度的相关要素后,建立了符合本国国情的国家和医院层面的器官捐献获取机构,通过设立全职或兼职器官捐献协调员在潜在捐献医院开展器官捐献协调工作,为第一时间发现潜在捐献者赢得了机会。
"美国模式"的成功在于其器官捐献体系经过多年发展已较为成熟,设立了专业机构,并构建了专业团队,还具有较为清晰的财务管理制度,为组织建设和工作开展提供了保障[34,61]。
我国的OPO仍处于发展阶段,在器官捐献与移植的"中国模式"下,我国已初步建立起省级独立OPO(独立法人)、全省统一OPO(挂靠医疗机构)、联合OPO、医疗机构OPO等4种模式的OPO,但是与起步较早的西班牙、美国比较,我国OPO的建设与管理还处于初级阶段,还需要进一步规划、规范和逐步完善[62]。
西班牙、美国、韩国的经验提示我们,通过对医疗卫生相关专业人员进行培训和对公众加强器官捐献理念宣传是提高捐献同意率的有效方法。潜在捐献医疗机构的工作人员,如急诊科、神经内科、ICU、社工部等科室的医护人员,既有一定的专业知识和素养,也熟悉当地文化,更容易与家属建立信任关系,在开展器官捐献工作中更有优势[63]。通过对上述专业人员进行捐献相关法律法规、捐献流程相关知识、沟通能力等方面的培训,一方面能帮助他们更好地完成器官捐献相关工作,另一方面可以潜移默化地使他们在工作中对公众产生积极的引导作用。此外,以不同形式开展器官捐献与移植知识、典型案例宣传,增加公众对器官捐献与移植事业的了解,弘扬社会正能量,有助于增强公众对器官捐献与移植体系的信任感,有利于在社会上形成支持器官捐献的文化氛围。
我国早在2013年5月就与西班牙DTI签订了合作协议[64],开展为期5年的器官获取组织专业培训合作项目以获取国外的先进经验。同时,从2022年开始,国家人体捐献器官获取质量控制中心在全国多地举办了器官捐献源头培训班,对潜在捐献医院各相关科室医护人员进行器官捐献政策、供体发掘、供体评估维护、家属沟通等方面培训,此类培训项目的开展为我国宣传器官捐献和发展器官捐献培训探索了新的途径。
综上所述,没有器官捐献就没有器官移植,供体器官短缺已经成为制约器官移植事业发展的瓶颈。我国器官捐献事业起步较晚,与国外器官捐献与移植事业较发达国家存在一定差距。尽管我国器官捐献与移植数量已经处于国际第二位,但PMP与欧美发达国家尚存在差距。我们必须借鉴器官捐献发达国家的经验,发挥我国政治优势,结合我国国情,创建国际认可的中国器官捐献与移植模式,通过优化和完善器官捐献与移植体系,推动我国器官捐献与移植事业健康、快速、高质量发展。
所有作者声明不存在利益冲突