
子痫前期是引起孕产妇死亡、医源性早产、围产儿死亡的重要原因之一。半个多世纪前就有学者发现使用低剂量阿司匹林可以降低高危孕妇子痫前期的发生率,此后关于阿司匹林预防子痫前期的研究在全球范围内不断出现。目前的研究证实,阿司匹林可预防子痫前期的发生,但如何进一步探究其预防作用机制、如何规范使用阿司匹林以期达到理想的效果,仍是母胎医学的研究方向,尤其是应该从阿司匹林预防子痫前期的研究得到启发,探索老药新用在产科重大疾病的预防和治疗前景。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
妊娠期高血压疾病一直是产科难题之一,其发病机制的复杂性导致了现阶段对子痫前期的筛查、预防、治疗的认识仍不清晰。而作为全球范围内古老的药物之一,阿司匹林在目前的研究中已被证实能够预防子痫前期发生。回顾阿司匹林的历史,最早的文献记载能追溯到公元前1534年[1],在埃及《纸莎草卷》中记载了从柳树中提取出阿司匹林相关化合物(柳树提取物)来治疗头痛。数千年后,即1828年,来自德国的Johann Buchner才提纯了这种化合物的活性成分,并命名为水柳素。随着研究的不断深入,1978年在《柳叶刀》上首次发表了阿司匹林与产科相关的病例报道,将阿司匹林与子痫前期的预防联系起来,而后Vane Samuelsson和Bergström共同阐明了阿司匹林的药理机制,并借此研究于1982年获得了诺贝尔奖,至此关于阿司匹林的传奇正式启程[2, 3]。在随后的40年时间里,全球范围内不断涌现出更多关于阿司匹林预防子痫前期的研究[3]。
子痫前期的发病机制涉及遗传、免疫和环境因素相互作用导致的母胎界面异常,其中滋养层细胞侵袭障碍和螺旋小动脉重铸异常是重要的发病原因之一。这种异常会导致血管生成和抗血管生成因子失衡、内皮细胞功能障碍、血管阻力增加、血小板聚集增强和凝血系统激活,进而激活环氧合酶(cyclooxygenase,COX),导致血栓素A2(thromboxane A2,TXA2)水平升高、内皮细胞前列环素(prostacyclin,PGI2)水平降低[3]。
早在1978年就有回顾性研究提出了阿司匹林在子痫前期预防中的有效性[4],但其作用机制经历了半个世纪的研究仍不清晰。根据现有研究分析,阿司匹林作为一种非甾体类的抗炎药物,可抑制前列腺素(prostaglandin,PG)生物合成所必需的2种COX同工酶,即COX-1和COX-2。阿司匹林对COX的影响是剂量依赖性的,小剂量(<300 mg/d)阿司匹林对PG和PGI2的影响极小,会优先抑制COX-1,使其不可逆地乙酰化[3,5],导致TXA2生成和血小板聚集减少,进而改善胎盘循环,降低胎盘梗死风险[6]。研究发现阿司匹林可抑制核因子-κB依赖的miR-155宿主基因表达,增加一氧化氮合酶表达,诱导一氧化氮释放,从而产生血管舒张和抗炎作用[7]。Lin等[8]的研究发现,阿司匹林可以通过人滋养层细胞和内皮细胞中的JNK/AP-1通路,减少缺氧诱导的可溶性fms样酪氨酸激酶-1的释放,下调缺氧引起的细胞凋亡,提升滋养细胞的增殖侵袭能力。考虑到子痫前期发病机制的复杂性,阿司匹林的预防作用应该是上述提到的多途径联合作用的效果[9]。
进入循证医学时代后,开展了更多关于阿司匹林预防子痫前期的研究。2017年发表了一项多中心、双盲、安慰剂对照研究,在欧洲6个国家的13所医院招募了1 776例子痫前期高风险孕妇,随机分为安慰剂组和150 mg阿司匹林组,从妊娠11~14周开始至妊娠36周结束,研究证实使用阿司匹林可降低子痫前期的发生率,其中早发型子痫前期的发生率降低了62%(1.6%与4.3%;OR=0.38,95%CI:0.20~0.74)[10]。对阿司匹林预防子痫前期试验数据的二次分析也证实了阿司匹林的预防效果,但也发现阿司匹林不能显著降低慢性高血压孕妇发生子痫前期的风险,推测这可能与慢性高血压患者妊娠前已经存在的血管内皮损伤有关[11]。Richards等[12]在2023年发表的一项系统综述分析提示慢性高血压孕妇使用阿司匹林预防子痫前期效果并不显著,但可改善早产、新生儿的预后。实际临床工作中,大部分医师仍会对慢性高血压孕妇使用阿司匹林进行预防治疗。
Wright等[13]对既往发表的多中心研究数据进行了二次分析,结论认为针对高危孕妇预防性使用150 mg阿司匹林,可使子痫前期发生率下降、新生儿生后住院治疗时间缩短。其中,阿司匹林组在新生儿科的平均住院时间为11.1 d,明显短于安慰剂组的31.4 d。同时需要关注到,阿司匹林的预防效果与患者服药依从性(规律按时服药)密切相关,在临床使用中,需要做好宣教,提高用药依从性[14]。
目前大部分的研究都显示阿司匹林在妊娠期使用是安全的。早在1994年妊娠期低剂量阿司匹林研究(Collaborative Low-dose Aspirin Study in Pregnancy,CLASP)协作小组(CLASP Collaborative Group)在《柳叶刀》发表了文章,提到接受低剂量阿司匹林后约10%的孕妇出现胃肠道症状,但并未增加其他不良事件(如流产、早产、感染等)的发生率[15]。后续更多的研究,无论是系统综述、meta分析,还是随机对照试验,均提示使用阿司匹林不增加胎盘早剥等妊娠期出血风险[16, 17, 18]。同时,Henderson等[19]和Duley等[16]发表的综述中也报道了阿司匹林的使用并不增加新生儿颅内出血风险。在临床应用中,服用阿司匹林后出现严重胃肠道反应、阴道出血、皮肤淤斑或鼻出血等情况偶有发生,一旦出现这些情况,应及时评估,了解血小板及凝血等功能,适时停药。严重者不建议再次尝试阿司匹林治疗。
另一方面,对于阿司匹林是否存在致畸性,Slone等[20]和Ahrens等[21]发表的多中心、随机双盲对照试验均证实无论暴露时间长短,低剂量阿司匹林均不增加胎儿畸形风险。Sibai等[22]和CLASP协作小组[23]发表的随机对照试验证实了妊娠晚期使用阿司匹林与胎儿动脉导管早闭无关。也有文献提及阿司匹林可能增加新生儿脑性瘫痪的发生风险[24],但由于是回顾性研究,阿司匹林使用的方式、剂量、频率及时间并不统一,此外,该研究也没有校正子痫前期对早产和胎儿生长受限的影响。
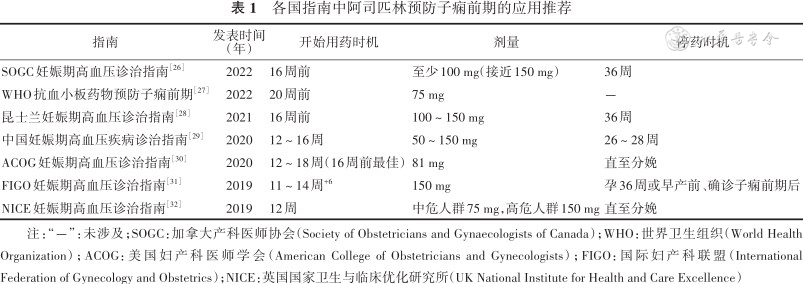
现有研究肯定了阿司匹林对子痫前期,特别是早发型子痫前期的预防效果[25],但在阿司匹林的使用时机和剂量上全球范围内尚未统一,见表1。
各国指南中阿司匹林预防子痫前期的应用推荐
各国指南中阿司匹林预防子痫前期的应用推荐
| 指南 | 发表时间 (年) | 开始用药时机 | 剂量 | 停药时机 |
|---|---|---|---|---|
| SOGC妊娠期高血压诊治指南[26] | 2022 | 16周前 | 至少100 mg(接近150 mg) | 36周 |
| WHO抗血小板药物预防子痫前期[27] | 2022 | 20周前 | 75 mg | - |
| 昆士兰妊娠期高血压诊治指南[28] | 2021 | 16周前 | 100~150 mg | 36周 |
| 中国妊娠期高血压疾病诊治指南[29] | 2020 | 12~16周 | 50~150 mg | 26~28周 |
| ACOG妊娠期高血压诊治指南[30] | 2020 | 12~18周(16周前最佳) | 81 mg | 直至分娩 |
| FIGO妊娠期高血压诊治指南[31] | 2019 | 11~14周+6 | 150 mg | 孕36周或早产前、确诊子痫前期后 |
| NICE妊娠期高血压诊治指南[32] | 2019 | 12周 | 中危人群75 mg,高危人群150 mg | 直至分娩 |
注:“-”:未涉及;SOGC:加拿大产科医师协会(Society of Obstetricians and Gynaecologists of Canada);WHO:世界卫生组织(World Health Organization);ACOG:美国妇产科医师学会(American College of Obstetricians and Gynecologists);FIGO:国际妇产科联盟(International Federation of Gynecology and Obstetrics);NICE:英国国家卫生与临床优化研究所(UK National Institute for Health and Care Excellence)
1.阿司匹林的适用人群:结合卫生经济学的考虑,采用危险因素分层方法有助于快速遴选出高危孕妇,并尽早使用阿司匹林,达到减少子痫前期发生、降低围产儿死亡率的目的[33]。目前全球比较公认的危险因素分层方式见表2。
由于早发型子痫前期临床风险的筛查灵敏度较低(41%)[34],为了提高筛查灵敏度,目前研究聚焦在生物物理标志物的开发方面,包括病史、平均动脉压、子宫动脉频谱超声、妊娠相关血浆蛋白A及胎盘生长因子等,联合这些因素进行预测可使筛查灵敏度升高至82%,是仅基于临床风险筛查灵敏度的2倍[35]。
但为了提高筛查算法的准确性或灵敏度,加入血清标志物和子宫动脉频谱超声等,导致检查费用增加、患者依从性降低,使阿司匹林的服药率降低,而阿司匹林的有效性又很大程度依赖于患者的服药依从性。有问卷调查研究显示,在需要使用阿司匹林的高危孕妇中,42%的孕妇不记得医生推荐过使用阿司匹林[36]。Krishnamurti等[37]使用手机应用程序进行调查研究,发现子痫前期高危孕妇16周前服用阿司匹林的使用率仅约46.0%。Mone等[38]进行了一项关于服用阿司匹林可行性、可接受性的多中心随机对照研究,该项研究纳入的所有孕妇均使用了阿司匹林,孕妇对于服用阿司匹林依从性超过预期,这与该研究采用低剂量阿司匹林(75 mg)有关,剂量降低后副作用较少,大大增加了孕妇接受度。
叶酸补充的历史沿革显示,开始应用时仅针对高危人群,但当其益处被更多证实后,就逐渐转为向所有人群推广。对于阿司匹林,是否也可能通过扩大使用人群来提高患者服药率,以达到更佳的预防效果?根据目前美国的数据分析,子痫前期高危孕妇超过50%,所以在孕妇人群中普遍使用阿司匹林可能更有效、更经济[39]。我国子痫前期的高危孕妇占比低于美国,且由于阿司匹林更多用于抗血小板聚集、而非广义上的预防[40],故从实用角度出发,仍然推荐病史结合生物标志物的筛查。
2.阿司匹林的使用时机:2017年Roberge等[41]对既往45项关于阿司匹林预防子痫前期的试验进行了汇总分析,证实阿司匹林能有效降低子痫前期、尤其可降低早发型子痫前期发生风险(RR=0.62,95%CI:0.45~0.87),但不能显著降低足月子痫前期的发生(RR=0.92,95%CI:0.70~1.21)。值得注意的是,该研究提出阿司匹林只有在孕16周前服药且剂量≥100 mg时对于降低子痫前期发生风险才有效(RR=0.33,95%CI:0.19~0.57)。而阿司匹林预防子痫前期随机试验(ASPRE)[42]是一项多中心研究,共纳入25 797例孕妇,其中高危孕妇在孕11~14周开始服用阿司匹林直至孕36周,显著降低了子痫前期发生风险,其中早发型子痫前期风险降低约60%。所以目前欧美国家指南多采用孕16周前作为最佳用药时机,这也符合目前对妊娠、胎盘发育的认识,因为胎盘主要在孕16~18周时完成发育,故在胎盘发育完成前使用阿司匹林更有效。
而Meher等[43]在meta分析中,纳入了31项随机对照试验共32 217例孕妇的数据,由于孕妇个体数据异质性很大,进行相关校正后分析发现,在子痫前期发生率、围产儿死亡率、<34周早产率、胎儿生长受限发生率方面,孕16周前后与孕20周前后使用阿司匹林的疗效并无明显差异,也未增加大出血或胎盘早剥风险。综上考虑,在孕妇明确有高危因素后,都应及时使用阿司匹林进行预防性治疗。
针对孕期阿司匹林的使用,Chaemsaithong等[34]进行了meta分析,结果显示尝试妊娠11周前开始使用阿司匹林治疗,并没有显著降低子痫前期的风险。值得注意的是,纳入的试验中只有2项试验的阿司匹林剂量为100 mg,其余试验的剂量均小于100 mg。所以不能明确是使用时间过早(孕早期),还是因为剂量过小不足以产生预期效果,因此阿司匹林孕早期应用的有效性尚不明确,且临床医生担忧可能增加孕早期出血风险,故暂未推荐。
3.阿司匹林的服药时间:Ayala等[44]的前瞻性、随机、双盲、安慰剂对照试验共纳入了350例高危孕妇,发现睡前服用阿司匹林对动态血压的调节作用更显著,并可降低子痫前期、妊娠期高血压、早产及胎儿生长受限的发生率。目前研究分析表明,清晨服用阿司匹林的吸收清除率高,不利于阿司匹林更好发挥作用,而且PGI2和TXA2的产生具有昼夜节律模式,睡前服药更契合这种节律性。同时另一项研究显示,相较于晨起服药,睡前服用阿司匹林对血压、血浆肾素活性,以及24 h尿液中皮质醇、多巴胺和去甲肾上腺素等的影响更小[45]。
4.阿司匹林的使用剂量:在几个大型、多中心、随机对照试验中,低剂量阿司匹林预防子痫前期的给药方案各不相同。1994年的分组试验(CLASP协作小组)共包括近7 000例有高危因素的孕妇,没有发现低剂量阿司匹林与子痫前期发生率降低的关联性,但后续的分析中显示该结果与受试者接受的阿司匹林剂量过小有关(60 mg)[15]。随着全球肥胖率的不断攀升,一项使用60 mg阿司匹林预防子痫前期治疗的大型随机对照试验中,数据二次分析后发现同样剂量阿司匹林对于肥胖孕妇的COX-1抑制率明显低于正常体重孕妇,揭示了阿司匹林的剂量依赖作用[46]。近年来越来越多的研究提出,大于100 mg的阿司匹林可提高COX-1的抑制率和预防子痫前期的有效率。Rolnik等[10]进行的一项前瞻性双盲对照研究显示,应用150~162 mg阿司匹林比75~81 mg更有效;150 mg阿司匹林组早发型子痫前期风险减少62%,早产率和小于胎龄儿发生率也有所降低。2022年《美国妇产科杂志》针对妊娠期高血压进行的专题讨论中也提出了81 mg剂量的问题(美国阿司匹林的剂型为每片81 mg),目前美国也正在开展高危孕妇使用162 mg阿司匹林(2片)预防子痫前期的前瞻性对照研究(NCT04070573、NCT05514847)。
低剂量阿司匹林预防子痫前期的另一个挑战是耐药性问题。如何诊断阿司匹林耐药,尚无统一标准。依从性差、服用其他影响阿司匹林吸收药物、同时服用其他非甾体抗炎药物是常见引起阿司匹林耐药的原因。排除这些干扰因素后,有研究提示阿司匹林耐药中有1/3是受到基因表型影响,参与编码阿司匹林机制的各种蛋白的基因变异可能导致活性药物浓度的差异[47]。Caron等[48]进行的一项前瞻性对照研究发现,孕妇使用阿司匹林81 mg后检测血小板功能无变化,剂量增加为162 mg后出现了血小板功能改变,耐药孕妇约下降到4%。这似乎提示增加阿司匹林的剂量可以减少耐药性发生。另一方面,阿司匹林耐药性与基因多态性的相关研究也是目前研究的重点及方向,后续有待更多的数据以指导临床,做到个体化评估和治疗,以达到更好预防子痫前期的目的。但对于是否存在阿司匹林耐药情况,临床并无有效监测手段,在内科心血管事件预防中,若定期摄入阿司匹林仍发生阻塞性心血管事件,会通过检测COX-1活性来判断是否存在阿司匹林耐药(COX-1持续具有活性是阿司匹林耐药标志),或者使用0.5~1.6 mg/ml花生四烯酸作为激动剂检测血小板聚集是否≥20%。而这些方法似乎并不适用于产科,在临床中做好患者宣教、增强用药依从性及减少其他药物对阿司匹林药效的影响是更有效的方式。但对于部分前次妊娠规律服用阿司匹林后仍发生高血压相关不良孕产史的孕妇,此次妊娠可以尝试增加剂量、更换剂型(肠溶型改为非肠溶型)、甚至进行COX-1活性检测等方式,防止不良事件再次发生。
目前关于阿司匹林应用效果的数据大部分来自于欧洲或美国的队列研究。正如前文所述,阿司匹林的效果具有剂量依赖,而我国孕产妇平均体重指数低于欧美孕产妇,因此国内对阿司匹林的应用是否需达到150 mg甚至更高剂量,仍然是需要探究的问题。现有的证据表明重度肥胖以上(体重指数>35 kg/m2)的孕产妇使用100 mg阿司匹林的有效抑制率低。而我国目前处于重度肥胖以上的孕产妇并不多见,仅从剂量依赖角度考虑,中国孕产妇服用100 mg足矣。Tolcher等[49]在2020年发表了随机对照研究,证实了基因多态性对阿司匹林效果的影响,该研究按族裔(西班牙裔、非西班牙裔白人、非西班牙裔黑人或其他)进行分层,结果显示阿司匹林对非西班牙裔白人妇女具有预防效果,而对西班牙裔或非西班牙裔黑人妇女没有明显预防效果。但2022年杨慧霞教授的团队发表的子痫前期高危孕妇的多中心研究[50]的分析结果显示,我国从孕12周开始至34周,每天服用100 mg阿司匹林并不能降低高危孕妇子痫前期的发生率。这一结果出乎意料。查阅了原文数据,发现阿司匹林对于慢性高血压患者并未显示出良好的预防效果,与前文提到的有效性研究中的结论类似。排除慢性高血压后的二次分析,发现对于1期高血压[130~139/80~89 mmHg(1 mmHg=0.133 kPa)]孕妇,阿司匹林具有良好预防效果。因此,在剂量依赖之外,是否有其他因素(如耐药性、族裔、高血压类型等)影响阿司匹林的效果,今后可尝试观察增加阿司匹林使用剂量后能否达到预期预防效果,同时是否应该扩展阿司匹林应用人群以达到更佳预防效果(如纳入1期高血压),期待更多的研究结果。
5.阿司匹林的停药时机:针对阿司匹林停药时机的研究甚少。大量研究表明,阿司匹林使用中出血、新生儿并发症相关的不良结局等均未增加[16,18, 19];并且美国局部麻醉和疼痛医学学会指南指出,低剂量阿司匹林不会增加脊髓硬膜外穿刺后的血肿发生风险[51],所以目前美国妇产科医师学会建议阿司匹林可使用至分娩前停药,或发生了早发型子痫前期时停药。我国在2017年更新的“椎管内阻滞并发症防治专家共识”[52]中,也提及单独服用阿司匹林并不影响硬膜外麻醉实施,也不增加麻醉部位血肿风险。但考虑到孕36周后或子痫前期发生后随时有终止妊娠的可能,而短时间内继续使用阿司匹林能否带来额外获益有待商榷,所以临床实践中多数仍然选择在孕34~36周停用阿司匹林。确切的最佳停药时机还需要更多的循证证据以便进行推荐。
阿司匹林对子痫前期的预防效果和对母儿的安全性已得到证实。结合我国最新“妊娠期高血压疾病诊治指南(2020)”[29],在孕早期对高危孕妇进行识别,采用母体因素、平均动脉压、子宫动脉多普勒、血清胎盘生长因子等联合筛查可提高子痫前期预测率。根据现有数据,阿司匹林预防用药的最佳启动时机是孕12~16周,每日用量100~150 mg,可将子痫前期、特别是早发型子痫前期的发病率降低60%以上。当发生了子痫前期、早产不可避免或妊娠达36周时,考虑停药,但仍需要更多研究论证,同时重视与孕妇沟通,提高用药的依从性。
李健鑫, 陈真, 漆洪波. 阿司匹林预防子痫前期:从证据到应用规范[J]. 中华围产医学杂志, 2024, 27(4): 265-271. DOI: 10.3760/cma.j.cn113903-20240115-00024.
所有作者声明无利益冲突




























