支气管哮喘(哮喘)是常见的慢性呼吸道疾病。全球哮喘的发病率逐年升高,中国哮喘的发病率同样呈逐年上升趋势,给患者和社会均造成了沉重的负担。哮喘的规范化诊断和治疗对于提高哮喘的控制水平,改善患者生活质量具有重要作用。随着哮喘基础研究的持续推进、循证证据不断涌现,哮喘的诊治策略不断完善。本文综述了2022年10月1日至2023年12月31日哮喘研究的进展和成果,以及多个指南和共识对哮喘指导意见的更新,为哮喘的发病机制、诊断和评估、以及治疗提供临床视角的思考。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
支气管哮喘(哮喘)是一种异质性疾病,通常以慢性气道炎症为特征,包括随时间不断变化和加剧的呼吸道症状如喘息、气短、胸闷和咳嗽,同时伴有气道高反应性(airway hyperresponsiveness,AHR)和可变性的呼气气流受限[1]。全球范围内,1990-2019年哮喘发病例数增加了15%,但死亡人数和伤残调整生命年(disability adjusted life year,DALY)有所下降[2]。根据《中国卫生统计年鉴》的调查结果,2011-2020年,我国哮喘总体患病率呈上升趋势,发病率存在地区差异,沿海地区发病率较高[3]。在1~19岁儿童和青少年(根据WHO定义,青少年的年龄界限为10~19岁[4])哮喘患者中观察到类似的结果,发病率和患病率上升,死亡率下降[5]。本文对2022年10月1日至2023年12月31日国内外发表的关于哮喘发病机制、诊断和评估,以及治疗进展的研究文献进行年度综述,以更好地结合实际,用于临床实践。
随着对哮喘发病机制的认识日益加深,哮喘炎症表型分类已经成为了哮喘领域备受瞩目和深入研究的焦点。2022年发表的《2型炎症性疾病机制及靶向治疗专家共识》[6]及2023年发表的《白细胞介素-4受体靶向治疗2型炎症性疾病临床应用中国专家共识(2023年版)》[7]、2023年版全球哮喘防治创议(global initiative for asthma,GINA)[1]依据是否存在2型炎症将哮喘分为:2型哮喘和非2型哮喘。
哮喘作为一种复杂的异质性疾病,包含多种临床表现(表型)和潜在的病理生理机制(内型)[8]。近几年发表的国内共识与GINA2023依据"免疫-炎症"介导特征将哮喘分为2型哮喘和非2型哮喘。根据这一炎症分型方法,2型哮喘包括过敏性哮喘、嗜酸粒细胞性哮喘与阿司匹林诱导加重性哮喘,非2型哮喘包括中性粒细胞性哮喘、寡粒细胞性哮喘与肥胖性哮喘[8,9]。
2型哮喘是一类以气道2型炎症为特征的哮喘,50%~70%的哮喘患者具有2型炎症特征[7,10]。机体暴露于环境刺激或过敏原时,一方面抗原提呈细胞如树突状细胞(dendritic cell,DC)可促使初始T细胞分化为2型辅助性T细胞(T helper 2 cell,Th2),另一方面来源于气道上皮的预警素可以活化2型固有淋巴细胞(type 2 innate lymphoid cell,ILC2)。Th2和ILC2产生的2型细胞因子IL-4、IL-5和IL-13等可介导2型炎症,通常以嗜酸性粒细胞(eosinophils,EOS)或呼出气一氧化氮(fractional exhaled nitric oxide,FeNO)水平升高为特征,伴或不伴有特应性[1,7]。IL-4与IL-13是2型哮喘的关键核心细胞因子。IL-4促进初始T细胞分化为Th2,产生2型细胞因子IL-4、IL-13和IL-5,由此形成正反馈循环,IL-13在改变气道平滑肌功能、黏液高分泌和气道重塑上发挥重要作用[7]。目前对非2型哮喘发病机制的了解有限,普遍认为上皮细胞来源的预警素可激活非2型炎症,其与Th1或Th17免疫反应相关。1型辅助性T细胞(T helper 1 cell,Th1)与17型辅助性T细胞(T helper 17 cell,Th17)能够产生募集中性粒细胞的细胞因子,如γ干扰素(interferon-γ,IFN-γ)与IL-17,进而参与非2型哮喘的发病机制,如中性粒细胞炎症与气道重塑[9]。此外,非2型哮喘还与3型固有淋巴细胞(type 3 innate lymphoid cell,ILC3)的激活相关[11]。非2型哮喘通常以中性粒细胞水平升高为特征,且不伴有2型生物标志物的升高[1,9]。
在过去一年多中,2型炎症和非2型炎症途径上的新靶点、新发现不断涌现,已经成为哮喘治疗新药研发的焦点和热点。IL-4受体α(IL-4 receptor α,IL-4Rα)是2型细胞因子IL-4受体与IL-13受体的共享亚基,目前已认为是治疗2型哮喘的重要靶点[7]。此外,胸腺基质淋巴细胞生成素(thymic stromal lymphoprotein,TSLP)、IL-33、IL-25等预警素在多个炎症级联反应中处于上游的地位,因此可视为一种有效的哮喘治疗靶点[12]。2型哮喘未来还可以探索的治疗靶点包括IL-31、IL-22、嗜酸性粒细胞的胞外陷阱(eosinophil extracellular traps,EETs)、S100钙结合蛋白A4(S100 calcium binding protein A4,S100A4)与胎盘生长因子(placental growth factor,PlGF)等;而非2型哮喘则集中在IL-6、IL-17等靶点[13,14,15,16,17,18,19,20]。
针对IL-4Rα靶点的药物与针对IL-4或IL-13单个靶点的药物不同,具有"双特异性":抗IL-4Rα抗体通过与IL-4Rα特异性结合,可同时阻断IL-4/IL-13的信号传导,并抑制2型细胞因子的释放,改善气道平滑肌功能、黏液高分泌和气道重塑等,从而减轻2型哮喘的炎症反应[7]。IL-4Rα已被认为是治疗2型哮喘的重要靶点,目前已有多项研究探索抗IL-4Rα抗体在2型哮喘中的临床获益[7]。
预警素IL-33可通过ILC2加剧哮喘,因此抗IL-33抗体可能是治疗2型哮喘的有效方法[13]。IL-31是一种Th2相关细胞因子,其受体IL-31RA主要在非造血上皮细胞和平滑肌细胞中表达,在过敏性哮喘中,IFN-γ、IL-4和IL-13均上调平滑肌细胞和肺中的IL-31RA,而不上调IL-31[14],因此抗IL-31RA抗体可能是未来靶向哮喘AHR的新兴疗法。IL-22可在2型哮喘中发挥促炎作用[15],有望成为治疗2型哮喘的重要靶点。
除此之外,目前正在探索其他针对2型哮喘的潜在治疗靶点:由DNA、组蛋白和颗粒蛋白组成的网状结构EETs可与ILC2相互作用并进一步激活固有免疫反应,加剧2型炎症,因此可作为重度哮喘的潜在生物标志物[16];S100A4是一种炎症因子,可引起上皮屏障功能障碍、气道炎症与2型细胞因子的分泌,可作为哮喘气道上皮屏障功能障碍的潜在治疗靶点[17];PIGF是一种糖基化二聚体蛋白,参与促进2型细胞因子的分泌和增加血管通透性,还可通过增强2型免疫反应和加重气道水肿来促进AHR,抑制PIGF可减轻或减缓哮喘相关的病理变化[18];前列腺素D2、白三烯E4和碳-碳趋化因子26在重度2型哮喘患者痰液中均有所增加[19],未来可作为治疗重度2型哮喘的新兴靶点。
非2型哮喘的研究靶点在过去的一年多中进展较少,目前暂无特异性治疗方法[21]。U-BIOPRED队列研究分析了哮喘患者痰样本的转录组和蛋白质组表达,确定非2型哮喘以中性粒细胞为主;还通过基因组变异分析,确定了由IL-6反式信号转导通路驱动、或由IL-6、IL-17和IL-22通路驱动的特定分子表型与混合粒细胞或中性粒细胞炎症有关。针对这些特定分子表型的生物疗法可能是非2型哮喘治疗策略之一[20]。
在过去一年多中,诸多关于哮喘检查和评估的工具呈现了新进展,助力完善哮喘临床管理实践,为哮喘患者提供更准确和个性化的诊疗方案。
过去一年多中,新兴的检查装置也有了进展。2023年ATS年会提出,脉冲振荡仪(impulse oscillometry,IOS)检查技术是一种无创、非用力依赖的测量气道阻力等呼吸系统力学特性的方法[22],基线IOS测量可能有助于检测AHR[23]。另外,IOS检测比肺活量检测更易发现小气道功能障碍的哮喘患者[24],且对于无法完成肺量计检查等传统肺功能检查的受检者,如老年人、儿童和重症患者,IOS似乎是一个不错的选择[22]。
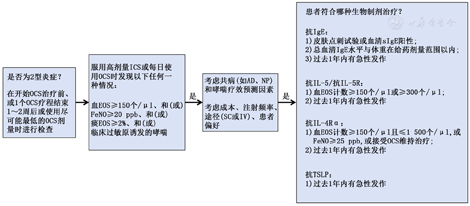
目前哮喘临床常用的2型炎症生物标志物包括血/痰EOS、FeNO、血清总免疫球蛋白E(immunoglobulin E,IgE)、过敏原特异性IgE(specific IgE,sIgE)和血清骨膜素等。GINA 2023指出,重度哮喘患者出现以下任何一种情况,即可判断为2型炎症:(1)血EOS≥150/μl、和(或)(2)痰EOS≥2%、和(或)(3)FeNO≥20 ppb、和(或)(4)哮喘由过敏原引起[1]。2型炎症生物标志物的评估对于指导难治性、重度哮喘的治疗决策至关重要(图1)。
哮喘肺功能检测包括第1秒用力呼气容积(forced expiratory volume in one second,FEV1)、呼气流量峰值(peak expiratory flow,PEF)、用力肺活量(forced vital capacity,FVC)等,其中FEV1占预计值百分比(FEV1%pred)是评估未来风险的重要组成部分[1]。已有研究显示,基线FEV1%pred水平与重度急性发作风险上升相关,表明基线肺功能是预测未来哮喘急性发作的重要因素[25]。
此外,哮喘的评估还可以结合肺功能与2型炎症标志物。当肺功能FEV1受损与2型炎症生物标志物升高相结合时,可观察到哮喘控制不佳的风险上升:如FEV1受损与FeNO水平升高结合时哮喘控制不佳的风险上升至81%,与IgE水平升高结合时可上升至75%,与血EOS水平升高结合时可上升至74%[26]。
历史性队列研究已经表明,对于哮喘患者,尤其是基线血EOS计数水平较高的哮喘患者,高剂量ICS无法有效预防需要口服糖皮质激素(oral corticosteroids,OCS)治疗的哮喘急性发作,因此生物制剂已成为了新的治疗决策[29]。在过去一年多中,生物制剂在重度哮喘患者中的应用已积累了丰富的循证依据。生物制剂治疗2型哮喘患者均可降低哮喘急性发作,改善肺功能,且具有良好的安全性[30]。此外,目前有多种其他新型治疗药物正在进行临床研究,结果仍待发表。
一项在亚太地区成人和青少年哮喘患者中进行的关键Ⅲ期临床研究(NCT03782532),旨在探索度普利尤单抗在亚太地区,尤其是中国哮喘患者中的疗效与安全性。2023年ATS年会公布了中国人群亚组分析结果,研究共纳入347例12岁及以上青少年与成人、经中高剂量ICS联合其他控制药物治疗后仍控制不佳、具有2型炎症特征的哮喘患者,按1∶1的比例随机给予度普利尤单抗(n=173)或安慰剂(n=174)治疗。研究结果表明,无论伴或不伴OCS治疗,与安慰剂相比,度普利尤单抗治疗12周显著改善FEV1(120 ml比460 ml,P<0.000 1),治疗24周显著改善ACQ-5评分(-1.13分比-1.32分,P=0.020 6),且度普利尤单抗24周治疗期间,年哮喘急性发作率显著降低74%(P=0.000 2)。该研究证实了度普利尤单抗在中国哮喘患者中的获益[31]。
度普利尤单抗开放标签扩展研究(TRAVERSE)已证实,无论基线哮喘急性发作史或基线ICS用量如何,度普利尤单抗在中重度2型哮喘或OCS依赖性哮喘患者中具有长达3年的获益,降低年哮喘急性发作率,并持续改善肺功能,减少OCS用量[32,33]。此外,Domingo等[34]在TRAVERSE事后分析研究中证实,度普利尤单抗在OCS依赖性重度哮喘患者中的获益可持续3年。TRAVERSE继续研究(TRAVERSE continuation study)进一步证实了度普利尤单抗长达6年的安全性,TRAVERSE研究中393例患者继续参与了长达3年的后续观察研究,其长期安全性结局与既往度普利尤单抗关键临床研究中的安全性特征一致,这些结果进一步支持了在中重度哮喘患者中长期使用度普利尤单抗[35]。
在真实世界环境下,度普利尤单抗治疗中重度哮喘患者的获益同样已被证实。Blaiss等[36]进行的回顾性研究中,共纳入2 400例接受度普利尤单抗附加治疗的美国患者,随访至患者死亡、转换为其他生物制剂治疗或至少1年。研究结果表明,启动度普利尤单抗治疗后,与未接受治疗的患者相比,哮喘急性发作风险降低44%(P≤0.000 1),系统性糖皮质激素(systemic corticosteroids,SCS,包括ICS与OCS[37])用量降低48%(P≤0.000 1),且新型冠状病毒感染发生率更低(P≤0.000 1)。
度普利尤单抗对于哮喘共病患者同样具有良好疗效。TRAVERSE研究亚组分析显示,与安慰剂相比,无论伴或不伴慢性鼻窦炎伴鼻息肉(chronic rhinosinusitis with nasal polyps,CRSwNP),度普利尤单抗治疗后哮喘患者的急性发作减少,肺功能、哮喘控制和生活质量评分均有所改善,且疗效维持3年[38]。
2023年ATS年会还更新了美泊利珠单抗中国Ⅲ期研究(NCT03562195),旨在评估美泊利珠单抗在中国哮喘人群中的疗效与安全性。研究共纳入300例中国重度嗜酸粒细胞性哮喘患者,结果显示,治疗第52周,与安慰剂相比,美泊利珠单抗治疗后哮喘急性发作率降低65%(P<0.001),圣乔治呼吸问卷(St.George′s Respiratory Questionnaire,SGRQ)评分改善(-7.20分比-14.29分,P=0.001),FEV1值改善(125.67 ml比262.79 ml,P=0.006),且安全性良好[39]。此外,已有研究证实美泊利珠单抗在重度嗜酸粒细胞性哮喘患者中疗效可维持4年,但直到研究数据截止时,47%的患者选择改用其他生物制剂或停止生物制剂治疗[40]。美泊利珠单抗的长期临床应用仍需要更大样本、更长时间的研究提供支持。
一项真实世界研究旨在评估本瑞利珠单抗在重度哮喘患者人群中的长期疗效。研究共纳入44例OCS依赖性重度哮喘。研究结果显示,本瑞利珠单抗治疗2年后,59.4%的患者停用OCS,继续使用OCS的患者平均剂量比基线减少了约85%。同时,85%的患者哮喘得到控制(ACT评分>20)且没有哮喘急性发作,41.6%的患者肺功能正常,表明本瑞利珠单抗2年疗效良好[41]。
奥马珠单抗中国真实世界研究评估了其在过敏性哮喘患儿中的有效性与安全性。该研究共纳入200例6~11岁过敏性哮喘患儿。研究结果表明,中重度过敏性哮喘患儿急性发作率每年降低了(2.00±5.68)次/人(P<0.001),中位ICS日剂量降低至0 μg,FEV1%pred改善至(92.80±10.50)%,且其安全性良好[42]。此外,奥马珠单抗在过敏性哮喘患者中疗效长达5年,且肺功能持续改善,OCS用量减少[43]。
特泽鲁单抗关键Ⅲ期NAVIGATOR研究与Ⅱb期PATHWAY研究汇总分析评估了其在控制不佳的重度哮喘患者中的获益。研究共纳入1 334例控制不佳的重度哮喘患者,按1∶1随机分为安慰剂组(n=669)或特泽鲁单抗组(n=665)。研究结果表明,与安慰剂相比,特泽鲁单抗治疗52周后年哮喘急性发作率显著降低(60%),肺功能、ACQ-6评分、生活质量评分等均有所改善,安全性良好[44]。此外,已有研究证实特泽鲁单抗疗效可维持2年,但并未减少OCS用量[45]。
Akenroye等[30]发表的meta分析研究比较了美泊利珠单抗、本瑞利珠单抗与度普利尤单抗之间的相对安全性与有效性。研究共纳入来自8项随机临床试验的7 592例嗜酸粒细胞性哮喘患者,根据生物制剂治疗方案分为美泊利珠单抗组(n=1 748)、本瑞利珠单抗组(n=3 166)与度普利尤单抗组(n=2 678)。结果显示,对于基线血EOS≥300个/μl的患者,度普利尤单抗在减少哮喘急性发作和改善肺功能方面优于其他两个生物制剂,在150个/μl≤血EOS<300个/μl的患者中,度普利尤单抗同样显著减少哮喘急性发作。Nopsopon等[46]发表的meta分析研究对特泽鲁单抗、美泊利珠单抗、本瑞利珠单抗与度普利尤单抗治疗嗜酸粒细胞性哮喘的疗效进行了间接对比。研究共纳入来自10项随机临床试验的12岁及以上、血EOS≥300个/μl的9 201例嗜酸粒细胞性哮喘患者,根据生物制剂治疗方案分为特泽鲁单抗组(n=1 609)、美泊利珠单抗组(n=1 748)、本瑞利珠单抗组(n=3 166)与度普利尤单抗组(n=2 678)。研究结果表明,在2型哮喘患者中,相比特泽鲁单抗、本瑞利珠单抗或美泊利珠单抗,度普利尤单抗在改善肺功能方面最显著[以特泽鲁单抗组的FEV1改善值为对照组(参考值为0 ml),度普利尤单抗与特泽鲁单抗之间的FEV1平均差为+20 ml,美泊利珠单抗为-66 ml,本瑞利珠单抗为-62 ml]。
除此之外,目前仍在探索着更多新型疗法[47],多项临床正在进行中:如Amlitelimab在中重度成人哮喘患者中的Ⅱ期临床研究(NCT05421598)[48];Rilzabrutinib在经中高剂量ICS联合长效β2受体激动剂(long-acting β2-agonist,LABA)治疗后仍控制不佳的中重度成人哮喘患者中的Ⅱ期临床研究(NCT05104892)[49];Atuliflapon在经低剂量ICS联合LABA或中高剂量ICS单独或联合LABA治疗后仍控制不佳的中重度成人哮喘患者中的Ⅱ期临床研究(NCT05251259)[50]等,上述研究结果仍待发表。
在过去一年多,GINA发布的哮喘相关指南[1]、中国发布的哮喘相关指南共识[6,7,51,52,53,54]、欧洲地区发布的哮喘相关指南共识[55,56]等多个哮喘指南、专家共识相继更新(表1)。
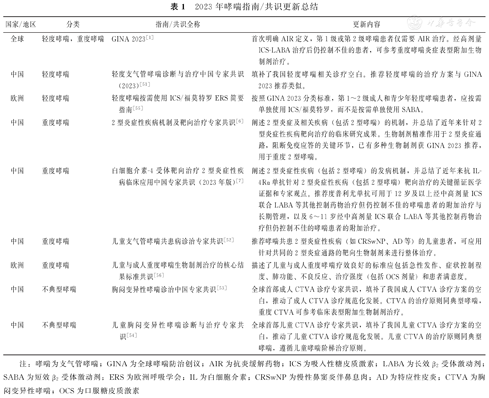
2023年哮喘指南/共识更新总结
2023年哮喘指南/共识更新总结
| 国家/地区 | 分类 | 指南/共识全称 | 更新内容 |
|---|---|---|---|
| 全球 | 轻度哮喘,重度哮喘 | GINA 2023[1] | 首次明确AIR定义,第1级或第2级哮喘患者仅需要AIR治疗。经高剂量ICS-LABA治疗后仍控制不佳的患者,可参考重度哮喘炎症表型附加生物制剂治疗。 |
| 中国 | 轻度哮喘 | 轻度支气管哮喘诊断与治疗中国专家共识(2023)[51] | 填补了我国轻度哮喘相关诊疗空白。推荐轻度哮喘的治疗方案与GINA 2023推荐类似。 |
| 欧洲 | 轻度哮喘 | 轻度哮喘按需使用ICS/福莫特罗ERS简要指南[55] | 按照GINA 2023分类标准,第1~2级成人和青少年轻度哮喘患者,应按需单独使用ICS/福莫特罗,而不是按需单独使用SABA。 |
| 中国 | 重度哮喘 | 2型炎症性疾病机制及靶向治疗专家共识[6] | 阐述2型炎症及相关疾病(包括2型哮喘)的机制,并总结了近年来针对2型炎症性疾病靶向治疗的临床研究成果。生物制剂精准作用于2型炎症通路,阻断免疫应答的关键环节,已有多种生物制剂获GINA 2023推荐,用于重度2型哮喘。 |
| 中国 | 重度哮喘 | 白细胞介素-4受体靶向治疗2型炎症性疾病临床应用中国专家共识(2023年版)[7] | 阐述2型炎症性疾病(包括2型哮喘)的发病机制,并总结了近年来抗IL-4Rα单抗针对2型炎症性疾病(包括2型哮喘)靶向治疗的关键循证医学证据和专家观点。推荐度普利尤单抗可用于12岁及以上经中高剂量ICS联合LABA等其他控制药物治疗但仍控制不佳的哮喘患者的附加治疗与长期管理,以及6~11岁经中高剂量ICS联合LABA等其他控制药物治疗但仍控制不佳的哮喘患者的附加治疗。 |
| 中国 | 重度哮喘 | 儿童支气管哮喘共患病诊治专家共识[52] | 推荐哮喘共患2型炎症性疾病(如CRSwNP、AD等)的儿童患者,可应用针对共同的2型炎症通路的靶向生物制剂来进行整体治疗。 |
| 欧洲 | 重度哮喘 | 儿童与成人重度哮喘生物制剂治疗的核心结果标准共识[56] | 描述了儿童与成人重度哮喘疗效良好的标准应包括急性发作、症状控制程度、肺功能、不良反应、治疗强度(包括OCS剂量)和患者满意度。 |
| 中国 | 不典型哮喘 | 胸闷变异性哮喘诊治中国专家共识[53] | 全球首部成人CTVA诊疗专家共识,填补了我国成人CTVA诊疗方案的空白,推动了成人CTVA诊疗规范化发展。CTVA的治疗原则同典型哮喘,重度CTVA可参考临床表型附加生物制剂治疗。 |
| 中国 | 不典型哮喘 | 儿童胸闷变异性哮喘诊断与治疗专家共识[54] | 全球首部儿童CTVA诊疗专家共识,填补了我国儿童CTVA诊疗方案的空白,推动了儿童CTVA诊疗规范化发展。儿童CTVA的治疗原则同典型哮喘,遵循儿童哮喘阶梯治疗原则。 |
注:哮喘为支气管哮喘;GINA为全球哮喘防治创议;AIR为抗炎缓解药物;ICS为吸入性糖皮质激素;LABA为长效β2受体激动剂;SABA为短效β2受体激动剂;ERS为欧洲呼吸学会;IL为白细胞介素;CRSwNP为慢性鼻窦炎伴鼻息肉;AD为特应性皮炎;CTVA为胸闷变异性哮喘;OCS为口服糖皮质激素
随着对哮喘的临床特征、发病机制和潜在的免疫病理学研究的加深,针对哮喘的生物制剂不断涌现,哮喘治疗已经进入了靶向生物治疗时代。组学的发展为哮喘的机制和靶向治疗提供了发展方向,并为进一步的研究奠定了基础。生物制剂改变了对重度哮喘的管理与目标,可帮助患者达到更高更有可能实现的目标,即"哮喘缓解"。
目前,哮喘的治疗目标集中在控制症状与预防急性发作[57]。而"哮喘缓解(asthma remission)"作为一个更加现实、更有可能实现的目标,可为患者带来更好的临床结局[58]。《将哮喘缓解作为治疗目标共识框架(2020)》专家组提出哮喘缓解包括"临床缓解"与"完全缓解"[58],其特征是高水平的疾病控制,包括无症状和无急性发作,以及在有或无持续治疗的情况下肺功能正常化或改善[57]。然而,目前对于哮喘缓解的定义仍未达成一致,不同生物制剂在各自研究中对于临床缓解给予了不同的定义(表2)。未来还需要通过更多循证证据来进一步完善其定义。
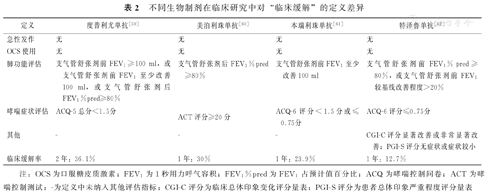
不同生物制剂在临床研究中对"临床缓解"的定义差异
不同生物制剂在临床研究中对"临床缓解"的定义差异
| 定义 | 度普利尤单抗[59] | 美泊利珠单抗[60] | 本瑞利珠单抗[61] | 特泽鲁单抗[62] |
|---|---|---|---|---|
| 急性发作 | 无 | 无 | 无 | 无 |
| OCS使用 | 无 | 无 | 无 | 无 |
| 肺功能评估 | 支气管舒张剂前FEV1≥100 ml,或支气管舒张剂前FEV1至少改善100 ml,或支气管舒张剂后FEV1%pred≥80% | 支气管舒张剂后FEV1%pred≥80% | 支气管舒张剂前FEV1至少改善100 ml | 支气管舒张剂前FEV1%pred≥80%,或支气管舒张剂前FEV1较基线改善程度>20% |
| 哮喘症状评估 | ACQ-5总分<1.5分 | ACT评分≥20分 | ACQ-6评分<1.5分或≤0.75分 | ACQ-6评分≤0.75分 |
| 其他 | - | - | - | CGI-C评分显著改善或非常显著改善;PGI-S评分无症状或症状较小 |
| 临床缓解率 | 2年:36.1% | 1年:30% | 1年:23.9% | 1年:12.7% |
注:OCS为口服糖皮质激素;FEV1为1秒用力呼气容积;FEV1%pred为FEV1占预计值百分比;ACQ为哮喘控制问卷;ACT为哮喘控制测试;-为定义中未纳入其他评估指标;CGI-C评分为临床总体印象变化评分量表;PGI-S评分为患者总体印象严重程度评分量表
生物制剂的临床应用为患者带来了更多的治疗选择和更好的临床预后。随着生物制剂治疗2型哮喘的持续时间增长,探索其长期临床获益、对哮喘疾病进展的影响、与变应原免疫治疗的联合应用,以及通过生物标志物指导临床应用的最佳路径显得尤为重要。
基于现有证据,GINA 2023建议,生物制剂治疗良好的患者,可考虑减少或停用OCS[1],且尽管目前暂无证据提示生物制剂治疗可降低ICS剂量,但仍推荐停用OCS且生物制剂治疗良好的患者可逐步减少ICS剂量至中等剂量[1]。未来将通过更大样本、更长时间的随访研究,更全面地评估生物制剂在2型哮喘患者中的长期获益,以及其对糖皮质激素用量的影响,探索生物制剂在维持2型哮喘患者长期疗效方面的巨大潜力。
"哮喘缓解"代表了哮喘治疗迈向新的阶段[57]。生物制剂在降低哮喘急性发作,改善哮喘症状与肺功能方面疗效突出,可为患者带来更好的临床结局。未来的哮喘研究应将"哮喘缓解"纳入临床评估与治疗计划,以更好地描述生物制剂的临床获益[63]。未来将通过更多循证证据来证实生物制剂在2型哮喘缓解中的获益。
在过去一年多的时间里,哮喘领域在基础研究与临床研究方面有了一些新的进展,基础研究不断探索哮喘的发病机制和可能的治疗靶点,大量的临床研究也为哮喘的诊断与治疗提供了新的循证证据。国内首次发布了轻度哮喘、CTVA等哮喘的指南或共识,并发表了国内首部系统性阐述IL-4R抗体临床应用的专家共识(即《白细胞介素-4受体靶向治疗2型炎症性疾病临床应用中国专家共识(2023年版)》),为哮喘的规范化诊疗、合理应用生物制剂提供了循证依据。重度哮喘,尤其是2型哮喘的治疗受到了更多的重视,可供选择的生物制剂仍在不断增加,已经上市的生物制剂临床应用证据也越来越多,相应的专家指导意见越来越成熟。未来,随着对哮喘炎症机制更全面、更深入地探索和研究,在高质量循证医学研究的支持下,哮喘的诊断和治疗将不断完善,为更多哮喘患者带来获益。
所有作者声明无利益冲突