
基于生物信息学方法筛选鼻咽癌预后和免疫相关的细胞轨迹差异表达基因。
从基因表达综合(GEO)数据库下载鼻咽癌单细胞测序数据集(GSE150825)和转录组测序数据集(GSE102349)。GSE150825数据集包括11例鼻咽癌和3例鼻咽淋巴增生(NLH)组织共66 627个细胞的单细胞RNA测序结果,数据更新时间为2021年3月。GSE102349数据集包括113例鼻咽癌患者临床信息,数据更新时间为2017年。将GSE150825数据集中数据进行标化和重新聚类,并选取髓系细胞进行重新聚类,采用moncle2法进行拟时序分析。计算不同细胞状态的差异基因(细胞轨迹差异基因),并取并集得到并集基因。采用ClusterProfiler和ConsensusClusterPlus包对并集基因进行基因本体(GO)富集分析和临床分型。在GSE102349数据集中,根据细胞轨迹差异基因的并集基因,将患者分为两个亚组,分析两个亚组无进展生存(PFS)、临床分期、肿瘤免疫微环境的差异;CIBERSORT分析两个亚组免疫细胞浸润差异。使用LASSO回归构建预后预测模型。收集江苏省肿瘤医院2018年1月至2023年12月收治的经病理检查证实为鼻咽癌(14例)和正常鼻咽上皮(4例)的病理组织切片,采用免疫组织化学法检测筛选出的靶基因在正常鼻咽上皮和鼻咽癌肿瘤组织中的表达,并根据患者治疗前后核磁共振成像结果分析靶基因表达与鼻咽癌患者淋巴结治疗效果关系。
对单细胞测序数据集GSE150825数据进行过滤和质控,共64 312个细胞(48 604个来自鼻咽癌,15 798个来自NLH)进行后续分析。对质控后的细胞进行重新聚类分析,主要分为8种细胞类型:B细胞、T细胞、先天淋巴细胞、髓样细胞、成纤维细胞、肥大细胞和肿瘤细胞。髓样细胞特异性地分布在鼻咽癌患者中。拟时序变化的细胞轨迹差异基因主要富集在细胞质翻译、核糖体、局灶黏附、钙黏蛋白结合和细胞因子受体结合。在验证集GSE102349数据集中提取细胞轨迹差异基因并集并进行临床分型,亚组1、2的PFS比较差异有统计学意义(P=0.035);亚组1预后较好,临床分期Ⅰ期患者比例大;亚组2预后较差,临床分期Ⅳ期患者比例大。亚组1微环境中免疫成分比例高,体现了较活跃的免疫活动;亚组2的肿瘤纯度高于亚组1,其肿瘤成分所占比例高;记忆B细胞在亚组2中低表达,T细胞滤泡辅助细胞、NK活化细胞、静息和活化树突细胞在亚组1中低表达。根据细胞轨迹差异基因构建预后风险模型,风险评分=SDC3×1.588+ ODC1×1.122+ PSIP1×11.310+ P4HB×4.043。14例鼻咽癌组织中PSIP1蛋白H-score评分高于正常鼻咽组织[(96±11)分比(69±23)分,t=-3.38,P=0.004],P4HB蛋白H-score评分高于正常鼻咽组织[(64±35)分比(17±9)分,t=-2.65,P=0.018]。在鼻咽癌患者中,以H-score评分的中位数为cut-off值(PSIP1为97分,P4HB为63分),PSIP1高表达(≥97分)患者活化T细胞比例高于低表达(<97分)患者[(21±7)%比(13±4)%,t=-2.69,P=0.020],P4HB高表达(≥63分)患者NK细胞比例高于低表达(<63分)患者[(24±10)%比(14±6)%,t= -2.24,P=0.040]。
PSIP1和P4HB可能是预测鼻咽癌预后和治疗效果的生物学标志物。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
鼻咽癌是一种异质性上皮肿瘤,多发于东南亚和南亚地区,我国的新发病例集中于南部,具有明显的地域分布特征[1]。由于鼻咽解剖位置特殊,毗邻组织较多,手术难以根治,目前的主要治疗手段为放化疗[2]。分子靶向治疗在鼻咽癌中尚未有重大进展,肿瘤免疫治疗可能是鼻咽癌的一种有前途的治疗方法[3]。既往已有较多研究报道了鼻咽癌发生的分子基础、易感基因和基因表达模式[4,5]。然而这些研究仅从整体角度研究肿瘤,一定程度上限制了对亚群特征,如肿瘤内异质性和肿瘤微环境等的理解。本研究整合公共数据库鼻咽癌单细胞测序与转录组测序数据,筛选影响预后和免疫相关性的关键靶基因,并根据其表达情况进行临床相关性分析和免疫疗效分析。
从基因表达综合(GEO)数据库(https://www.ncbi.nlm.nih.gov/)下载鼻咽癌单细胞测序数据集(GSE150825)和转录组测序数据集(GSE102349)。GSE150825数据集包括11例鼻咽癌和3例鼻咽淋巴增生(NLH)组织共66 627个细胞的单细胞RNA测序结果,数据更新时间为2021年3月。GSE102349数据集包括113例鼻咽癌患者临床信息,包括年龄、分期、无进展生存(PFS)以及生存状态(生存或死亡)等,数据更新时间为2017年。在GSE150825数据集中,选择min.cells=3、min.features=300,构建Seurat对象,计算总基因数(nFeature)、Count与测序深度的相关性。计算线粒体基因、核糖体基因、红细胞基因的比例。过滤总基因数RNA>4 000、线粒体基因比例>15%、Count数>10 000、红细胞基因比例>1%的细胞。使用"NormalizeData"函数的normalization.method="LogNormalize"、scale.factor=10 000进行标准化,"FindVariableFeatures"计算前3 000个高变基因。计算细胞周期,发现不同周期的细胞聚成一簇,说明细胞周期影响后续分析,因此使用"ScaleData"对前3 000个高变基因进行缩放,同时移除线粒体、核糖体、细胞周期对数据缩放的影响。使用"harmony"对样本进行整合。选择PC数为18,分辨率为0.5进行分析。使用R4.1.3软件进行数据分析。
选取髓系细胞进行重新聚类,并进行moncle2拟时序分析。选择monocle的高变基因进行后续分析。计算不同细胞状态的差异基因(细胞轨迹差异基因),并取并集得到并集基因,采用ClusterProfiler包对差异基因进行基因本体(GO)富集分析和临床分型等。
将GSE102349数据集中数据取log值并进行校正,提取细胞轨迹差异基因的并集基因,使用ConsensusClusterPlus将患者分为两个亚组,并使用survminer和survival包计算两个亚组PFS差异。分析两个亚组临床分期、肿瘤免疫微环境的差异。对GSE102349数据集的FPKM数据进行CIBERSORT分析,计算两个亚组免疫细胞浸润差异。
将GSE102349数据集中转录组数据的FPKM转成TPM并取log值,合并随访时间构成矩阵,使用LASSO回归构建预后预测模型。
纳入标准:(1)鼻咽部病变为初诊初治;(2)既往未接受过抗肿瘤治疗;(3)具有完整的临床随访资料。收集我院2018年1月至2023年12月收治的经病理检查证实为鼻咽癌(14例)和正常鼻咽上皮(4例)的病理组织切片,采用免疫组织化学法检测筛选出的靶基因在正常鼻咽上皮和鼻咽癌肿瘤组织中的表达,收集患者治疗前后核磁共振成像资料,分析靶基因表达与鼻咽癌患者临床治疗效果的相关性。本研究经江苏省肿瘤医院伦理委员会批准(批准文号:2023科-086),所有患者均签署知情同意书。
抗PSIP1抗体购自武汉三鹰生物技术有限公司(25504-1-AP),抗P4HB抗体购自美国Santa Cruz Biotechnology公司(sc-74551)。将病理切片脱蜡、脱水,枸橼酸盐缓冲液修复后用3%双氧水冲洗。在组织处画圈并用血清封闭20 min,弃血清,加相应一抗4 ℃过夜培养。室温培养二抗,加二氨基联苯胺(DAB)显色,冲洗后苏木素染核。接着对切片进行脱水、透明、封片。显微镜下全景扫描并拍照。采用Aipathwell软件分析染色结果,采用H-score方法计算蛋白在组织切片中的表达。
采用R 4.1.3、Graph Pad 7.0统计学软件进行数据分析。呈正态分布的计量资料以 ±s表示,两组间比较采用t检验。P<0.05为差异有统计学意义。
±s表示,两组间比较采用t检验。P<0.05为差异有统计学意义。
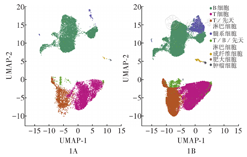
对单细胞测序数据集GSE150825数据进行过滤和质控。根据总基因数、mRNA分子数、线粒体基因、红细胞基因和核糖体基因比例进行质控,去除质量差的细胞,计算前3 000个高变基因。经过质控和过滤,共64 312个细胞(48 604个来自鼻咽癌,15 798个来自NLH)进行后续分析。对质控后的细胞进行重新聚类分析(图1),主要分为8种细胞类型:B细胞、T细胞、先天淋巴细胞、髓样细胞、成纤维细胞、肥大细胞和肿瘤细胞。T细胞和B细胞是微环境中最主要的细胞类型。髓样细胞特异性地分布在鼻咽癌患者中,表明这群细胞在肿瘤微环境中表现出强烈的偏好。进一步对髓样细胞进行细胞轨迹分析,发现根据进化程度,细胞分化方向为3-2-1-4(图2A),也符合髓样细胞向其他细胞类型分化的规律(图2B)。

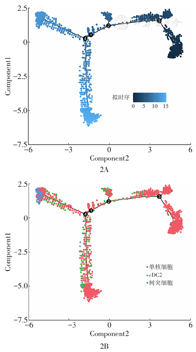

为了筛选随拟时序变化的差异基因,即不同分化时期细胞状态的差异基因,提取不同细胞状态的并集基因,共获得1 914个细胞轨迹差异基因。GO分析结果显示,这些基因主要富集在细胞质翻译、核糖体、局灶黏附、钙黏蛋白结合和细胞因子受体结合(表1)。
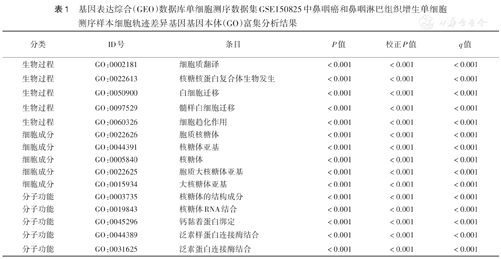
基因表达综合(GEO)数据库单细胞测序数据集GSE150825中鼻咽癌和鼻咽淋巴组织增生单细胞测序样本细胞轨迹差异基因基因本体(GO)富集分析结果
基因表达综合(GEO)数据库单细胞测序数据集GSE150825中鼻咽癌和鼻咽淋巴组织增生单细胞测序样本细胞轨迹差异基因基因本体(GO)富集分析结果
| 分类 | ID号 | 条目 | P值 | 校正P值 | q值 |
|---|---|---|---|---|---|
| 生物过程 | GO:0002181 | 细胞质翻译 | <0.001 | <0.001 | <0.001 |
| 生物过程 | GO:0022613 | 核糖核蛋白复合体生物发生 | <0.001 | <0.001 | <0.001 |
| 生物过程 | GO:0050900 | 白细胞迁移 | <0.001 | <0.001 | <0.001 |
| 生物过程 | GO:0097529 | 髓样白细胞迁移 | <0.001 | <0.001 | <0.001 |
| 生物过程 | GO:0060326 | 细胞趋化作用 | <0.001 | <0.001 | <0.001 |
| 细胞成分 | GO:0022626 | 胞质核糖体 | <0.001 | <0.001 | <0.001 |
| 细胞成分 | GO:0044391 | 核糖体亚基 | <0.001 | <0.001 | <0.001 |
| 细胞成分 | GO:0005840 | 核糖体 | <0.001 | <0.001 | <0.001 |
| 细胞成分 | GO:0022625 | 胞质大核糖体亚基 | <0.001 | <0.001 | <0.001 |
| 细胞成分 | GO:0015934 | 大核糖体亚基 | <0.001 | <0.001 | <0.001 |
| 分子功能 | GO:0003735 | 核糖体的结构成分 | <0.001 | <0.001 | <0.001 |
| 分子功能 | GO:0019843 | 核糖体RNA结合 | <0.001 | <0.001 | <0.001 |
| 分子功能 | GO:0045296 | 钙黏着蛋白绑定 | <0.001 | <0.001 | <0.001 |
| 分子功能 | GO:0044389 | 泛素样蛋白连接酶结合 | <0.001 | <0.001 | <0.001 |
| 分子功能 | GO:0031625 | 泛素蛋白连接酶结合 | <0.001 | <0.001 | <0.001 |
为了验证细胞轨迹差异基因的临床适用性,在验证集GSE102349数据集中提取细胞轨迹差异基因并集的表达情况并进行临床分型。一致性聚类分析结果显示,当代表类簇个数的k值为2时,组内相关性最强,组间相关性最弱,据此将113例患者可以分为亚组1和亚组2,两个亚组PFS比较差异有统计学意义(P=0.035)。两个亚组不同临床分期患者的比例不同,亚组1预后较好,Ⅰ期患者比例大;亚组2预后较差,Ⅳ期患者比例大。
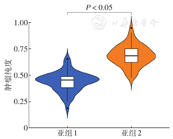
分析亚组1和2免疫细胞评分、基质细胞评分和基质免疫总评分的差异。结果表明亚组1微环境中免疫成分比例高,体现了较活跃的免疫活动(图3)。亚组2的肿瘤纯度高于亚组1,其肿瘤成分所占比例高(图4)。免疫细胞浸润分析表明,记忆B细胞在亚组2中低表达,T细胞滤泡辅助细胞、NK活化细胞、静息和活化树突细胞在亚组1中低表达(图5)。
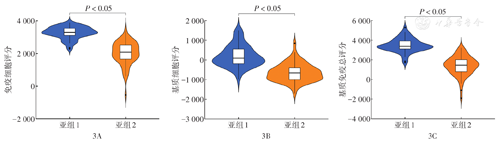

注:根据细胞轨迹差异基因并集的一致性聚类分析结果分为亚组1和亚组2

注:根据细胞轨迹差异基因并集的一致性聚类分析结果分为亚组1和亚组2
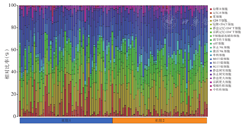

注:根据细胞轨迹差异基因并集的一致性聚类分析结果分为亚组1和亚组2
根据细胞轨迹差异基因表达量构建预后风险模型,得到模型公式为:风险评分= SDC3×1.588+ODC1×1.122+PSIP1×11.310+P4HB×4.043。鉴于PSIP1和P4HB的风险系数高,因此选择这两个基因进行进一步的研究。
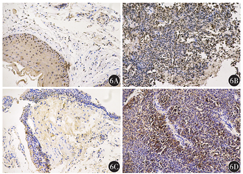
本中心共18例鼻咽癌患者纳入研究,其中4例为正常鼻咽组织,14例为肿瘤组织。免疫组织化学结果显示,鼻咽癌肿瘤组织中PSIP1和P4HB蛋白的表达均高于正常鼻咽组织(图6);鼻咽癌肿瘤组织中PSIP1蛋白H-score评分高于正常鼻咽组织[(96± 11)分比(69±23)分,t=-3.38,P=0.004],P4HB蛋白H-score评分高于正常鼻咽组织[(64±35)分比(17± 9)分,t=-2.65,P=0.018]。

在鼻咽癌患者中,以H-score评分的中位数为cut-off值(PSIP1为97分,P4HB为63分)。在肿瘤组织中,PSIP1高表达(≥97分)患者活化T细胞比例高于低表达(<97分)患者[(21±7)%比(13±4)%,t= -2.69,P=0.020],P4HB高表达(≥63分)患者NK细胞比例高于低表达患者(<63分)[(24±10)%比(14±6)%, t=-2.24,P=0.040]。结果表明PSIP1和P4HB高表达预示着更亢进的免疫微环境。
PSIP1和P4HB均高表达患者经过治疗前后临床影像学评估后,疗效都为有效,治疗后鼻咽淋巴结退缩明显(图7A、7B)。而PSIP1、P4HB均低表达鼻咽癌患者,淋巴结无显著改变(图7C、7D),提示PSIP1和P4HB基因高表达预示着更好的临床治疗效果。
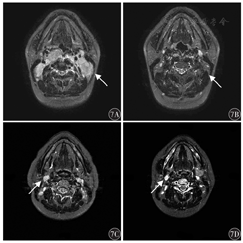

注:箭头所指为转移淋巴结
本研究基于公共数据库单细胞测序和转录组测序数据,筛选鼻咽癌预后和治疗相关的细胞轨迹差异基因PSIP1和P4HB,并在转录组测序数据集中进行验证,在鼻咽癌患者中进行临床相关性分析和免疫疗效分析,结果提示PSIP1和P4HB可能是鼻咽癌诊断和近期治疗疗效的新型生物标志物。
本研究从单细胞测序数据集中提取了64 312个细胞的数据,聚类分析发现14例患者的组织细胞可分为8类,提示肿瘤存在异质性;其中T细胞和B细胞两类亚群是微环境中最主要的细胞类型;本研究发现髓样细胞特异性地分布在鼻咽癌患者中,这类细胞具有向其他细胞类型分化的潜能,表明肿瘤中细胞存在旺盛的增殖和分化环境。细胞轨迹差异基因主要富集在细胞质翻译、核糖体和局灶黏附等途径中。并且在转录组测序验证集中,根据这些差异基因分组的患者PFS差异有统计学意义。本研究构建了4个基因构成的风险模型,筛选出PSIP1和P4HB,在本中心的临床样本验证其表达,都证实了研究结果的可靠性。
PSIP1是一种染色质相关蛋白,可作为转录共激活剂以及RNA结合蛋白,影响乳腺癌和卵巢癌患者的预后[6,7]。在头颈部肿瘤中,PSIP1促进口咽癌的侵袭和转移[8]。P4HB是一种多功能蛋白质,可以作为分子伴侣来改正错误折叠的蛋白质以响应内质网应激。P4HB在多种实体肿瘤中均升高,如膀胱癌、肺癌、卵巢癌、前列腺癌等[9,10,11,12]。研究表明,P4HB在MGMT启动子甲基化状态和TMZ治疗的临床决策过程中的细微病理分层中的潜在作用[13]。此外,P4HB的表达水平有助于识别早期膀胱癌患者并预测患者预后,可能可以作为膀胱癌的诊断和预后生物标志物[14]。此外,其在胃癌中的表达和预后关系也得到了临床验证,是预测肺癌患者辅助化疗效果的潜在生物标志物[15]。一项荟萃分析关于P4HB表达与各种癌症预后之间的关系,共纳入4 121例患者,发现P4HB过表达与9种肿瘤的总生存和11种肿瘤的无病生存(DFS)相关[16]。这些结果表明,P4HB在不同类型的肿瘤中表达,提示其在不同肿瘤类型表达存在相似性。本研究中,鼻咽癌患者PSIP1和P4HB的表达和淋巴结治疗效果有关,PSIP1和P4HB高表达的患者淋巴结减少效果更明显,可能是判断淋巴结治疗效果的生物靶标。PSIP1和P4HB在鼻咽癌中预后和疗效预测的价值值得进一步探究。
本研究仍存在一定局限性:只纳入了14例鼻咽癌和4例正常鼻咽组织,样本量偏少,需进一步地扩大组织样本量,验证PSIP和P4HB在鼻咽癌患者中的临床价值。其调控肿瘤细胞发生侵袭转移的分子机制需进一步阐明,为鼻咽癌发生、发展提供理论依据。
综上所述,本研究通过单细胞、转录组公共数据库和本临床中心样本分析并筛选出预后和免疫治疗相关的靶基因,并分析了其在鼻咽癌中的表达并可能参与肿瘤对免疫浸润的调节。本研究为鼻咽癌诊疗提供了新的治疗靶点,为探索预后和免疫生物标志物提供了新思路。
问静,吴婧,罗燕红,等.基于生物信息学方法鼻咽癌预后和免疫相关细胞轨迹差异表达基因的筛选[J].肿瘤研究与临床,2024,36(4):268-274. DOI:10.3760/cma.j.cn115355-20231214-00233.
所有作者声明无利益冲突



























