
儿童过敏性哮喘(AA)的患病率呈现不断增长的趋势,尘螨是最常见的吸入性过敏原,尘螨过敏原特异性免疫治疗(AIT)是过敏性疾病的对因治疗。当前我国临床医师在儿童AA的尘螨AIT实践中存在诸多问题。为此,基于国内外循证医学证据,结合专家经验,组织专家组制定本指南,就尘螨AIT的适应证、治疗时机、治疗途径、临床疗效评估、不良反应的防治管理、联合用药等方面进行详细阐述,旨在进一步规范AA患儿尘螨AIT的应用,提高儿童AA的诊疗管理水平。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
过敏性疾病是一种常见病和多发病,是世界卫生组织(World Health Organization,WHO)定义的全球第六大疾病[1]。哮喘是常见的过敏性疾病之一。研究已证实,哮喘的本质是气道慢性炎症,病理生理特征主要为气道高反应性和气道重构,其临床症状和气流受限具有可变性。近年来哮喘发病率呈上升趋势,截至2010年,中国儿童哮喘患病率较20年前增长了193%,达到3.02%[2],哮喘具有不同的临床表型,而过敏性哮喘(allergic asthma,AA)是其中一个重要的表型,在儿童哮喘中占比高达80%以上,给患儿学习生活和社会经济带来严重影响[3]。一项对中国26个城市36家医院的过敏性鼻炎(allergic rhinitis,AR)和/或AA患者的流行病学调查显示,过去10年,尘螨(户尘螨65.4%,粉尘螨65.1%)仍然是AR和/或AA患儿中最常见的过敏原[4]。尘螨是中国南方儿童发生AA的主要过敏原[5]。尘螨广泛分布于居室环境中,单纯依靠避免螨过敏原暴露进行症状控制非常困难,且长期药物治疗导致患者依从性和耐受性较低。因此,尘螨过敏原特异性免疫治疗(allergen immunotherapy,AIT)对儿童气道过敏性疾病尤为重要,是唯一能够改变疾病自然病程的治疗方式。目前国内外尚缺乏AA患儿尘螨AIT的诊疗指南,导致临床工作中出现诊断与治疗不规范、理论与实践脱节等现象,不仅影响治疗效果,同时造成医疗资源的浪费。因此,有必要制订切实可行的临床循证指南以指导儿科、变态反应科医师以及基层医师如何正确认识及管理儿童AA。本指南围绕儿童AA诊疗实践中的热点话题,基于国内外循证证据和专家经验,在2018年《儿童气道过敏性疾病螨特异性免疫治疗专家共识》[6]基础上进行更新并制订推荐意见。
本指南制订参考《世界卫生组织指南制订手册》[7]和《中国制订/修订临床诊疗指南的指导原则(2022版)》[8],撰写参考指南研究与评价工具(appraisal of guidelines for research and evaluation,AGREE Ⅱ)[9]和卫生保健实践指南报告条目(reporting items for practice guidelines in health care,RIGHT)[10]。指南设立指导委员会、专家组和秘书组,由儿童呼吸科、消化科、皮肤科、变态反应科、药学、循证医学等学科领域的37名专家、学者和研究人员组成,均声明不存在经济或学术等利益冲突。指南目标使用者为儿科医师、变态反应科医师及基层医师等医务工作者,目标人群为疑似或诊断为AA的儿童(0~18岁)。
本指南通过问卷调研拟定了19个临床问题,检索外文数据库(PubMed、Embase)、中文数据库(中国知网、万方数据),检索词主要包括AA、IgE介导、皮肤点刺试验(skin-prick tests,SPT)、总IgE(total IgE,tIgE)、特异性IgE(specific IgE,sIgE)、严重过敏反应、皮下免疫治疗(subcutaneous immunotherapy,SCIT)、舌下免疫治疗(sublingual immunotherapy,SLIT)、抗IgE治疗等,检索时限为建库至2023年10月31日,并对证据进行整合与质量评价。本指南采用证据推荐分级评估、制订与评价方法(grading of recommendations assessment,development and evaluation,GRADE)系统对证据进行分级(表1),并形成推荐意见。指南专家组对推荐意见进行投票并征求意见(同意率≥90%为强推荐;同意率在75%~90%为弱推荐;同意率<75%不形成推荐),秘书组根据反馈意见进行全文修改,再交由指导委员会审核批准后,指南最终定稿[11]。指南工作组将根据证据更新情况,在5年内适时启动更新[12]。指南撰写流程见图1。
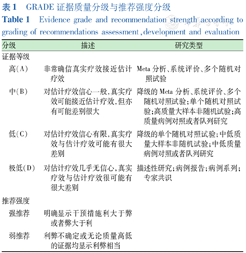
GRADE证据质量分级与推荐强度分级
Evidence grade and recommendation strength according to grading of recommendations assessment,development and evaluation
GRADE证据质量分级与推荐强度分级
Evidence grade and recommendation strength according to grading of recommendations assessment,development and evaluation
| 分级 | 描述 | 研究类型 |
|---|---|---|
| 证据等级 | ||
| 高(A) | 非常确信真实疗效接近估计疗效 | Meta分析、系统评价、多个随机对照试验 |
| 中(B) | 对估计疗效信心一般,真实疗效可能接近估计疗效,但亦有可能差别很大 | 降级的Meta分析、系统评价、多个随机对照试验;单个随机对照试验;高质量大样本非随机试验;高质量病例对照或者队列研究 |
| 低(C) | 对估计疗效信心有限,真实疗效与估计疗效可能有很大差别 | 降级的单个随机对照试验;中低质量大样本非随机试验;中低质量病例对照或者队列研究 |
| 极低(D) | 对估计疗效几乎无信心,真实疗效与估计疗效很可能有很大差别 | 描述性研究;病例报告;病例系列;专家共识 |
| 推荐强度 | ||
| 强推荐 | 明确显示干预措施利大于弊或者弊大于利 | |
| 弱推荐 | 利弊不确定或无论质量高低的证据均显示利弊相当 |
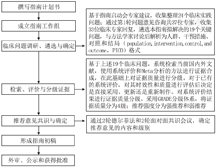

指南围绕AA诊断、治疗中存在的相关问题展开,旨在规范AA患儿尘螨AIT诊疗实践,提高诊疗水平并加强过敏性疾病的管理。尘螨AA诊疗流程见图2。
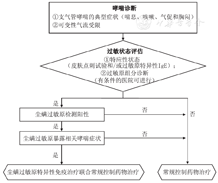

临床实践中,尘螨AIT适用于以下AA患儿:(1)轻-中度AA患儿,过敏原检测证实尘螨是唯一(或主要)的过敏原,且无法完全避免接触。(2)轻-中度AA合并AR(和/或过敏性结膜炎)患儿,过敏原检测证实尘螨是其唯一(或主要)的过敏原,且无法完全避免接触。(3)轻-中度AA合并特应性皮炎患儿,过敏原检测证实尘螨是其唯一(或主要)的过敏原,且无法完全避免接触[6]。
问题1:SPT检测结果是否可以指导患儿的AIT选择?
推荐意见:SPT检测结果可以指导患儿的AIT选择。推荐SPT与尘螨暴露后出现AA相关症状(喘息、咳嗽、气促和胸闷,伴或不伴鼻部、眼部症状)或者尘螨引起的AA规范治疗后控制仍不理想相结合,即SPT与病史相结合,以指导患儿的AIT选择,不建议仅依据SPT检测结果指导患儿的AIT选择(强推荐)。
推荐依据:SPT具有快速、灵敏、简便、成本低等优点,是目前临床上最常用的过敏原体内检测方法。SPT阳性仅代表患儿对某种过敏原致敏,并不意味着患儿一定出现临床过敏症状,不能诊断患儿对某种过敏原过敏[13,14],SPT风团平均直径越大与临床过敏性疾病越相关,但与疾病严重程度无关[15](证据等级D)。皮肤反应性(如皮肤不敏感、局部过敏或皮肤划痕征阳性)、酒精(乙醇)过敏、近期用药、操作手法、操作部位、其他疾病和过敏原点刺液质量等因素均可导致SPT检测结果出现假阴性或假阳性[14,16]。国外多项研究显示,仅依靠SPT检测进行过敏诊断出现假阴性的概率达25.0% ~ 45.2%[17,18,19]。同时SPT阳性反应等级仅反映患者对该过敏原的敏感程度,不能反映过敏性疾病的严重程度[16]。尘螨AIT选择需同时具备SPT结果(++以上)和临床尘螨暴露后AA相关症状[6,20]。临床专科医师需结合病史解读SPT阳性的临床意义,以指导患者的AIT选择[14,16](证据等级D)。虽然证据级别较低,但鉴于SPT检测是目前临床常规检测手段,因此仍为强推荐。
问题2:血清过敏原sIgE和tIgE是否可以指导患儿AIT选择?
推荐意见:(1)血清过敏原sIgE可以指导患儿AIT选择。推荐sIgE水平与尘螨暴露后出现AA相关症状(同问题1描述)或者AA规范治疗后控制仍不理想相结合,即血清过敏原sIgE与病史相结合,以指导患儿的AIT选择,不建议仅依据sIgE指导患儿的AIT选择(强推荐)。
(2)血清tIgE水平不可以指导患儿的AIT选择(强推荐)。
推荐依据:过敏性疾病的体外血清学诊断包括血清过敏原sIgE和tIgE检测。2017年欧洲过敏及临床免疫学会(European Academy of Allergy and Clinical Immunology,EAACI)指出,sIgE和接触过敏原后出现症状是过敏性疾病的唯一诊断标准,也是临床上启动AIT的标准[21](证据等级D)。sIgE检测包括定性检测和定量检测。定性检测可以明确致敏的主要过敏原,但不能检测出sIgE浓度,目前不推荐作为sIgE检测方法[22,23]。定量检测(含量测定)可精准检测血清中slgE水平,客观反映机体的致敏情况,但试剂质量、检测仪器、检测方法灵敏度和特异度等因素导致检测结果存在差异,所以要求严格控制实验室质量。sIgE检测适用于任何年龄的患者,不受服药情况限制,临床上sIgE水平需结合病史评估过敏性疾病严重程度,sIgE水平≥0.70 kUA/L且有螨暴露后AA相关症状,可以考虑启动尘螨AIT[6](证据等级D)。虽然证据级别较低,但鉴于sIgE是目前临床常规检测手段,因此仍为强推荐。
单独血清tIgE水平不能作为判定过敏状态的可靠标志[24,25]。tIgE水平高于正常阈值仅代表Ⅰ型过敏反应的可能性大,不能诊断为过敏性疾病;低值或正常值也不能排除存在IgE介导的疾病[13,16,26]。且tIgE水平受年龄、性别等因素影响[27],多项研究发现,AIT期间患者tIgE变化水平与疗效无相关性[28,29,30]。临床中不推荐血清tIgE水平指导患者AIT选择(证据等级D)。
问题3:AIT对含尘螨的多重过敏原过敏患儿是否有效?
推荐意见:尘螨AIT对以尘螨为主要过敏原的多重过敏原过敏患儿有效(强推荐)。
推荐依据:多项研究证实尘螨AIT可改善对含尘螨的多重过敏原过敏患儿的哮喘症状评分(asthma symptom scores,TASS)和药物评分(total medication scores,TMS)[31,32,33]。国内一项关于单一尘螨过敏和尘螨合并霉菌的儿童AA行尘螨AIT临床疗效研究显示,尘螨AIT 12个月和24个月后,组间哮喘控制问卷(asthma control questionnaire,ACQ)评分、TMS、肺功能改善程度差异均无统计学意义(均P>0.05),提示尘螨AIT对尘螨单致敏和多致敏AA患儿均有效[32](证据等级B)。少数研究结果显示,尘螨AIT对尘螨单致敏AA患儿的疗效优于多致敏患儿[34,35]。Kim等[34]研究纳入130例AA患儿,年龄6~8岁,研究结果显示,尘螨AIT 18个月后,尘螨单致敏组的TASS和sIgE水平均显著低于多致敏组患儿(均P<0.05)(证据等级C)。影响不同研究结果差异的因素可能有主要过敏原不同、研究指标选择差异以及疗效判定标准不一致,但研究均提示尘螨AIT对以尘螨为主要过敏原的多重过敏原过敏的AA患儿有效。
问题4:尘螨AA患儿开始AIT的最低年龄是多大?
推荐意见:推荐尘螨SCIT用于≥5岁尘螨AA患儿,尘螨SLIT用于≥4岁尘螨AA患儿(强推荐)。
推荐依据:2018年我国《儿童气道过敏性疾病螨特异性免疫治疗专家共识》推荐SCIT可用于≥5岁患儿[6],美国哮喘教育和预防项目(national asthma education and prevention program,NAEPP)建议≥5岁轻-中度AA患儿,在哮喘得到控制的情况下使用SCIT作为标准药物的辅助治疗[36](证据等级D)。多项临床研究证实,SCIT治疗≥5岁AA伴或不伴AR患儿可改善鼻炎和哮喘临床症状,减少哮喘基础用药量,减少哮喘复发,且安全性良好[35,37,38,39]。一项随机对照研究纳入48例≥5岁的尘螨AA/AR患儿,与单纯药物治疗相比,尘螨SCIT联合药物治疗1年后可显著降低鼻炎和哮喘症状总评分(total symptom scores,TSS)、TMS、视觉模拟评分(visual analogue scale,VAS)、皮肤对尘螨的反应性(均P<0.05)和尘螨sIgE水平(P=0.03)[40](证据等级B)。一项观察性研究纳入125例≥5岁的尘螨AA患儿,与治疗前相比,尘螨SCIT治疗26周和52周后均可显著减少哮喘基础用药数量(均P<0.01)且第52周末随访发现哮喘复发率仅为10.3%,治疗期间未发生严重不良反应[39](证据等级C)。
2018年我国《儿童气道过敏性疾病螨特异性免疫治疗专家共识》推荐SLIT可用于≥3岁患儿[6],NAEPP指南建议SLIT可用于≥5岁患儿[36]。多项临床研究显示,尘螨SLIT治疗≥4岁AA伴或不伴AR患儿可改善鼻炎和哮喘临床症状,并可预防哮喘进展,减少产生新的过敏原,且安全性良好[41,42,43]。一项观察性研究显示,与治疗前相比,尘螨SLIT 1年后,可显著改善≥4岁AA伴AR患儿的TASS、鼻炎症状评分(total rhinitis symptom scores,TRSS)、TSS、TMS、VAS(均P<0.01)[44](证据等级C)。一项随机对照研究显示,与单独药物治疗相比,尘螨SLIT联合药物治疗≥5岁尘螨AR伴或不伴AA患儿,3年后可显著降低新的过敏原出现(3.1%比34.8%;RR=16.85,95%CI:5.73~49.13),并预防哮喘进展(1.5%比28.8%;RR=0.04,95%CI:0.01~0.17)[45](证据等级B)。SLIT也可考虑作为过敏高风险患儿的一级预防措施,一些研究在<18个月的过敏高风险婴儿预防性使用SLIT[46,47]。有研究发现,与安慰剂相比,SLIT 2年后可显著降低对过敏原的敏感性(9.4%比25.5%,P=0.03)[47],6年后哮喘患病率降低(2.9%比13.5%,P=0.11)[48](证据等级C)。这为更低年龄组哮喘高风险患儿早期进行SLIT提供了依据,但仍需进一步开展大样本、多中心的临床研究加以验证。
回顾性队列研究显示,与青少年(12~17岁)患儿相比,SCIT在儿童(5~11岁)中的依从性更高(47.9%比41.3%,P<0.001)[49](证据等级B)。且与年龄较小的患儿(5岁以下)相比,SCIT在6~15岁的患儿中引起全身不良反应的发生率更低(<30%比>45%,P<0.01)[50](证据等级B)。同时考虑到医师或监护人与5岁以下患儿的沟通较为困难,全身不良反应发生早期难以及时发现,且皮下注射属有创治疗,年龄较小的患儿难以接受等原因[6,51],≥5岁的患儿使用SCIT治疗的安全性和依从性更高。目前大多数SLIT在儿童人群中的临床研究纳入的螨AA患儿≥4岁,且SLIT已在国外<18个月的高风险患儿中开展相关研究,因此未来AIT有望在更低年龄组的患儿中广泛应用。
问题5:螨AA患儿是否应该尽早启动AIT?
推荐意见:推荐螨AA控制不理想的患儿尽早启动AIT(强推荐)。
推荐依据:WHO指出,儿童期是接受AIT的最佳时期,应尽早启动AIT以阻断过敏性疾病的进展[52]。2018年我国《儿童气道过敏性疾病螨特异性免疫治疗专家共识》以及2014年世界过敏组织(World Allergy Organization,WAO)指出,只要临床诊断明确,AIT应尽早开始,尤其在儿童,不需要以药物治疗无效为前提,尽早启动AIT对过敏性疾病的预后具有重要意义[6,53]。
2019年EAACI指南和2020年NAEPP指南推荐AIT作为AA患儿常规治疗的附加治疗,以减轻症状和减少对症药物的使用[20,36]。基于AIT(SLIT)在≥14岁螨AA/AR患者中的数据[54,55],全球哮喘防治创议(Global Initiative For Asthma,GINA) 2017版首次将AIT(SLIT)引入哮喘治疗[56]。GINA 2022版明确指出≥12岁儿童和成人哮喘患者中,在GINA阶梯治疗第2步即可联合尘螨SLIT作为附加治疗[57](证据等级D)。多项研究显示,AIT可明显减轻尘螨单致敏或以尘螨为主要过敏原的AA和/或AR患儿哮喘、鼻炎症状,减少用药,降低VAS评分和气道高反应,在停药后数年仍能维持长期疗效,且安全性较好[35,58,59,60]。AIT可降低螨AA患儿新发过敏原的致敏风险[61,62]。一项随机对照研究显示,尘螨单致敏患儿在药物治疗的基础上进行3年的SCIT,与单纯药物治疗组相比,SCIT组未出现新发过敏原,且研究期间未发生局部或全身不良反应[62](证据等级B)。一项观察性研究显示,≥14岁患者接受AIT治疗可显著降低哮喘从GINA第1步进展到GINA第3步(HR=0.87,95%CI:0.80~0.95)的可能性,以及从GINA第3步进展到GINA第4步(HR=0.66,95%CI:0.60~0.74)的可能性[63](证据等级C)。药物经济学研究通过比较总用药成本、增量用药成本和治疗效果,调查SCIT与常规药物治疗螨AA儿童和青少年患者的效益,结果显示,与基础药物治疗组相比,SCIT联合基础药物治疗组在治疗1年后药物成本稳步下降。治疗3年后,成本效益差异有统计学意义[64](证据等级D)。对于尘螨单致敏或以尘螨为主要过敏原的AA和/或AR患儿,AIT可显著改善哮喘、鼻炎症状,减少患儿用药,同时可降低新发过敏原的致敏风险。建议螨AA患儿尽早启动AIT。
问题6:儿童AA尘螨AIT方式包括哪些?
推荐意见:儿童AA尘螨AIT方式主要包括SCIT和SLIT。SCIT初始治疗阶段的方式包括常规免疫治疗和集群免疫治疗。SLIT剂型有舌下滴剂、舌下喷剂和舌下片剂(强推荐)。
推荐依据:目前临床上用于治疗过敏性疾病的AIT方式主要有SCIT和SLIT,分为初始治疗和维持治疗2个阶段,治疗时间一般不低于3年[65,66,67](证据等级D)。
SCIT是AIT最传统的给药途径[68]。根据初始治疗阶段注射频率的不同,分为常规免疫治疗和加速免疫治疗,集群免疫治疗属于加速免疫治疗方式[69](证据等级D)。国内目前应用更为广泛的治疗方式是常规免疫治疗与集群免疫治疗,SCIT常规治疗方案在初始治疗阶段一般每周治疗1次,每次注射1针,14~16周达到维持剂量[70]。多项研究表明,集群免疫治疗与常规免疫治疗的安全性无显著差异,二者不良反应发生率低,但集群免疫治疗可更早改善症状并减少药物使用[70,71,72,73](证据等级B)。目前国内获批上市的SCIT制剂仅有2种,分别为"屋尘螨变应原制剂"和"螨变应原注射液"。研究显示,SCIT制剂在治疗AR/AA方面疗效显著,全身不良反应发生率低,安全性好[74,75](证据等级C)。
SLIT是AIT另外一种给药途径,在国际临床研究中,其安全性和有效性较好[76,77,78](证据等级B)。SLIT剂型包括滴剂、喷剂和片剂。目前国内上市的SLIT制剂仅有粉尘螨滴剂,用于粉尘螨过敏引起的AR、AA[79]。临床研究(NCT04145219)显示,尘螨变应原舌下片剂在5~11岁AR伴或不伴AA患儿中有效性与安全性良好。目前尘螨变应原舌下片剂、舌下喷剂已在中国部分地区先行使用,为中国尘螨过敏患者提供新的治疗选择。
问题7:对于尘螨AA患儿是否考虑集群疗法?集群方案如何选择?
推荐意见:(1)尘螨AA患儿可以考虑集群疗法。建议在设施完善的治疗中心对尘螨AA患儿进行集群免疫治疗,并加强安全性观察(弱推荐)。
(2)SCIT集群方案缩短初始治疗阶段,在4~8周内加速进入维持治疗阶段,维持治疗阶段每4~6周注射1次(弱推荐)。
推荐依据:集群免疫治疗是近年来提出的AIT方案,国内外多项研究证实,集群免疫治疗有效性及安全性与常规免疫治疗相比无显著差异[72,80,81],但常规免疫治疗在初始治疗阶段需频繁注射(几乎每周1次),所需时间较长(共16次),持续时间4个月余,频繁就诊导致患者依从性差(证据等级B)。集群免疫治疗可明显缩短初始治疗阶段时间,但方案未统一,目前常用方案为:初始治疗阶段每周进行2~3针次的注射,一般4~8周可达到维持治疗阶段[82](证据等级D)。2009年,Zhang等[83]开创了国内集群免疫治疗的先河,他们采用的集群免疫治疗方案目前在我国应用较为广泛(证据等级C)。2018年尘螨过敏原制剂(ALK-depot SQ® 503)的集群免疫治疗方案获德国药监局批准,首次注射剂量为300 SQ-U,7周后剂量达到100 000 SQ-U,累计注射针次为7针[84]。两种方案维持治疗阶段均每4~8周注射1次,具体注射间隔时间需根据患者个体差异和药物耐受情况进行调整。
多项研究发现,在尘螨AA患儿中,集群免疫治疗较常规免疫治疗可更快达到维持剂量[73,85,86]。另有研究发现与常规免疫治疗相比,集群免疫治疗可更快改善临床症状,提高患者依从性,减少医疗费用[72,87]。随机双盲对照研究显示,集群免疫治疗达到维持剂量的时间较常规免疫治疗缩短46%,起效时间较常规免疫治疗提前6周[72](证据等级B)。前瞻性随机对照研究显示,集群免疫治疗在初始治疗阶段可节省成本244.95欧元/人[87](证据等级B)。
有研究显示,常规免疫治疗与集群免疫治疗局部不良反应发生率、速发全身不良反应发生率、迟发全身不良反应发生率无明显差异,且集群免疫治疗全身不良反应均为轻度[73](证据等级C)。但目前临床应用集群免疫治疗AA患儿的循证医学证据较少,需进一步加强安全性观察。
问题8:如何选择评估AIT的疗效指标?
推荐意见:(1)评估AIT疗效的核心指标:需对患儿临床症状、用药情况、自我感受进行评估。疗效评估工具包括:症状用药综合评分(combined symptom-medication scores,CSMS)(或TASS、TMS)、VAS、哮喘控制测试(asthma control test,ACT)(≥12岁儿童)、儿童哮喘控制测试(childhood asthma control test,C-ACT)(4~11岁儿童)、儿童哮喘生活质量问卷(paediatric asthma quality of life questionnaire,PAQLQ)(强推荐)。
(2)评估AIT疗效的其他指标:包括肺功能、改良中文版儿童呼吸和哮喘控制测试(test for respiratory and asthma control in kids,TRACK)(适用于<5岁儿童)、吸入性糖皮质激素(inhaled corticosteroid,ICS)减量或停药、SPT、sIgE、特异性免疫球蛋白G4抗体(specific immunologic G4 antibody,sIgG4)以及其他生物标志物(强推荐)。
推荐依据:CSMS(或TASS、TMS)作为AIT疗效评估指标,临床一致性高,数据易获得。VAS在呼吸道过敏的病情评估方面有重要作用,可直观反映患者症状改变及生活质量受影响程度[6]。研究显示,与标准治疗/安慰剂相比,SLIT/SCIT后患儿TASS和TMS显著降低,VAS显著下降[31,40,78,88,89,90](证据等级B)。在欧洲,推荐PAQLQ、ACT、C-ACT、第1秒用力呼气容积(forced expiratory volume in one second,FEV1)、哮喘每年加重程度及口服皮质类固醇使用情况作为儿童重症哮喘的核心指标集。结合我国应用情况,推荐ACT或C-ACT、PAQLQ、FEV1作为核心指标。ACT(适用于≥12岁儿童)或C-ACT(适用于4~11岁儿童)是对哮喘病情定期评价的重要参考依据[6],国内应用广泛。研究显示,AIT后患儿ACT或C-ACT有显著改善[35,91,92](证据等级C)。PAQLQ是目前已知在国际上应用最为广泛的生命质量量表之一,研究显示,中文版的PAQLQ信度、效度检验均符合统计学的要求[93](证据等级D)。
2019年中国过敏性哮喘诊治指南(第一版)指出肺功能情况可用于评估AIT的远期疗效[65],FEV1和呼气峰流速(peak expiratory flow,PEF)反映气道阻塞的严重程度,是客观判断哮喘病情最常用的评估指标[94]。研究显示,AIT后患儿FEV1等各项肺功能指标逐步改善[31,91,95,96,97](证据等级B)。TRACK是客观评估5岁以下儿童哮喘控制水平的量化工具,其有效性和可靠性在国际上已得到验证[98]。改良中文版TRACK可作为一种有效及可靠的辅助工具,对5岁以下哮喘患儿症状进行量化评估[99,100](证据等级D)。ICS减量或停药是临床上评估尘螨AIT疗效的终点指标之一,临床相关性好,哮喘相关指南建议一旦哮喘得到控制即可减量[101](证据等级D)。SPT在过敏原体内检测中应用广泛。相关研究显示,AIT后皮肤对尘螨的反应性降低[40,78,89](证据等级B)。过敏原体外检测包括血清sIgE、sIgG4以及特异性细胞因子。研究显示,螨AA患儿行SLIT/SCIT后,血清sIgE水平降低[40,102],sIgG4水平有升高趋势[78,103](证据等级B)。目前尚无明确用于预测尘螨AIT临床疗效的生物标志物,有研究发现白细胞介素(interleukin,IL)-33、IL-23、γ干扰素(interferon-γ,IFN-γ)、IL-17A可作为AIT早期临床疗效的生物标志物,但仍需进一步研究证实[104](证据等级D)。
问题9:AIT期间进行疗效评估的时点是什么?
推荐意见:(1)起效时点:建议AIT后3~6个月进行治疗效应评估。若治疗1年后仍无效,且排除影响疗效的相关因素后,建议终止AIT(强推荐)。
(2)维持疗效时点:建议在尘螨AIT后1年进行维持治疗效应评估,以指导患儿后续治疗药物的使用(强推荐)。
推荐依据:目前国内外尚缺乏AA相关尘螨AIT疗效评估的指南/共识推荐。2019年中国AA指南将AIT的疗效分为近期疗效和远期疗效,近期疗效即评估哮喘的控制水平,远期疗效需评估哮喘急性发作的风险及肺功能下降的趋势[65]。2019年EAACI指南建议将AIT后1年的疗效作为是否继续AIT的指标[20]。
2018年我国《儿童气道过敏性疾病螨特异性免疫治疗专家共识》指出,AIT通常2~4个月起效,与疾病类型、症状严重程度、个体因素等相关[6]。多项临床研究结果显示,尘螨SCIT治疗AA患儿3~6个月后,可显著改善TASS、TMS和血清sIgG4水平(均P<0.05)[105,106,107]。随机对照研究结果显示,尘螨SLIT治疗AA和AR患儿6个月后显著降低TSS(P<0.05)[108](证据等级B)。尘螨变应原舌下片剂作为另外一种SLIT手段,可用于中-重度尘螨AR患儿的治疗。随机对照研究发现,中-重度尘螨AR患儿应用尘螨变应原舌下片剂治疗1年后显著改善平均每日鼻炎综合总评分(total combined rhinitis score,TCRS)(P<0.05)[76,109,110](证据等级B),但尚缺乏在螨AA患儿中开展相关研究。综上所述,建议AIT后3~6个月进行治疗效应评估。尘螨AIT 1年后,过敏症状得以改善并维持,可考虑降低合并用药的剂量或减少合并用药的种类。观察性研究纳入螨AA患儿125例,SCIT 1年后,AA症状缓解且对症用药显著减少(P<0.05),提示AIT 1年后评估可指导患儿后续治疗药物的使用[39](证据等级C)。
问题10:AIT疗程结束后的维持疗效有多久?
推荐意见:AIT疗程结束后的维持疗效可达5~10年(强推荐)。
推荐依据:AIT疗程完成后,在很长一段时间可持续获益(证据等级C)。国内一项调查研究显示,AR伴AA患者行AIT 3~5年,在停止AIT 5年后,仍可观察到症状减轻[35]。回顾性研究显示,尘螨SCIT治疗可明显减轻螨AA伴AR患儿的症状,在停止治疗后可维持长期疗效长达6年[58]。另外一项回顾性研究表明,SCIT可显著改善患儿症状,在停止治疗后5~10年仍能维持长期疗效,且研究发现治疗后10年的疗效与5年疗效的差异无统计学意义(P>0.05)[35]。Marogna等[111]研究显示,螨AR伴或不伴AA成人患者行SLIT后,气道高反应性症状在停药5~6年后仍有改善,且SLIT 4年后患者TASS改善可持续7~8年。Ren等[112]的一项观察性研究纳入58例5~14岁螨AR伴或不伴AA患儿,行SCIT 3年后,远期疗效可维持3年,并且该研究对3例患儿进行了长达13年的随访后发现,患儿的症状/药物评分、生活质量评分显著低于基线(均P<0.05),这是目前已知的国内外随访时间最长的研究。
此外,2018年我国《儿童气道过敏性疾病螨特异性免疫治疗专家共识》指出,AIT疗程越长,疗效越巩固[6]。一项前瞻性研究显示,螨单致敏AR伴或不伴AA成人患者SLIT 3年后其临床获益可维持7年,SLIT 4~5年后其临床获益可维持8年[61](证据等级C)。
问题11:影响AIT的疗效因素有哪些?
推荐意见:影响AIT疗效的因素有多种,其中病程短、疗程足、治疗总剂量高及依从性好的患儿,AIT疗效更为显著。过敏原数量、过敏严重程度、患儿年龄及合并其他过敏史也会影响AIT的疗效(强推荐)。
推荐依据:患儿的病程越短,AIT早期临床疗效越显著[95,113](证据等级C)。回顾性研究显示,CSMS与AR伴/不伴AA的病程显著相关,SCIT 3年和5年后,与病程>10年的患者相比,病程≤10年患者的CSMS改善更为显著(P<0.05)[114]。AIT的长期疗效与疗程长短和总剂量呈正相关,长期规范的AIT有利于哮喘的最终控制,基础疗程需1~2年,并随着疗程的延长、剂量的增高,临床疗效随之增加[113,115,116](证据等级D)。AR伴AA患儿SLIT 3年的疗效优于1年或2年[96,117],SLIT 4年的临床获益维持时间优于3年[61,111]。患儿依从性是影响AIT疗效的重要因素,良好的依从性是患儿AIT获益的前提[116,118]。
AIT疗效与患儿是否合并多重过敏及过敏严重程度密切相关(证据等级B)。合并多重过敏是否会造成AIT疗效更差存在争议,有研究显示AIT对含尘螨的多重过敏原过敏的患儿有效,疗效与单致敏患儿相当(P>0.05)[33,119,120,121]。另有研究显示,单致敏患儿其AIT疗效优于多致敏患儿[35,91,116,122],基线期CSMS和最高呼气流量值(peak expiratory flow rate,PEFR)会影响AIT疗效(证据等级C)。研究表明,基线期PEFR% pred(PEFR实测值/PEFR预计值,即PEFR变化率)越低,AIT临床疗效更显著,基线期CSMS越高,AIT临床疗效越显著[113]。年龄越小,AIT疗效越好(证据等级D)。国内外指南/共识均推荐,AIT应尽早开始[6,52,53]。研究显示,儿童AA患者在AIT后的满意率显著高于成人AA患者(P<0.05)[123]。此外,有其他过敏史(包括食物、药物等)的患儿疗效优于无其他过敏史的患儿(OR=0.097)[122],但仍需进一步循证证据验证(证据等级D)。
问题12:AIT期间出现轻中度局部不良反应时应如何考虑剂量调整?
推荐意见:SCIT期间出现轻度局部不良反应时无需进行剂量调整;出现中度局部不良反应(局部肿胀、硬结直径较大)预示未来全身不良反应的发生风险可能增加,需要进行剂量调整,具体剂量调整方案参考相应产品说明书。SLIT期间局部不良反应症状轻微,无需进行剂量调整(强推荐)。
推荐依据:接受SCIT的AA患者发生局部不良反应的情况较为常见,其发生率占总注射人数的26%~86%,总注射次数的0.7%~4.0%[124],主要临床症状为注射局部出现瘙痒、风团、肿胀、硬结、坏死等[125](证据等级D)。SCIT局部不良反应严重程度依据肿胀、硬结直径大小和发生时间分为轻度、中度及重度[126,127],见表2(证据等级D)。SLIT的耐受性优于SCIT[53](证据等级D)。研究发现60%~85%的AA患者接受SLIT后会发生局部不良反应,但通常为轻微的瘙痒和口唇肿胀[128](证据等级D)。大多数变态反应学专家(91.9%)认为应根据局部不良反应情况对AIT进行剂量调整,进行剂量调整的主要原因包括局部不良反应会引起不适,可能导致患者无法坚持治疗(88.9%);局部不良反应可能预示未来全身不良反应风险增加(29.2%)[129](证据等级D)。SCIT后出现局部不良反应,需根据不良反应程度对注射剂量进行调整[135,130,131](证据等级D)。具体剂量调整方案参考相应产品说明书[130,132]。SLIT后局部不良反应多在服药后数分钟或数小时内出现,通常持续时间短(<2周),一般无需进行剂量调整,具有自限性[128](证据等级D)。

SCIT局部不良反应分级
Grade of local adverse reactions with SCIT
SCIT局部不良反应分级
Grade of local adverse reactions with SCIT
| 分级 | 表现 |
|---|---|
| 轻度 | 肿胀、硬结直径<4 cm(红肿、瘙痒、伪足) |
| 中度 | 肿胀、硬结直径≥4 cm(发红、瘙痒刺激、伪足),注射15 min后出现 |
| 重度 | 肿胀、硬结直径≥4 cm(发红、瘙痒刺激、伪足),立即/注射15 min内出现 |
注:SCIT:皮下免疫治疗 SCIT:subcutaneous immunotherapy
问题13:AIT期间出现轻-中度全身不良反应时应如何考虑剂量调整?
推荐意见:SCIT初始治疗阶段出现轻-中度全身不良反应,下次注射时剂量后退1~2级;SCIT维持治疗阶段出现轻-中度全身不良反应,下次注射量减少20%~40%。SLIT治疗期间出现轻-中度全身不良反应的处理原则同SCIT(强推荐)。
推荐依据:AIT期间出现的全身不良反应包括荨麻疹、AR、AA、过敏性结膜炎、过敏性胃肠炎、严重过敏反应以及过敏性休克等[125,133](证据等级D)。参照WAO和EAACI标准,SCIT全身不良反应均可分为5级[125,134]。我国临床实践中更倾向于应用EAACI标准对SCIT全身不良反应进行分级,见表3(证据等级D)。AIT期间全身不良反应较为常见,可能是由于患者对治疗中的过敏原产生过度免疫反应所致。调整治疗剂量可降低免疫反应,并减少不良反应的发生[135](证据等级D)。AA患者SCIT后出现轻-中度全身不良反应,需口服或肌注抗组胺药进行治疗,当全身不良反应症状缓解后,可根据不同的阶段进行剂量调整后继续治疗。初始治疗阶段,下次注射时剂量后退1~2级;维持治疗阶段,下次注射量减少20%~40%。SLIT相关不良事件发生率低于SCIT[136,137,138](证据等级D)。AA患者SLIT后出现轻-中度全身不良反应的处理原则同SCIT[125,139](证据等级D)。

SCIT全身不良反应分级
Grade of systemic adverse reactions with SCIT
SCIT全身不良反应分级
Grade of systemic adverse reactions with SCIT
| 分级 | 程度 | 症状 |
|---|---|---|
| 0级 | - | 无症状或症状与免疫治疗无关 |
| Ⅰ级 | 轻度 | 局部荨麻疹、鼻炎或轻度哮喘(峰流速自基线下降<20%) |
| Ⅱ级 | 中度 | 缓慢发生(>15 min)全身荨麻疹和/或中度哮喘(峰流速自基线下降<40%) |
| Ⅲ级 | 重度 | 快速发生(<15 min)全身荨麻疹、血管性水肿或重度哮喘(峰流速自基线下降>40%) |
| Ⅳ级 | 过敏性休克 | 立即发生瘙痒、面部潮红、红斑、全身荨麻疹、血管性水肿出现喉梗阻表现、速发型哮喘、低血压,甚至死亡 |
注:SCIT:皮下免疫治疗 SCIT:subcutaneous immunotherapy
问题14:AIT期间出现轻-中度不良反应时是否需要联合其他对症治疗药物?
推荐意见:AIT治疗期间出现轻度局部不良反应,无需联合对症治疗药物,多可自行缓解(SCIT轻度局部不良反应也可局部冷敷或外用对症药物);出现中度局部不良反应,可局部冷敷,也可外用、口服、肌内或静脉注射对症药物。AIT治疗期间出现轻-中度全身不良反应,可外用、口服、肌内或静脉注射对症药物,需结合具体症状表现进行处理,若出现轻度荨麻疹症状,无其他不适,可予口服抗组胺药,延长观察时间至1 h以上。若出现过敏性鼻结膜炎症状,主要处理措施可予口服抗组胺药,观察时间不少于1 h,监测PEF。若出现咳嗽喘息等哮喘症状,及时予吸入速效β2受体激动剂;必要时予静脉或皮下注射β2受体激动剂;必要时静脉滴注糖皮质激素;吸氧(强推荐)。
推荐依据:SCIT轻度局部不良反应多在24 h内自行缓解,一般无需对症治疗,可酌情进行局部冷敷处理,或涂搽抗组胺药乳剂/类固醇乳剂;中度局部不良反应可局部冷敷、涂搽类固醇乳剂或口服抗组胺药,必要时可肌内或静脉注射抗组胺药,或使用0.1~0.2 mL肾上腺素液(1∶1 000)在过敏原注射部位周围封闭注射[125](证据等级D)。SCIT全身不良反应的严重程度参照EAACI标准均分为5级[140],轻-中度全身不良反应可局部涂搽类固醇乳剂,或用0.1~0.2 mL肾上腺素液(1∶1 000)在过敏原注射部位周围封闭注射,必要时可多次注射,1次/15 min,也可酌情口服或肌内注射抗组胺药、使用速效β2受体激动剂,必要时静脉使用氨茶碱或水溶性皮质类固醇[6,65](证据等级D)。
SLIT全身不良反应极少见,多为局部不良反应。WAO将SLIT局部不良反应分为3级[141],轻度局部不良反应无需对症治疗,绝大部分可自行缓解;中度局部不良反应可酌情口服对症药物(如抗组胺药、止吐药、解痉药)[6,65,142](证据等级D)。SLIT轻-中度全身不良反应的处理方式与SCIT轻-中度全身不良反应相同[143](证据等级D)。
问题15:AIT期间出现重度局部不良反应和严重过敏反应时如何处理?
推荐意见:AIT后严重过敏反应常累及多个系统,在数分钟至数小时出现,≥Ⅱ级时需立即启动急救流程。首先应考虑终止AIT,肾上腺素是治疗严重过敏反应的一线用药,诊断为严重过敏反应后应立即应用,儿童的给药途径为肌内注射(大腿中部前外侧)、给药浓度为1∶1 000,推荐剂量参照表4。重度局部不良反应可外用、口服、肌内或静脉注射对症药物(强推荐)。
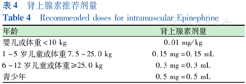
肾上腺素推荐剂量
Recommended doses for intramuscular Epinephrine
肾上腺素推荐剂量
Recommended doses for intramuscular Epinephrine
| 年龄 | 肾上腺素剂量 |
|---|---|
| 婴儿或体重<10 kg | 0.01 mg/kg |
| 1~5岁儿童或体重7.5~25.0 kg | 0.15 mg=0.15 mL |
| 6~12岁儿童或体重≥25.0 kg | 0.3 mg=0.3 mL |
| 青少年 | 0.5 mg=0.5 mL |
推荐依据:严重过敏反应临床表现为速发、危及生命、可累及全身多系统的超敏反应,多伴有皮肤黏膜系统表现,过敏性休克为危重症表现。儿童严重过敏反应诊断的主要依据为详细的发作史,包括症状和体征以及症状、体征突然出现之前数分钟至数小时内所有暴露的已知或可疑过敏原、可疑环境相关的详细信息[144]。儿童的诊断标准相似于成人,见表5。

儿童严重过敏反应诊断标准
Diagnosis criteria of child anaphylaxis
儿童严重过敏反应诊断标准
Diagnosis criteria of child anaphylaxis
| 1.数分钟至数小时内急性发作的皮肤和/或黏膜症状(如全身荨麻疹、瘙痒或潮红、唇-舌-腭垂水肿),并伴发以下至少1种症状 |
| a.呼吸道症状(如呼吸困难、喘息/支气管痉挛、喘鸣、呼气流速峰值下降、低氧血症) |
| b.血压下降或伴终末器官功能不全(循环衰竭、晕厥、尿便失禁) |
| c.严重的胃肠道症状(如剧烈腹绞痛、反复呕吐) |
| 2.数分钟至数小时内a,急性发作的血压降低b或支气管痉挛,或喉部症状c,可无典型的皮肤黏膜症状 |
| a.暴露变应原1~2 h,一般可能更快 |
| b.低血压定义:婴儿和儿童收缩压低于年龄正常值或较基础值下降>30%[儿童低收缩压定义:1月龄~1岁,<70 mmHg;1~10岁,<70 mmHg+(2×年龄);11~17岁,<90 mmHg] |
| c.喉部症状包括:喉鸣、声音改变、吞咽困难 |
注:1 mmHg=0.133 kPa
AIT后出现Ⅰ级严重过敏反应,可先观察,准备好肾上腺素注射液;出现≥Ⅱ级严重过敏反应时,需立即启动急救流程。首先应考虑终止AIT,肾上腺素是治疗严重过敏反应的一线用药,强调急救过程中及时应用[69,125,130](证据等级D)。需注意儿童肾上腺素药物的使用剂量[144]。SCIT重度局部不良反应和严重过敏反应分级标准及处理原则见表6。SLIT严重不良反应极少见,临床应用至今,国内外尚未见导致死亡的病例报道[6]。SLIT后出现严重过敏反应的救治同SCIT[143](证据等级D)。
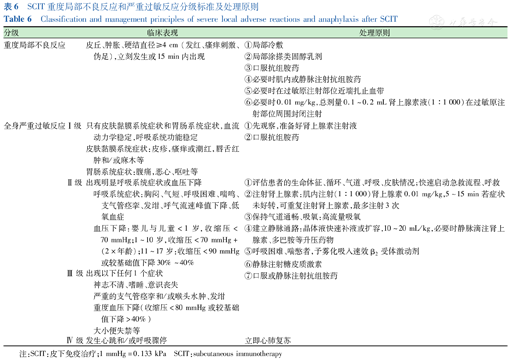
SCIT重度局部不良反应和严重过敏反应分级标准及处理原则
Classification and management principles of severe local adverse reactions and anaphylaxis after SCIT
SCIT重度局部不良反应和严重过敏反应分级标准及处理原则
Classification and management principles of severe local adverse reactions and anaphylaxis after SCIT
| 分级 | 临床表现 | 处理原则 | |
|---|---|---|---|
| 重度局部不良反应 | 皮丘、肿胀、硬结直径≥4 cm (发红、瘙痒刺激、伪足),立刻发生或15 min内出现 | ①局部冷敷 | |
| ②局部涂搽类固醇乳剂 | |||
| ③口服抗组胺药 | |||
| ④必要时肌内或静脉注射抗组胺药 | |||
| ⑤必要时在过敏原注射部位近端扎止血带 | |||
| ⑥必要时0.01 mg/kg,总剂量0.1~0.2 mL肾上腺素液(1∶1 000)在过敏原注射部位周围封闭注射 | |||
| 全身严重过敏反应 | Ⅰ级 | 只有皮肤黏膜系统症状和胃肠系统症状,血流动力学稳定,呼吸系统功能稳定 | ①先观察,准备好肾上腺素注射液 |
| ②口服抗组胺药 | |||
| 皮肤黏膜系统症状:皮疹,瘙痒或潮红,唇舌红肿和/或麻木等 | |||
| 胃肠系统症状:腹痛,恶心、呕吐等 | |||
| Ⅱ级 | 出现明显呼吸系统症状或血压下降 | ①评估患者的生命体征、循环、气道、呼吸、皮肤情况;快速启动急救流程、呼救 | |
| 呼吸系统症状:胸闷、气短、呼吸困难、喘鸣、支气管痉挛、发绀、呼气流速峰值下降、低氧血症 | ②注射肾上腺素:肌内注射(1∶1 000)肾上腺素0.01 mg/kg,5~15 min若症状未好转,可重复注射肾上腺素,最多注射3次 | ||
| ③保持气道通畅、吸氧:高流量吸氧 | |||
| 血压下降:婴儿与儿童<1岁,收缩压<70 mmHg;1~10岁,收缩压<70 mmHg+(2×年龄);11~17岁:收缩压<90 mmHg或较基础值下降30%~40% | ④建立静脉通路:晶体液快速补液或扩容,10~20 mL/kg,必要时静脉滴注肾上腺素、多巴胺等升压药物 | ||
| ⑤呼吸困难、喘憋者,予雾化吸入速效β2受体激动剂 | |||
| ⑥静脉注射糖皮质激素 | |||
| Ⅲ级 | 出现以下任何1个症状 | ⑦口服或静脉注射抗组胺药 | |
| 神志不清、嗜睡、意识丧失 | |||
| 严重的支气管痉挛和/或喉头水肿、发绀 | |||
| 重度血压下降(收缩压<80 mmHg或较基础值下降>40%) | |||
| 大小便失禁等 | |||
| Ⅳ级 | 发生心跳和/或呼吸骤停 | 立即心肺复苏 |
注:SCIT:皮下免疫治疗;1 mmHg=0.133 kPa SCIT:subcutaneous immunotherapy
问题16:在启动AIT时如何实施综合管理?
推荐意见:启动AIT前,患儿评估包括哮喘病情、过敏状态、一般情况、依从性。治疗中心评估包括规范标准、设施规范、急救药物齐全、专业医护人员充足,定期接受培训、安全监管,以最大程度避免不良反应的发生(强推荐)。
推荐依据:AIT的综合管理可最大程度的降低不良事件的发生,是取得满意疗效的关键。需对患儿情况、治疗中心情况、专业医护人员情况及患儿及家属健康教育情况进行评估[6,65,125,145](证据等级D),具体评估内容见表7。

启动AIT前的评估内容
Assessment before initiation of AIT
启动AIT前的评估内容
Assessment before initiation of AIT
| 评估对象或评估内容 | 内容或措施 |
|---|---|
| 患儿情况评估 | ①首先需确保患儿哮喘得到有效控制,峰流速仪测量值大于预计值80% |
| ②了解患儿近日哮喘症状是否加重,前次治疗是否出现不良反应,并询问近期健康状态、药物使用情况等 | |
| 治疗中心设施评估 | ①AIT治疗中心需经过认证且设施规范化,需包括4个独立区域,即医师诊区、治疗区、观察区和检查资料区 |
| ②AIT场地应具备应急抢救能力,配置抢救设备和药品 | |
| ③抢救设备定期维护,抗组胺药、肾上腺素、血管加压素、糖皮质激素等抢救药物需做到定期审计,输液、氧气、建立人工气道用物、面罩、简易呼吸气囊、血压计等需确保备用状态完好 | |
| 医护人员评估 | ①保证医师、护士和技术员的人员配备,各级人员需针对AIT进行严格地岗前培训并参加定期学习,包括过敏原体内外检测流程、标准化免疫治疗流程等 |
| ②严格掌握AIT适应证和禁忌证、不良反应处理流程,建议抢救模拟演习每月进行1次,内容需包含AIT后局部/全身不良反应的诊治、严重过敏反应的处理、心肺复苏等 | |
| ③定期更新学习AIT新知识 | |
| ④建立完备的患儿治疗档案,评估患儿在AIT过程中的治疗反应并监测免疫治疗的安全性等 | |
| ⑤需确保AIT后观察时间不少于30 min,必要情况下可以延长至1~2 h | |
| 患儿及家属健康教育评估 | ①增强患儿及家属对螨过敏性哮喘的认知,普及识别、处理和避免不良反应的方法,如定期开展健康讲座等 |
| ②讲解AIT的方法、疗程、治疗费用、疗效及安全性性等,指导患儿规范化用药 | |
| ③指导患儿及家属如何减少或避免螨的环境暴露 |
注:AIT:过敏原特异性免疫治疗 AIT:allergen immunotherapy
问题17:在AIT疗程中如何联合哮喘控制药物治疗?
推荐意见:(1)建议AA患儿接受AIT的同时进行AA规范化治疗,并做好过敏原环境控制(强推荐)。
(2)AA患儿在接受AIT 1~3年后,哮喘临床症状消失、肺功能正常,可停用哮喘控制药物治疗,定期随诊,根据病情随时调整AA治疗方案(强推荐)。
推荐依据:2019年EAACI指南提出,临床实践中是否启动尘螨AIT应考虑患者实际情况,临床症状未控制的AA患者建议在药物维持治疗的基础上联合尘螨AIT[20](证据等级D)。
多项研究显示,AIT联合糖皮质激素药物、抗组胺药等基础药物能够显著改善AA/AR、特应性皮炎、荨麻疹等过敏性疾病患者的临床症状,主要表现为改善哮喘症状,增强肺功能及提高免疫耐受[146,147,148,149,150,151]。一项随机对照研究纳入73例AA患儿,研究结果显示,与布地奈德单药治疗相比,舌下含服粉尘螨滴剂联合布地奈德可显著改善FEV1、用力肺活量(forced vital capacity,FVC)、FEV1%预计值、FVC%预计值及FEV1/FVC(均P<0.05)[146](证据等级C)。一项多中心、随机对照试验纳入65例AA患儿,研究结果显示,与丙酸氟替卡松单药治疗相比,尘螨AIT联合丙酸氟替卡松治疗可显著降低丙酸氟替卡松的使用剂量(P<0.05),且显著改善晨呼气峰流量(P=0.0315)[148](证据等级C)。
一项前瞻性、开放性、平行对照研究纳入90例螨AA患儿,比较3年SLIT联合哮喘控制药物治疗与单独哮喘控制药物治疗的疗效,研究结果发现,联合治疗组停用哮喘控制药物达6个月的患儿比例显著升高(52.4%比9.1%,P<0.001)[41]。说明在哮喘控制药物治疗的基础上进行3年的SLIT可有效减少基础药物治疗的持续时间和剂量,并成功停药,且改善了AA患儿的肺功能(证据等级C)。
问题18:AIT期间如何联合使用生物制剂?
推荐意见:AIT期间,对于哮喘控制不佳、集群免疫治疗、剂量初始治疗阶段反复发生不良反应、伴特应性皮炎的患儿,可提前使用或者联合使用生物制剂,见表8(强推荐)。

联合生物制剂的情况及联合使用时机
Combined utilization and opportunity of biological agent
联合生物制剂的情况及联合使用时机
Combined utilization and opportunity of biological agent
| 情况 | 联合使用时机 |
|---|---|
| 哮喘控制不佳 | 奥马珠单抗治疗3~9个月后,启动AIT |
| 集群免疫治疗 | 奥马珠单抗治疗1周后,启动AIT集群免疫治疗 |
| 剂量初始治疗阶段反复发生不良反应 | 奥马珠单抗治疗2个月后,启动AIT |
| AIT期间联合奥马珠单抗治疗 | |
| 伴特应性皮炎 | 奥马珠单抗治疗2~5个月后,启动AIT |
| AIT期间联合度普利尤单抗治疗 |
注:AIT:过敏原特异性免疫治疗 AIT:allergen immunotherapy
推荐依据:不能耐受AIT或不良反应高风险的重度未控制哮喘患者,奥马珠单抗预治疗可帮助患者成功启动AIT。回顾性队列研究显示,SCIT前或治疗过程中联合使用奥马珠单抗可显著降低中-重度AA患儿严重不良反应发生风险(0.3%比1.2%,P=0.011)[152](证据等级C)。一项纳入17例不能耐受AIT的重度未控制AA患儿的观察性研究结果显示,奥马珠单抗治疗后12例(70.6%)可成功启动AIT并维持治疗,其中4例(33.3%)在接受奥马珠单抗治疗3个月后启动,5例(41.7%)在6个月后启动,3例(25.0%)在9个月后启动[153](证据等级C)。奥马珠单抗预处理可减少集群免疫治疗严重不良反应的发生[154]。病例报告显示,AA合并AR患儿在AIT剂量初始治疗阶段发生严重过敏反应,奥马珠单抗治疗1周后成功启动AIT集群免疫治疗[154](证据等级D)。2017年EAACI制定的AIT指南指出,如果在AIT剂量初始治疗阶段反复发生全身不良反应,推荐使用奥马珠单抗进行预治疗[155](证据等级D)。回顾性研究显示,3例螨AA患儿因SCIT初始治疗阶段出现全身不良反应导致剂量难以递增,经联合奥马珠单抗治疗后顺利达到目标维持剂量,其中2例在加用奥马珠单抗治疗2个月后继续SCIT,1例患儿SCIT未中断,并有效改善哮喘患儿症状、提高生活质量、减少急性发作次数及减少ICS用量,治疗期间患儿均未出现全身不良反应,耐受良好[156](证据等级D)。为避免皮损进一步加重,建议合并特应性皮炎患儿在AIT期间联合生物制剂治疗。回顾性研究显示,2例AA合并特应性皮炎患儿在奥马珠单抗治疗2~5个月后皮损严重程度明显减轻,皮炎面积减少,后联合尘螨AIT,过程顺利,未见不良反应[157]。回顾性研究显示,3例AA合并特应性皮炎、AR患儿在SCIT期间联合度普利尤单抗治疗≥16周后特应性皮炎评分显著下降,哮喘症状控制良好,C-ACT、ACQ均较基线显著改善(均P<0.05)[158](证据等级D)。目前生物制剂治疗时机、持续时间和剂量尚未达成一致,仍需进一步研究。
问题19:儿童患者AIT过程中是否可以接种疫苗?
推荐意见:儿童患者AIT过程中可以接种疫苗。需注意儿童患者AIT过程中接种疫苗均应间隔一定时间,但狂犬病疫苗等特殊类型疫苗无须注意间隔时间(弱推荐)。
推荐依据:中国和德国新型冠状病毒疫苗接种专家共识均指出,对于AR患儿,SCIT与接种新型冠状病毒疫苗间隔1周;SLIT最后1次舌下含服后次日接种新型冠状病毒疫苗,接种后3 d内如无异常反应,可继续进行SLIT[159,160](证据等级D)。2022年中国过敏性鼻炎过敏原特异性免疫治疗指南明确提出,患者在接种新型冠状病毒疫苗1周后进行SCIT的剂量应为前1次剂量的一半(但并未在临床实施)[161](证据等级D)。临床经验发现,在过敏症状控制良好的健康状态下,SCIT前或SCIT维持治疗阶段接种新型冠状病毒疫苗,可最大限度降低新型冠状病毒疫苗对SCIT的影响[162](证据等级B)。人乳头瘤病毒(human papilloma virus,HPV)疫苗接种补助项目实施方案中明确指出,HPV疫苗与新型冠状病毒疫苗或其他疫苗的接种间隔应大于14 d[163](证据等级D)。狂犬病疫苗等特殊类型疫苗无须注意间隔时间。
多项指南指出,SCIT与其他疫苗的间隔时间至少为1周,且再次启动SCIT时须减量[69,126,164,165](证据等级D)。屋尘螨变应原制剂说明书中指出,SCIT治疗前后1周内不应接种其他类型疫苗[130](证据等级D)。螨变应原注射液说明书指出,对于同时接种抗病毒或抗细菌疫苗的患者,AIT与其他疫苗之间应至少间隔1周,再次启动AIT的时间应间隔2周且剂量减半[132](证据等级D)。粉尘螨滴剂说明书指出,对于同时接种抗病毒或抗细菌疫苗的患者,AIT与其他疫苗之间应至少间隔半周,再次启动AIT的时间应间隔2周[79](证据等级D)。其他疫苗与AIT的间隔时间需遵循说明书/生产厂家的建议。AIT期间接种疫苗的间隔时间及剂量调整方式,见表9。

AIT期间接种疫苗的间隔时间及剂量调整方式
Interval time of vaccination and dose adjustment during AIT
AIT期间接种疫苗的间隔时间及剂量调整方式
Interval time of vaccination and dose adjustment during AIT
| 疫苗 | SCIT | SLIT |
|---|---|---|
| 新型冠状病毒疫苗 | 间隔1周,再次启动SCIT的时间应间隔1周且剂量减半 | 间隔1 d,再次启动SLIT的时间应间隔3 d |
| HPV疫苗 | 接种间隔应>14 d | |
| 狂犬病疫苗等特殊疫苗 | 无须注意间隔时间 | |
| 其他疫苗 | 屋尘螨变应原制剂:SCIT前后1周内不接种其他类型疫苗 | 粉尘螨滴剂:间隔0.5周,再次启动SLIT的时间应间隔2周 |
| 螨变应原注射液:间隔1周,再次启动SCIT的时间应间隔2周且剂量减半 | ||
| 遵循说明书/生产厂家的建议 | ||
注:AIT:过敏原特异性免疫治疗;HPV:人乳头瘤病毒;SCIT:皮下免疫治疗;SLIT:舌下免疫治疗 AIT:allergen immunotherapy;HPV:human papilloma virus;SCIT:subcutaneous immunotherapy;SLIT:sublingual immunotherapy
过敏原组分诊断(component resolved diagnostics,CRD)是指使用天然或重组的单体过敏原来鉴定引起过敏的特定分子,是过敏性疾病精准诊断与治疗的方向[16,166]。CRD有助于鉴别交叉过敏、识别主要致敏蛋白组分、提示与严重过敏反应相关的组分以及提高诊断准确性[16]。WAO共识推荐有经验的临床医师可将CRD作为二线诊断依据[167]。EAACI分子过敏学指南2.0和过敏原诊断中国专家共识均指出,临床医师可依据CRD结果筛选AIT人群以提高AIT疗效[16,166]。且多项研究均证实,在尘螨AA/AR患者中,依据CRD结果筛选AIT患者,可提高治疗成功率[168,169]。同时Stringari等[170]研究显示,在临床病史和SPT诊断的基础上进行CRD,47%的AR患儿AIT处方会发生改变。尽管大规模的应用尚需时日,但CRD为今后过敏性疾病的个体化诊断、治疗及预防开拓了广阔前景。
冲击免疫治疗虽然能够缩短初始治疗阶段的时间,但其安全性远低于常规免疫治疗[171],因此不建议在临床上对尘螨AA患儿使用冲击免疫治疗。若临床应用冲击免疫治疗AA患儿,为避免患儿发生全身不良反应,可在冲击免疫治疗之前预防性使用奥马珠单抗[172]。当前国内外冲击免疫治疗在AA领域的应用较少,未来或可开展相关研究进一步探讨其有效性和安全性。此外,度普利尤单抗等其他生物制剂联合AIT治疗儿童AA有望在未来进行更深入的研究。
(向莉 赵京 鲍燕敏 陈实 陈星 陈德晖 陈莉娜 陈志敏 丁圣刚 董晓艳 韩志英 郝创利 李明 李孟荣 林荣军 刘传合 刘恩梅 刘长山 卢根 卢燕鸣 陆小霞 农光民 彭晓霞 尚云晓 邵洁 孙新 唐力行 唐素萍 田曼 王秀芳 殷勇 张蓉芳 郑跃杰 钟礼立 陈育智 申昆玲 执笔)
向莉和赵京对本文有同等贡献
参与本指南制定和审校的专家(按姓氏拼音排序):鲍燕敏(深圳市儿童医院);陈实(海南省人民医院);陈星(山东第一医科大学附属省立医院);陈德晖(广州医科大学附属第一医院);陈莉娜(四川大学华西第二医院);陈育智(首都儿科研究所附属儿童医院);陈志敏(浙江大学医学院附属儿童医院);丁圣刚(安徽医科大学第一附属医院);董晓艳(上海交通大学医学院附属儿童医院);韩志英(山西省儿童医院);郝创利(苏州大学附属儿童医院);李明(昆明市儿童医院);李孟荣(温州医科大学附属第二医院);林荣军(青岛大学附属医院);刘传合(首都儿科研究所附属儿童医院);刘恩梅(重庆医科大学附属儿童医院);刘长山(天津医科大学第二医院);卢根(广州医科大学附属妇女儿童医疗中心);卢燕鸣(上海交通大学附属仁济医院);陆小霞(武汉儿童医院);农光民(广西医科大学第一附属医院);彭晓霞(国家儿童医学中心,首都医科大学附属北京儿童医院,国家呼吸系统疾病临床医学研究中心);尚云晓(中国医科大学附属盛京医院);邵洁(上海交通大学医学院附属瑞金医院);申昆玲(国家儿童医学中心,首都医科大学附属北京儿童医院,国家呼吸系统疾病临床医学研究中心,深圳市儿童医院);孙新(空军军医大学西京医院);唐力行(国家儿童医学中心,首都医科大学附属北京儿童医院,国家呼吸系统疾病临床医学研究中心);唐素萍(福州市第一总院儿童专科院区);田曼(南京医科大学附属儿童医院);王秀芳(郑州大学第三附属医院);向莉(国家儿童医学中心,首都医科大学附属北京儿童医院,国家呼吸系统疾病临床医学研究中心);殷勇(国家儿童医学中心,上海交通大学医学院附属儿童医学中心);张蓉芳(甘肃省妇幼保健院);赵京(首都儿科研究所附属儿童医院);郑跃杰(深圳市儿童医院);钟礼立(湖南省人民医院)
指南撰写组秘书:皇惠杰(国家儿童医学中心,首都医科大学附属北京儿童医院,国家呼吸系统疾病临床医学研究中心);侯晓玲(国家儿童医学中心,首都医科大学附属北京儿童医院,国家呼吸系统疾病临床医学研究中心);姜楠楠(国家儿童医学中心,首都医科大学附属北京儿童医院,国家呼吸系统疾病临床医学研究中心);刘微(国家儿童医学中心,首都医科大学附属北京儿童医院,国家呼吸系统疾病临床医学研究中心);关辉(国家儿童医学中心,首都医科大学附属北京儿童医院,国家呼吸系统疾病临床医学研究中心)
所有作者均声明不存在利益冲突


























