
口服抗凝药广泛用于需行血栓栓塞性疾病防治患者的居家期间治疗,但抗凝药的不合理应用可能会导致血栓和出血等不良反应。目前国内外尚无相关指南或共识对口服抗凝药居家期间的管理提供推荐性建议。因此,中国药学会医院药学专业委员会组织国内临床药学、心血管外科、心血管内科、血管外科、呼吸科、检验科等相关领域专家梳理相关问题,发布口服抗凝药居家管理专家共识。本共识主要内容包括口服抗凝药的药学监护要点,开展居家管理的流程和注意事项,以及居家管理时特殊情况的处理等,旨在提高口服抗凝药居家期间使用的安全性和有效性,减少不良事件发生。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
合并血栓栓塞性疾病的患者需要长期或终身接受抗凝治疗。抗凝药广泛用于深静脉血栓(deep vein thrombosis,DVT)和肺栓塞的预防和治疗,以及心房颤动(简称房颤)、人工心脏瓣膜置换术后、髋关节或膝关节置换术后血栓形成的预防。相较于肝素类等肠外抗凝药物,口服抗凝药使用方便,适合长期应用,目前普遍用于上述疾病的居家治疗。
口服抗凝药的不合理应用可引发栓塞和出血事件。研究显示,华法林位列因药物不良反应导致急诊住院的十大药物之首,给患者健康造成严重伤害[1]。居家用药管理是指医疗机构或专业人员为患者居家期间药物治疗提供个体化、全程的药学服务和健康知识普及,开展用药评估、用药教育,帮助患者提高用药依从性,保障用药的安全、有效、经济、合理[2]。慢病患者居家治疗管理十分重要,但是掌握合理用药知识的居民占比仅26.05%[3]。因此本共识的目的是规范口服抗凝药在居家期间的使用与监测,提高患者用药的安全性和有效性,促进提升我国口服抗凝药管理水平。
本共识制订由中国药学会医院药学专业委员会(依托中南大学湘雅二医院)发起,专家组成员以临床药学专家为主体,同时邀请心血管外科、心血管内科、血管外科、呼吸科、检验科等相关领域专家参与。本共识制定专家组分为写作专家组和审核专家组。写作专家组基于文献检索结果初拟临床问题,审核专家组投票确定临床问题;写作专家组开展文献检索筛选、证据提取和汇总,并撰写初步推荐意见,审核专家组投票确定最终推荐意见。共识制订工作于2022年12月启动,于2023年10月定稿。
本共识适用于各级医疗机构和管理机构组织开展口服抗凝药居家管理工作。本共识的使用者包括但不限于各级医疗机构适合开展口服抗凝药居家管理的临床医师和临床药师。共识推荐意见的应用目标人群为需要长期使用口服抗凝药并适宜接受居家管理的患者。
共识制订工作组成立了证据检索与评价小组,针对最终纳入的关键问题,按照人群、干预、对照和结局原则进行文献检索,以“口服抗凝药、华法林、新型口服抗凝药、直接口服抗凝药、血栓、出血、栓塞、居家、自我监测”等词作为检索词,在Pubmed、Web of Science、EMBASE、中国知网、万方知识服务平台等数据库中检索口服抗凝药居家管理相关文献。证据检索时间为建库至2023年9月30日,语言为中、英文不限,纳入文献类型不限。
基于循证医学证据,通过三轮德尔菲法,将第一轮达成共识的专家意见纳入;第一轮未达成共识及新提出的推荐意见进入第二、三轮,将最终≥80%的审核专家意见一致定义为达成共识,并确定推荐意见强度。
目前国际尚无共识证据评价及推荐意见形成统一标准。经本共识制定专家组讨论,根据《循证临床实践指南的制定与实施》[4]建议并参考2022年中华医学会临床药学分会《磺达肝癸钠药学实践专家共识》[5]制定方法学,将推荐级别分为强推荐和弱推荐,证据质量高、在中国临床实践中得到较好的循证证据、价值观念与偏好越清晰越趋同、成本与资源耗费越小,考虑为强推荐,反之,则考虑为弱推荐。证据质量分为A、B、C、D和良好实践主张五类(表1)。

证据质量分类及依据
证据质量分类及依据
| 证据质量 | 依据 |
|---|---|
| A | 证据基于多项高质量的随机对照试验(RCT)或荟萃分析 |
| B | 证据基于单项临床RCT或多项非随机对照研究 |
| C | 证据基于单项非随机对照研究 |
| D | 证据基于病例观察、个案报道 |
| 良好实践主张 | 部分无证据支持的临床问题,依据专家临床经验,形成基于专家共识的推荐意见 |
口服抗凝药分为直接口服抗凝药(direct oral anticoagulants,DOAC)和维生素K1拮抗剂(主要是华法林)两大类。DOAC通过直接抑制凝血酶(凝血因子Ⅱa)或凝血因子Ⅹa抑制血栓形成。由于作用机制单一,受食物、药物等影响较小,无需常规监测凝血功能等优势,DOAC已成为非瓣膜性房颤、DVT、肺栓塞等疾病预防和治疗的一线用药。
华法林主要通过抑制维生素K1依赖的凝血因子Ⅱ、Ⅶ、Ⅸ、Ⅹ的羧基化发挥强效抗凝作用。华法林对已合成的凝血因子无直接作用,必须待上述凝血因子相对耗竭后才能在体内发挥抗凝作用。因此,华法林抗凝起效较慢,通常在连续服药3~7 d后达稳定抗凝效果,若急性期使用需与肝素类药物桥接。华法林的药效学及药动力学个体间差异大,抗凝疗效受遗传、合并用药、饮食等多因素影响。华法林治疗窗窄,临床通过定期监测凝血酶原时间/国际标准化比值(prothrombin time/international standardized ratio,PT/INR)评估华法林抗凝强度,并通过调整剂量使患者INR维持在目标范围内以保证药物使用的有效性及安全性。相较于DOAC,华法林使用更加繁琐,目前已逐步被取代,但仍是房颤合并中重度二尖瓣狭窄、人工心脏机械瓣膜置换术后等患者血栓预防的一线推荐用药。常用口服抗凝药的药学特点见表2。
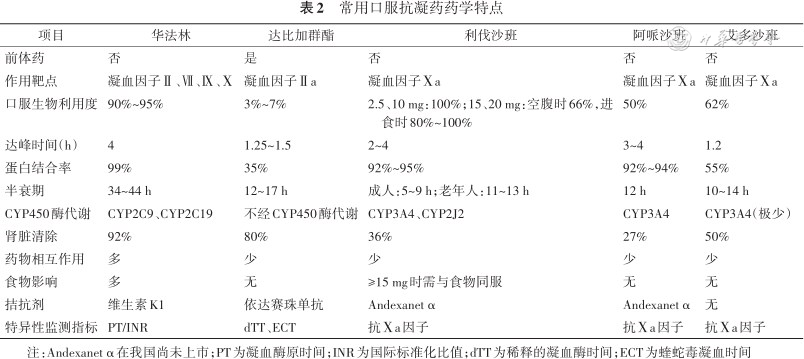
常用口服抗凝药药学特点
常用口服抗凝药药学特点
| 项目 | 华法林 | 达比加群酯 | 利伐沙班 | 阿哌沙班 | 艾多沙班 |
|---|---|---|---|---|---|
| 前体药 | 否 | 是 | 否 | 否 | 否 |
| 作用靶点 | 凝血因子Ⅱ、Ⅶ、Ⅸ、Ⅹ | 凝血因子Ⅱa | 凝血因子Ⅹa | 凝血因子Ⅹa | 凝血因子Ⅹa |
| 口服生物利用度 | 90%~95% | 3%~7% | 2.5、10 mg:100%;15、20 mg:空腹时66%,进食时80%~100% | 50% | 62% |
| 达峰时间(h) | 4 | 1.25~1.5 | 2~4 | 3~4 | 1.2 |
| 蛋白结合率 | 99% | 35% | 92%~95% | 92%~94% | 55% |
| 半衰期 | 34~44 h | 12~17 h | 成人:5~9 h;老年人:11~13 h | 12 h | 10~14 h |
| CYP450酶代谢 | CYP2C9、CYP2C19 | 不经CYP450酶代谢 | CYP3A4、CYP2J2 | CYP3A4 | CYP3A4(极少) |
| 肾脏清除 | 92% | 80% | 36% | 27% | 50% |
| 药物相互作用 | 多 | 少 | 少 | 少 | 少 |
| 食物影响 | 多 | 无 | ≥15 mg时需与食物同服 | 无 | 无 |
| 拮抗剂 | 维生素K1 | 依达赛珠单抗 | Andexanet α | Andexanet α | 无 |
| 特异性监测指标 | PT/INR | dTT、ECT | 抗Ⅹa因子 | 抗Ⅹa因子 | 抗Ⅹa因子 |
注:Andexanet α在我国尚未上市;PT为凝血酶原时间;INR为国际标准化比值;dTT为稀释的凝血酶时间;ECT为蝰蛇毒凝血时间
血栓栓塞性疾病的抗凝疗程取决于疾病类型、患者健康状况、是否存在已知的诱因等多种因素,因此抗凝疗程需要根据患者的具体情况和疾病特点制定个体化方案,并在治疗过程中进行密切监测和调整。常见血栓栓塞性疾病的抗凝疗程见表3。
口服抗凝药的非瓣膜性房颤和静脉血栓栓塞症(venous thromboembolism,VTE)高风险人群出现临床特征和治疗方案变化时,应及时就医评估血栓栓塞风险;由于血栓栓塞的危险因素呈动态变化,即使病情稳定,这类居家管理患者也应定期门诊就诊,评估血栓风险。
瓣膜性房颤特指合并人工心脏机械瓣膜置换术后或中、重度二尖瓣狭窄的房颤。其他类型的房颤均属于非瓣膜性房颤[11]。多项RCT研究已证实CHA2DS2-VASc评分是评估非瓣膜性房颤栓塞风险的有效工具[12, 13, 14],中华医学会心电生理和起搏分会等颁布的《心房颤动:目前的认识和治疗建议(2021)》及国内外多部指南[9, 10, 11,15, 16]均建议CHA2DS2-VASc评分≥2分的男性和≥3分的女性患者应接受口服抗凝药治疗,首选DOAC;男性=1分或女性=2分,可以考虑口服抗凝药治疗。由于卒中的危险因素是动态变化的,2023年中华医学会心血管病学分会等发布的《心房颤动诊断和治疗中国指南》[17]及亚太心律学会(Asia Pacific Heart Rhythm Society,APHRS)发布的《2021APHRS房颤卒中预防共识指南》[16]均建议非瓣膜性房颤患者至少每年应进行1次卒中风险评估,以及时调整抗凝策略。
《心房颤动诊断和治疗中国指南》[17]建议所有接受心脏机械瓣膜置换,或合并中重度二尖瓣狭窄的房颤患者,无论CHA2DS2-VASc评分高低,均应使用华法林进行抗凝治疗。由于长期使用肝素类药物可能导致骨质疏松等不良反应,不建议使用肝素类药物长期替代华法林。
推荐意见1:对于非瓣膜性房颤的居家管理患者,建议定期应用CHA2DS2-VASc评分评估血栓栓塞风险。如无抗凝禁忌证,评分≥2分的男性和≥3分的女性患者均应接受口服抗凝药治疗,首选DOAC。(同意率:100%;推荐强度:强推荐;证据质量:A)
推荐意见2:对于房颤合并心脏机械瓣膜或中重度二尖瓣狭窄的居家管理患者,其卒中风险高,无需评估栓塞风险,均需抗凝治疗,推荐使用华法林,禁止使用DOAC。(同意率:96%;推荐强度:强推荐;证据质量:A)
我国《医院内静脉血栓栓塞症防治质量评价与管理指南(2022版)》[18]建议对住院患者选择合适的评估量表进行VTE风险评估。手术患者建议采用 2005年版的Caprini评估量表,根据评估分值将VTE风险分为低危(0~2分)、中危(3~4分)和高危(≥5分)[19];非手术患者建议采用 Padua 评估量表,根据评估分值将VTE风险分为低危(0~3分)和高危(≥4分)[20];需进行放化疗的内科和门诊肿瘤患者建议采用Khorana 评估量表,根据评估分值将肿瘤患者VTE风险分为低危(0分)、中危(1~2分)和高危(≥3分),需外科手术治疗的肿瘤患者建议采用Caprini评估量表[21];妊娠期和产褥期患者建议参考中华医学会妇产科学分会产科学组于2021年发布的《妊娠期及产褥期静脉血栓栓塞症预防和诊治专家共识》综合评估[22]。
根据2018年发布的《中国血栓性疾病防治指南》[23],VTE低危患者建议机械预防;中危患者建议药物预防或机械预防;高危患者建议药物预防,或药物联合机械预防;具有VTE风险,但同时存在较高出血风险或抗凝禁忌,建议机械预防。对合并中高危VTE风险的恶性肿瘤患者如无抗凝禁忌证推荐药物预防。《医院内静脉血栓栓塞症防治质量评价与管理指南(2022版)》[18]建议具有VTE中、高风险且出血风险低的患者,推荐首选药物预防,或药物预防联合机械预防。
推荐意见3:推荐对外科患者使用Caprini评估量表,对内科患者使用Padua评估量表,对门诊或内科放化疗的肿瘤患者使用Khorana评估量表,对外科肿瘤患者使用Caprini评估量表,评估VTE风险。(同意率:100%;推荐强度:强推荐;证据质量:A)
推荐意见4:VTE低危患者,建议机械预防;中危患者建议药物预防或机械预防;高危患者建议药物预防,或药物联合机械预防;合并中高危VTE风险的恶性肿瘤患者建议药物预防;具有VTE风险,但同时存在较高出血风险或抗凝禁忌,建议机械预防。(同意率:100%;推荐强度:强推荐;证据质量:A)
人工心脏机械瓣膜置换术后患者的血栓风险极高,需要终生抗凝治疗,首选华法林。研究发现血栓栓塞事件主要发生于术后3个月内,导致栓塞的高危因素为:缺乏抗凝治疗、二尖瓣膜置换、既往有栓塞病史、高龄[24]。因此,2022年中华医学会胸心血管外科分会发布的《心脏瓣膜外科抗凝治疗中国专家共识》[10]指出,主动脉瓣或二尖瓣生物瓣置换术后早期给予华法林抗凝治疗3~6个月;对于存在血栓高危因素的生物瓣膜置换术后患者(如房颤、左心室功能低下、既往有血栓病史或存在高凝状态者),在没有抗凝禁忌的情况下,需考虑长期抗凝治疗。
推荐意见5:人工心脏机械瓣膜置换术后患者需终生华法林抗凝治疗。生物瓣膜置换术后患者接受3~6个月抗凝治疗后,根据是否存在血栓高危因素(如房颤、栓塞史、左心室射血分数<35%、高凝状态等)决定是否需长期抗凝治疗。(同意率:96%;推荐强度:强推荐;证据质量:B)
抗凝治疗会增加患者的出血风险。2022年欧洲心脏病学会(European Society of Cardiology,ESC)联合欧洲心律协会(European Heart Rhythm Association,EHRA)等多学会发布的《ESC/EHRA/急性心血管病护理和治疗协会(Acute Cardiovascular Care Association,AACA)/APHRS意见书:房颤和静脉血栓栓塞出血风险的评估和缓解》[25]指出,出血风险并非基于基线因素的静态一次性评估,而是动态变化的,它受年龄、合并症、手术/介入操作、是否应用质子泵抑制剂或药物治疗等的影响。在无抗凝绝对禁忌证的情况下,高出血风险不能作为患者启用抗凝治疗预防卒中的禁忌证,而应该定期评估出血风险,及时发现并干预可纠正的出血危险因素。因此,口服抗凝药的居家管理患者需要定期进行出血风险评估,通常在门诊复诊时由专业医务人员评估。
多项研究证实HAS-BLED评分评估非瓣膜性房颤患者抗凝治疗出血风险的准确性较好[26, 27],因此,美国心脏协会(American Heart Association,AHA)、美国心脏病学会(American College of Cardiology,ACC)联合美国心律学会(Heart Rhythm Society,HRS)发布的《2019年 AHA/ACC/HRS房颤患者管理指南》[11],以及ESC与欧洲心胸外科协会(European Association of Cardio-Thoracic Surgery,EACTS)发布的《2020年ESC房颤诊断和管理指南》[15]均推荐应用该评分作为非瓣膜性房颤抗凝出血风险评估工具。
目前大部分VTE相关指南并未推荐特定的抗凝出血风险评估量表。2021年美国胸科医师学会(American College of Chest Physicians,ACCP)发布的第十版《静脉血栓栓塞症抗栓治疗及血栓预防实践指南》[28]建议,应用《外科住院患者出血风险评估表》评估外科住院患者出血风险,应用IMPROVE评分评估内科住院患者出血风险。然而,与缺血风险评估相比,VTE抗凝出血风险预测评估量表可操作性尚不明确。
推荐意见6:建议采用HAS-BLED评分对使用口服抗凝药的非瓣膜性房颤患者进行出血风险评估,≥3分为出血风险高危人群。应动态评估出血风险,特别是当患者临床特征和治疗方案变化时,应重新评估出血风险。(同意率:92%;推荐强度:强推荐;证据质量:A)
1. PT/INR:PT是监测华法林抗凝强度的最常用指标[29, 30],临床均采用INR对PT进行标准化[31]。根据2013年中华医学会心血管病学分会和中国老年学学会心脑血管病专业委员会发布的《华法林抗凝治疗的中国专家共识》,对于VTE和房颤患者,INR目标范围为2.0~3.0[32]。《心脏瓣膜外科抗凝治疗中国专家共识》[10]建议对于普通出血和栓塞风险的患者,主动脉瓣或二尖瓣置换术后INR目标范围为1.8~2.5;三尖瓣置换术后目标INR范围为2.0~3.0。
2. 治疗窗内时间百分比(time in the therapeutic range,TTR):TTR是衡量长期华法林抗凝控制质量的一个较好指标[33]。国外指南建议平均TTR应>65%(理想情况下>70%)[16,34]。对于TTR<65%的非瓣膜性房颤患者,建议采取措施改善TTR或改用DOAC[34]。
3. 心、肝、肾功能:肝功能不全可引起凝血因子合成减少[35],增强华法林抗凝作用;当机体营养不良、手术创伤等导致血浆蛋白水平降低时,华法林游离药物浓度升高,抗凝作用显著提高[36]。中至重度肾损伤患者华法林剂量减少10%~20%[37];重度肾损伤是华法林不良结局(出血和血栓形成)的危险因素[16];过度抗凝的患者在治疗过程中可能出现急性肾功能下降[38, 39]。心力衰竭会影响INR的稳定[40],并导致INR控制不佳[41, 42]。
4. 基因多态性:大量证据表明CYP2C9与VKORC1基因多态性和华法林剂量显著相关[43],但RCT研究并未一致性提示基因指导的华法林剂量调整方案的优越性[44, 45]。华法林长期治疗且INR稳定的患者,基因检测获益不明显[46, 47]。因此并不推荐对服用华法林的患者常规进行基因检测指导剂量调整[48]。
推荐意见7:不同个体间华法林的剂量-效应关系差异较大,患者应定期监测PT/INR,以防止用药过量或不足。建议使用TTR评估患者抗凝达标质量,目标TTR>65%。(同意率:100%;推荐强度:强推荐;证据质量:A)
推荐意见8:心、肝和肾功能会影响华法林抗凝疗效和INR稳定性,心、肝或肾功能不全的患者应加强PT/INR监测,并积极治疗原发病,改善相应器官功能。(同意率:92%;推荐强度:强推荐;证据质量:B)
由于治疗窗宽,食物及药物相互作用较少,出血和血栓事件发生率低,临床应用DOAC时无需常规监测。然而,某些特殊情况下可能需要定性甚至定量评价DOAC的抗凝作用。根据临床情况,建议重点关注以下患者,必要时监测相关指标[49, 50, 51]:(1)肾功能不全;(2)同时合用其他药物可能影响抗凝疗效和安全性;(3)可能发生致命大出血或血栓栓塞事件;(4)体重过低或超重;(5)儿童、高龄或孕妇;(6)胃肠道吸收不良;(7)需要紧急手术或有创干预;(8)可能需要接受溶栓治疗的急性脑卒中患者。
由于DOAC主要经肾脏排泄,常规行肾功能监测可以预防不良事件的发生,建议至少每6个月评估1次肾功能[52]。对于肾功能损害(CrCl<60 ml/min)或合并可能导致肾功能短暂恶化的急性疾病(如感染、急性心力衰竭)时,建议每3至6个月监测1次肾功能[52]。
Ⅹa因子抑制剂除经肾脏代谢外,还部分经肝脏代谢。肝损害患者使用Ⅹa因子抑制剂后游离血浆药物浓度增加[53, 54]。因此,Ⅹa因子抑制剂禁用于重度肝功能损伤的患者。使用Ⅹa因子抑制剂一般至少每年监测1次肝功能,有肝功能损伤风险的患者建议每6个月监测1次。
2018年国际血液学标准化理事会(International Committee for Standardization in Haematology,ICSH)推荐液相色谱串联质谱(liquid chromatography tandem mass spectrometry,LC-MS/MS)法是测量DOAC浓度的金标准[49]。然而,由于LC-MS/MS设备昂贵,检测流程复杂,难以在临床常规应用。目前临床上监测DOAC的主要手段是凝血试验。
1. 活化部分凝血活酶时间(activated partial thromboplastin time,APTT):APTT对达比加群酯血药浓度变化中度敏感,患者服用常规剂量达比加群酯后,APTT呈剂量依赖性延长的变化可有效反映其药物浓度[55]。APTT只能用于定性评估,有些病例APTT延长虽并不明显,但已发生出血[56]。《2021年EHRA心房颤动患者使用非维生素K拮抗剂口服抗凝剂实用指南》中建议紧急医疗情况时可通过监测APTT评估达比加群出血风险,达比加群酯谷浓度时APTT>2倍正常高值提示高出血风险[57, 58]。
2. 凝血酶时间(thrombin time,TT):TT对血中达比加群酯浓度高度敏感,低浓度时(<30 ng/ml)TT已明显延长,TT正常可排除血液中达比加群酯的存在[49, 50]。TT可以作为定性评估,监测达比加群酯残留的抗凝活性。
3. 稀释的凝血酶时间(diluted thrombin time,dTT)与蝰蛇毒凝血时间(ecarin clotting time,ECT):dTT与ECT均与达比加群的血药浓度呈线性相关,且敏感性和精确度良好。达比加群酯谷浓度时dTT>65 s、ECT>正常值上限3倍均提示较高出血风险,可用于定量监测达比加群酯的有效性和安全性[58, 59]。
1. 抗Ⅹa活性检测:抗Ⅹa活性检测精确且敏感[60, 61, 62],研究发现抗Ⅹa活性测定是可媲美LC-MS/MS的定量分析方法。受最低定量的限制,只有利伐沙班、阿哌沙班和艾多沙班在血药浓度分别>30、15和10 ng/ml时才能通过抗Ⅹa活性测定进行定量评估[61, 62]。
2. PT:利伐沙班在治疗剂量下对PT的延长作用相对较弱[63],当超出治疗浓度范围时,PT值明显延长[52],因此PT可作为利伐沙班抗凝治疗的定性评估。但阿哌沙班和艾多沙班在治疗剂量下对PT影响幅度很小,且具有高度变异性,PT不能用于以上两药的定性评估。
推荐意见9:服用DOAC时无需常规监测凝血指标,在特定临床情况下(如急诊手术、严重出血或血栓事件、可疑过量等)建议进行凝血指标监测。(同意率:100%;推荐强度:强推荐;证据质量:B)
推荐意见10:对于达比加群酯,谷浓度时APTT值>2倍正常上限提示高出血风险,TT值正常提示无残留抗凝活性。dTT和ECT值与达比加群酯血药浓度成线性关系,可较好预测该药的疗效与安全性。(同意率:88%;推荐强度:强推荐;证据质量:B)
推荐意见11:对于Ⅹa因子抑制剂,可参考的监测指标有抗Ⅹa因子活性检测和肝肾功能。(同意率:92%;推荐强度:强推荐;证据质量:B)
服用华法林的患者若采用居家自我检测(patient self-testing,PST)INR的模式应满足以下条件:需要长期抗凝,自己愿意参与治疗,眼手灵活,且具有良好心理素质能使用便携式凝血仪自我检测INR[64]。此外,患者还必须承担自我治疗的责任,完成结构化的培训课程,并表现出自我检测的能力。如果患者能进行PST且能自我调整华法林剂量,还可以进一步实施华法林自我管理(patient self-management,PSM)。所有能够独立生活的患者理论上都有潜力进行华法林自我管理[65]。对于有兴趣但不能自己进行PST或者PSM的患者,家庭成员或护理人员也可为他们承担这项工作。2005年国际口服抗凝药自我监测协会《患者自我检测和患者自我管理口服抗凝药物的实施指南》建议:对于长期口服抗凝药合并人工心脏瓣膜置换术后、心房颤动、血栓性疾病(如反复发生腿部DVT和肺栓塞后)或心肌梗死后左心室功能受损的患者,应考虑实施PST/PSM模式[66]。
推荐意见12:适合居家抗凝管理的患者应同时满足以下条件:(1)需要长期口服抗凝药物的非住院患者,病情较为稳定;(2)能遵医嘱进行口服抗凝药管理,包括按时服药、调整用药剂量、监测相关指标、保持良好的生活及饮食习惯,及时反馈不良反应、及时随访等;(3)对于服用华法林并愿意开展居家自我检测或自我管理的患者,还应完成结构化的培训课程,并且必须承担自我管理的责任。(同意率:100%;推荐强度:弱推荐;证据质量:良好实践主张)
2019年中国医院协会药事专业委员会发布的《医疗机构药学服务规范》明确医疗机构从事居家药学服务工作的药师应满足以下条件之一:具有药师及以上专业技术职务任职资格并有2年及以上医疗机构药学服务工作经验;取得临床药师岗位培训证书[2]。2019年中国心胸血管麻醉学会心血管药学分会发布《抗凝(栓)门诊标准操作规程专家共识》中指出,理想的抗凝(栓)门诊医务人员应具备:(1)确定抗凝药物应用的适应证、剂量、疗程等,以及为患者进行用药教育的能力;(2)处理特殊人群的抗凝问题及不良反应的能力等[67]。2018年《家庭药师服务标准与路径专家共识》中指出:家庭药师必须获得临床药学、药学、中药学等相关专业大学本科及以上学历,取得药师及以上专业技术资格或执业药师资格,从事临床药学一线工作至少1年或其他药学服务一线工作至少3年[68]。
推荐意见13:适合开展居家抗凝管理的医师应同时符合如下要求:(1)具备医师及以上专业技术职务任职资格,并至少有2年抗凝治疗工作经验;(2)熟练掌握抗凝药物应用的适应证、剂量、疗程、药物相互作用等,具备为患者提供用药教育、处置不良反应和指导特殊人群用药的能力。(同意率:84%;推荐强度:弱推荐;证据质量:良好实践主张)
推荐意见14:适合开展居家抗凝管理的药师应同时符合如下要求:(1)具备药师及以上专业技术职务任职资格,并至少有2年抗凝治疗工作经验,或取得抗凝/心血管专业临床药师资格证书;(2)熟练掌握抗凝药物应用的适应证、剂量、疗程、药物相互作用等,具备为患者提供用药教育、提供不良反应处置咨询、指导特殊人群用药的能力。(同意率:84%;推荐强度:弱推荐;证据质量:良好实践主张)
便携式凝血仪于20世纪80年代末开始用于华法林抗凝治疗管理。美国血液学学会(American Society of Hematology,ASH)发布的《2018年静脉血栓栓塞管理指南:抗凝治疗的优化管理》认为,优先推荐患者通过便携式凝血仪进行INR的PST,并且优先推荐可进行PST且能自我调整华法林剂量的患者实施PSM[69]。《抗凝(栓)门诊标准操作规程专家共识》也鼓励有条件的家庭配备便携式凝血仪,在充分掌握华法林使用方法的情况下自我监测和自我管理[67]。
与传统门诊管理模式相比,利用便携式凝血仪开展华法林居家管理可以提高患者INR监测依从性、改善TTR、减少血栓栓塞事件。THINRS研究显示80%的患者有能力进行PST,PST模式下患者TTR增加,满意度明显更高[70]。一项纳入26个随机对照试验(randomized controlled trial,RCT)研究的荟萃分析发现,PST可显著降低血栓栓塞事件的风险和全因死亡率,但不降低出血事件[71]。一项为期10年的成本效益分析研究显示,PST有80%的机会具有成本效益[71]。与使用DOAC相比,使用PST的华法林患者可以显著减少医保支出[72]。而2014年英国血液学标准委员会(British Committee for Standards in Haematology,BCSH)发布的指南《口服维生素K拮抗剂进行抗凝治疗患者的自我检测和管理》认为PST/PSM可以节约时间成本,但只对特定患者具备成本效益[73]。
便携式凝血仪检测INR 值的准确性已在多项研究中证实。需要注意的是,当INR超过4.0时,便携式凝血仪的准确性降低[74, 75, 76]。因此便携式凝血仪需要定期采用内部或外部校正法进行仪器校正。内部校准采用仪器制造商提供的特定方法。外部校准通常是在同一时段比较便携式凝血仪获得的INR值与医院实验室检测的INR值,当两者差异不超过±0.5认为便携式凝血仪结果可靠。此外,还可以与五个认证的冻干血浆样本INR值进行比较和校准,当获得的INR值与认证INR值相比≤15%差异,便携式凝血仪结果认为准确[73]。
推荐意见15:对于能正确操作且经济上可负担便携式凝血仪的患者,在医务人员和专业人员指导下,可以考虑利用经过定期校正的便携式凝血仪开展华法林居家管理。(同意率:96%;推荐强度:弱推荐;证据质量:A)
开展华法林居家管理的具体流程见图1。患者在确定需长期使用华法林后,应接受华法林用药教育,包括华法林的用药依从性、监测指标和频率、不良反应的识别、影响华法林抗凝作用的食物、药物和疾病等。患者根据自我意愿选择基于传统门诊或者利用便携式凝血仪开展华法林居家管理。
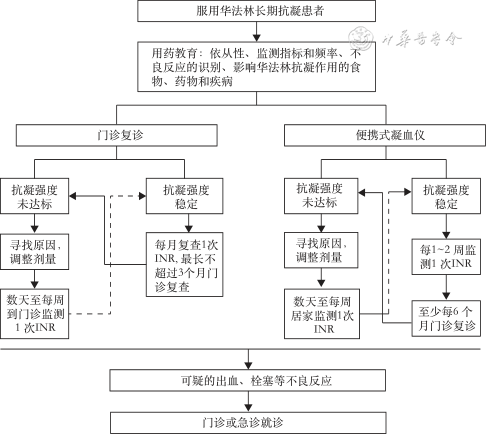

注:INR为国际标准化比值
《华法林抗凝治疗的中国专家共识》推荐门诊患者在华法林剂量稳定前应该数天至每周监测1次INR,INR稳定后可以每4周监测1次。如果需调整剂量,应重复上述监测频率直至INR再次稳定。INR稳定的患者最长可以3个月监测1次INR[32]。《2018年静脉血栓栓塞管理指南:抗凝治疗的优化管理》建议对于接受华法林治疗的VTE患者,当华法林剂量调整后4周或更短时间内在门诊复查INR;对于INR控制稳定的患者,建议每6~12周门诊复查[69]。研究证实增加居家抗凝监测频率可以改善TTR[77]。1项荟萃分析也发现至少每周1次的PST/PSM能更有效控制INR达标水平[78]。《口服维生素K拮抗剂进行抗凝治疗患者的自我检测和管理》推荐,经主管医务人员同意后,开展PST或PSM的患者至少应每6个月门诊随访一次[73]。
推荐意见16:服用华法林居家管理的患者应该得到充分的用药教育,使用便携式凝血仪的患者还应该得到针对仪器和远程医疗沟通手段的详细教育。基于传统门诊管理的患者,INR稳定后如果情况允许,建议每个月1次门诊复诊,最长不超过3个月1次门诊复查。基于便携式凝血仪管理的患者,INR稳定后建议每1~2周使用仪器复查1次INR,并且至少每6个月1次门诊复诊。患者出现不良反应后,应及时就医。(同意率:88%;推荐强度:强推荐;证据质量:B)
服用DOAC患者的居家管理流程见图2。《2021年EHRA心房颤动患者使用非维生素K拮抗剂口服抗凝剂实用指南》建议启动DOAC抗凝治疗前需要评估患者血常规、凝血指标及肝肾功能,在门诊随访时根据患者用药依从性、合并疾病、是否有药物不良反应等因素,调整药物种类及药物剂量[57]。根据患者病情预约下一次随访时间或申请多学科专家评估。《2018年EHRA心房颤动患者使用非维生素K拮抗剂口服抗凝剂实用指南》[79]建议服用DOAC患者的随访频率应根据患者特点(如肾功能、年龄、合并症等)确定,建议每3个月左右进行1次门诊随访,时间区间为1~6个月。患者在居家监测过程中,如果出现新的出血或血栓事件,应立即就诊。研究显示,与常规监护相比,动态监测患者HAS-BLED评分和相关危险因素(例如出血史、合并疾病、合并用药、肾功能等),能显著降低出血风险[80]。
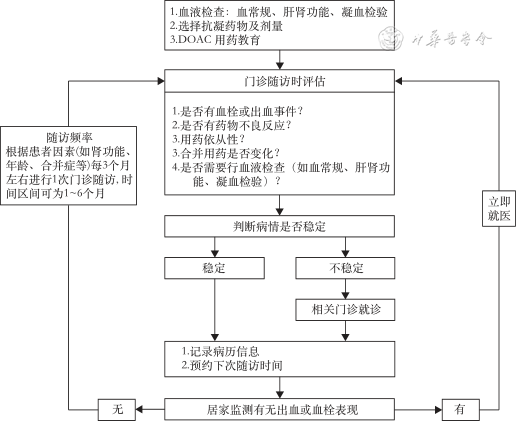

推荐意见17:服用DOAC居家管理的患者应该得到充分的用药教育,患者应根据情况(如肾功能、年龄、合并症等)每3个月左右进行1次门诊随访(时间区间为1~6个月),最长不超过6个月。患者出现不良反应后,应及时到门/急诊就诊。(同意率:100%;推荐强度:弱推荐;证据质量:C)
《2021年EHRA心房颤动患者使用非维生素K拮抗剂口服抗凝剂实用指南》[57]建议可以从以下几个方面考虑提高口服抗凝药患者居家治疗期间依从性:(1)患者教育:主要包括药物用法用量、生化指标、凝血指标检测频率等[81, 82, 83],教育的方式包括初始治疗时提供患者教育手册和宣传单,提供患者抗凝记录表,开展患者小组活动,每次随访时进行再教育,发放抗凝知识问卷等[15,84, 85, 86]。(2)患者家属参与:应积极引导患者家属参与到患者监护中,使家属共同认识用药依从的重要性,从而督促患者的用药依从行为。(3)医药护沟通:医师、药师和护士应就患者依从性问题进行充分沟通,在每个治疗环节充分提醒患者提高用药依从性。一项系统评价显示,多学科团队支持和社区支持,可显著降低全因死亡率和心血管住院率[87]。(4)技术辅助:带有用药提醒功能的药盒、用药提醒移动应用程序(applications,APP)[88]、微信推送或短信提醒等手段均可帮助提高用药依从性。(5)优化给药方案:有研究显示,服用DOAC的患者中,每日1次给药的依从性优于每日2次给药[89]。另有研究显示,相比每日2次给药,每日1次给药能显著降低卒中风险,不增加大出血风险[90]。但另一项在老年患者中的研究发现,使用每日2次给药阿哌沙班的患者其卒中风险低于使用每日1次给药的利伐沙班或艾多沙班的患者[91]。
推荐意见18:患者的依从性对抗凝治疗的有效性和安全性至关重要,建议从患者教育、患者家属参与、医药护沟通、技术辅助、优化给药方案等方面提高患者居家治疗期间用药依从性。(同意率:100%;推荐强度:弱推荐;证据质量:C)
国内外远程管理的形式经历了从电话随访、大众社交平台到包括门户网站、远程电子服务系统以及APP在内的专业抗凝管理工具的转变[92]。远程管理内容包括健康档案管理、用药教育、用药提醒、在线咨询及药物治疗方案调整等,如图3所示。《抗凝(栓)门诊标准操作规程专家共识》鼓励酌情对于未能按时前来门诊或通过电话进行咨询的抗凝患者进行主动追访[67]。
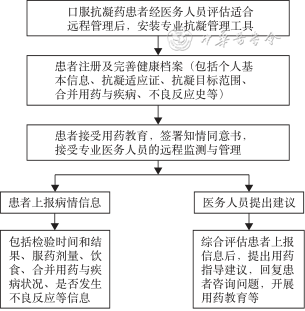

注:如果患者出现大出血、栓塞以及其他急重症情况,应即刻就医处理,不建议通过远程监测系统向医务人员咨询,以免耽误就诊时间
有荟萃分析证实,与常规抗凝管理相比,利用远程监测系统进行口服抗凝药居家管理具有良好的安全性[93],但这些临床研究多为低质量研究。近年来,利用远程监测工具管理抗凝稳定患者的安全性和有效性已经在国内外多项研究中证实[94, 95, 96]。一项系统性评价证实,通过智能手机或平板电脑对华法林患者进行抗凝管理,可以改善临床结果,提高患者抗凝知识水平、依从性和满意度[97]。
推荐意见19:推荐患者利用包括但不限于电话、电子邮件、互联网站、微信公众号和抗凝APP等远程监测工具,向医务人员进行咨询。(同意率:96%;推荐强度:强推荐;证据质量:A)
出血是口服抗凝药最主要的不良反应,评估患者的出血严重程度对于实施止血和保护器官功能的治疗决策至关重要[98]。依据2011年出血学术研究会(Bleeding Academic Research Consortium,BARC)制定的出血分类标准将抗血栓药物相关出血分为5级[99],其中0~2型为轻度出血,3~4型为严重出血,5级为致死性出血。另外,出血也可简化分为大出血和非大出血,大出血增加死亡风险[100, 101, 102, 103]。满足下列因素中任意1条被归类为大出血:①关键部位出血;②血流动力学不稳定;③明显出血,且血红蛋白下降≥2 g/dL或需输血≥2单位红细胞[104]。
《2020年ACC关于口服抗凝剂患者出血管理的专家共识决策途径:美国心脏病学会解决方案集监督委员会的报告》指出,对于无需特殊处理、无需住院或者输血就可实现止血的非大出血患者,建议继续接受口服抗凝药的治疗,并可通过局部治疗或者手动压迫止血。当患者出现大出血及任何需要通过住院、手术或输血治疗的出血,应停用抗凝血药物。当初始措施无法有效管理危及生命的出血或大出血时,应考虑使用抗凝逆转剂或止血剂[98]。《2020年ESC房颤诊断和管理指南》推荐轻微出血事件应采取支持性措施,如机械压迫或小手术止血。存在严重活动性出血的患者,先中断口服抗凝药治疗,直到确定出血原因并解决活动性出血[15]。
抗凝治疗能够显著减少血栓事件的发生,但对于抗凝疗效欠佳的患者,仍然可能发生血栓事件。抗凝治疗为连续性治疗,如因药物不良反应(如发生大出血)而停药,应考虑替代方案评估重启抗凝治疗时间。若患者出现下列情况,建议延迟重启抗凝治疗:(1)关键部位出血;(2)再出血或因再出血导致残疾/死亡的风险较高;(3)未确定出血来源;(4)计划进行侵入性手术。若患者存在高血栓形成风险,建议在实现止血且达到临床稳定后尽快重新开始抗凝治疗[98]。
推荐意见20:口服抗凝药患者应接受正确识别出血、栓塞等症状的教育,在居家抗凝期间,患者出现出血或栓塞症状时,应及时到医院就诊,接受医师指导并监测凝血指标。若为大出血或严重活动性出血,建议立即停用口服抗凝药,并紧急就诊。(同意率:92%;推荐强度:强推荐;证据质量:A)
推荐意见21:口服抗凝药患者居家期间发生栓塞时,应紧急就诊,积极治疗,防止错过最佳治疗时间。(同意率:100%;推荐强度:强推荐;证据质量:A)
2022年ACCP颁布的《抗血栓治疗的围手术期管理美国胸科医师学会临床实践指南》,推荐对于需要牙科手术的华法林治疗患者,建议使用止血剂或止血措施并继续使用华法林抗凝治疗[105]。2022年《口服抗栓药物患者门诊围手术期管理的专家共识》建议服用DOAC的患者拔牙时无需停药,同时研究指出将手术时间安排在服药6 h后,出血率较低[106]。2020年中国心胸血管麻醉学会非心脏麻醉分会、中国医师协会心血管内科医师分会和中国心血管健康联盟颁布的《抗血栓药物围手术期管理多学科专家共识》推荐进行简单牙科操作时,继续使用华法林,同时局部使用止血药物,或者在操作前停用2~3 d[107]。
2022年美国胃肠病学会(The American College of Gastroenterology,ACG)和加拿大胃肠病学会(Canadian Association of Gastroenterology,CAG)发布《ACG/CAG临床实践指南:急性消化道出血和内镜操作围术期抗凝剂和抗血小板的管理》推荐计划择期胃肠镜检查的患者:服用华法林的患者,建议继续服药;针对高出血风险的内镜操作(息肉切除术≥1 cm),应当暂时中断抗凝5 d并不使用肝素桥接;对于服用DOAC的患者,建议暂时中断服用[108]。2021年英国胃肠病学会(British Society of Gastroenterology,BSG)和欧洲胃肠内镜学会(European Society of Gastrointestinal Endoscopy,ESGE)联合颁布的《抗血小板或抗凝治疗患者的内镜诊治指南》建议针对诊断性胃肠镜检查患者:服用华法林的患者,建议继续治疗;服用DOAC的患者,建议在内镜操作当天停用早晨剂量的DOAC[109]。《抗血栓药物围手术期管理多学科专家共识》指出内镜下活检和息肉切除术属于高危出血风险外科手术操作,建议服用华法林的患者,术前5 d停药,并与医师或临床药师讨论是否桥接治疗;建议服用DOAC的患者,术前2 d停药[107]。2016年发布的《抗栓治疗消化道损伤防治中国专家建议》建议长期使用抗凝药物的患者,应充分评估心血管病及消化道出血的风险,权衡利弊,进行内镜下检查或治疗[110]。
推荐意见22:对于需行简单牙科操作的患者,根据患者具体情况,在征得医师同意后,患者可继续抗凝治疗或者提前停用抗凝药。如果继续抗凝治疗,使用华法林的患者术中建议局部使用止血药物。(同意率:80%;推荐强度:强推荐;证据质量:B)
推荐意见23:对于需行可能伴有活检或息肉切除等操作的胃肠镜检查时,患者应提前告知医师正在口服抗凝药。建议服用华法林的患者,术前5 d停药,并与医师或临床药师讨论是否桥接治疗;建议服用DOAC的患者,术前2 d停药。(同意率:80%;推荐强度:弱推荐;证据质量:良好实践主张)
对于人工心脏机械瓣膜置换术后、伴严重泵功能减退的心脏病或房颤患者,以及有血栓栓塞高危因素的患者,妊娠期需要进行抗凝治疗。抗凝药物种类的选择应根据疾病、孕周、母亲和胎儿安全性等综合考虑。目前尚无一种抗凝方案对母体与胎儿均最佳,需综合考虑受益-风险选择最合适的抗凝方案[10,32,111, 112, 113, 114, 115]。
需要长期使用口服抗凝药的女性患者妊娠后发生不良母婴结局的风险高于正常女性。如需备孕,应至抗凝专科门诊评估综合状况和妊娠风险。口服抗凝药可能导致妊娠早期的流产风险增加及胎儿畸形。华法林在体内无蓄积作用,故备孕期使用对胎儿无影响。ESC颁布的《2018 ESC妊娠合并心血管疾病管理指南》建议在明确妊娠前继续华法林抗凝治疗直至确认怀孕[111]。由于缺乏足够的循证证据支持DOAC在备孕期使用,2016年国际血栓和止血学会(International Society on Thrombosis and Haemostasis,ISTH)下属的科学与标准化委员会(Scientific and Standardization Committee,SSC)颁布的《育龄妇女直接口服抗凝血剂的管理:ISTH/SSC指导》[116]建议在备孕期将DOAC更换为华法林或低分子肝素直至怀孕;在DOAC治疗过程中怀孕,建议立即停用DOAC,并开始使用低分子肝素。
由于潜在的生殖毒性,DOAC禁用于妊娠患者。目前妊娠期抗凝治疗主要有4种策略[10,32,111, 112, 113, 114, 115]:(1)妊娠全程使用华法林;(2)妊娠全程使用普通肝素;(3)妊娠全程使用低分子肝素;(4)采用序次治疗,妊娠早期使用普通肝素或者低分子肝素,中晚期使用华法林。
华法林能穿过胎盘,可能导致流产、死胎、华法林胚胎病等。发育中的胎儿在妊娠6~12周左右最容易受到华法林的影响[117, 118]。华法林胚胎病和其他华法林相关并发症的风险可能呈剂量依赖性,当华法林日剂量≤5 mg时,华法林胚胎病及其他华法林相关并发症风险较低[119, 120, 121]。
对人工心脏机械瓣膜置换术后的妊娠患者,多项荟萃分析均证实妊娠期全程使用华法林对母亲最安全,低分子肝素抗凝治疗对胎儿最安全[119,122],而妊娠全程使用普通肝素对胎儿和母亲的安全性均有限。序次治疗不能消除抗凝相关的胎儿/新生儿不良事件。
参考国内外指南,根据患者妊娠孕周、华法林日剂量,以及患者使用意愿,推荐妊娠期抗凝方案见图4[10,32,111, 112, 113, 114, 115]。需要注意的是,如果使用普通肝素,需要监测APTT;如果使用低分子肝素,需要监测抗Ⅹa水平。如患者拒绝使用华法林,可考虑使用低分子肝素抗凝。


华法林基本不从母乳分泌[123],现有指南多数认为母亲服用华法林对母乳喂养婴儿的风险很小[32,115,124, 125];《药物与哺乳数据库》认为,服用华法林的乳母无需采取特殊预防措施[126]。研究发现,母亲服用华法林抗凝,其母乳和母乳喂养婴儿的血浆中均未检测到华法林,婴儿的凝血功能均在正常范围内且未出现不良反应[127, 128, 129]。
《药物与哺乳数据库》资料显示,达比加群酯、利伐沙班、阿哌沙班均可分泌入乳汁[130, 131, 132],虽然分泌入乳汁的量较少,但由于缺乏足够的循证证据,哺乳期不推荐使用DOAC。
推荐意见24:对于居家口服抗凝药的女性患者,推荐备孕期间到抗凝专科门诊评估是否适合妊娠及妊娠风险。备孕期间应加强妊娠监测,尽早发现妊娠,口服华法林的患者推荐备孕期继续华法林抗凝治疗直至确认怀孕,不建议提前更换为低分子肝素或肝素抗凝治疗。不推荐备孕期使用DOAC。(同意率:92%;推荐等级:强推荐;证据质量:B)
推荐意见25:目前尚无一种对母婴均最佳的抗凝方案,抗凝方案的选择需要根据疾病、孕周、母亲和胎儿安全性等综合考虑。对于机械瓣膜置换术后、伴严重泵功能减退的心脏病或房颤患者以及有血栓、栓塞高危因素的患者,华法林是妊娠期可以选择的口服抗凝药,DOAC禁用于妊娠期。(同意率:88%;推荐等级:强推荐;证据等级:A)
推荐意见26:哺乳期可以使用华法林抗凝治疗,需加强母亲INR监测,维持在目标范围内,并监测母乳喂养的婴儿是否有皮肤瘀青等出血表现。DOAC不推荐哺乳期使用。(同意率:80%;推荐强度:强推荐;证据等级:B)
多种药物通过各种机制与华法林发生相互作用,改变华法林的药代动力学。因此,建议服用华法林的患者在加用、减用或停用其他任何药物(包括中药、食品补充剂)时应加强INR监测。华法林与药物相互作用信息可参考《华法林抗凝治疗的中国专家共识》[32]。
影响DOAC的药物较少,根据药品说明书,除转换抗凝治疗,或给予维持中心静脉或动脉导管通畅所需剂量的普通肝素等特殊情况外,一般不与其他抗凝药联用。达比加群酯禁止联用环孢菌素、全身性酮康唑、伊曲康唑和决奈达隆,不推荐与他克莫司联用。艾多沙班可与P-糖蛋白(P-gp)抑制药(环孢素、决奈达隆、红霉素或酮康唑)联用,推荐剂量减为30 mg 每日1次。与DOAC避免联用的药物见表4。

与直接口服抗凝药(DOAC)避免联用药物
与直接口服抗凝药(DOAC)避免联用药物
| 药物名称 | 避免合用药物 |
|---|---|
| 达比加群酯 | P-糖蛋白诱导药:如利福平、圣约翰草、卡马西平、苯妥英 |
| 利伐沙班/阿哌沙班 | P-糖蛋白和强效CYP 3A4双重诱导药:如卡马西平、苯妥英、利福平、圣约翰草;P-糖蛋白和细胞色素P450(CYP)3A4双重抑制药:吡咯类抗真菌药(如酮康唑、伊曲康唑、伏立康唑及泊沙康唑)和HIV蛋白酶抑制剂(如利托那韦);利伐沙班避免合用决奈达隆 |
| 艾多沙班 | P-糖蛋白诱导药:利福平 |
绿叶蔬菜等多种食物可改变华法林的药代动力学,在服用华法林期间应注意保持饮食习惯稳定,常见食物与华法林相互作用见表5[133, 134]。

食物与华法林相互作用
食物与华法林相互作用
| 作用 | 食物 |
|---|---|
| 增强华法林药效 | 大量的大蒜、生姜、花椒、胡萝卜、西柚、芒果、葡萄柚、酒精(如合并肝疾病)、鱼油等 |
| 减弱华法林药效 | 富含维生素K1的食物(包括绿叶蔬菜、带皮的黄瓜、西芹、水芹、西兰花、甘蓝、动物肝脏)、绿茶、牛油果、紫菜等藻类、黄豆及豆制品等 |
《2021中国静脉血栓栓塞症防治抗凝药物的选用与药学监护指南》关于进食对口服抗凝药物的影响推荐意见为:(1)食物对华法林的抗凝作用影响较大,建议教育患者在华法林服药期间尽量保持饮食习惯稳定,尽量避免大量服用对抗凝作用影响较大的食物。对于饮食结构波动较大的患者,建议增加INR监测频率;(2)推荐服用15 mg或20 mg的利伐沙班时,与食物同服;其他DOAC和10 mg利伐沙班与食物相互作用不明显,可与或不与食物同时服用[133]。
10 mg利伐沙班的绝对生物利用度高(80%~100%),进食对药时曲线下面积(area under curve,AUC)或无影响。但是对于15 mg或20 mg的利伐沙班,空腹条件下服用吸收并不完全,与食物同服后,有较高的生物利用度,因此15 mg或20 mg利伐沙班应与食物同服。进食会使艾多沙班的生物利用度增加6%~22%。其他DOAC与食物相互作用不明显,可与或不与食物同时服用。
推荐意见27:多种药物可与华法林发生相互作用,服用华法林的患者如果在医师/药师的指导下需要加用或停用任何可能产生相互作用的药物(包括中药、保健品)时,应加强INR监测;如果INR波动较大,应在医师/药师的指导下调整华法林剂量,使INR在目标范围内。(同意率:84%;推荐强度:弱推荐;证据等级:良好实践主张)
推荐意见28:DOAC与少量药物存在药物相互作用,一些强效P-gp和CYP3A4的抑制剂/诱导剂会显著影响DOAC的血药浓度,应避免联合使用。(同意率:84%;推荐强度:弱推荐;证据等级:良好实践主张)
推荐意见29:绿叶蔬菜等食物对华法林的抗凝作用影响较大,患者在华法林服药期间应保持饮食习惯稳定,避免一次大量服用对抗凝作用影响较大的食物。对于饮食结构波动较大的患者,应增加INR监测频率。(同意率:84%;推荐强度:弱推荐;证据等级:良好实践主张)
推荐意见30:对于需口服单次剂量≥15 mg利伐沙班的患者,应与餐同服药物;其他DOAC和单次剂量≤10 mg利伐沙班受食物影响小。(同意率:88%;推荐强度:弱推荐;证据等级:良好实践主张)
随着血栓栓塞性疾病防治经验的积累及相关研究的开展,本共识在发展中可能会表现出临床应用中的局限性。为此,专家组将与时俱进,继续跟进相关研究证据,并及时更新。本共识内容仅供临床药师和临床医师实践参考,不具有法律约束性质;专家组不承担应用本共识产生不良后果的任何法律责任。本共识以循证医学为依据,为提高口服抗凝药的安全有效使用提供推荐意见,专家组人员与所提及的药品、检测仪器等相关机构不存在利益往来,此共识是所有专家组人员基于平等、互助、发展的前提下参与制订的。
共识制订专家组
组长:张毕奎(中南大学湘雅二医院药学部)
副组长:张玉(华中科技大学同济医学院附属协和医院);周新民(中南大学湘雅二医院心血管外科);肖颖彬(陆军军医大学第二附属医院心血管外科)
执笔专家:谭胜蓝(中南大学湘雅二医院药学部);刘易慧(华中科技大学同济医学院附属协和医院药学部);徐航(南京大学医学院附属鼓楼医院药学部);董淑杰(北京大学第三医院药学部)
秘书组(按姓氏汉语拼音排序):戴婷婷(中南大学湘雅医院药学部);顾智淳(上海交通大学医学院附属仁济医院药学部);李波霞(兰州大学第一医院药学部);林琦(福建医科大学附属协和医院药学部);秦琼(苏州大学附属第一医院药学部);易秋莎(四川大学华西第二医院药学部);尹文俊(中南大学湘雅三医院药学部)
审核专家(按姓氏汉语拼音排序):陈孝(中山大学附属第一医院药学部);葛卫红(南京大学医学院附属鼓楼医院药学部);胡敏(中南大学湘雅二医院检验医学科);胡信群(中南大学湘雅二医院心血管内科);李鑫(中南大学湘雅二医院血管外科);林厚文(上海交通大学医学院附属仁济医院药学部);刘茂柏(福建医科大学附属协和医院药学部);刘韶(中南大学湘雅医院药学部);刘志刚(泰达国际心血管病医院);罗红(中南大学湘雅二医院呼吸内科);缪丽燕(苏州大学附属第一医院);舒畅(中国医学科学院阜外医院血管外科中心 中南大学湘雅二医院血管中心);孙爱军(复旦大学附属中山医院心血管内科);唐可京(中山大学附属第一医院呼吸与危重症医学科/药学部);武新安(兰州大学第一医院药学部);肖颖彬(陆军军医大学第二附属医院心血管外科);许建屏(中国医学科学院阜外医院心血管外科);张毕奎(中南大学湘雅二医院药学部);张伶俐(四川大学华西第二医院);张玉(华中科技大学同济医学院附属协和医院);赵荣生(北京大学第三医院);郑英丽(中国医学科学院阜外医院药学部);周新民(中南大学湘雅二医院心血管外科);周洲(中国医学科学院阜外医院实验诊断中心);左笑丛(中南大学湘雅三医院)
中国药学会医院药学专业委员会. 口服抗凝药居家管理中国专家共识(2024版)[J]. 中华医学杂志, 2024, 104(28): 2595-2612. DOI: 10.3760/cma.j.cn112137-20231102-00987.
所有作者声明不存在利益冲突




























