
探讨艾米替诺福韦(TMF)在治疗65岁以上慢性乙型肝炎及肝硬化患者中的有效性及安全性。
纳入临沂市人民医院45例慢性乙型肝炎及肝硬化患者,TMF治疗48周比较治疗第12、24、48周时病毒学应答率、HBV DNA较基线下降水平,治疗前后乙型肝炎表面抗原(HBsAg)、丙氨酸转氨酶(ALT)、肾小球滤过率(eGFR)、肌酐、甘油三酯(TG)、总胆固醇(TC)、高密度脂蛋白胆固醇(HDL-C)、低密度脂蛋白胆固醇(LDL-C)及血磷、血脂的变化及48周时ALT复常率变化。以P<0.05表示差异具有统计学意义。
入组患者年龄为69.0(67.0,72.5)岁。TMF治疗12、24、48周的完全病毒学应答率为32.4%(12/37)、70.0%(28/40)、84.6%(33/39),HBV DNA较基线有明显下降(P值均<0.05)。治疗48周后HBsAg水平下降(P<0.05),未出现HBsAg转阴及血清转换患者。治疗48周后ALT水平下降(P<0.05)。治疗48周时ALT复常率分别为88.9%(16/18)、70.4%(19/27)。基线与治疗48周后的eGFR、肌酐、磷、TG、TC、HDL-C、LDL-C水平差异无统计学意义(P值均>0.05),暂未观察到严重不良反应事件发生。
对于65岁以上慢性乙型肝炎及肝硬化患者,TMF可显著抑制HBV DNA复制,且ALT复常率高、耐受性好。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
乙型肝炎病毒(hepatitis B virus,HBV)感染是全球公共卫生问题。我国是HBV感染中高流行区域[1],虽然我国乙型肝炎表面抗原(hepatitis B surface antigen,HBsAg)流行率逐年下降,但由于我国人群基数大,HBV感染仍数量众多。随着人口老龄化进程,慢性乙型肝炎患者中肝脏并存病的发生率会逐渐增加,抗病毒药物的应用能延缓肝病的进展,但同时其对于骨、肾等的相关不良反应也应引起重视。
对于慢性乙型肝炎患者的抗病毒治疗方案,我国《慢性乙型肝炎防治指南(2022年版)》[2]推荐的一线用药为恩替卡韦、富马酸替诺福韦酯(tenofovir disoproxil fumarate,TDF)、富马酸丙酚替诺福韦(tenofovir alafenamide fumarate,TAF)和艾米替诺福韦(tenofovir amibufenamide,TMF)。TDF具有强效抑制病毒复制,但血浆稳定性差,药物经肾脏代谢负担较大,观察性研究提示使用TDF的患者,尤其是高龄或绝经期患者,有新发或者加重肾功能损伤及骨质疏松的风险[3]。TMF属于核苷(酸)类逆转录酶抑制剂,是替诺福韦磷酰胺酯化后的前药,药物脂溶性增加,能够较为容易地被动转运进入肝细胞,进而提高肝细胞内活性代谢产物二磷酸替诺福韦的浓度,最终提高治疗效果[4],也具有良好的骨、肾安全性。目前研究较少关注TMF在65岁以上慢性乙型肝炎及肝硬化患者的临床研究,本研究将探讨TMF在治疗该类人群上的有效性及安全性。
1.研究对象:收集2021年11月至2023年9月临沂市人民医院感染科门诊接受TMF抗病毒治疗的65岁以上慢性乙型肝炎及肝硬化患者资料,纳入标准:(1)符合我国《慢性乙型肝炎防治指南(2022年版)》[1]诊断标准的慢性乙型肝炎及肝硬化初治及恩替卡韦或TDF经治患者;(2)年龄65岁以上,性别不限;(3)可检测到HBV DNA。排除标准:(1)合并其他肝病患者,包括丙型病毒性肝炎、酒精性肝炎、药物性肝炎、自身免疫性肝病等;(2)合并肝细胞癌或其他恶性肿瘤患者;(3)乳糖不耐受者或对该药过敏者;(4)妊娠及哺乳期患者。本研究已通过临沂市人民医院医学伦理委员会批准(YX200399),所有受试者入组前均签署了知情同意书。本研究项目已在中国临床试验注册中心注册(注册号:ChiCTR2200064306)。
2.研究方法:入组后给予25 mg TMF,每日1次,随食物服用。收集患者的人口学资料、基础病史、随访基线及治疗过程临床资料,包括HBsAg、HBV DNA、总胆红素(total bilirubin,TBil)、丙氨酸转氨酶(alanine transaminase,ALT)、估算肾小球滤过率(estimated glomerular filtration rate,eGFR)、肌酐、磷、甘油三酯(triglyceride,TG)、总胆固醇(cholesterol total,TC)、高密度脂蛋白胆固醇(high density lipoprotein cholesterol,HDL-C)、低密度脂蛋白胆固醇(low density lipoprotein cholesterol,LDL-C)。同时收集治疗过程中的不良反应事件。
3.观察指标:主要终点为治疗12、24、48周完全病毒学应答(HBV DNA<100 IU/ml定义为完全病毒学应答)及HBV DNA较基线下降程度;次要终点为HBsAg转阴率及血清转换率,基于实验室标准(正常上限值:男≤50 U/L,女≤40 U/L)及美国肝病学会(AASLD)2018版指南[5](正常上限值:男≤35 U/L,女≤25 U/L)的ALT复常率,治疗前后HBsAg、ALT、eGFR、肌酐、磷、TG、TC、HDL-C、LDL-C的变化情况。
4.检测方法:QuantStudio 5实时荧光定量PCR系统(美国ThermoFisher Scientific公司)及配套试剂检测血清HBV DNA;使用AU5800全自动生化分析仪(美国贝克曼库尔特有限公司)检测ALT;使用生产的Architect i2000化学发光免疫分析仪(美国雅培公司)及配套试剂检测血清HBV标志物[HBsAg<0.05 IU/ml定义为HBsAg转阴,血清乙型肝炎表面抗体(抗-HBs)≥10 IU/ml定义为抗-HBs阳性]。
5.统计学方法:采用SPSS 26.0软件进行数据分析。非正态分布的计量资料采用中位数及四分位数[M(Q1,Q3)]表示,配对样本的比较采用Wilcoxon符号秩检验进行分析。正态分布的连续变量资料采用均值±标准差(±s)表示,配对样本的比较采用配对t检验进行分析。计数资料采用百分比(%)描述,采用χ2检验进行分析,组间多重比较采用Bonferroni校正的χ2检验进行分析。P<0.05表示差异具有统计学意义。
1.一般资料:本研究共入组45例患者,年龄为69.0(67.0,72.5)岁,其中初治27例,经治患者18例;乙型肝炎e抗原(hepatitis B e antigen,HBeAg)阳性27例,HBeAg阴性18例;肝硬化患者15例,非肝硬化患者30例;合并糖尿病患者8例,合并高血压和/或冠心病患者6例。基线资料见表1。
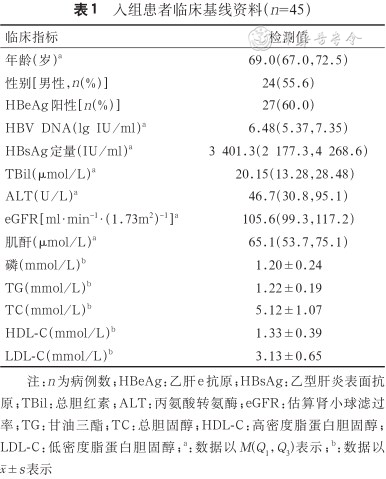
入组患者临床基线资料(n=45)
入组患者临床基线资料(n=45)
| 临床指标 | 检测值 |
|---|---|
| 年龄(岁)a | 69.0(67.0,72.5) |
| 性别[男性,n(%)] | 24(55.6) |
| HBeAg阳性[n(%)] | 27(60.0) |
| HBV DNA(lg IU/ml)a | 6.48(5.37,7.35) |
| HBsAg定量(IU/ml)a | 3 401.3(2 177.3,4 268.6) |
| TBil(μmol/L)a | 20.15(13.28,28.48) |
| ALT(U/L)a | 46.7(30.8,95.1) |
| eGFR[ml·min-1·(1.73m2)-1]a | 105.6(99.3,117.2) |
| 肌酐(μmol/L)a | 65.1(53.7,75.1) |
| 磷(mmol/L)b | 1.20±0.24 |
| TG(mmol/L)b | 1.22±0.19 |
| TC(mmol/L)b | 5.12±1.07 |
| HDL-C(mmol/L)b | 1.33±0.39 |
| LDL-C(mmol/L)b | 3.13±0.65 |
注:n为病例数;HBeAg:乙肝e抗原;HBsAg:乙型肝炎表面抗原;TBil:总胆红素;ALT:丙氨酸转氨酶;eGFR:估算肾小球滤过率;TG:甘油三酯;TC:总胆固醇;HDL-C:高密度脂蛋白胆固醇;LDL-C:低密度脂蛋白胆固醇;a:数据以M(Q1,Q3)表示;b:数据以±s表示
2.病毒学应答情况:TMF治疗12、24、48周后,完全病毒学应答率在所有患者中分别为32.4%(12/37)、70.0%(28/40)、84.6%(33/39),差异具有统计学意义(χ2=23.471,P<0.001;12周对比24周:χ2=10.867,P=0.003;12周对比48周:χ2=21.407,P<0.001;24周对比48周:χ2=2.398,P=0.366)(图1A)。HBeAg阳性及阴性患者的12、24、48周完全病毒学应答率分别为22.7%(5/22)对比46.7%(7/15)、56.5%(13/23)对比88.2%(15/17)、78.3%(18/23)对比93.8%(15/16)(图1B);初治及经治患者的完全病毒学应答率分别为33.3%(7/21)对比33.3%(5/15)、76.9%(20/26)对比64.3%(9/14)、95.3%(20/21)对比72.2%(13/18)(图1C);肝硬化及非肝硬化患者的完全病毒学应答率分别为33.3%(4/12)对比32.0%(8/25)、73.3%(11/15)对比68.0%(17/25)、100%(13/13)对比76.9%(20/26)(图1D)。
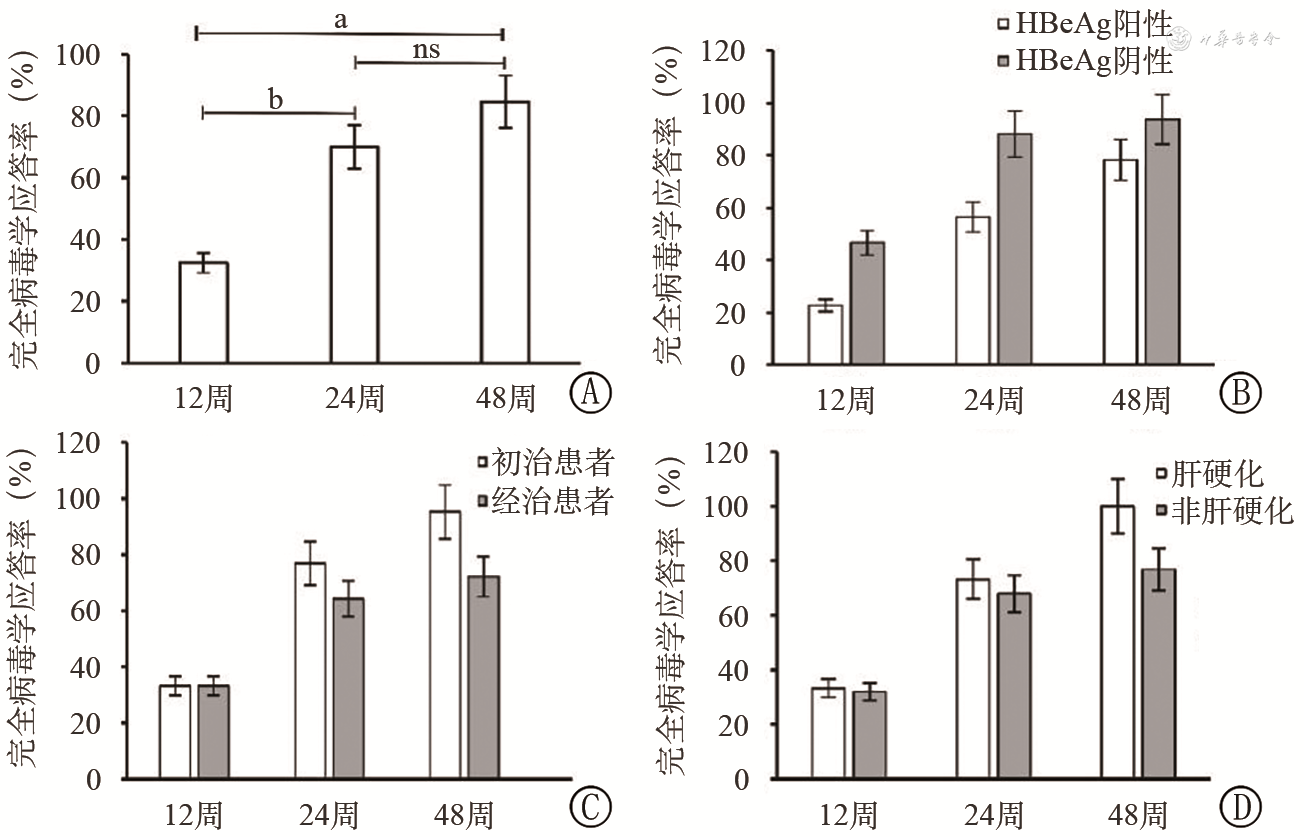

注:HBeAg:乙型肝炎e抗原;A:45例患者在治疗12、24、48周的完全病毒学应答率;B:HBeAg阳性(n=23)及阴性(n=17)患者对应治疗周期的完全病毒学应答率;C:初治(n=26)及经治(n=18)患者对应治疗周期的完全病毒学应答率,经治患者为使用恩替卡韦或富马酸替诺福韦酯治疗;D:肝硬化(n=15)及非肝硬化(n=26)患者对应治疗周期的完全病毒学应答率;ns:差异无统计学意义;a:P<0.05;b:P<0.001
12、24、48周HBV DNA较基线下降水平(lg值)分别为3.17(2.79,3.80)、4.07(3.13,4.66)、4.38(3.07,5.22),与基线比较差异均具有统计学意义(P值均<0.001)(图2)。
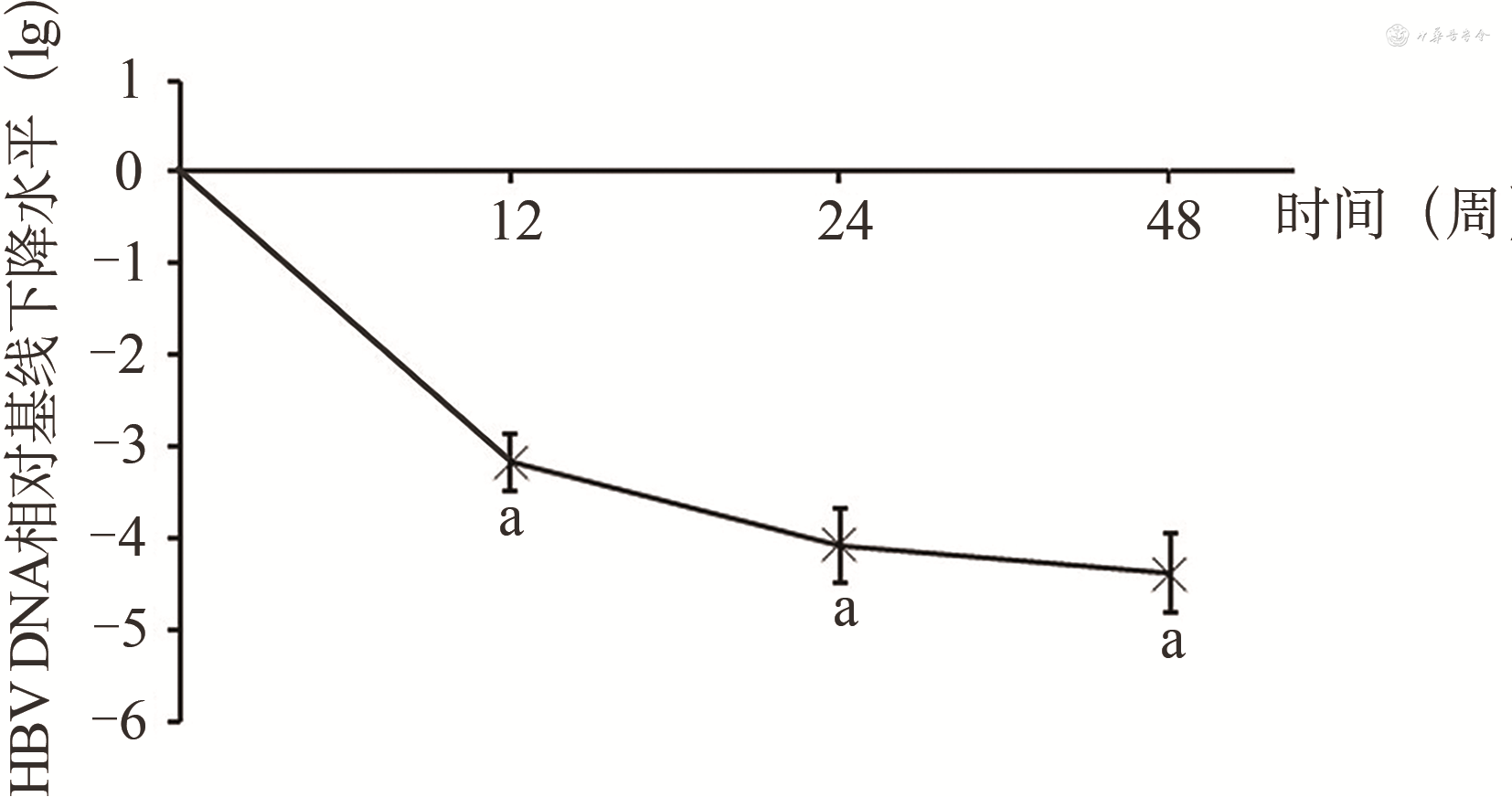

注:HBV:乙型肝炎病毒;a:P<0.001
3.HBsAg水平变化情况:治疗48周时患者HBsAg水平为2 150.8(661.1,4 276.3)IU/ml,与基线数据相比,差异具有统计学意义(Z=-2.040,P=0.041)(图3A)。暂未出现HBsAg转阴及血清转换患者。
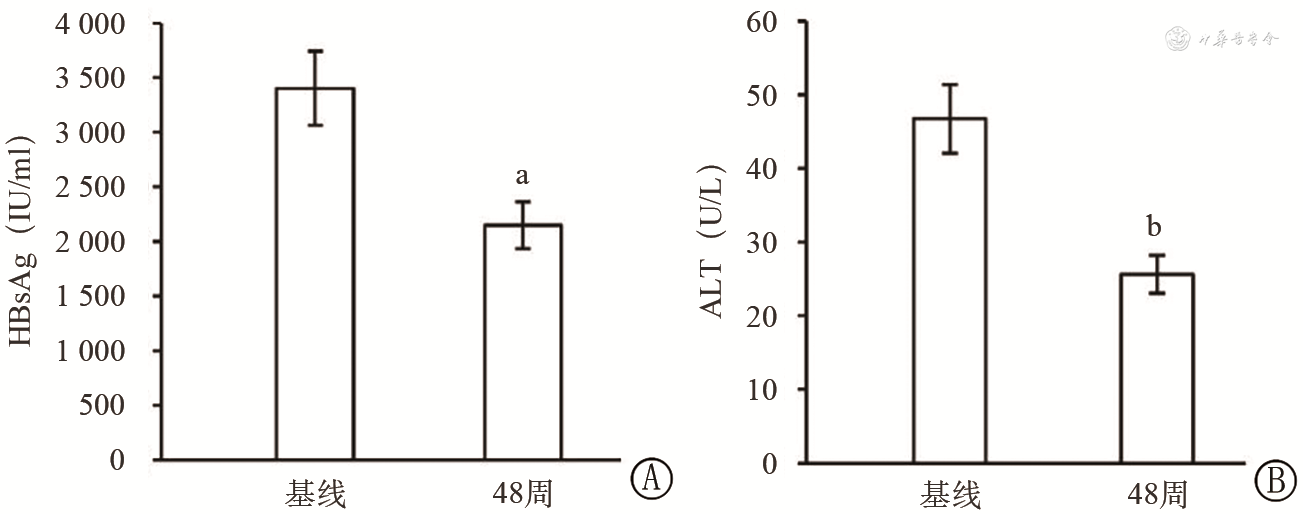

注:HBsAg:乙型肝炎表面抗原;ALT:丙氨酸转氨酶;a:P<0.05;b:P<0.001
4.生物化学应答情况:治疗48周时ALT水平为25.6(18.7,33.4)U/L,与基线数据相比,差异具有统计学意义(Z=-3.672,P<0.001)(图3B)。48周时ALT复常率分别为88.9%(16/18)、70.4%(19/27)。
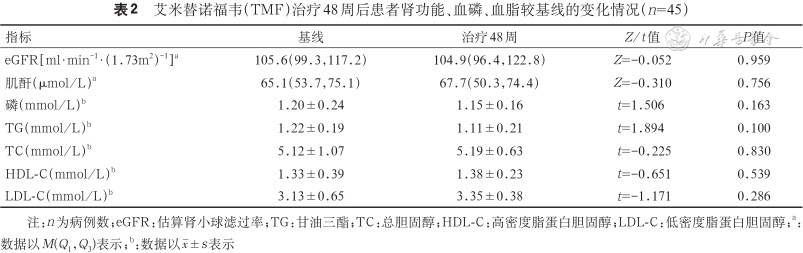
5.肾功能、血磷、血脂变化及不良事件的评估:治疗前后eGFR、肌酐、血磷、TG、TC、HDL-C、LDL-C水平差异无统计学意义(P值均>0.05)。所有患者口服TMF后耐受性良好,暂未观察到严重不良反应事件发生(表2)。
艾米替诺福韦(TMF)治疗48周后患者肾功能、血磷、血脂较基线的变化情况(n=45)
艾米替诺福韦(TMF)治疗48周后患者肾功能、血磷、血脂较基线的变化情况(n=45)
| 指标 | 基线 | 治疗48周 | Z/t值 | P值 |
|---|---|---|---|---|
| eGFR[ml·min-1·(1.73m2)-1]a | 105.6(99.3,117.2) | 104.9(96.4,122.8) | Z=-0.052 | 0.959 |
| 肌酐(μmol/L)a | 65.1(53.7,75.1) | 67.7(50.3,74.4) | Z=-0.310 | 0.756 |
| 磷(mmol/L)b | 1.20±0.24 | 1.15±0.16 | t=1.506 | 0.163 |
| TG(mmol/L)b | 1.22±0.19 | 1.11±0.21 | t=1.894 | 0.100 |
| TC(mmol/L)b | 5.12±1.07 | 5.19±0.63 | t=-0.225 | 0.830 |
| HDL-C(mmol/L)b | 1.33±0.39 | 1.38±0.23 | t=-0.651 | 0.539 |
| LDL-C(mmol/L)b | 3.13±0.65 | 3.35±0.38 | t=-1.171 | 0.286 |
注:n为病例数;eGFR:估算肾小球滤过率;TG:甘油三酯;TC:总胆固醇;HDL-C:高密度脂蛋白胆固醇;LDL-C:低密度脂蛋白胆固醇;a:数据以M(Q1,Q3)表示;b:数据以±s表示
TMF作为我国首个原研口服抗HBV药物,通过磷酰胺酯化前药技术,实现替诺福韦肝细胞靶向输送,提高了肝细胞内活性代谢产物浓度的同时,降低血浆中替诺福韦的暴露量,进而高效抑制病毒复制的同时,也降低了长期使用的安全风险,有利于患者长期获益[4]。本研究为应用TMF治疗65岁以上慢性乙型肝炎及肝硬化患者的真实世界研究。
本研究中,基线HBV DNA为6.48 lg10IU/ml,治疗12、24、48周后总体完全病毒学应答率分别为32.4%、70.0%、84.6%,高于TMF Ⅲ期临床试验中治疗48周时总体病毒学应答率的60.7%[6]。其中在HBeAg阳性患者,治疗12、24、48周时完全病毒学应答率分别为22.7%、56.5%、78.3%,高于TMF Ⅲ期临床试验中治疗48周的50.2%和TDF治疗48周的53.7%[6, 7, 8]。在HBeAg阴性患者中,治疗12、24、48周时完全病毒学应答率分别为46.7%、88.2%、93.8%,高于TMF Ⅲ期临床试验中治疗48周的88.9%和TDF治疗48周的87.8%[6, 7, 8]。本研究TMF治疗HBeAg阳性患者48周的完全病毒学应答率高于TMF Ⅲ期临床试验中治疗96周的70.8%和TDF治疗96周的72%[9, 10],而HBeAg阴性患者48周的完全病毒学应答率与TMF Ⅲ期临床试验中治疗96周的93.9%和TDF治疗96周的93.9%结果相当[9, 10]。另外,TMF用于治疗肝硬化仅在TMF治疗48周及96周随访结果的Ⅲ期临床试验中有报道[9],研究纳入了125例有乙型肝炎肝硬化患者,经过24、48、96周随访显示出与TDF有相当的抗病毒疗效,于96周时达到完全病毒学应答的患者,HBV DNA低于69 IU/ml大约为52%。最近一项TMF治疗乙型肝炎肝硬化患者的研究表明,TMF治疗24周时代偿期HBV相关肝硬化患者的病毒学应答率为100%[11]。本研究显示,TMF治疗24周时代偿期HBV相关肝硬化患者的病毒学应答率为73.3%,于治疗48周时病毒学应答率达到100%,本研究病毒学应答率普遍偏高,考虑与年龄大于65岁尤其是存在肝硬化的患者的病毒载量基线水平偏低,以及本研究用于评估完全病毒学应答的HBV DNA标准有关。若采用HBV DNA<20 IU/ml的标准评估,将会发现更多未能实现完全病毒学应答的患者。老年患者因肝肾等器官功能减退,是否会减缓药物的代谢排泄,从而影响病毒学应答仍是值得探讨的问题。此外,在经治患者中TMF治疗12、24、48周时病毒学应答率分别为33.3%、64.3%、72.2%,提示换用TMF仍然可以获得良好的病毒学应答。
HBsAg转阴可改善慢性乙型肝炎患者预后[12],TMF的Ⅲ期临床试验中仅有0.6%患者实现HBsAg转阴,本研究中暂未出现HBsAg转阴及血清转换患者。考虑与该研究治疗时间短,老年患者免疫功能相对低下,且部分患者存在基础疾病,尚不足以使患者出现HBsAg转阴甚至发生血清学转换有关,其次是存在经治患者抗病毒治疗效果相对欠佳的问题。但在HBsAg水平上,本研究基线与治疗48周的差异具有统计学意义,但本研究样本量小,且随访时间短,需进一步扩大样本量及延长随访时间进一步评估。在本研究设定的标准下,48周ALT复常率分别为88.9%(16/18)、70.4%(19/27)。实验室设定标准的ALT复常率略高于TMF Ⅲ期临床试验中48周时的83.8%[6]。AASLD标准的ALT复常率略低于TMF Ⅲ期临床试验中48周时的72.1%[6],但高于TAF治疗48周时的50%和TDF治疗48周时的64.6%[6]。这提示TMF治疗65岁以上慢性乙型肝炎及肝硬化患者可以获得良好的生化学应答率。
慢性乙型肝炎患者应用核苷酸类药物抗病毒治疗期间的骨、肾安全性和对血脂的影响是临床医师关注的问题,尤其是高龄合并高危因素患者。因此,在抗病毒药物的选择上要求具有更高的安全性。目前,指南推荐的TDF抗病毒效果显著[13, 14],但在一项随访近10年的临床研究中,使用该药物治疗期间大约5.1%的患者出现肾功能损伤[15]。TMF的Ⅲ期临床研究数据显示,与TDF组相比,TMF组抗病毒治疗48周时出现eGFR下降、肌酐增加的比率降低,TDF组出现肾损伤的患者比TMF组高8.67%[6]。本研究结果显示,eGFR、肌酐在治疗前后差异无统计学意义,表明TMF对65岁以上患者具有良好的肾安全性。在治疗前后患者的血磷水平差异无统计学意义,但未对入组的患者进行骨密度的检测,尚需完善骨密度的检测评估骨安全性。在血脂方面,我国学者Chen等[16]研究表明TMF治疗的患者可出现某些血脂指标的轻微异常,但其临床意义尚未清楚。因其研究样本量较少,相关结论有待大样本临床研究验证。在本研究中表现为在治疗48周时TG轻微下降,TC、HDL-C、LDL-C均轻微升高,但差异无统计学意义,老年患者口服TMF治疗48周,目前未发现对血脂有明显影响,但患者血脂受饮食等混杂因素影响比较大,尚需进一步扩大样本量、延长随访时间,并尽量减少饮食等对血脂影响的混杂因素,进一步评估TMF对老年患者血脂的影响。目前核苷(酸)类药物引起脂质代谢异常原因尚未明确,长期影响有待更长时间的随访及监测,同时提示对于合并心血管系统疾病的患者,在使用抗病毒药物期间注意监测血脂变化,必要时使用降脂药物。
本研究对于65岁以上慢性乙型肝炎及肝硬化患者使用TMF治疗发现,TMF能快速抑制HBV DNA复制,且ALT复常率高,耐受性好。但本研究样本量少,随访时间短,未获取组织学证据及检测骨密度,病毒载量未进行高敏定量检测,仍需进一步扩大样本量、延长随访时间,进一步评估在65岁以上患者中TMF的有效性及安全性。
褚萨萨, 刘兴, 徐成, 等. 艾米替诺福韦治疗65岁以上慢性乙型肝炎及肝硬化患者的有效性及安全性[J]. 中华肝脏病杂志, 2024, 32(10): 904-909. DOI: 10.3760/cma.j.cn501113-20240829-00402.
所有作者均声明不存在利益冲突



























