
研究早产儿动脉导管未闭(PDA)对脑血流动力学的影响及其与脑室周围-脑室内出血(PIVH)的相关性。
对85例胎龄≤34周、出生体质量≤2 000 g的早产儿进行前瞻性病例-对照研究,在其出生后至48 h、48~96 h、96~120 h、120~168 h进行床旁超声心动图和颅脑超声检查,监测有无PDA发生和大脑前、中动脉(ACA、MCA)的收缩期峰流速(Vs)、舒张末期流速(Vd)、平均流速(Vm)、搏动指数(PI)和阻力指数(RI),观察有无PIVH的发生。
根据出生后72 h内的超声心动图结果及相应临床症状,将观察对象分为以下3组:(1)有血流动力学意义的PDA组(hsPDA组)23例;(2)无血流动力学意义的PDA组(nhsPA组)38例;(3)无PDA组(non-PDA,nPDA组)24例。3组在胎龄、体质量方面差异无统计学意义。单因素及多因素Logistic回归分析发现出生后48 h内有创机械通气与hsPDA有相关性(χ2=11.182,P=0.019; OR=10.06,P=0.039);对3组脑血流动力学参数进行重复测量方差分析发现hsPDA组大脑ACA、MCA的Vd值显著低于nhsPDA组(P=0.000,P=0.001)和nPDA组(P=0.003,P=0.013),而ACA、MCA的搏动指数(PI)、阻力指数(RI)值显著高于其他2组。hsPDA组在出生后7 d复查,PDA关闭组(n=7)的RI、PI值较未闭组(n=16)降低,而Vd值升高;生后7 d PDA关闭组与nPDA组(n=24)比较各血流参数的差异无统计学意义。PDA关闭与否各组间PIVH的严重程度差异无统计学意义,然而hsPDA组发生重度PIVH的比例高于其他2组(17.39%比8.33%比5.26%, χ2=2.405,P=0.280)。
早产儿出生后48 h内有创机械通气与发生hsPDA有相关性;早产儿hsPDA可造成脑血流动力学变化,并可能增加重度PIVH的发生率。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
动脉导管(ductus ateriosus,DA)是胎儿期连接降主动脉与肺动脉的重要通路,使右心室流出血液不经过无通气功能的胎儿肺[1]直接进入体循环。健康足月新生儿多在出生后72 h内关闭。早产儿DA未闭(patent ductus ateriosus,PDA),又称早产儿动脉导管持续开放,主要由于其动脉导管平滑肌发育不成熟,对高体积分数氧的敏感性低,而对前列腺素敏感性高,在出生后早期仍保持开放状态,且胎龄越小,体质量越低,PDA发生率越高:小于28周早产儿PDA的发病率高达75%[2]。当DA循环中左向右分流量大,超过体循环的50%时,可出现肺血流增多,体循环血流减少,引起体循环各脏器灌注减少,出现血流动力学变化,可能与发生脑室内出血[3]、肺水肿[4]、坏死性小肠结肠炎、支气管肺发育不良等有关[5],严重者可导致死亡。早产儿脑血管发育不成熟,血流动力学变化明显时易出现脑室周围-脑室内出血(periventricular-intraventricular hemorrhages,PIVH),从而增加早产儿脑损伤、脑室周围白质软化、脑积水的风险,75%的患儿出现神经系统发育异常[6]。本研究主要通过床旁超声心动图和颅脑超声检查观察早产儿出生后早期PDA对脑血流动力学的影响及其与PIVH的相关性,为临床指导早产儿PDA的干预治疗以及预防脑损伤提供相关依据。
2012年10月至2013年9月于出生后24 h内入住北京大学第三医院NICU,胎龄≤34周、出生体质量≤2 000 g的早产儿。出生后有严重先天畸形、重度窒息、休克、严重贫血的早产儿不纳入研究。将出生后7 d内死亡及放弃治疗的早产儿剔除研究组。
监测和记录研究对象的生命体征、经皮氧饱和度、呼吸支持方式、喂养方式、肺表面活性物质(PS)的应用等;记录患儿母亲可能与PDA发生相关的产前高危因素(产前感染、胎膜早破、妊娠高血压病、妊娠糖尿病、胎盘早剥、产前出血、产前应用糖皮质激素等);在出生后~48 h、48~96 h、96~120 h、120~168 h进行床旁超声心动图、颅脑超声检查。根据超声心动图结果分为PDA组和非PDA(nPDA)组,根据PDA的内径大小、有无临床症状将PDA组分为有血流动力学意义的PDA(hsPDA)组(PDA内径≥1.6 mm,导管分流量大,伴有明显心脏杂音、心动过速、呼吸增快、脉压差增大、低血压、机械通气治疗)[7,8]和无血流动力学意义的PDA(nhsPDA)组。对hsPDA组患儿予口服布洛芬治疗:首剂10 mg/kg,第2、3剂每次5 mg/kg,每剂间隔时间24 h。出生后7 d,根据床旁超声心动图结果将hsPDA组分为治疗后关闭组和未闭组。行颅脑超声观察有无PIVH;监测大脑前动脉(ACA)、中动脉(MCA)的5个脑血流参数值,包括收缩期峰流速(Vs)、舒张末期流速(Vd)、平均流速(Vm)、搏动指数(PI)、阻力指数(RI)。超声检查由儿科具有超声资质的同一专业人员完成,超声仪器:mindray UMT-200,超声探头频率8 MHz。
根据Papil诊断标准将早产儿PIVH分为Ⅰ~Ⅳ度,颅内出血Ⅰ~Ⅱ度为轻度,Ⅲ~Ⅳ度为重度。本研究中早产儿PIVH分度以床旁颅脑超声检查颅内出血程度最重时为准,宫内即发生颅内出血并处于稳定期的患儿纳入PIVH对照组。
本研究中,早产儿疾病诊断标准、机械通气指征均参照《实用新生儿学》第4版[9],布洛芬治疗方法参照《早产儿管理指南》[10]。维持患儿的经皮氧饱和度在88%~93%,机械通气患儿均予保护性肺通气策略,维持动脉血二氧化碳分压[pa(CO2)]在60 mmHg(1 mmHg=0.133 kPa)以内,以减少因动脉血氧分压[pa(O2)]或pa(CO2)波动引起的脑血流动力学变化。
本研究于2012年10月通过北京大学第三医院伦理委员会审核,试验前均经过患儿直系亲属的知情同意。
采用SPSS 20软件进行统计分析,计量资料用 ±s表示,采用t检验或方差分析。计数资料计算其构成比,采用χ2检验。以产前感染、48 h机械通气、72 h机械通气为自变量,以PDA分组为应变量,用后退法筛选变量进行多因素Logistic回归分析。每组样本量为自变量个数的5倍以上,符合样本量要求。多组间脑血流参数比较采用重复测量方差分析。P<0.05为差异有统计学意义。
±s表示,采用t检验或方差分析。计数资料计算其构成比,采用χ2检验。以产前感染、48 h机械通气、72 h机械通气为自变量,以PDA分组为应变量,用后退法筛选变量进行多因素Logistic回归分析。每组样本量为自变量个数的5倍以上,符合样本量要求。多组间脑血流参数比较采用重复测量方差分析。P<0.05为差异有统计学意义。
符合入选标准的病例共91例,其中3例患儿出生7 d内放弃治疗,3例资料不全,被剔除出研究组,最终85例早产儿纳入研究组。其中男54例,女31例;胎龄(31.27±1.88)周(25~34周);出生体质量(1 417±316) g(800~1 999 g);剖宫分娩60例,自然分娩25例;单胎38例,双胎47例;轻度窒息6例。根据出生后2~3 d超声心动图结果及临床症状,将85例分为hsPDA组(23例)、nhsPDA组(38例)、nPDA组(24例)。单因素分析结果显示,3组间性别、胎龄、双胎、生产方式、出生体质量、产前应用地塞米松、出生后应用PS差异均无统计学意义。母亲产前高危因素:妊娠期高血压病、妊娠期糖尿病、宫内窘迫、胎盘早剥、产前出血、胎膜早破在3组间的差异无统计学意义。而母亲产前感染、出生后48 h、72 h通气模式在3组间差异有统计学意义,见表1;通过多因素Logistic回归分析结果发现出生后48 h内机械通气与hsPDA有相关性(OR=10.06,P=0.039)。
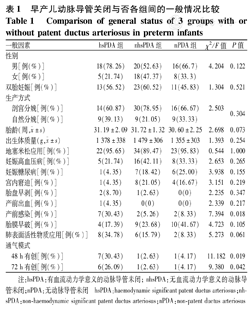
早产儿动脉导管关闭与否各组间的一般情况比较
Comparison of general status of 3 groups with or without patent ductus arteriosus in preterm infants
早产儿动脉导管关闭与否各组间的一般情况比较
Comparison of general status of 3 groups with or without patent ductus arteriosus in preterm infants
| 一般因素 | hsPDA组 | nhsPDA组 | nPDA组 | χ2/F值 | P值 | |
|---|---|---|---|---|---|---|
| 性别 | ||||||
| 男[例(%)] | 18(78.26) | 20(52.63) | 16(66.7) | 4.204 | 0.122 | |
| 女[例(%)] | 5(21.74) | 18(47.37) | 8(33.3) | |||
| 双胎妊娠[例(%)] | 13(56.52) | 23(60.52) | 11(45.83) | 1.304 | 0.521 | |
| 生产方式 | ||||||
| 剖宫分娩[例(%)] | 14(60.87) | 30(78.95) | 16(66.67) | 2.503 | 0.304 | |
| 自然分娩[例(%)] | 9(39.13) | 9(21.05) | 9(33.33) | |||
胎龄(周, ±s) ±s) | 31.19±2.09 | 31.72±1.32 | 30.60±2.25 | 2.698 | 0.073 | |
出生体质量(g, ±s) ±s) | 1 378±338 | 1 479±306 | 1 355±303 | 1.393 | 0.254 | |
| 地塞米松应用[例(%)] | 22(95.65) | 34(89.47) | 23(95.83) | 0.544 | 1.000 | |
| 妊娠高血压病[例(%)] | 5(21.74) | 16(42.11) | 8(33.33) | 2.653 | 0.265 | |
| 妊娠糖尿病[例(%)] | 1(4.35) | 7(18.42) | 6(25.00) | 3.938 | 0.155 | |
| 宫内窘迫[例(%)] | 1(4.35) | 8(21.05) | 4(16.67) | 3.151 | 0.219 | |
| 胎盘早剥[例(%)] | 2(8.70) | 1(2.63) | 0(0) | 2.235 | 0.347 | |
| 产前出血[例(%)] | 1(4.35) | 0(0) | 0(0) | 2.339 | 0.217 | |
| 产前感染[例(%)] | 7(30.43) | 2(5.26) | 2(8.33) | 7.394 | 0.018 | |
| 胎膜早破[例(%)] | 4(17.39) | 9(23.68) | 10(41.67) | 4.723 | 0.105 | |
| 肺表面活性物质应用[例(%)] | 8(34.78) | 6(15.79) | 2(8.33) | 5.273 | 0.061 | |
| 通气模式 | ||||||
| 48 h有创[例(%)] | 7(30.43) | 1(2.63) | 1(4.17) | 11.182 | 0.019 | |
| 72 h有创[例(%)] | 6(26.09) | 1(2.63) | 1(4.17) | 9.380 | 0.042 | |
注:hsPDA:有血流动力学意义的动脉导管未闭;nhsPDA:无血流动力学意义的动脉导管未闭;nPDA:无动脉导管未闭 hsPDA:haemodynamic significant patent ductus arteriosus;nhsPDA:non-haemodynamic significant patent ductus arteriosus;nPDA:non-patent ductus arteriosus
本研究中,对3组患儿出生后~48 h、48~96 h、96~120 h、120~168 h脑血流参数进行重复测量方差分析发现:hsPDA组ACA、MCA的Vd值显著低于nhsPDA和nPDA组(P=0.000,P=0.001;P=0.003,P=0.013),见图1,图2;ACA的PI、MCA的PI、ACA的RI、MCA的RI值显著高于nhsPDA和nPDA组(P=0.000,P=0.000;P=0.002,P=0.002;P=0.000,P=0.000;P=0.000,P=0.000),见图3,图4,图5,图6;nhsPDA组和nPDA组间上述参数比较差异无统计学意义(P>0.05)。3组间Vs、Vm比较差异无统计学意义(P>0.05)。
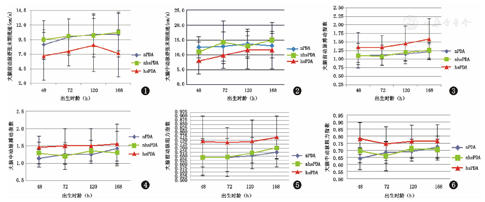
Influence on end-diastolic velocity of anterior cerebral artery due to haemodynamic significant patent ductus arteriosus in preterm infants
Influence on end-diastolic velocity of middle cerebral artery due to haemodynamic significant patent ductus arteriosus in preterm infants
Influence on pulsatility index of anterior cerebral artery due to haemodynamic significant patent ductus arteriosus in preterm infants
Influence on pulsatility index of middle cerebral artery due to haemodynamic significant patent ductus arteriosus in preterm infants
Influence on resistant index of anterior cerebral artery due to haemodynamic significant patent ductus arteriosus in preterm infants
Influence on resistant index of middle cerebral artery due to haemodynamic significant patent ductus arteriosus in preterm infants

注:hsPDA:有血流动力学意义的动脉导管未闭;nhsPDA:无血流动力学意义的动脉导管未闭;nPDA:无动脉导管未闭 hsPDA:haemodynamic significant patent ductus arteriosus;nhsPDA:non-haemodynamic significant patent ductus arteriosus;nPDA:non-patent ductus arteriosus
Influence on end-diastolic velocity of anterior cerebral artery due to haemodynamic significant patent ductus arteriosus in preterm infants
Influence on end-diastolic velocity of middle cerebral artery due to haemodynamic significant patent ductus arteriosus in preterm infants
Influence on pulsatility index of anterior cerebral artery due to haemodynamic significant patent ductus arteriosus in preterm infants
Influence on pulsatility index of middle cerebral artery due to haemodynamic significant patent ductus arteriosus in preterm infants
Influence on resistant index of anterior cerebral artery due to haemodynamic significant patent ductus arteriosus in preterm infants
Influence on resistant index of middle cerebral artery due to haemodynamic significant patent ductus arteriosus in preterm infants
出生后7 d hsPDA组中,PDA关闭组7例,未闭组16例,2组间ACA、MCA血流参数比较,PDA关闭组PI、RI值均低于未闭组,ACA的Vd显著高于关闭组,而MCA的Vd在2组间无统计学差异(P=0.096),见表2。出生后7 d hsPDA关闭组与nPDA组ACA、MCA血流参数比较,2组间ACA、MCA各血流参数比较差异均无统计学意义,见表3。
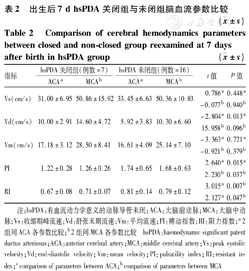
出生后7 d hsPDA关闭组与未闭组脑血流参数比较( ±s)
±s)
Comparison of cerebral hemodynamics parameters between closed and non-closed group reexamined at 7 days after birth in hsPDA group( ±s)
±s)
出生后7 d hsPDA关闭组与未闭组脑血流参数比较( ±s)
±s)
Comparison of cerebral hemodynamics parameters between closed and non-closed group reexamined at 7 days after birth in hsPDA group( ±s)
±s)
| 指标 | hsPDA关闭组(例数=7) | hsPDA未闭组(例数=16) | t值 | P值 | |||
|---|---|---|---|---|---|---|---|
| ACAa | MCAb | ACAa | MCAb | ||||
| Vs(cm/s) | 31.00±6.95 | 50.86±15.92 | 33.45±6.63 | 50.36±10.83 | 0.786a | 0.448a | |
| -0.077b | 0.940b | ||||||
| Vd(cm/s) | 10.00±2.91 | 14.60±4.72 | 5.92±3.83 | 10.30±6.60 | -2.804a | 0.013a | |
| 15.958b | 0.096b | ||||||
| Vm(cm/s) | 17.18±3.12 | 28.50±8.41 | 16.61±4.09 | 25.14±7.10 | -3.363a | 0.721a | |
| -0.921b | 0.379b | ||||||
| PI | 1.22±0.28 | 1.26±0.26 | 1.74±0.65 | 1.68±0.63 | 2.640a | 0.015a | |
| 2.230b | 0.037b | ||||||
| RI | 0.67±0.08 | 0.71±0.07 | 0.81±0.14 | 0.79±0.12 | 3.015a | 0.007b | |
| 2.127a | 0.047b | ||||||
注:hsPDA:有血流动力学意义的动脉导管未闭;ACA:大脑前动脉;MCA:大脑中动脉;Vs:收缩期峰流速;Vd:舒张末期流速;Vm:平均流速;PI:搏动指数;RI:阻力指数;a 2组间ACA各参数比较;b 2组间MCA各参数比较 hsPDA:haemodynamic significant patent ductus arteriosus;ACA:anterior cerebral artery;MCA:middle cerebral artery;Vs:peak systolic velocity;Vd:end-diastolic velocity;Vm:mean velocity;PI:pulsatility index;RI:resistant index;a comparison of parameters between ACA;b comparison of parameters between MCA
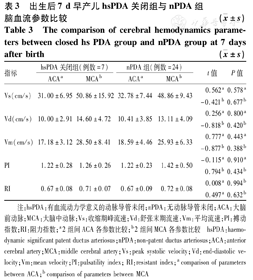
出生后7 d早产儿hsPDA关闭组与nPDA组脑血流参数比较( ±s)
±s)
The comparison of cerebral hemodynamics parameters between closed hs PDA group and nPDA group at 7 days after birth( ±s)
±s)
出生后7 d早产儿hsPDA关闭组与nPDA组脑血流参数比较( ±s)
±s)
The comparison of cerebral hemodynamics parameters between closed hs PDA group and nPDA group at 7 days after birth( ±s)
±s)
| 指标 | hsPDA关闭组(例数=7) | nPDA组(例数=24) | t值 | P值 | |||
|---|---|---|---|---|---|---|---|
| ACAa | MCAb | ACAa | MCAb | ||||
| Vs(cm/s) | 31.00±6.95 | 50.86±15.92 | 32.78±7.44 | 48.86±9.43 | 0.562a | 0.578a | |
| -0.421b | 0.677b | ||||||
| Vd(cm/s) | 10.00±2.91 | 14.60±4.72 | 10.41±3.85 | 13.11±4.09 | 0.256a | 0.800a | |
| -0.818b | 0.420b | ||||||
| Vm(cm/s) | 17.18±3.12 | 28.50±8.41 | 18.59±4.46 | 25.93±6.33 | 0.777a | 0.443a | |
| -0.877b | 0.388b | ||||||
| PI | 1.22±0.28 | 1.26±0.26 | 1.22±0.23 | 1.42±0.50 | -0.115a | 0.910a | |
| 0.794b | 0.434b | ||||||
| RI | 0.67±0.08 | 0.71±0.07 | 0.67±0.09 | 0.72±0.08 | 0.008a | 0.994b | |
| 0.497a | 0.632b | ||||||
注:hsPDA:有血流动力学意义的动脉导管未闭;nPDA:无动脉导管未闭;ACA:大脑前动脉;MCA:大脑中动脉;Vs:收缩期峰流速;Vd:舒张末期流速;Vm:平均流速;PI:搏动指数;RI:阻力指数;a 2组间ACA各参数比较;b 2组间MCA各参数比较 hsPDA:haemodynamic significant patent ductus arteriosus;nPDA:non-patent ductus arteriosus;ACA:anterior cerebral artery;MCA:middle cerebral artery;Vs:peak systolic velocity;Vd:end-diastolic velocity;Vm:mean velocity;PI:pulsatility index; RI:resistant index;a comparison of parameters between ACA;b comparison of parameters between MCA
出生后7 d内连续动态监测患儿床旁颅脑超声发现,85例患儿中,重度PIVH 8例,轻度PIVH 25例。hsPDA组、nhsPDA组和nPDA组3组间比较,PIVH的严重程度差异无统计学意义(P=0.452),然而hsPDA组重度PIVH比例占17.39%,高于nPDA组(8.33%)和nhsPDA组(5.26%)(χ2=2.405,P=0.280),见表4。
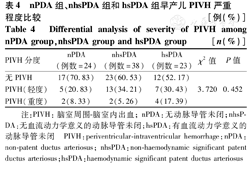
nPDA 组、nhsPDA组和hsPDA组早产儿PIVH严重程度比较[例(%)]
Differential analysis of severity of PIVH among nPDA group,nhsPDA group and hsPDA group[n(%)]
nPDA 组、nhsPDA组和hsPDA组早产儿PIVH严重程度比较[例(%)]
Differential analysis of severity of PIVH among nPDA group,nhsPDA group and hsPDA group[n(%)]
| PIVH分度 | nPDA(例数=24) | nhsPDA(例数=38) | hsPDA(例数=23) | χ2值 | P值 |
|---|---|---|---|---|---|
| 无PIVH | 17(70.83) | 23(60.53) | 12(52.17) | ||
| PIVH(轻度) | 5(20.83) | 13(34.21) | 7(30.43) | 3.720 | 0.452 |
| PIVH(重度) | 2(8.33) | 2(5.26) | 4(17.39) |
注:PIVH:脑室周围-脑室内出血;nPDA:无动脉导管未闭;nhsPDA:无血流动力学意义的动脉导管未闭;hsPDA:有血流动力学意义的动脉导管未闭 PIVH:periventricular-intraventricular hemorrhage;nPDA:non-patent ductus arteriosus; nhsPDA:non-haemodynamic significant patent ductus arteriosus;hsPDA:haemodynamic significant patent ductus arteriosus
早产儿发生PDA的高危因素有胎龄小、低出生体质量、合并感染、暂时性甲状腺功能低下和血小板减少等[11,12]。感染可使前列腺素、炎性介质释放增多,而早产儿DA平滑肌对前列腺素的敏感性高,因此感染可导致早产儿DA开放;而炎性介质本身可影响DA的关闭。本研究单因素分析发现母亲产前感染可能增加hsPDA的发生,但多因素分析结果显示二者无相关性,可能与样本量小有关。早产儿出生后易发生肺透明膜病,在疾病恢复期由于肺血管阻力下降,体循环压力高于肺循环压力,易出现DA左向右分流,出现相关并发症,从而可能延长机械通气时间[13]。本研究单因素、多因素分析发现早产儿出生后48 h内应用有创机械通气可能是hsPDA的危险因素,可能原因为机械通气的患儿肺部疾病往往较重,肺血管阻力高;且出生后机械通气造成胸腔压力升高,肺血管阻力也相应增加,使体循环和肺循环的血管阻力平衡紊乱,可能会影响DA的分流[14]。由此推测,hsPDA的发生和应用机械通气可能互为因果。
Noori等[15]在出生后20 min、24~48 h观察DA分流量对20例足月新生儿大脑中动脉血流的影响,结果发现动脉导管分流量增加可致脑血流减少,MCA的Vm与DA分流呈负相关。本研究观察85例早产儿PDA对大脑前、中动脉血流的影响,分流量大的hsPDA对脑血流可产生不良影响,主要影响Vd、RI、PI值,未发现对Vm有显著影响。Jim等[16]观察了77例极低出生体质量儿hsPDA对脑血流动力学的影响,分别在出生后早期和吲哚美辛或手术结扎DA关闭后进行超声心动图和颅脑超声检查,结果发现左心房内径/主动脉内径比值与大脑动脉血流RI呈正相关,和Vd值呈负相关,从而认为RI值升高,Vd值降低预示着可能存在hsPDA,而随着RI、Vd值的恢复提示hsPDA可能关闭。本研究对3组病例进行重复测量方差分析显示hsPDA组ACA的Vd、MCA的Vd值降低,而RI、PI值升高。出生后7 d hsPDA关闭组和未闭组比较发现,关闭组RI、PI值较未闭组降低,而Vd值升高,与nPDA组比较各血流参数的差异无统计学意义。本研究表明早产儿hsPDA可导致脑血流动力学变化,此时需要积极干预PDA,促使其关闭,以稳定脑血流,减少脑损伤。
早产儿DA开放使左向右分流明显增加时,体循环血流显著降低,可引起脑血流灌注减少,从而导致脑缺氧缺血改变及再灌注损伤[17],甚至造成PIVH。Jim等[16]通过病例对照方法,观察符合hsPDA标准的极低出生体质量儿,即使采用药物或手术结扎治疗,脑室内出血(IVH)发生率仍高于对照组,虽其分级及严重程度比较无显著差异,但严重脑室内出血均在PDA组。本研究发现DA关闭与否与PIVH严重程度无相关,与Jim的研究相符。Sarkar等[18]对7年562例极低出生体质量儿进行回顾性分析,其中59例罹患严重脑室内出血(Ⅲ/Ⅳ级),研究发现早产儿严重脑室内出血与hsPDA相关;2012年Jodeiry等[19]研究了64例极低出生体质量儿颅内出血的影响因素,发现早产儿颅内出血与PDA显著相关。虽本研究中hsPDA与PIVH严重程度无相关性,但重度PIVH的比例在hsPDA组较高,这可能与分组中样本量较少有关。因此,早产儿hsPDA与PIVH可能存在一定相关性,尤其是重度PIVH,对有hsPDA的患儿因常规监测颅脑超声检查,随访观察有无急性PIVH的发生及其严重程度,积极进行干预。
本研究通过对85例胎龄≤34周的早产儿进行前瞻性病例-对照研究发现,出生后48 h内机械通气可能是hsPDA的高危因素;早产儿hsPDA可导致脑血流动力学变化,并且与PIVH可能有一定相关性,尤其是重度PIVH,因此对有hsPDA的患儿,应常规监测颅脑超声,观察脑血流动力学变化和PIVH的发生及其严重程度,积极进行干预以减少脑损伤、稳定脑血流。本研究由于样本量较少,且早产儿本身疾病的混杂因素较难控制,研究结果可能有一定偏差,尚需扩大样本量进一步证实本研究结论。



























