
利用CONSORT声明统计和评价《中国小儿急救医学》杂志上临床试验研究报告的质量。
检索万方数据库,收集从2011年1月至2015年11月发表在《中国小儿急救医学》杂志的所有文章,利用2010年CONSORT声明,对临床试验类的文章进行评价和分析。
在检索出的1 317篇文章中,有62篇(4.7%)属于临床试验。参照CONSORT声明,所有文章均满足从1b到6b项标准(包括摘要,引言,方法中的实验设计、受试者、干预及结局报告的各项要求),而满足项目8a(描述产生随机分配顺序的方法)的有30篇(48.4%),满足项目8b(描述随机化的种类及任何限制)的有4篇(6.5%),没有文章满足项目9(描述实施随机分配顺序的方法,在实施干预前隐蔽分配顺序的步骤)和项目10(谁产生的分配顺序,谁登记的参加者,谁将参加者分配到各组中)。在这62篇文章中,33篇(53.2%)所关注的结局为呼吸系统相关疾病,而关注结局为神经系统、循环系统和消化系统疾病的文章分别有5篇(8.1%)、4篇(6.5%)和4篇(6.5%)。虽然62篇文章均提示结果有统计学意义,但只有38篇(61.3%)文章提及随机分组、7篇(11.3%)文章提及随访、5篇(8.1%)文章提及盲法,而在文中画出流程图的只有1篇(1.6%)。
国内临床医生在《中国小儿急救医学》杂志上发表的临床试验报告并没有完全参照CONSORT声明。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
随机对照临床试验(randomized controlled trials,RCTs)为临床试验的一部分。有资料显示,Ⅲ期随机对照临床试验是评估临床干预措施的金标准[1]。为了提高RCT的报告质量,报告试验的标准(Standards of Reporting Trials,SORT)小组于1995年发布了第一版报告试验的强化标准(Consolidated Standards of Reporting Trials,CONSORT),并发布了一个声明即CONSORT声明[2]。此声明于2010年重新修订,并逐渐被国际上各大主流医学期刊所认可[3],因此,不管是临床医生,还是医学期刊的编辑,了解并学习CONSORT声明的每一项内容都是十分必要的。根据2010年CONSORT声明,我们分类统计并评价了2011年1月以来发表在《中国小儿急救医学》杂志并被万方数据库收录的所有临床试验研究的文章,现将结果报告如下。
通过检索万方数据库,以"中国小儿急救医学"为检索关键词,搜索到了2011年1月至2015年11月在《中国小儿急救医学》上发表的全部1 317篇文章。临床试验是以患者或志愿者为受试对象,评价比较临床干预措施所产生的临床效应有无实用价值的前瞻性实验研究[4]。根据临床试验的定义,排除了病例报告、综述、回顾性研究以及Meta分析等文章,属于临床试验类的文章共有62篇,并将这62篇文章全部作为本次统计和评价的样本。我们参照2010年CONSORT声明的每一项标准,统计了所有文章中满足每一项标准的情况;最后又统计整理了试验的主要信息,包括研究方向、研究因素、研究结果等内容。
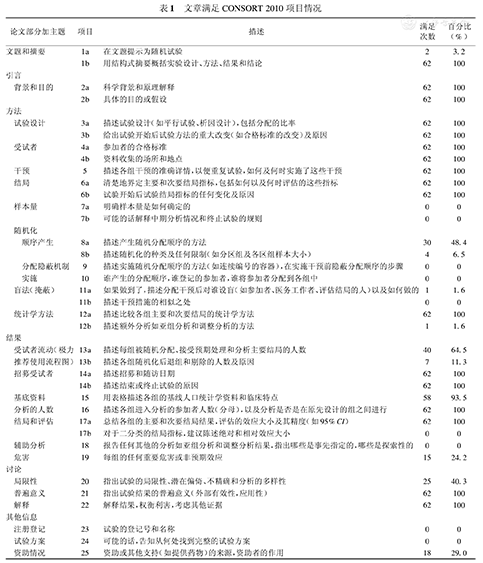
表1是2010年CONSORT声明的每一项在62篇文章中的满足次数,由此可以看出:62篇文章全部满足CONSORT声明中除1a以外的其他前6项标准,相比之下,所有文章均不满足项目7。而满足项目8a标准的文章有30篇,62篇文章全部不满足项目9、10。项目12a和14满足情况很好,同样达到了100%,但满足13a和13b的项目分别只有40篇和7篇。62篇文章全部满足项目16和17a,但均不满足项目17b和18。虽然所有文章均满足项目21、22,但满足项目20的只有25篇文章,而满足项目25的文章也只有18篇,所有文章均不满足项目23和24。
文章满足CONSORT 2010项目情况
文章满足CONSORT 2010项目情况
| 论文部分加主题 | 项目 | 描述 | 满足次数 | 百分比(%) | ||
|---|---|---|---|---|---|---|
| 文题和摘要 | 1a | 在文题提示为随机试验 | 2 | 3.2 | ||
| 1b | 用结构式摘要概括实验设计、方法、结果和结论 | 62 | 100 | |||
| 引言 | ||||||
| 背景和目的 | 2a | 科学背景和原理解释 | 62 | 100 | ||
| 2b | 具体的目的或假设 | 62 | 100 | |||
| 方法 | ||||||
| 试验设计 | 3a | 描述试验设计(如平行试验、析因设计),包括分配的比率 | 62 | 100 | ||
| 3b | 给出试验开始后试验方法的重大改变(如合格标准的改变)及原因 | 62 | 100 | |||
| 受试者 | 4a | 参加者的合格标准 | 62 | 100 | ||
| 4b | 资料收集的场所和地点 | 62 | 100 | |||
| 干预 | 5 | 描述各组干预的准确详情,以便重复试验,如何及何时实施了这些干预 | 62 | 100 | ||
| 结局 | 6a | 清楚地界定主要和次要结局指标,包括如何以及何时评估的这些指标 | 62 | 100 | ||
| 6b | 试验开始后试验结局指标的任何变化及原因 | 62 | 100 | |||
| 样本量 | 7a | 明确样本量是如何确定的 | 0 | 0 | ||
| 7b | 可能的话解释中期分析情况和终止试验的规则 | 0 | 0 | |||
| 随机化 | ||||||
| 顺序产生 | 8a | 描述产生随机分配顺序的方法 | 30 | 48.4 | ||
| 8b | 描述随机化的种类及任何限制(如分区组及各区组样本大小) | 4 | 6.5 | |||
| 分配隐蔽机制 | 9 | 描述实施随机分配顺序的方法(如连续编号的容器),在实施干预前隐蔽分配顺序的步骤 | 0 | 0 | ||
| 实施 | 10 | 谁产生的分配顺序,谁登记的参加者,谁将参加者分配到各组中 | 0 | 0 | ||
| 盲法(掩蔽) | 11a | 如果做到了,描述分配干预后对谁设盲(如参加者、医务工作者、评估结局的人)以及如何做的 | 1 | 1.6 | ||
| 11b | 描述干预措施的相似之处 | 0 | 0 | |||
| 统计学方法 | 12a | 描述比较各组主要和次要结局的统计学方法 | 62 | 100 | ||
| 12b | 描述额外分析如亚组分析和调整分析的方法 | 1 | 1.6 | |||
| 结果 | ||||||
| 受试者流动(极力 | 13a | 描述每组被随机分配、接受预期处理和分析主要结局的人数 | 40 | 64.5 | ||
| 推荐使用流程图) | 13b | 描述各组随机化后退组和剔除的人数及原因 | 7 | 11.3 | ||
| 招募受试者 | 14a | 描述招募和随访日期 | 62 | 100 | ||
| 14b | 描述结束或终止试验的原因 | 62 | 100 | |||
| 基底资料 | 15 | 用表格描述各组的基线人口统计学资料和临床特点 | 58 | 93.5 | ||
| 分析的人数 | 16 | 描述各组进入分析的参加者人数(分母),以及分析是否是在原先设计的组之间进行 | 62 | 100 | ||
| 结局和评估 | 17a | 总结各组的主要和次要结局结果,评估的效应大小及其精度(如95%CI) | 62 | 100 | ||
| 17b | 对于二分类的结局指标,建议陈述绝对和相对效应大小 | 0 | 0 | |||
| 辅助分析 | 18 | 报告任何其他的分析如亚组分析和调整分析结果,指出哪些是事先指定的,哪些是探索性的 | 0 | 0 | ||
| 危害 | 19 | 每组的任何重要危害或非预期效应 | 15 | 24.2 | ||
| 讨论 | ||||||
| 局限性 | 20 | 指出试验的局限性、潜在偏倚、不精确和分析的多样性 | 25 | 40.3 | ||
| 普遍意义 | 21 | 指出试验结果的普遍意义(外部有效性,应用性) | 62 | 100 | ||
| 解释 | 22 | 解释结果,权衡利害,考虑其他证据 | 62 | 100 | ||
| 其他信息 | ||||||
| 注册登记 | 23 | 试验的登记号和名称 | 0 | 0 | ||
| 试验方案 | 24 | 可能的话,告知从何处找到完整的试验方案 | 0 | 0 | ||
| 资助情况 | 25 | 资助或其他支持(如提供药物)的来源,资助者的作用 | 18 | 29.0 | ||
在全部62篇临床试验研究的文章中,提及随机分组的文章有38篇,其他24篇文章只提及将试验对象分为试验组和对照组;从文章研究方向来看,有33篇文章与呼吸系统疾病相关,5篇与神经系统疾病相关,与循环系统和消化系统疾病相关的文章各有4篇;从研究类型来看,所有文章均属于探索性类型;从研究因素来看,31篇文章研究临床因素,12篇文章研究生化因素,而同时研究这两种因素的有19篇文章。在这62篇文章中,提及设计盲法的有5篇,提及试验后随访工作的有7篇。62项试验结果均显示亚组之间差异具有统计学意义,且所有的研究者均采用P值或CI值表示统计学结果。只有1篇文章根据CONSORT标准画出了流程图。
RCT的结果能够为临床医生提供诊治建议、评估不同治疗措施之间的利弊,进而加快临床决策[5]。而CONSORT声明则起到了规范临床医生报告RCT的作用。通过对近5年发表在《中国小儿急救医学》的临床试验研究文章进行统计分析,我们发现尽管CONSORT声明已经发布20余年,国内临床医生在《中国小儿急救医学》杂志上发表的临床试验研究报告并没有完全参照CONSORT声明。在这62篇文章中,只有2篇文章在题目中提及随机试验,这应该引起更多的临床医生注意,做好试验报告文题撰写工作。同时,在报告临床试验的过程中,随机化分组以及设盲工作并没有得到很好地描述:在提及随机分组的38篇文章中,虽然有30篇文章描述了产生随机分配顺序的方法,但提及设盲的文章只有5篇,并只有1篇文章对设盲工作进行了描述;而其他24篇文章,则完全没有提及随机化分组,只向读者说明了试验分为实验组和对照组。只有1篇文章根据CONSORT声明画出了流程图,表明试验过程中受试者的登记、分配、随访以及分析等工作的描述还有待完善。由此可知,要想提高国内小儿重症医学领域临床试验研究报告的质量,临床医生在做好试验工作的同时,参照CONSORT标准进行试验报告的撰写是十分必要的。
根据研究方向,33篇文章所关注的结局与呼吸系统疾病相关,表明近5年在《中国小儿急救医学》发表的临床试验,过半数的研究局限在呼吸系统领域,笔者认为这与PICU科室自身性质和收治的患者类型密切相关。然而,小儿重症医学包含领域十分广泛,如何开展和完善其他领域的临床试验研究是今后讨论的热点之一。必要时可以进行医院之间病例信息共享、多中心联合进行某一项临床试验研究,这样不仅能扩大样本量,也促进了医院之间的相互交流。就研究类型而言,本次统计的临床试验均属于探索性研究,而有基金资助的试验项目较少,如果能将研究项目申请为课题,则会为试验的开展提供更为便利的条件。试验报告中,普遍缺乏对设盲工作和随访工作的描述也是本次统计发现的问题之一,说明在《中国小儿急救医学》杂志中发表的大部分临床试验类文章忽略了对这两项工作的描述。
从严格意义上讲,CONSORT声明是用来评价随机对照临床试验的标准,但由于发表在《中国小儿急救医学》杂志上完全符合随机对照临床试验的文章很少,为了扩大样本量,我们将近5年所有的临床试验相关的文章全部采纳并作为评价样本,这也从某种程度上反映出国内小儿重症医学领域随机对照临床试验的报告不够规范的问题。因此,为了提高国内小儿重症医学领域的研究水平,我们呼吁试验者以认真设计和进行临床试验为前提,能够按照CONSORT声明更加规范地报告临床试验。
我们的研究根据CONSORT声明对近5年发表在《中国小儿急救医学》杂志的临床试验研究报告做了详细的对比和评价,这有利于推动和完善今后国内小儿重症医学领域临床试验的发展;其次,通过对文章信息的分类统计,总结归纳出了近5年发表在《中国小儿急救医学》试验的研究方向,对于近期小儿重症医学领域的研究趋势和热点有了初步了解;另外,我们是第一篇报道有关国内小儿重症医学领域临床试验研究报告质量的文章。但本次研究也有不足之处:由于本次抽样只针对《中国小儿急救医学》杂志,并且只统计分析了2011年1月至2015年11月符合要求的临床试验研究,所以存在着抽样范围小、文章发表年份相对局限等问题。要对国内小儿重症医学领域的临床试验研究做出整体评价,需要再全面收集文献做进一步分析。
总而言之,我们的统计分析表明,发表在《中国小儿急救医学》杂志的临床试验报告还不够完善,主要问题暴露在试验报告对随机化设计、设盲、试验后期随访等方面描述不全面。希望更多小儿重症医学领域的临床医生在进行临床试验的同时,牢记以CONSORT声明为标准撰写试验报告,从而提高国内小儿重症医学领域的文章质量。同时期刊编辑在接收临床试验类投稿时,应该根据CONSORT声明对文章进行严格的评价,从而提高收录文章的质量。



























