
探索小儿先天性心脏病(congenital heart disease,CHD)术后早期死亡原因,为改善此类患儿的临床预后提供帮助。
回顾性分析2013至2018年就诊于上海交通大学医学院附属上海儿童医学中心心胸外科的CHD术后死亡患儿临床资料,探讨其死亡流行病学特征及主要死亡原因。
CHD术后病死率呈逐年下降趋势, 2013至2018年间病死率从2.2%降至1.2%。死亡时年龄<1岁患儿最多(250例,72.0%),死亡主要发生在术后1周(254例,73.2%),尤其是术后24 h内(101例,29.1%)和术后第2天(51例,14.7%)。死亡原因以术后残余或残留解剖问题为主(103例,29.7%),其次是心律失常(66例,19.0%)和肺高压(57例,16.4%)。与双心室患儿相比,功能性单心室患儿术后心力衰竭和肺高压的并发症发生率较高,差异有统计学意义(P<0.05)。
随着外科手术、体外循环技术的进步以及术后监护能力的提高,近6年CHD患儿术后病死率逐年下降;术后残余或残留解剖问题是主要的死亡原因,临床工作中仍需加强对小年龄CHD患儿围术期的管理。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
先天性心脏病(congenital heart disease,CHD)是一种严重危害儿童身心健康的疾病,其发病率约占出生婴儿的4‰~9‰[1],生后1年病死率约占所有出生缺陷死亡患儿的50%[2]。近年来,随着临床诊疗手段和外科手术技术的进步,CHD患儿的病死率也逐年下降,在成功进行外科修复的CHD患儿中,大部分患儿在术后能获得接近正常的身体状态,然而,仍有一部分患儿在术后早期死亡[3,4]。本研究拟通过对近6年CHD死亡患儿的临床资料进行回顾性分析,探讨CHD患儿术后早期死亡的流行病学特征及其主要死亡因素,以期改善这一患儿群体的长期预后。
选择2013年1月至2018年12月在上海交通大学医学院附属上海儿童医学中心心胸外科进行CHD修复手术术后住院死亡患儿。排除入院但未做手术、开关术、术中死亡、气管狭窄合并小型房间隔缺损行气管狭窄根治术、早产儿行动脉导管未闭结扎和起搏器植入的CHD患儿。收集患儿术前基本信息、手术记录和术后护理单、实验室检查、床旁超声心动图、心电图、心血管影像及医嘱等资料,记录术后至死亡相关并发症。根据患儿术前超声心动图和心血管影像,以及术中诊断明确患儿疾病类型。
根据患儿术中及术后相关临床资料确定患儿主要死亡原因。主要死亡原因不一定与患儿死亡过程中最先出现或者死亡即刻前临床事件相同,将其定义为最初的引起后续一系列恶性临床事件而致患儿死亡的初始原因。
采用描述性分析方法统计总体队列和并发症发生率,利用SPSS 23.0统计软件进行数据分析。计数资料以例(%)表示,两组间比较采用卡方检验。所有数据均为双侧检验,P<0.05为差异有统计学意义。
2013至2018年进行CHD修复术患儿共19 651例,术后死亡患儿共347例,6年间CHD患儿术后总病死率为1.8%。年龄小于1岁的患儿250例,1~3岁 40例,大于3岁57例。2013至2018年CHD患儿术后病死率整体呈逐年下降趋势,从2013年2.2%降至2018年1.2%,其中72.0%患儿死亡时年龄小于1岁(图1)。
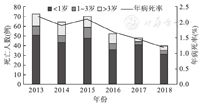

死亡患儿中有100例行姑息术,247例行根治术。功能性单心室患儿81例,双心室患儿266例,死亡患儿以复杂型CHD为主,房间隔缺损、室间隔缺损和动脉导管未闭等简单CHD仅占所有死亡患儿的6.0%,6年平均病死率仅为0.18%(表1)。

2013至2018年先心病术后早期死亡患儿诊断分类(例)
2013至2018年先心病术后早期死亡患儿诊断分类(例)
| 诊断 | 例数 | |
|---|---|---|
| 功能性单心室 | 81 | |
| 房坦(Fontan) | 33 | |
| 体肺分流 | 28 | |
| 格林(Glenn) | 17 | |
| 诺伍德(Norwood) | 3 | |
| 双心室 | 266 | |
| 大动脉转位 | 44 | |
| 法洛四联症 | 40 | |
| 肺动脉闭锁/重度肺动脉狭窄 | 36 | |
| 右室双出口 | 29 | |
| 主动脉缩窄/主动脉弓中断/主动脉瓣下狭窄 | 28 | |
| 室间隔缺损/房间隔缺损/动脉导管未闭 | 21 | |
| 完全性/部分性肺静脉异位引流 | 18 | |
| 完全性房室间隔缺损 | 11 | |
| 瓣膜疾病 | 11 | |
| 冠状动脉异常起源 | 10 | |
| 共同动脉干 | 7 | |
| 威廉姆斯综合征 | 5 | |
| 其他 | 6 | |
术后第1天死亡101例,术后第2天死亡51例,术后第3天死亡18例,术后第4~7天死亡84例,术后第8~14天死亡45例,术后2周以后死亡48例(图2)。术后早期死亡主要发生在术后1周(73.2%),术后第1天死亡患儿占比最多,约为29.1%,但死亡人数比例逐年下降,从2013年34.2%降至2018年20.0%。术后3 d内死亡人数约为总死亡人数的一半(49.0%)。
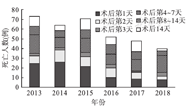

患儿主要死亡原因有术后残余或残留解剖问题、心律失常、肺高压、心脏骤停、出凝血、脓毒症、低氧和其他。主要死亡原因分析结果显示,死于术后残余或残留解剖问题的患儿最多,达到29.7%,其次是心律失常(19.0%)、肺高压(16.4%)、心脏骤停(10.7%)和出凝血问题(8.4%)。
死亡患儿术后各并发症中(表2),心力衰竭的发生率最高(51.6%),其次为心律失常(23.1%)、低心排综合征(21.6%)和肺高压(20.2%)。将死亡患儿进行单心室和双心室修补分类后,结果显示在单心室修补患儿中,术后心力衰竭发生率最高(42.0%),其次是肺高压(35.8%)。在双心室修补患儿中,术后并发症发生率最高的是心力衰竭(54.5%)、而肺高压仅为15.4%,且单心室修补患儿术后心力衰竭(χ2=3.907,P=0.048)和肺高压(χ2=16.029,P< 0.001)发生率较双心室修补患儿明显升高,差异具有统计学意义。
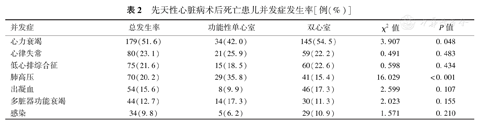
先天性心脏病术后死亡患儿并发症发生率[例(%)]
先天性心脏病术后死亡患儿并发症发生率[例(%)]
| 并发症 | 总发生率 | 功能性单心室 | 双心室 | χ2值 | P值 |
|---|---|---|---|---|---|
| 心力衰竭 | 179(51.6) | 34(42.0) | 145(54.5) | 3.907 | 0.048 |
| 心律失常 | 80(23.1) | 21(25.9) | 59(22.2) | 0.491 | 0.483 |
| 低心排综合征 | 75(21.6) | 15(18.5) | 60(22.6) | 0.598 | 0.434 |
| 肺高压 | 70(20.2) | 29(35.8) | 41(15.4) | 16.029 | <0.001 |
| 出凝血 | 54(15.6) | 8(9.9) | 46(17.3) | 2.599 | 0.107 |
| 多脏器功能衰竭 | 44(12.7) | 14(17.3) | 30(11.3) | 2.023 | 0.155 |
| 感染 | 34(9.8) | 5(6.2) | 29(10.9) | 1.571 | 0.210 |
由于CHD患儿长期生活在非生理性循环的环境中,以及根治及多次分期手术带来的附加风险,导致部分患儿在术后早期死亡[5,6],且各中心病死率存在较大差异,这就表明术后病死率存在改善可能[7,8]。分析CHD术后早期死亡的流行病学特点及其主要死亡模式,可为高质量CHD术后监护奠定基础,并根据关键信息进行针对性的预防、识别和治疗,可有效降低术后病死率[9,10]。本研究初步分析了于本中心就诊的CHD患儿术后住院期间死亡流行病学特征及其主要死亡原因,以期帮助临床提供计划性干预措施,减少可预防的死亡。
随着无创诊疗技术、手术方法、体外循环及监护技术等医疗水平的进步,CHD患儿病死率明显改善,早期术后病死率降至1%~6%,简单CHD的病死率已经和普通人群病死率基本相同,但复杂CHD的病死率仍然较高[11,12,13,14]。本中心近6年CHD术后住院总病死率为1.8%,病死率从2013年2.2%降至2018年1.2%。且随着近年体外膜肺氧合技术的成熟,近一半应用体外膜肺氧合的重症患儿生命得以延续,也在一定程度上降低了术后病死率[15,16]。术后住院期间死亡患儿中绝大部分为功能性单心室、大动脉转位、法洛四联症、肺动脉闭锁、右室双出口等复杂型CHD,房间隔缺损、室间隔缺损和动脉导管未闭等简单CHD死亡人数所占比例较少,死亡患儿占该类手术患儿的比例约为0.18%。回顾其临床资料,发现大部分患儿术前有心力衰竭、重症肺炎、依赖呼吸机、并发肺高压、手术时机过晚或漏诊其他合并心脏问题(如心肌疏松症),术后早期发生心律失常和术后肺高压或肺高压危象。由于CHD患儿,尤其是复杂型CHD趋向于早期手术,因此小年龄段CHD患儿所占比例较高,手术难度及术后监护较难,因此病死率也偏高[10,17]。本中心,死亡年龄<1岁的患儿占72.0%,其中<6个月的患儿有56.2%,占所有死亡患儿的一半以上。住院死亡主要发生在术后1周(73.2%),术后3 d病死率为49.0%,术后第1天病死率最高约为29.1%。因此,临床工作中应特别注意小年龄复杂CHD手术及术后1周监护,以降低术后住院病死率。
CHD患儿本身原有的心脏畸形以及手术干预、体外循环等导致患儿术后心肌功能下降、心脏负荷改变,一般于术后24 h内发生较为严重的并发症,并引起后续一系列不良事件,导致患儿死亡[10,18,19]。在主要死亡原因分析中,本研究结果显示术后残余或残留解剖问题是主要致死原因(29.7%),这部分患儿心脏畸形较为复杂,病情较重,综合目前相关文献报道,复杂CHD患儿的病死率仍然较高,同时合适的手术时机、手术方式的选择、术者的技术问题以及目前医疗技术的局限性等多种原因共同影响患儿预后。其次,术后心律失常(19.0%)和肺高压(16.4%)也是影响患儿预后的重要因素。以往研究主要以心力衰竭或体循环衰竭等进行死因分类,发现其为主要死亡原因,但具体是患儿本身心功能较差,还是术中心肌保护不良,心肌损伤较重,或是术后残余心脏病变等导致的心力衰竭尚不清楚。本研究在对主要死亡原因进行分类时,将心力衰竭的根本原因进一步细化,以期帮助临床医生早期识别和干预,改善患儿预后。此外,研究表明,肺循环血流动力学在患儿术后恢复中具有重要作用,尤其是在功能性单心室的手术治疗中,肺高压严重影响该类患儿术后早期预后,增加患儿病死率[20,21,22]。本研究中,功能性单心室患儿约有23.3%,其术后肺高压发生率较高,仅次于术后心力衰竭,且明显高于双心室修补患儿,导致其死于术后肺高压的比例较高。
术后并发症的管理严重影响患儿的死亡时间及模式,因此,临床工作中应重视术后残余或残留解剖引起的各并发症问题,以及心律失常、肺高压等问题的管理,在术前明确诊断,必要时行心导管检查以明确有无手术指征;术后尽早干预,行CT或心导管检查,明确残余或者残留解剖及其他各严重并发症问题后,积极再手术或药物治疗,做好积极的防治措施。
本研究为回顾性研究,主要依靠医疗记录来确定患儿术后临床资料及死亡因素,尽管对患儿的住院资料进行了详细分析,但仍可能存在一些其他未知因素对患儿死亡有影响。
本研究通过对本中心近6年CHD术后住院期间死亡患儿的临床资料进行回顾性分析,探索患儿术后死亡的主要因素。随着外科手术技术、体外循环及术后监护能力的提升, CHD术后病死率逐年降低;在所有死亡患儿中<1岁患儿死亡人数较多,且多于术后1周死亡,尤其是术后3 d,主要死亡原因以术后残余或残留解剖问题为主。因此,临床工作中仍需加强对小年龄CHD患儿围术期管理。
所有作者均声明不存在利益冲突



























