
了解PIK3CD基因突变所致PI3Kδ过度活化综合征(APDS)的临床特点及基因改变。
回顾性分析2020年湖南省儿童医院呼吸二科临床及基因诊断的1例APDS患儿的临床特征。
患儿,男,4岁,因咳嗽1年余入院,反复皮疹、肝脾淋巴结肿大,支气管镜检查示气道黏膜弥漫滤泡样增生。采用全外显子基因测序对先证者进行基因筛查,发现可疑致病基因,利用二代测序进行验证分析发现患儿PIK3CD基因存在c.3061G>A(E1021 K)杂合突变。经双亲验证,父母未存在该突变,表明患儿为新发基因突变。对该患儿予以积极抗感染治疗,病情好转,定期予以静脉丙种球蛋白调节免疫,病情控制尚稳定。
APDS临床表现包括反复呼吸道感染、肝脾淋巴结肿大、巨细胞病毒及EB病毒以及气道弥漫滤泡样增生改变等,其中气道弥漫性滤泡样增生改变为APDS相对特异性改变。PIK3CD基因C.3061G>A(E1021 K)为常见的新生突变类型。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
PI3Kδ过度活化综合征[activated phosphoinositide 3-kinase-δ(PI3Kδ)syndrome,APDS]是一种于2013年首次由Angulo等[1]报道的罕见的常染色体显性遗传原发性免疫缺陷病(primary immunodeficiency disease,PID)。APDS系由基因突变致PI3Kδ活化,最终导致p110δ过度活化表达,出现T细胞衰老、淋巴结病和免疫缺陷综合征。临床表现主要为反复呼吸道感染、肝脾淋巴结肿大、巨细胞病毒及EB病毒感染血症。目前已发现两个基因功能获得性突变可导致APDS,即PIK3CD基因(编码PI3Kδ催化亚基)及PIK3R1基因(编码PI3KIA类调节亚基P85α)突变,分别称为APDS 1型和APDS 2型[2,3]。本患儿为APDS 1型,通过回顾分析该患儿临床表现,为提高对APDS疾病的认识提供一定帮助。
患儿,男,4岁,主因咳嗽1年余于2020年2月26日入住我科。患儿1年余前无明显诱因出现咳嗽,1年中咳嗽反复,外院静脉输液治疗后,可好转,病程中反复伴有发热,期间多次输液及口服药物治疗,咳嗽仍反复,2020年1月17日因咳嗽加重入我院门诊行胸部CT检查提示:肺部感染并右肺中叶部分实变。完善支气管镜检查提示:(1)支气管内膜炎症(重度,可见弥漫性滤泡增生),建议完善真菌、结核相关检查;(2)左下叶、右中叶管腔狭窄变形。患儿平日易患皮疹。系第2胎第2产,足月顺产。3个月能抬头,6个月能独坐,1岁1个月走路。目前就读幼儿园。患儿有一哥哥,10岁,有鼻炎病史。
体格检查:体重14.5 kg,发育正常,躯干部可见少许散在红色皮疹,部分可见陈旧性皮疹,双侧颈部及双侧腹股沟可扪及数粒散在蚕豆大小淋巴结肿大,质软,活动度可,无压痛。呼吸运动正常,肋间隙正常,双肺呼吸音粗,未闻及干湿啰音。肝脏肋下3 cm可及,质中,无压痛,脾脏肋下3 cm可及,质中。无杵状指。余无阳性体征。
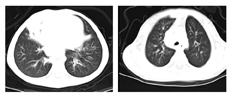
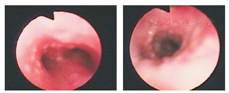
辅助检查:血常规:WBC 8.86×109/L,RBC 4.92×1012/L,PLT 193×109/L,L 1.93×109/L,N 6.36×109/L。血生化正常。过敏源阴性。血沉、降钙素原及CRP均正常。免疫全套:IgG 6.61 g/L,IgA 0.24 g/L,IgM 1.19 g/L,IgE<5 IU/mL,补体C3 0.68 g/L,补体C4 0.16 g/L。T淋巴细胞亚群:总T淋巴细胞数1 191个/μL(正常1 500~2 900个/μL);总B淋巴细胞646个/μL(正常500~1 200个/μL);辅助/诱导性T淋巴细胞(CD4+细胞)565个/μL(正常1 000~2 100个/μL);抑制/细胞毒性T淋巴细胞(CD8+细胞)607个/μL(正常700~1 100个/μL);NK细胞481个/μL(正常300~600个/μL);CD4+/CD8+细胞比值0.93(正常1.1~2.0)。真菌D葡聚糖及曲霉菌抗原阴性。痰培养为流感嗜血杆菌(+)。PPD皮试阴性,结核感染斑点T试验阴性。胸部CT示肺部感染并右肺中叶部分实变;双肺门、纵隔及腋下淋巴结肿大,纵隔点状钙化灶;建议必要时胸部增强CT扫描及结合临床、实验室检查排除特殊感染(结核?)和淋巴瘤(?)(图1)。腹部B超示:肝大;脾大、脾实质回声不均匀;腹腔及腹膜后淋巴结肿大并部分融合;提示结核(?),真菌感染(?),腹腔胀气。入院前支气管镜检查可见各段支气管黏膜弥漫性滤泡样增生,以中下叶及下叶为重(图2)。黏膜活检病理:支气管黏膜上皮脱落、坏死及炎症;上皮细胞表面纤毛结构异常。肺泡灌洗液宏基因检查结果示人类腺病毒C、巨细胞病毒及EB病毒阳性。


基因检测:经家属书面签署知情同意书后,采集患儿及其父母的外周血各2 mL。首先对先证者进行全外显子组测序,结果显示先证者PIK3CD基因存在C.3061G>A(E1021K)点突变。进行二代测序验证,证实存在C.3061G>A(E1021K)点杂合突变。患者为新发变异,且无家族史(经双亲验证)(图3)。


①:参照序列;②:患儿PIK3CD基因第24外显子存在C.3061G>A纯合错义突变;③:患儿父亲相同位点无突变;④:患儿母亲相同位点无突变。
诊治经过:患儿在入院后针对痰培养细菌阳性结果予以哌拉西林他唑巴坦抗感染,加强化痰等对症支持治疗,同时辅以支气管肺泡灌洗治疗,予阿昔洛韦治疗,患儿临床症状缓解出院。电话随访患儿服用阿昔洛韦1个月后,2次复查EB病毒阴性。出院后1个月复诊,患儿无咳嗽等不适,结合基因检查结果,最终确诊APDS,建议定期输注丙种球蛋白,家属拒绝用雷帕霉素治疗。最新随访确认,患儿后续前往上海复旦大学附属儿童医学中心就诊后,每月输注丙种球蛋白治疗,已用雷帕霉素半年余,数月来无咳嗽症状,复查肺部CT可见病灶明显吸收。
APDS本质上是一种单基因相关的原发性联合免疫缺陷病,PIK3CD及PIK3R1基因突变均可造成PI3Kδ过度活化,从而引起一系列免疫相关临床表现。本文主要讨论由PIK3CD基因突变所致疾病APDS1。Hartman等[4]证实PIK3CD基因的突变会导致免疫功能缺失,出现以反复发作的呼吸道感染和EB病毒、巨细胞病毒血症为主要表现的原发性免疫缺陷(primary immunodeficiency,PID)。APDS患者的治疗方法包括预防性抗生素、免疫球蛋白替代治疗、使用免疫及生物抑制剂和造血干细胞移植。其中PI3K-AKT-mTOR通路上重要分子的生物抑制剂雷帕霉素以及几种选择性PI3Kδ抑制剂靶向治疗药物Leniolisib(CDZ173)及Idelalisib(gs-1101)等研究较多。由于该疾病首次在2013年报道,目前对该疾病随访时间普遍不长。国内唐文静等[5]对15例APDS患者进行了1~29个月随访,15例患儿存活13例,2例患儿因严重感染、脓毒性休克死亡。从本病例随访结果看,患儿定期输注丙种球蛋白,使用靶向药物雷帕霉素治疗后,病情尚稳定。
采用关键词"PIK3CD"及"APDS"在"万方医学网"以及"中国知网"搜索结果显示共有4篇个案报道[6,7,8,9]以及2篇[5,10]临床分析,共涉及23个APDS病例,同样以"PIK3CD+"及"APDS"在"迈特思创"综合外文网搜索结果示1篇中国15个病例的英文文献报道[11]以及1篇发现新的基因突变位点的个案报道[12],外文网搜索到中国病例共16例,截至目前国内病例共报道39例。国外病例报道中,Jamee等[13]从55篇文章中筛选出243例APDS患者。这些APDS患者最常见的临床表现为呼吸道感染肺炎(43.6%),其次为中耳炎(28.8%)、鼻窦炎(25.9%)、淋巴细胞增殖(70.4%)、自身免疫性疾病(28.0%)、发育不全(20.6%)和恶性肿瘤(12.8%)。主要的免疫表型为高IgM综合征(48.1%)。
该病具有高度异质性。虽然大多数表现发生在儿童时期,成人发病和无症状的过程也被报道[14]。我国目前报道病例较少,可能与其临床表现无特异性,未早期进行基因检测明确诊断相关。大量的研究已证实PIK3CD基因广泛表达于以B细胞为主的血细胞中。当PIK3CD因过度表达或基因突变而表达异常时,其中经典的磷酸肌醇3激酶(PI3K)-蛋白激酶B(Akt)-哺乳动物雷帕霉素靶蛋白(mTOR)信号通路会被激活,血液细胞会发生不可控制的增殖、分化异常及细胞转移,最终形成肿瘤及转移病灶。由此可见,PIK3CD基因与肿瘤的发生发展有着密切的联系。因此总结目前所报道病例的临床特点,找到早期发现该疾病的相对特异的临床表现,利于早发现该基因突变是有意义的。本病例患儿出现多发淋巴结肿大,目前随访时间较短,暂未发现肿瘤证据。
本例患儿临床表现为反复呼吸道感染,肝脾淋巴结肿大与国内最早由刘辉等[10]报道的2例患儿表现相似。但该患儿外周血IgM 1.19 g/L,为正常范围,且外周血T淋巴细胞计数下降不明显,CD4+/CD8+细胞比值0.93,比值倒置提示细胞免疫功能低下。由于感染本身可造成继发性免疫功能低下,外周血表现对该患儿最终诊断无明确提示意义。
回顾本例患儿的诊断过程,我们从其气道弥漫性滤泡样改变获得线索。分析国内所报道病例来看,其中存在广泛气道黏膜滤泡样增生的病例为6例[5,10],另外有1例便血起病的患儿表现为电子结肠镜检查见较多颗粒样滤泡增生[6]。其中Wang等[11]综合了中国15例APDS患者,提到1个病例胃肠镜可见消化道黏膜结节改变。而国外文献中鲜少提到APDS纤维支气管镜检查发现气道改变。该患儿目前随访时间较短,气道内滤泡样改变尚未复查,是否随治疗有所改变尚需观察。
本例患儿的发现从其气道弥漫性滤泡样改变获得线索,该患儿外周血中淋巴细胞亚群分析及免疫球蛋白均无明显异常提示,当然需要结合其反复呼吸道感染病史以及肝脾及淋巴结肿大的临床表现综合分析,最终完成基因检测明确了诊断。总结分析目前国内发现的该疾病的病例,认为气道弥漫性滤泡样或结节样改变为APDS相对特异性改变,以期为认识并发现该疾病提供一定的帮助。
所有作者均声明不存在利益冲突



























