
通过研究血流感染的病原菌分布及对其耐药性监测,准确掌握我国细菌耐药状况。
收集全国血流感染细菌耐药监测联盟成员单位2018年1月至2019年12月所有按操作规程分离自血培养的感染病原菌,按美国临床和实验室标准化研究所推荐的琼脂稀释法或肉汤稀释法进行抗菌药物药敏性测定。采用WHONET5.6进行统计分析。
2018年1月至2019年12月共收集50家成员单位14 778株病原菌,其中革兰阳性菌为4 117株(27.9%),革兰阴性菌10 661株(72.1%)。最常见的前10位病原菌为大肠埃希菌5 500株(37.2%)、肺炎克雷伯菌2 519株(17.0%)、金黄色葡萄球菌1 438株(9.7%)、凝固酶阴性葡萄球菌1 285株(8.7%)、铜绿假单胞菌546株(3.7%)、屎肠球菌504株(3.4%)、鲍曼不动杆菌501株(3.4%)、阴沟肠杆菌424株(2.9%)、其他链球菌属414株(2.8%)和粪肠球菌344株(2.3%)。耐甲氧西林金黄色葡萄球菌(MRSA)和耐甲氧西林凝固酶阴性葡萄球菌检出率分别为27.4%(394/1 438)和70.4%(905/1 285),未检测到对糖肽类耐药的葡萄球菌;金黄色葡萄球菌对阿米卡星、利福平和复方磺胺甲噁唑的敏感率均在95%以上。屎肠球菌对万古霉素的耐药率为0.4%(2/504),未检测到耐万古霉素的粪肠球菌。产超广谱β-内酰胺酶非耐碳青霉烯类大肠埃希菌、碳青霉烯敏感肺炎克雷伯菌、变形杆菌属分别为50.4%(2 731/5 415)、24.6%(493/2 001)、35.2%(31/88);耐碳青霉烯类大肠埃希菌、肺炎克雷伯菌分别为1.5%(85/5 500)、20.6%(518/2 519);碳青霉烯类耐药肺炎克雷伯菌对头孢他啶/阿维巴坦的耐药率为8.3%(27/325)。鲍曼不动杆菌对多黏菌素B和替加环素的耐药率分别为2.8%(14/501)和3.4%(17/501);铜绿假单胞菌对碳青霉烯类的耐药率为18.9%(103/546)。
我国血流感染病原体以革兰阴性菌为主,大肠埃希菌为最常见的病原菌,产超广谱β-内酰胺酶为主要耐药现象;MRSA的检出率显著降低;耐碳青霉烯大肠埃希菌处于较低水平,耐碳青霉烯肺炎克雷伯菌仍呈上升趋势。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
血流感染是临床常见且严重威胁患者生命安全的严重感染。据Goto等[1]估计,欧洲每年约有120万血流感染病例,其中约15.7万患者死亡;美国住院患者血流感染发生率为6.0%,其中54.7%需入住ICU,病死率为15.8%[2]。根据《2016国际严重脓毒症和脓毒性休克治疗指南》,及时有效的抗菌药物治疗可以改善血流感染患者的预后[3];相反,不合理的抗菌药物治疗会增加患者死亡风险[2]。因此,掌握血流感染病原菌构成及其耐药谱,有助于提高抗菌药物使用针对性,降低患者死亡率,减少细菌耐药的发生[4]。
为了全面了解我国血流感染病原菌的构成和细菌耐药的变迁规律,全国血流感染细菌耐药监测联盟(Blood bacterial resistant investigation collaborative system,BRICS)组织国内相关医院,开展系统性血流感染细菌耐药监测。本研究深入分析了BRICS在2018至2019年血流感染细菌的构成和耐药性监测结果,以期掌握耐药变化动态,为临床血流感染治疗与耐药控制提供参考。
参加2018至2019年全国血流感染细菌耐药监测的单位包括来自全国18家省级医院和32家地市级医院,参加单位均有独立的微生物实验室和固定微生物检验人员,拥有血培养仪以及微生物鉴定和药敏分析仪器,均采用规范化微生物检验流程,室间和室内质控合格。
按照BRICS监测方案及《全国临床检验操作规程》(第四版)[5]的规范要求进行标本采集、培养及菌株鉴定,包括常规生化鉴定和自动化仪器鉴定,分离自患者血液的细菌,除外单瓶培养阳性的凝固酶阴性葡萄球菌、各种污染细菌和所有布鲁杆菌,并剔除同一患者重复菌株;菌株统一保存于Microbank冻存管并于-80 ℃贮存。成员单位将临床分离的菌株每三个月统一寄送至传染病诊治国家重点实验室,中心实验室收到菌种后进行复核鉴定、留存入库保存。同时收集患者及菌株的基本信息,包括(1)患者基本信息:患者年龄、性别、基础疾病和所在科室等;(2)菌株分离信息:标本类型和分离时间等。
青霉素G(批号:130437-201707,效价:94.1%)、氨苄西林(批号:130618-201202,效价:98%)、苯唑西林(批号:130482-201402,效价:90%)、哌拉西林/他唑巴坦(批号:130419-201907/130511-201904,效价:95%/99.5%)、头孢唑啉(批号:130421-201204,效价:99%)、头孢呋辛(批号:130492-201703,效价:85.5%)、头孢曲松(批号:130480-201504,效价:98%)、头孢他啶(批号:130484-201806,效价:94%)、头孢吡肟(批号:130524-201404,效价:84.4%)、头孢哌酮/舒巴坦(批号:130420-201105/130430-201408,效价:99%/99%)、氨曲南(批号:130507-201303,效价:95%)、头孢西丁(批号:130572-201603,效价:95.1%)、美罗培南(批号:130506-201403,效价:87%)、庆大霉素(批号:130326-201716,效价:59%)、阿米卡星(批号:130335-200204,效价:65.5 %)、左氧氟沙星(批号:130455-201607,效价:97%)、莫西沙星(批号:510140-201701,效价:99%)、复方磺胺甲噁唑(批号:100031-201606/100025-201505,效价:99%/99%)、克林霉素(批号:130422-201807,效价:87.2%)、红霉素(批号:130307-201417,效价:93.3%)、四环素(批号:130306-201419效价:96.9%)、利福平(批号:130496-201403,效价:98.8%)为中国食品药品生物制品检定所商品;阿莫西林(批号:F0130A,效价:90%)、克拉维酸(批号:A0402AS,效价:95%)、拉氧头孢(批号:O0701A,效价:99%)、环丙沙星(批号:D1201A,效价:99%)、亚胺培南(批号:A0401A,效价:95%)、厄他培南(批号:S0802A,效价:95%)、磷霉素(批号:M0101A,效价:96%)为大连美仑生物技术有限公司商品;哌拉西林(批号:P1200717,效价:95%)为苏州二叶制药有限公司商品;舒巴坦(批号:03191203,效价:95%)为山东二叶制药有限公司商品;头孢他啶/阿维巴坦(4:1)(批号:MP8X,效价:98%)为美国辉瑞公司商品;替加环素、利奈唑胺、万古霉素和达托霉素肉汤稀释法药敏测定板为温州康泰生物科技有限公司商品;抗菌药物纸片(头孢他啶、头孢他啶/克拉维酸、头孢噻肟、头孢噻肟/克拉维酸和头孢西丁纸片)为英国Oxoid公司商品。
大肠埃希菌ATCC25922、铜绿假单胞菌ATCC27853、肺炎克雷伯菌ATCC700603、金黄色葡萄球菌ATCC29213、粪肠球菌ATCC29212、肺炎链球菌ATCC49619为本实验室常备菌株。
Mueller-Hinton(MH)琼脂为英国Oxoid公司商品,液体培养基经钙离子调节的Mueller-Hinton肉汤(CAMHB)和6-磷酸-葡萄糖为北京索莱宝科技有限公司商品,CaCl2、NaOH、NaCl均为生工生物工程(上海)股份有限公司商品,脱脂羊血为南京茂捷微生物科技有限公司商品,磷酸盐缓冲液(PBS)为吉诺生物医药技术有限公司商品。
按美国临床和实验室标准化研究所(CLSI)推荐的双纸片扩散法进行ESBLs表型确证试验检测大肠埃希菌、肺炎克雷伯菌和变形杆菌属产ESBLs菌株[6]。头孢他啶(30 μg)、头孢他啶/克拉维酸(30 μg/10 μg)、头孢噻肟(30 μg)、头孢噻肟/克拉维酸(30 μg/10 μg)纸片,按常规KB法进行。判读标准:两个组合中任何一组加克拉维酸的纸片比不加克拉维酸的纸片抑菌圈直径增大≥5 mm,即可确证产ESBLs。
按CLSI推荐的头孢西丁(30 μg)纸片法进行耐甲氧西林葡萄球菌的检测,培养24 h判读结果[6]。判断标准:对于金黄色葡萄球菌和路邓葡萄球菌,头孢西丁纸片扩散法的抑菌圈直径≥22 mm,判读为甲氧西林敏感金黄色葡萄球菌(MSSA);直径≤21 mm,判读为耐甲氧西林金黄色葡萄球菌(MRSA);对于凝固酶阴性葡萄球菌(除外路邓葡萄球菌、伪中间葡萄球菌和施氏葡萄球菌),头孢西丁纸片扩散法的抑菌圈直径≥25 mm,判读为甲氧西林敏感凝固酶阴性葡萄球菌(MSCNS);直径≤24 mm,判读为耐甲氧西林凝固酶阴性葡萄球菌(MRCNS);伪中间葡萄球菌和施氏葡萄球菌采用苯唑西林(1 μg)纸片法,纸片扩散法的抑菌圈直径≥18 mm,判读为甲氧西林敏感葡萄球菌。
按CLSI推荐的红霉素(12 μg)和克林霉素(2 μg)纸片法[6],对红霉素耐药且克林霉素非耐药的金黄色葡萄球菌、凝固酶阴性葡萄球菌、肺炎链球菌和β溶血链球菌进行克林霉素诱导试验。
根据不同的抗菌药物,采用琼脂稀释法或肉汤稀释法,操作按照CLSI推荐的要求进行[6],结果判读抗菌药物折点参照CLSI或欧洲抗菌药物敏感性试验委员会(EUCAST)标准[7];替加环素的折点参照美国食品和药品监督管理局(FDA)的标准:对葡萄球菌属≤0.5 mg/L判断为敏感;革兰阴性菌以≤2 mg/L为敏感,≥8 mg/L为耐药。阿莫西林/克拉维酸按照2∶1的比例;哌拉西林/他唑巴坦固定他唑巴坦浓度为4 mg/L。此外,哌拉西林/舒巴坦按照2∶1的比例;头孢他啶/阿维巴坦按照4∶1的比例;头孢哌酮/舒巴坦按照2∶1的比例进行测定。
采用微量肉汤稀释法进行药敏试验的抗菌药物:多黏菌素B、替加环素、利奈唑胺、达托霉素、青霉素G(肠球菌、链球菌)、克林霉素(肠球菌、链球菌),以及测定链球菌对红霉素、复方磺胺甲噁唑、头孢呋辛、头孢曲松、头孢吡肟、美罗培南、万古霉素、四环素、左氧氟沙星、莫西沙星。其他药物采用琼脂稀释法进行药敏试验。
磷霉素的药敏试验为琼脂稀释法,在琼脂培养基中补充浓度至25 mg/L的6-磷酸-葡萄糖。肺炎链球菌、α溶血链球菌和β溶血链球菌的肉汤稀释法使用CAMHB培养基,含有细胞溶解马血(LHB)(2.5%~5%,v/v);在检测达托霉素时添加钙离子浓度至50 mg/L;进行苯唑西林药敏检测时,需在MH琼脂中加入终浓度为2%的NaCl。
采用Whonet 5.6进行分析统计。
2018年1月至2019年12月来自全国18个省市区的50家BRICS成员单位共收集到16 325株细菌,经复核,删除1 547株不符合要求的菌株,包括1 220株经复核后菌名有误,238株为重复菌株,15株为污染菌株,74株单瓶阳性的凝固酶阴性葡萄球菌;14 778株细菌进行药物敏感性测定,其中2018年收集菌株5 209株,2019年9 569株。
14 778株细菌中,革兰阳性菌为4 117株(27.9%),革兰阴性菌10 661株(72.1%)。大肠埃希菌、肺炎克雷伯菌、金黄色葡萄球菌、凝固酶阴性葡萄球菌和铜绿假单胞菌为前5位的主要分离病原菌,占总病原菌分离数的76.4%(11 288/14 778)。主要分离菌种类及构成比在2018年和2019年差异无统计学意义(P>0.05)。详见表1。
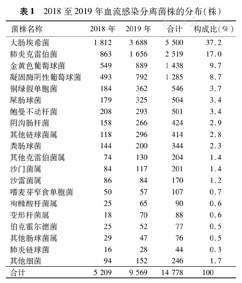
2018至2019年血流感染分离菌株的分布(株)
2018至2019年血流感染分离菌株的分布(株)
| 菌株名称 | 2018年 | 2019年 | 合计 | 构成比(%) |
|---|---|---|---|---|
| 大肠埃希菌 | 1 812 | 3 688 | 5 500 | 37.2 |
| 肺炎克雷伯菌 | 863 | 1 656 | 2 519 | 17.0 |
| 金黄色葡萄球菌 | 549 | 889 | 1 438 | 9.7 |
| 凝固酶阴性葡萄球菌 | 493 | 792 | 1 285 | 8.7 |
| 铜绿假单胞菌 | 184 | 362 | 546 | 3.7 |
| 屎肠球菌 | 179 | 325 | 504 | 3.4 |
| 鲍曼不动杆菌 | 208 | 293 | 501 | 3.4 |
| 阴沟肠杆菌 | 158 | 266 | 424 | 2.9 |
| 其他链球菌属 | 118 | 296 | 414 | 2.8 |
| 粪肠球菌 | 144 | 200 | 344 | 2.3 |
| 其他克雷伯菌属 | 74 | 130 | 204 | 1.4 |
| 沙门菌属 | 84 | 117 | 201 | 1.4 |
| 沙雷菌属 | 86 | 84 | 170 | 1.2 |
| 嗜麦芽窄食单胞菌 | 50 | 57 | 107 | 0.7 |
| 枸橼酸杆菌属 | 25 | 65 | 90 | 0.6 |
| 变形杆菌属 | 18 | 70 | 88 | 0.6 |
| 伯克霍尔德菌 | 25 | 52 | 77 | 0.5 |
| 其他肠球菌属 | 29 | 47 | 76 | 0.5 |
| 肺炎链球菌 | 16 | 28 | 44 | 0.3 |
| 其他细菌 | 94 | 152 | 246 | 1.7 |
| 合计 | 5 209 | 9 569 | 14 778 | 100 |
共分离到1 438株金黄色葡萄球菌,其中MRSA占27.4%(394/1 438);在1 285株凝固酶阴性葡萄球菌中,MRCNS占70.4%(905/1 285)。未分离到对万古霉素、替考拉宁和达托霉素耐药的葡萄球菌。金黄色葡萄球菌对青霉素G的敏感率为9.2%,对阿米卡星、利福平和复方磺胺甲噁唑的敏感率均在95%以上。MRSA对红霉素、克林霉素和四环素等耐药率明显高于MSSA。凝固酶阴性葡萄球菌对万古霉素、替考拉宁和达托霉素均敏感,对阿米卡星和利福平敏感率均超过90%;分离到24株耐利奈唑胺的凝固酶阴性葡萄球菌(20株头状葡萄球菌、2株科氏葡萄球菌、1株人葡萄球菌和1株木糖葡萄球菌)(表2、表3)。
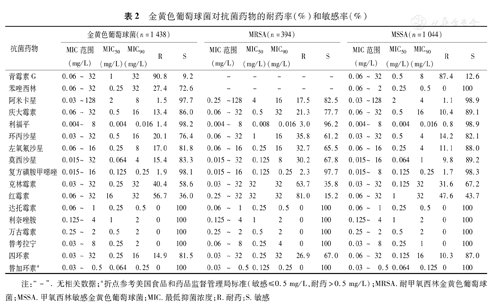
金黄色葡萄球菌对抗菌药物的耐药率(%)和敏感率(%)
金黄色葡萄球菌对抗菌药物的耐药率(%)和敏感率(%)
| 抗菌药物 | 金黄色葡萄球菌(n=1 438) | MRSA(n=394) | MSSA(n=1 044) | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| MIC范围(mg/L) | MIC50(mg/L) | MIC90(mg/L) | R | S | MIC范围(mg/L) | MIC50(mg/L) | MIC90(mg/L) | R | S | MIC范围(mg/L) | MIC50(mg/L) | MIC90(mg/L) | R | S | |
| 青霉素G | 0.06~32 | 1 | 32 | 90.8 | 9.2 | - | - | - | - | - | 0.06~32 | 0.5 | 8 | 87.4 | 12.6 |
| 苯唑西林 | 0.06~32 | 0.25 | 32 | 27.4 | 72.6 | - | - | - | - | - | 0.06~2 | 0.25 | 0.5 | 0 | 100 |
| 阿米卡星 | 0.03~128 | 2 | 8 | 1.5 | 97.7 | 0.25~128 | 4 | 16 | 17.5 | 82.5 | 0.03~128 | 2 | 4 | 1.1 | 98.9 |
| 庆大霉素 | 0.06~32 | 0.5 | 16 | 13.4 | 86.0 | 0.06~32 | 0.5 | 32 | 21.3 | 77.7 | 0.06~32 | 0.5 | 16 | 10.4 | 89.1 |
| 利福平 | 0.004~8 | 0.004 | 0.016 | 1.4 | 98.2 | 0.004~8 | 0.008 | 0.016 | 3.0 | 96.2 | 0.004~8 | 0.004 | 0.016 | 0.8 | 98.9 |
| 环丙沙星 | 0.03~32 | 0.5 | 16 | 20.1 | 76.4 | 0.06~32 | 1 | 16 | 35.8 | 61.2 | 0.03~32 | 0.5 | 4 | 14.2 | 82.1 |
| 左氧氟沙星 | 0.06~16 | 0.25 | 8 | 17.0 | 81.8 | 0.06~16 | 0.25 | 16 | 32.7 | 65.5 | 0.06~16 | 0.25 | 4 | 11.1 | 88.0 |
| 莫西沙星 | 0.015~32 | 0.064 | 4 | 15.4 | 83.3 | 0.015~32 | 0.125 | 8 | 30.2 | 67.8 | 0.015~16 | 0.064 | 1 | 9.8 | 89.2 |
| 复方磺胺甲噁唑 | 0.015~16 | 0.125 | 0.25 | 1.9 | 98.1 | 0.015~16 | 0.125 | 0.25 | 2.3 | 97.7 | 0.015~8 | 0.125 | 0.25 | 1.7 | 98.3 |
| 克林霉素 | 0.03~32 | 0.25 | 32 | 40.4 | 58.6 | 0.03~32 | 32 | 32 | 63.7 | 35.8 | 0.03~32 | 0.125 | 32 | 31.6 | 67.2 |
| 红霉素 | 0.06~32 | 16 | 32 | 56.7 | 36.0 | 0.25~32 | 32 | 32 | 81.0 | 15.2 | 0.06~32 | 1 | 32 | 47.6 | 43.7 |
| 达托霉素 | 0.06~1 | 0.25 | 0.5 | 0 | 100 | 0.06~1 | 0.25 | 0.5 | 0 | 100 | 0.06~1 | 0.25 | 0.5 | 0 | 100 |
| 利奈唑胺 | 0.125~4 | 1 | 2 | 0 | 100 | 0.125~4 | 1 | 2 | 0 | 100 | 0.125~4 | 1 | 2 | 0 | 100 |
| 万古霉素 | 0.25~2 | 0.5 | 2 | 0 | 100 | 0.25~2 | 0.5 | 2 | 0 | 100 | 0.25~2 | 0.5 | 2 | 0 | 100 |
| 替考拉宁 | 0.03~8 | 0.25 | 2 | 0 | 100 | 0.06~8 | 0.25 | 4 | 0 | 100 | 0.03~8 | 0.25 | 1 | 0 | 100 |
| 四环素 | 0.03~32 | 0.25 | 16 | 14.9 | 81.5 | 0.03~32 | 0.25 | 32 | 26.9 | 67.0 | 0.06~32 | 0.125 | 16 | 10.3 | 87.0 |
| 替加环素a | 0.03~0.5 | 0.064 | 0.25 | 0 | 100 | 0.03~0.5 | 0.125 | 0.25 | 0 | 100 | 0.03~0.5 | 0.064 | 0.125 | 0 | 100 |
注:"-".无相关数据;a折点参考美国食品和药品监督管理局标准(敏感≤0.5 mg/L,耐药>0.5 mg/L);MRSA.耐甲氧西林金黄色葡萄球菌;MSSA.甲氧西林敏感金黄色葡萄球菌;MIC.最低抑菌浓度;R.耐药;S.敏感
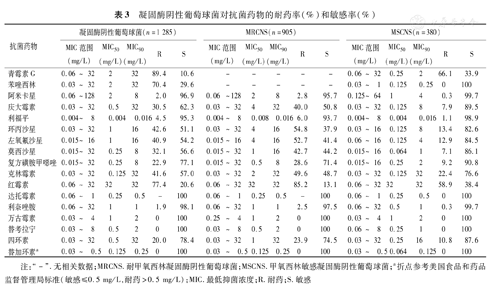
凝固酶阴性葡萄球菌对抗菌药物的耐药率(%)和敏感率(%)
凝固酶阴性葡萄球菌对抗菌药物的耐药率(%)和敏感率(%)
| 抗菌药物 | 凝固酶阴性葡萄球菌(n=1 285) | MRCNS(n=905) | MSCNS(n=380) | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| MIC范围(mg/L) | MIC50(mg/L) | MIC90(mg/L) | R | S | MIC范围(mg/L) | MIC50(mg/L) | MIC90(mg/L) | R | S | MIC范围(mg/L) | MIC50(mg/L) | MIC90(mg/L) | R | S | |
| 青霉素G | 0.06~32 | 2 | 32 | 89.4 | 10.6 | - | - | - | - | - | 0.06~32 | 0.25 | 2 | 66.1 | 33.9 |
| 苯唑西林 | 0.03~32 | 2 | 32 | 70.4 | 29.6 | - | - | - | - | - | 0.03~1 | 0.125 | 0.25 | 0 | 100 |
| 阿米卡星 | 0.06~128 | 2 | 8 | 2.0 | 96.9 | 0.06~128 | 2 | 8 | 2.8 | 95.7 | 0.125~64 | 1 | 4 | 0.3 | 99.7 |
| 庆大霉素 | 0.03~32 | 0.5 | 32 | 30.5 | 62.3 | 0.03~32 | 4 | 32 | 40.0 | 50.8 | 0.03~32 | 0.125 | 8 | 7.9 | 89.5 |
| 利福平 | 0.004~8 | 0.004 | 0.016 | 4.5 | 95.3 | 0.004~8 | 0.008 | 0.016 | 6.0 | 93.7 | 0.004~8 | 0.004 | 0.016 | 1.1 | 98.9 |
| 环丙沙星 | 0.03~32 | 1 | 16 | 42.6 | 51.1 | 0.03~32 | 4 | 16 | 54.8 | 37.9 | 0.03~16 | 0.125 | 8 | 13.4 | 82.6 |
| 左氧氟沙星 | 0.015~16 | 1 | 16 | 40.9 | 54.2 | 0.015~16 | 4 | 16 | 52.7 | 41.4 | 0.06~16 | 0.125 | 4 | 12.9 | 84.5 |
| 莫西沙星 | 0.015~32 | 0.25 | 8 | 32.1 | 56.6 | 0.015~32 | 1 | 16 | 42.7 | 44.2 | 0.015~16 | 0.064 | 1 | 7.1 | 86.1 |
| 复方磺胺甲噁唑 | 0.015~32 | 0.25 | 8 | 22.9 | 77.1 | 0.015~32 | 0.5 | 8 | 28.6 | 71.4 | 0.015~16 | 0.25 | 2 | 9.2 | 90.8 |
| 克林霉素 | 0.03~32 | 0.125 | 32 | 41.6 | 57.0 | 0.03~32 | 2 | 32 | 49.6 | 48.7 | 0.03~32 | 0.125 | 32 | 22.4 | 76.6 |
| 红霉素 | 0.06~32 | 32 | 32 | 77.4 | 20.6 | 0.06~32 | 32 | 32 | 85.2 | 13.1 | 0.06~32 | 32 | 32 | 58.9 | 38.4 |
| 达托霉素 | 0.06~1 | 0.25 | 0.5 | - | 100 | 0.06~1 | 0.25 | 0.5 | - | 100 | 0.06~1 | 0.25 | 0.5 | 0 | 100 |
| 利奈唑胺 | 0.06~32 | 1 | 1 | 1.9 | 98.1 | 0.06~32 | 1 | 1 | 2.5 | 97.5 | 0.06~32 | 0.5 | 1 | 0.3 | 99.7 |
| 万古霉素 | 0.03~4 | 1 | 2 | 0 | 100 | 0.25~4 | 1 | 2 | 0 | 100 | 0.03~4 | 1 | 2 | 0 | 100 |
| 替考拉宁 | 0.03~8 | 0.5 | 2 | 0 | 100 | 0.03~ 8 | 0.5 | 2 | 0 | 100 | 0.06~8 | 0.25 | 1 | 0 | 100 |
| 四环素 | 0.03~32 | 0.5 | 32 | 20.0 | 78.4 | 0.03~32 | 1 | 32 | 23.9 | 74.5 | 0.03~32 | 0.25 | 16 | 10.8 | 87.6 |
| 替加环素a | 0.03~0.5 | 0.125 | 0.25 | 0 | 100 | 0.03~0.5 | 0.125 | 0.25 | 0 | 100 | 0.03~0.5 | 0.064 | 0.125 | 0 | 100 |
注:"-".无相关数据;MRCNS.耐甲氧西林凝固酶阴性葡萄球菌;MSCNS.甲氧西林敏感凝固酶阴性葡萄球菌;a折点参考美国食品和药品监督管理局标准(敏感≤0.5 mg/L,耐药>0.5 mg/L);MIC.最低抑菌浓度;R.耐药;S.敏感
924株肠球菌属,以屎肠球菌为主(54.5%,504/924),其次为粪肠球菌(37.2%,344/924)和其他肠球菌(8.2%,76/924)。有2株(0.4%,2/504)耐万古霉素的屎肠球菌,未检出对万古霉素耐药的粪肠球菌;分别有3株屎肠球菌(0.6%,3/504)和5株粪肠球菌(1.5%,5/344)对利奈唑胺耐药;未检出对达托霉素耐药的屎肠球菌和粪肠球菌;屎肠球菌对青霉素G、利福平、氟喹诺酮类和红霉素的耐药率均高于粪肠球菌;粪肠球菌对氨苄西林具有较高的敏感性。其他肠球菌对利福平、环丙沙星的敏感率均高于屎肠球菌和粪肠球菌。详见表4。
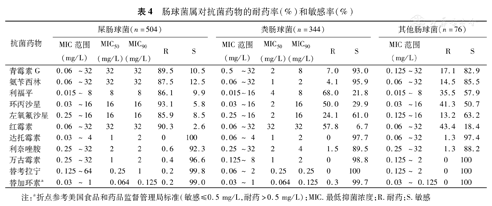
肠球菌属对抗菌药物的耐药率(%)和敏感率(%)
肠球菌属对抗菌药物的耐药率(%)和敏感率(%)
| 抗菌药物 | 屎肠球菌(n=504) | 粪肠球菌(n=344) | 其他肠球菌(n=76) | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| MIC范围(mg/L) | MIC50(mg/L) | MIC90(mg/L) | R | S | MIC范围(mg/L) | MIC50(mg/L) | MIC90(mg/L) | R | S | MIC范围 (mg/L) | R | S | |
| 青霉素G | 0.06~32 | 32 | 32 | 89.5 | 10.5 | 0.5~32 | 2 | 8 | 7.0 | 93.0 | 0.125~32 | 17.1 | 82.9 |
| 氨苄西林 | 0.06~32 | 32 | 32 | 87.5 | 12.5 | 0.06~32 | 1 | 2 | 4.1 | 95.9 | 0.06~32 | 14.5 | 85.5 |
| 利福平 | 0.015~8 | 8 | 8 | 86.1 | 9.9 | 0.015~16 | 4 | 8 | 68.0 | 21.8 | 0.015~8 | 35.5 | 57.9 |
| 环丙沙星 | 0.03~16 | 16 | 16 | 93.1 | 5.8 | 0.03~16 | 2 | 16 | 50.0 | 29.9 | 0.03~16 | 41.3 | 50.7 |
| 左氧氟沙星 | 0.25~16 | 16 | 16 | 85.9 | 8.5 | 0.25~16 | 2 | 16 | 24.1 | 61.0 | 0.125~16 | 13.2 | 63.2 |
| 红霉素 | 0.06~32 | 32 | 32 | 90.3 | 2.6 | 0.06~32 | 32 | 32 | 57.8 | 6.7 | 0.06~32 | 43.4 | 18.4 |
| 达托霉素 | 0.03~4 | 1 | 2 | 0 | 100 | 0.06~4 | 1 | 2 | 0 | 97.7 | 0.06~32 | 1.3 | 97.4 |
| 利奈唑胺 | 0.25~32 | 2 | 2 | 0.6 | 92.3 | 0.25~32 | 2 | 4 | 1.5 | 89.5 | 0.25~32 | 1.3 | 88.2 |
| 万古霉素 | 0.25~32 | 1 | 2 | 0.4 | 96.6 | 0.125~8 | 1 | 2 | 0 | 98.8 | 0.125~2 | 0 | 100 |
| 替考拉宁 | 0.125~64 | 0.25 | 1 | 0.2 | 99.8 | 0.06~2 | 0.25 | 0.25 | 0 | 100 | 0.125~2 | 0 | 100 |
| 替加环素a | 0.03~1 | 0.064 | 0.125 | 0.2 | 99.0 | 0.03~1 | 0.064 | 0.125 | 0.3 | 99.7 | 0.03~0.125 | 0 | 100 |
注:a折点参考美国食品和药品监督管理局标准(敏感≤0.5 mg/L,耐药>0.5 mg/L);MIC.最低抑菌浓度;R.耐药;S.敏感
按青霉素G非脑膜炎注射给药折点,未发现对青霉素G耐药的肺炎链球菌,但以脑膜炎注射给药折点则耐药率高达77.3%。肺炎链球菌对利奈唑胺、万古霉素、替考拉宁和达托霉素均敏感。α溶血链球菌中未检出对美罗培南、达托霉素、万古霉素、替考拉宁和利奈唑胺耐药的菌株;β溶血链球菌对青霉素G、头孢菌素、达托霉素、万古霉素、替考拉宁和利奈唑胺均敏感。β溶血链球菌对左氧氟沙星、克林霉素、红霉素和四环素的耐药率均高于α溶血链球菌。链球菌对红霉素和克林霉素耐药突出,经诱导克林霉素耐药试验,24.2%的菌株诱导耐药(表5)。
链球菌属对不同抗菌药物的耐药率(%)和敏感率(%)
链球菌属对不同抗菌药物的耐药率(%)和敏感率(%)
| 抗菌药物 | 肺炎链球菌(n=44) | α溶血链球菌(n=242) | β溶血链球菌(n=186) | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 折点 | MIC范围(mg/L) | R | S | MIC范围(mg/L) | MIC50 (mg/L) | MIC90 (mg/L) | R | S | MIC范围(mg/L) | MIC50 (mg/L) | MIC90 (mg/L) | R | S | |
| 青霉素G | 非脑膜炎(注射) | 0.03~4 | 0 | 97.7 | 0.015~ 8 | 0.125 | 0.5 | 1.7 | 66.5 | 0.015~0.125 | 0.064 | 0.125 | 0 | 100 |
| 青霉素G | 非脑膜炎(口服) | 0.03~4 | 40.9 | 22.7 | - | - | - | - | - | - | - | - | - | - |
| 青霉素G | 脑膜炎 | 0.03~4 | 77.3 | 22.7 | - | - | - | - | - | - | - | - | - | - |
| 头孢呋辛 | 口服 | 0.015~16 | 50.0 | 43.2 | - | - | - | - | - | - | - | - | - | - |
| 头孢呋辛 | 注射 | 0.015~16 | 56.8 | 43.2 | - | - | - | - | - | - | - | - | - | - |
| 头孢曲松 | 脑膜炎 | 0.015~4 | 18.2 | 61.4 | - | - | - | - | - | - | - | - | - | - |
| 头孢曲松 | 非脑膜炎 | 0.015~4 | 9.1 | 81.8 | 0.006~ 8 | 0.064 | 0.5 | 5.4 | 93.4 | 0.015~0.5 | 0.064 | 0.064 | 0 | 100 |
| 头孢吡肟 | 脑膜炎 | 0.03~ 8 | 25.0 | 45.5 | ||||||||||
| 头孢吡肟 | 非脑膜炎 | 0.03~8 | 4.5 | 75.0 | 0.015~ 8 | 0.064 | 0.5 | 5.4 | 93.8 | 0.015~0.5 | 0.064 | 0.125 | 0 | 100 |
| 美罗培南 | 0.015~0.5 | 0 | 88.6 | 0.006~ 2 | 0.016 | 0.25 | 0 | 95.5 | 0.015~0.5 | 0.016 | 0.064 | 0 | 100 | |
| 左氧氟沙星 | 0.06~4 | 0 | 97.7 | 0.015~16 | 0.5 | 4 | 7.0 | 89.7 | 0.015~16 | 0.5 | 16 | 31.7 | 67.7 | |
| 莫西沙星a | 0.06~2 | 0 | 97.7 | - | - | - | - | - | - | - | - | - | - | |
| 复方磺胺甲噁唑b | 0.03~4 | 22.7 | 54.5 | - | - | - | - | - | - | - | - | - | - | |
| 克林霉素 | 0.03~16 | 86.4 | 13.6 | 0.015~16 | 4 | 16 | 55.0 | 43.8 | 0.03~16 | 4 | 16 | 76.9 | 22.6 | |
| 红霉素 | 0.03~16 | 88.6 | 11.4 | 0.015~16 | 4 | 16 | 67.8 | 29.3 | 0.03~16 | 4 | 16 | 85.5 | 14.0 | |
| 达托霉素 | 0.06~0.25 | 0 | 100 | 0.03~ 8 | 0.5 | 2 | 0 | 86.8 | 0.03~1 | 0.5 | 1 | 0 | 100 | |
| 利奈唑胺 | 0.03~1 | 0 | 100 | 0.015~16 | 0.5 | 1 | 0 | 99.6 | 0.015~2 | 1 | 1 | 0 | 100 | |
| 万古霉素 | 0.015~0.5 | 0 | 100 | 0.015~ 1 | 0.5 | 0.5 | 0 | 100 | 0.03~1 | 0.25 | 0.5 | 0 | 100 | |
| 替考拉宁 | 0.015~0.25 | 0 | 100 | 0.015~ 0.125 | 0.032 | 0.064 | 0 | 100 | 0.015~0.25 | 0.032 | 0.064 | 0 | 100 | |
| 四环素 | 0.06~16 | 72.7 | 20.5 | 0.015~16 | 4 | 16 | 39.4 | 50.0 | 0.125~16 | 8 | 16 | 68.3 | 25.0 | |
| 替加环素c | 0.03~0.125 | 0 | 93.8 | 0.015~ 0.125 | 0.064 | 0.125 | 0 | 100 | 0.015~0.125 | 0.032 | 0.125 | 0 | 100 | |
注:"-".无相关数据;aβ溶血链球菌对莫西沙星的折点参考欧洲抗菌药物敏感性试验委员会(EUCAST)标准(敏感≤0.5 mg/L,耐药>0.5 mg/L);bβ溶血链球菌对复方磺胺甲噁唑的折点参考EUCAST标准(敏感≤1 mg/L,耐药>2 mg/L);c肺炎链球菌对替加环素的折点参考美国食品和药品监督管理局标准(敏感≤0.12 mg/L);α溶血链球菌和β溶血链球菌对替加环素的折点参考EUCAST标准(敏感≤0.125 mg/L,耐药>0.125 mg/L);MIC.最低抑菌浓度;R.耐药;S.敏感
共分离到85株耐碳青霉烯大肠埃希菌(CRE),占1.5%(85/5 500);磷霉素、多黏菌素B和替加环素对CRE均具有较好的抗菌活性,同时,CRE对阿米卡星敏感率超过70%;CRE对头孢他啶/阿维巴坦的敏感率为39.3%,其最低抑菌浓度(MIC)值分布见图1A。厄他培南、亚胺培南和美罗培南对CRE的MIC≤8 mg/L的菌株分别占50.0%、50.0%和62.9%(图2A)。5 415株非耐碳青霉烯类大肠埃希菌中,产ESBLs占50.4%(2 731/5 415),产ESBLs大肠埃希菌对氨基糖苷类、氟喹诺酮类和复方磺胺甲噁唑的耐药率均高于不产ESBLs的大肠埃希菌,但二者对磷霉素、多黏菌素B和替加环素均表现为敏感(表6)。
大肠埃希菌对抗菌药物的耐药率(%)及敏感率(%)
大肠埃希菌对抗菌药物的耐药率(%)及敏感率(%)
| 抗菌药物 | 大肠埃希菌(n=5 500) | ESBLs+大肠埃希菌(n=2 731) | ESBLs-大肠埃希菌(n=2 684) | 耐碳青霉烯类大肠埃希菌(n=85) | ||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| MIC范围(mg/L) | MIC50(mg/L) | MIC90(mg/L) | R | S | MIC范围(mg/L) | MIC50(mg/L) | MIC90(mg/L) | R | S | MIC范围(mg/L) | MIC50(mg/L) | MIC90(mg/L) | R | S | MIC范围(mg/L) | R | S | |
| 阿莫西林 | 0.25~256 | 128 | 128 | 83.8 | 14.8 | - | - | - | - | - | 0.25~256 | 128 | 128 | 67.1 | 30.1 | - | - | - |
| 阿莫西林/克拉维酸 | 0.25~128 | 16 | 128 | 37.5 | 41.6 | 0.25~128 | 16 | 128 | 43.6 | 31.6 | 0.25~128 | 8 | 128 | 29.5 | 53.1 | - | - | - |
| 哌拉西林/他唑巴坦 | 0.125~256 | 4 | 64 | 7.3 | 85.6 | 0.125~256 | 4 | 64 | 9.4 | 80.3 | 0.125~128 | 2 | 16 | 3.0 | 93.6 | - | - | - |
| 哌拉西林/舒巴坦a | 0.5~256 | 8 | 64 | 6.1 | 76.8 | 0.5~256 | 16 | 64 | 7.2 | 66.3 | 0.5~256 | 4 | 32 | 2.3 | 89.6 | - | - | - |
| 头孢唑啉 | 0.125~128 | 128 | 128 | 56.4 | 38.7 | - | - | - | - | - | 0.125~128 | 1 | 8 | 11.9 | 78.4 | - | - | - |
| 头孢呋辛 | 0.25~128 | 128 | 128 | 53.0 | 43.1 | - | - | - | - | - | 0.25~128 | 4 | 16 | 5.8 | 86.9 | - | - | - |
| 头孢他啶 | 0.03~128 | 1 | 64 | 27.4 | 64.4 | 0.125~128 | 8 | 64 | 49.5 | 35.6 | 0.03~64 | 0.125 | 0.5 | 2.6 | 95.7 | - | - | - |
| 头孢他啶/阿维巴坦b | 0.03~32 | 0.25 | 1 | 1.0 | 99.0 | 0.03~8 | 0.5 | 1 | 0 | 100 | 0.06~8 | 0.25 | 0.5 | 0 | 100 | 0.5~32 | 60.7 | 39.3 |
| 头孢曲松 | 0.03~128 | 8 | 64 | 52.9 | 46.8 | - | - | - | - | - | 0.03~64 | 0.125 | 0.25 | 5.4 | 94.4 | - | - | - |
| 头孢哌酮/舒巴坦 | 0.06~128 | 4 | 32 | - | - | 0.125~128 | 16 | 64 | - | - | 0.06~128 | 0.5 | 4 | - | - | - | - | - |
| 头孢吡肟 | 0.015~64 | 0.5 | 32 | 17.1 | 63.9 | - | - | - | - | - | 0.015~64 | 0.032 | 0.125 | 1.0 | 98.4 | - | - | - |
| 头孢西丁 | 0.25~128 | 4 | 32 | 11.9 | 79.7 | 0.25~128 | 8 | 32 | 15.0 | 72.5 | 0.25~ 128 | 4 | 16 | 6.2 | 89.3 | - | - | - |
| 拉氧头孢 | 0.06~128 | 0.25 | 2 | 2.4 | 96.2 | 0.06~128 | 0.5 | 2 | 1.4 | 96.2 | 0.125~128 | 0.25 | 0.5 | 0.6 | 99.2 | - | - | - |
| 氨曲南 | 0.03~256 | 2 | 64 | 35.2 | 57.2 | - | - | - | - | - | 0.03~256 | 0.125 | 0.5 | 2.6 | 96.5 | 0.125~256 | 78.8 | 15.3 |
| 厄他培南 | 0.007~32 | 0.016 | 0.064 | 1.5 | 97.9 | 0.007~1 | 0.016 | 0.125 | 0 | 99.0 | 0.007~1 | 0.016 | 0.032 | 0 | 99.8 | 2~32 | 100 | 0 |
| 亚胺培南 | 0.015~32 | 0.25 | 0.5 | 1.5 | 98.3 | 0.015~2 | 0.25 | 0.5 | 0 | 99.7 | 0.015~2 | 0.25 | 0.5 | 0 | 99.9 | 0.5~32 | 96.5 | 2.4 |
| 美罗培南 | 0.007~32 | 0.016 | 0.064 | 1.5 | 98.5 | 0.007~1 | 0.016 | 0.064 | 0 | 100 | 0.015~1 | 0.016 | 0.064 | 0 | 100 | 1~32 | 97.6 | 1.2 |
| 阿米卡星 | 0.25~128 | 4 | 8 | 2.3 | 97.5 | 0.25~128 | 4 | 8 | 3.5 | 96.3 | 0.25~128 | 4 | 8 | 0.5 | 99.4 | 0.5~128 | 22.4 | 74.1 |
| 庆大霉素 | 0.25~128 | 2 | 128 | 36.9 | 62.3 | 0.25~128 | 4 | 128 | 43.9 | 55.0 | 0.25~128 | 2 | 128 | 28.8 | 70.7 | 0.25~128 | 64.7 | 32.9 |
| 环丙沙星 | 0.007~32 | 2 | 32 | 62.4 | 27.7 | 0.007~32 | 32 | 32 | 78.7 | 14.8 | 0.007~32 | 0.5 | 32 | 44.7 | 41.6 | 0.03~32 | 96.5 | 3.5 |
| 左氧氟沙星 | 0.007~64 | 2 | 32 | 50.9 | 38.7 | 0.015~64 | 16 | 32 | 69.2 | 22.0 | 0.007~32 | 0.5 | 16 | 31.0 | 56.8 | 0.06~32 | 94.1 | 3.5 |
| 复方磺胺甲噁唑 | 0.015~32 | 8 | 8 | 55.2 | 44.8 | 0.015~32 | 8 | 8 | 64.3 | 35.7 | 0.015~32 | 0.25 | 8 | 45.2 | 54.8 | 0.015~8 | 78.8 | 21.2 |
| 磷霉素 | 0.125~256 | 0.5 | 2 | 2.8 | 95.6 | 0.5~256 | 0.5 | 8 | 4.8 | 92.6 | 0.125~256 | 0.5 | 1 | 0.3 | 99.4 | 0.5~256 | 17.6 | 70.6 |
| 多黏菌素Bc | 0.03~32 | 0.5 | 2 | 0 | 98.5 | 0.03~32 | 0.5 | 2 | 0 | 98.2 | 0.06~32 | 0.5 | 2 | 0 | 98.8 | 0.25~32 | 0 | 96.5 |
| 替加环素d | 0.015~4 | 0.25 | 0.25 | 0 | 100 | 0.015~4 | 0.25 | 0.25 | 0 | 100 | 0.015~2 | 0.25 | 0.25 | 0 | 100 | 0.03~2 | 0 | 100 |
注:"-".无相关数据;EBSLs.产超广谱β-内酰胺酶;a大肠埃希菌哌拉西林/舒巴坦检测数为3 687株,哌拉西林/舒巴坦折点参考哌拉西林折点;b大肠埃希菌对头孢他啶/阿维巴坦检测数为3 687株;c折点参考欧洲抗菌药物敏感性试验委员会标准(敏感≤2 mg/L,耐药>2 mg/L);d折点参考美国食品和药品监督管理局标准(敏感≤2 mg/L,中敏4 mg/L,耐药>4 mg/L);MIC.最低抑菌浓度;R.耐药;S.敏感
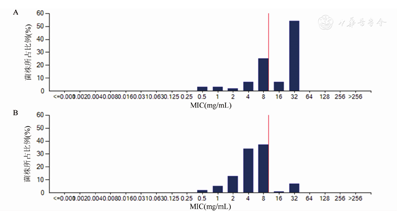

注:A.头孢他啶/阿维巴坦对耐碳青霉烯大肠埃希菌MIC值的分布图;B.头孢他啶/阿维巴坦对耐碳青霉烯肺炎克雷伯菌MIC值的分布图
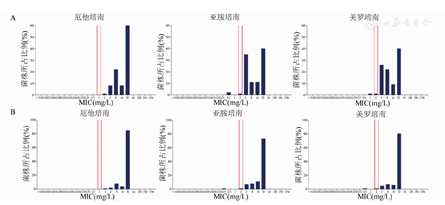

注:A.厄他培南、亚胺培南和美罗培南对耐碳青霉烯大肠埃希菌MIC值的分布图;B.厄他培南、亚胺培南和美罗培南对耐碳青霉烯肺炎克雷伯菌MIC值的分布图
共分离到518株耐碳青霉烯肺炎克雷伯菌(CRKP),占20.6%(518/2 519);8.3% CRKP对头孢他啶/阿维巴坦耐药,其MIC值分布见图1B;多黏菌素B和替加环素对CRKP抗菌活性较好,而CRKP对阿米卡星则有较高的耐药率(表7)。厄他培南、亚胺培南和美罗培南对CRKP的MIC≤8 mg/L的菌株数分别占20.6%、20.6%和19.0%(图2B)。在2 001株对碳青霉烯敏感肺炎克雷伯菌中,产ESBL为24.6%(493/2 001)。不产ESBL肺炎克雷伯菌对包括头孢菌素、氟喹诺酮类、氨基糖苷类、复方磺胺甲噁唑等抗菌药物均有较好的敏感性(耐药率低于20%),产ESBLs肺炎克雷伯菌则对氟喹诺酮类和复方磺胺甲噁唑等耐药率均较高(高于50%)。无论肺炎克雷伯菌是否产ESBLs,阿米卡星、磷霉素、多黏菌素B和替加环素均有较好的体外抗菌活性(表7)。
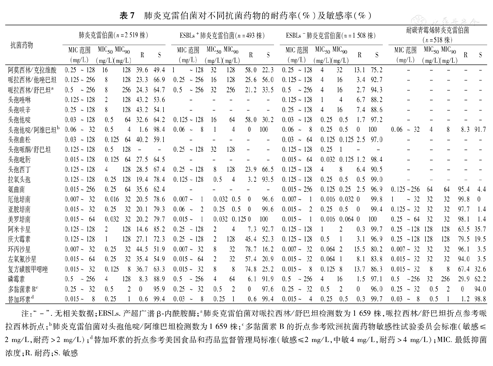
肺炎克雷伯菌对不同抗菌药物的耐药率(%)及敏感率(%)
肺炎克雷伯菌对不同抗菌药物的耐药率(%)及敏感率(%)
| 抗菌药物 | 肺炎克雷伯菌(n=2 519株) | ESBLs+肺炎克雷伯菌(n=493株) | ESBLs-肺炎克雷伯菌(n=1 508株) | 耐碳青霉烯肺炎克雷伯菌(n=518株) | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| MIC范围(mg/L) | MIC50(mg/L) | MIC90(mg/L) | R | S | MIC范围(mg/L) | MIC50(mg/L) | MIC90(mg/L) | R | S | MIC范围(mg/L) | MIC50(mg/L) | MIC90(mg/L) | R | S | MIC范围(mg/L) | MIC50(mg/L) | MIC90(mg/L) | R | S | |
| 阿莫西林/克拉维酸 | 0.25~128 | 16 | 128 | 39.6 | 49.4 | 1 ~128 | 32 | 128 | 58.0 | 22.3 | 0.25~128 | 4 | 32 | 13.1 | 75.2 | - | - | - | - | - |
| 哌拉西林/他唑巴坦 | 0.125~256 | 8 | 128 | 23.3 | 66.9 | 0.25~256 | 16 | 128 | 25.6 | 56.0 | 0.125~128 | 4 | 16 | 3.4 | 92.7 | - | - | - | - | - |
| 哌拉西林/舒巴坦a | 0.5~256 | 8 | 256 | 24.3 | 64.7 | 0.5~256 | 32 | 256 | 21.2 | 33.5 | 0.5~256 | 4 | 16 | 2.7 | 94.3 | - | - | - | - | - |
| 头孢唑啉 | 0.125~128 | 2 | 128 | 43.2 | 53.6 | - | - | - | - | - | 0.125~128 | 1 | 4 | 6.7 | 88.2 | - | - | - | - | - |
| 头孢呋辛 | 0.25~128 | 8 | 128 | 43.2 | 54.1 | - | - | - | - | - | 0.25~128 | 4 | 16 | 7.4 | 88.6 | - | - | - | - | - |
| 头孢他啶 | 0.03~128 | 0.5 | 64 | 32.6 | 64.2 | 0.125~128 | 16 | 64 | 58.0 | 30.2 | 0.03~128 | 0.25 | 0.5 | 1.7 | 97.2 | - | - | - | - | - |
| 头孢他啶/阿维巴坦b | 0.06~32 | 0.5 | 4 | 1.6 | 98.4 | 0.06~8 | 1 | 4 | 0 | 100 | 0.06~8 | 0.25 | 0.5 | 0 | 100 | 0.06~32 | 4 | 8 | 8.3 | 91.7 |
| 头孢曲松 | 0.03~128 | 0.125 | 64 | 40.2 | 59.1 | - | - | - | - | - | 0.03~64 | 0.125 | 0.125 | 2.5 | 97.0 | - | - | - | - | - |
| 头孢哌酮/舒巴坦 | 0.125~128 | 0.5 | 128 | - | - | 0.25~128 | 32 | 128 | - | - | 0.125~128 | 0.25 | 1 | - | - | - | - | - | - | - |
| 头孢吡肟 | 0.015~128 | 0.125 | 64 | 27.5 | 64.5 | - | - | - | - | - | 0.015~64 | 0.032 | 0.125 | 1.2 | 98.4 | - | - | - | - | - |
| 头孢西丁 | 0.125~128 | 4 | 128 | 28.5 | 67.4 | 0.25~128 | 8 | 128 | 23.9 | 66.5 | 0.125~128 | 4 | 8 | 6.4 | 90.5 | - | - | - | - | - |
| 拉氧头孢 | 0.125~128 | 0.25 | 128 | 19.4 | 78.4 | 0.125~128 | 0.5 | 4 | 3.2 | 93.5 | 0.125~128 | 0.25 | 0.5 | 0.5 | 99.0 | - | - | - | - | - |
| 氨曲南 | 0.015~256 | 0.25 | 64 | 35.6 | 62.4 | - | - | - | - | - | 0.015~256 | 0.125 | 0.25 | 2.5 | 96.9 | 0.125~256 | 64 | 64 | 95.4 | 4.4 |
| 厄他培南 | 0.007~32 | 0.016 | 32 | 20.5 | 78.6 | 0.007~1 | 0.032 | 0.5 | 0 | 96.6 | 0.007~1 | 0.016 | 0.032 | 0 | 99.8 | 1~32 | 32 | 32 | 99.8 | 0 |
| 亚胺培南 | 0.015~32 | 0.25 | 32 | 20.1 | 79.3 | 0.06~2 | 0.25 | 0.5 | 0 | 99.6 | 0.015~2 | 0.25 | 0.5 | 0 | 99.4 | 0.125~32 | 32 | 32 | 97.7 | 1.4 |
| 美罗培南 | 0.015~64 | 0.032 | 32 | 20.2 | 79.7 | 0.015~1 | 0.032 | 0.125 | 0 | 100 | 0.015~1 | 0.016 | 0.064 | 0 | 100 | 0.25~64 | 32 | 32 | 98.1 | 1.4 |
| 阿米卡星 | 0.125~128 | 2 | 128 | 14.6 | 85.2 | 0.25~128 | 2 | 4 | 7.3 | 92.7 | 0.125~128 | 1 | 2 | 0.3 | 99.7 | 0.25~128 | 128 | 128 | 63.5 | 35.7 |
| 庆大霉素 | 0.125~128 | 1 | 128 | 27.1 | 72.3 | 0.25~128 | 2 | 128 | 45.4 | 52.3 | 0.125~128 | 0.5 | 1 | 3.1 | 96.9 | 0.25~128 | 128 | 128 | 79.5 | 19.5 |
| 环丙沙星 | 0.007~32 | 0.25 | 32 | 44.5 | 51.9 | 0.007~32 | 8 | 32 | 78.7 | 16.2 | 0.007~32 | 0.064 | 2 | 15.5 | 80.2 | 0.007~32 | 32 | 32 | 96.1 | 3.5 |
| 左氧氟沙星 | 0.015~64 | 0.25 | 32 | 35.4 | 54.9 | 0.015~64 | 2 | 32 | 57.4 | 20.9 | 0.015~32 | 0.064 | 1 | 8.1 | 83.8 | 0.015~32 | 32 | 32 | 94.0 | 3.5 |
| 复方磺胺甲噁唑 | 0.015~32 | 0.125 | 8 | 36.7 | 63.3 | 0.015~32 | 8 | 8 | 74.8 | 25.2 | 0.015~8 | 0.125 | 8 | 13.7 | 86.3 | 0.015~32 | 8 | 8 | 67.4 | 32.6 |
| 磷霉素 | 0.5~256 | 4 | 128 | 8.3 | 88.9 | 0.5~256 | 4 | 64 | 6.1 | 91.9 | 0.5~256 | 4 | 16 | 1.5 | 97.1 | 0.5~256 | 32 | 256 | 29.9 | 62.2 |
| 多黏菌素Bc | 0.25~32 | 0.5 | 2 | 0 | 95.9 | 0.25~32 | 0.5 | 2 | 0 | 97.6 | 0.25~32 | 0.5 | 2 | 0 | 96.0 | 0.25~32 | 0.5 | 2 | 0 | 94.0 |
| 替加环素d | 0.015~8 | 0.25 | 1 | 0.6 | 99.4 | 0.03~8 | 0.25 | 1 | 0.6 | 99.4 | 0.015~4 | 0.25 | 0.5 | 0.3 | 99.7 | 0.03~8 | 0.5 | 1 | 1.2 | 98.8 |
注:"-".无相关数据;EBSLs.产超广谱β-内酰胺酶;a肺炎克雷伯菌对哌拉西林/舒巴坦检测数为1 659株,哌拉西林/舒巴坦折点参考哌拉西林折点;b肺炎克雷伯菌对头孢他啶/阿维巴坦检测数为1 659株;c多黏菌素B的折点参考欧洲抗菌药物敏感性试验委员会标准(敏感≤2 mg/L,耐药>2 mg/L);d替加环素的折点参考美国食品和药品监督管理局标准(敏感≤2 mg/L,中敏4 mg/L,耐药>4 mg/L);MIC.最低抑菌浓度;R.耐药;S.敏感
变形杆菌属经双纸片确认产ESBLs的阳性率为35.2%(31/88);其他克雷伯菌属、变形杆菌属、阴沟肠杆菌、沙雷菌属和沙门菌属对头孢他啶/阿维巴坦有较高的敏感性(均在90%以上),但枸橼酸杆菌属的敏感性为83.1%(54/65);肠杆菌目细菌对3种碳青霉烯抗菌药物的敏感率均在80%以上,但亚胺培南与其他2种碳青霉烯抗菌药物相比,对变形杆菌属和沙雷菌属细菌敏感性均偏低。检测细菌对磷霉素的耐药率均低于10%;其他克雷伯菌属、阴沟肠杆菌、沙雷菌属、枸橼酸杆菌属和沙门菌属细菌对替加环素的敏感性均超过98%(表8、表9)。
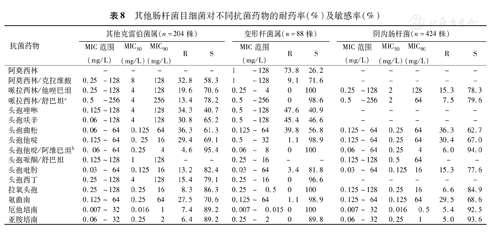
其他肠杆菌目细菌对不同抗菌药物的耐药率(%)及敏感率(%)
其他肠杆菌目细菌对不同抗菌药物的耐药率(%)及敏感率(%)
| 抗菌药物 | 其他克雷伯菌属(n=204株) | 变形杆菌属(n=88株) | 阴沟肠杆菌(n=424株) | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| MIC范围(mg/L) | MIC50(mg/L) | MIC90(mg/L) | R | S | MIC范围(mg/L) | R | S | MIC范围(mg/L) | MIC50(mg/L) | MIC90(mg/L) | R | S | |
| 阿莫西林 | - | - | - | - | - | 1 ~128 | 73.8 | 26.2 | - | - | - | - | - |
| 阿莫西林/克拉维酸 | 0.25~128 | 8 | 128 | 32.8 | 58.3 | 1 ~128 | 9.1 | 71.6 | - | - | - | - | - |
| 哌拉西林/他唑巴坦 | 0.25~128 | 4 | 128 | 19.6 | 70.6 | 0.25~4 | 0 | 100 | 0.25~128 | 2 | 128 | 15.3 | 78.3 |
| 哌拉西林/舒巴坦a | 0.5~256 | 4 | 256 | 13.4 | 78.2 | 0.5~256 | 0 | 98.6 | 0.5~256 | 2 | 64 | 7.5 | 79.6 |
| 头孢唑啉 | 0.125~128 | 4 | 128 | 34.3 | 40.7 | 0.5~128 | 47.6 | 40.9 | - | - | - | - | - |
| 头孢呋辛 | 0.06~128 | 4 | 128 | 30.8 | 65.2 | 0.5~128 | 45.4 | 46.6 | - | - | - | - | - |
| 头孢曲松 | 0.06~64 | 0.125 | 64 | 36.3 | 61.3 | 0.125~64 | 39.8 | 56.8 | 0.125~64 | 0.25 | 64 | 36.3 | 62.7 |
| 头孢他啶 | 0.125~64 | 0. 25 | 16 | 29.4 | 69.1 | 0.5~32 | 1.1 | 98.9 | 0.125~64 | 0.25 | 64 | 30.4 | 67.0 |
| 头孢他啶/阿维巴坦b | 0. 06~64 | 0.25 | 4 | 4.6 | 95.4 | 0.06~8 | 0 | 100 | 0.06~64 | 0.25 | 4 | 6.0 | 94.0 |
| 头孢哌酮/舒巴坦 | 0.125~128 | 1 | 128 | - | - | 0.25~16 | - | - | 0.125~128 | 0.5 | 64 | - | - |
| 头孢吡肟 | 0.03~64 | 0.125 | 16 | 13.2 | 82.4 | 0.03~64 | 3.4 | 81.8 | 0.03~64 | 0.125 | 16 | 15.3 | 77.6 |
| 头孢西丁 | 0.25~128 | 4 | 128 | 15.4 | 79.1 | 0.25~16 | 0 | 96.6 | - | - | - | - | - |
| 拉氧头孢 | 0.25~128 | 0.25 | 16 | 8.3 | 86.3 | 0.25~0.5 | 0 | 100 | 0.125~128 | 0.25 | 16 | 6.6 | 84.9 |
| 氨曲南 | 0.125~64 | 0.25 | 64 | 27.5 | 70.6 | 0.125~64 | 1.1 | 98.9 | 0.125~64 | 0.125 | 64 | 29.5 | 68.6 |
| 厄他培南 | 0.007~32 | 0.016 | 1 | 7.4 | 89.2 | 0.007~0.015 | 0 | 100 | 0.007~32 | 0.016 | 0.5 | 5.4 | 92.5 |
| 亚胺培南 | 0.06~32 | 0.25 | 2 | 6.4 | 89.2 | 0.25~2 | 0 | 89.8 | 0.06~32 | 0.25 | 1 | 5.0 | 93.6 |
| 美罗培南 | 0.015~32 | 0.032 | 0.25 | 6.4 | 93.1 | 0.015~ 0.125 | 0 | 100 | 0.015~32 | 0.032 | 0.125 | 5.0 | 95.0 |
| 阿米卡星 | 0.125~128 | 1 | 4 | 1.0 | 99.0 | 0.5~128 | 2.3 | 93.2 | 0.125~128 | 1 | 4 | 1.7 | 98.1 |
| 庆大霉素 | 0.125~128 | 1 | 2 | 7.4 | 91.7 | 0.5~128 | 34.1 | 50.0 | 0.25~128 | 1 | 64 | 15.6 | 82.1 |
| 环丙沙星 | 0.007~32 | 0.064 | 16 | 20.6 | 77.0 | 0.007~32 | 58.0 | 35.2 | 0.007~64 | 0.032 | 32 | 24.8 | 71.0 |
| 左氧氟沙星 | 0.015~32 | 0.064 | 8 | 16.7 | 79.4 | 0.015~32 | 50.0 | 42.0 | 0.015~32 | 0.064 | 8 | 16.3 | 74.8 |
| 复方磺胺甲噁唑 | 0.015~8 | 0.125 | 8 | 14.2 | 85.8 | 0.03~8 | 59.1 | 40.9 | 0.015~8 | 0.125 | 8 | 22.9 | 77.1 |
| 磷霉素 | 0.5~256 | 8 | 64 | 3.9 | 93.1 | 0.5~256 | 3.4 | 83.0 | 0.5~256 | 8 | 64 | 1.9 | 94.1 |
| 多黏菌素Bc | 0.125~32 | 1 | 2 | 0 | 94.6 | - | - | - | 0.25~32 | 2 | 32 | 0 | 61.1 |
| 替加环素d | 0.03~4 | 0.25 | 0.5 | 1.0 | 99.0 | - | - | - | 0.03~4 | 0.25 | 0.5 | 1.7 | 98.3 |
注:"-".无相关数据;a其他克雷伯菌、变形杆菌属细菌和阴沟肠杆菌对哌拉西林/舒巴坦的检测数分别为142、70和265株,哌拉西林/舒巴坦折点参考哌拉西林折点;b其他克雷伯菌、变形杆菌属细菌和阴沟肠杆菌对头孢他啶/阿维巴坦检测数为142、70和265株;c折点参考欧洲抗菌药物敏感性试验委员会标准(敏感≤2 mg/L,耐药>2 mg/L);d折点参考美国食品和药品监督管理局标准(敏感≤2 mg/L,中敏4 mg/L,耐药>4 mg/L);MIC.最低抑菌浓度;R.耐药;S.敏感
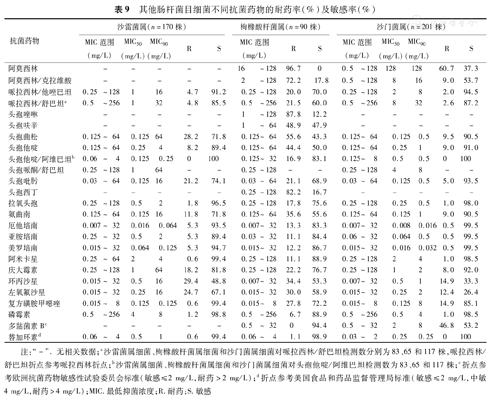
其他肠杆菌目细菌不同抗菌药物的耐药率(%)及敏感率(%)
其他肠杆菌目细菌不同抗菌药物的耐药率(%)及敏感率(%)
| 抗菌药物 | 沙雷菌属(n=170株) | 枸橼酸杆菌属(n=90株) | 沙门菌属(n=201株) | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| MIC范围(mg/L) | MIC50(mg/L) | MIC90(mg/L) | R | S | MIC范围(mg/L) | R | S | MIC范围(mg/L) | MIC50(mg/L) | MIC90(mg/L) | R | S | |
| 阿莫西林 | - | - | - | - | - | 16 ~128 | 96.7 | 0 | 0.5~128 | 128 | 128 | 60.7 | 37.3 |
| 阿莫西林/克拉维酸 | - | - | - | - | - | 2 ~128 | 72.2 | 17.8 | 0.5~128 | 8 | 16 | 9.0 | 53.7 |
| 哌拉西林/他唑巴坦 | 0.25~128 | 1 | 16 | 4.7 | 91.2 | 0.25~128 | 20.0 | 70.0 | 0.25~128 | 2 | 8 | 2.0 | 94.5 |
| 哌拉西林/舒巴坦a | 0.5~256 | 1 | 32 | 4.8 | 85.5 | 0.5~256 | 21.5 | 60.0 | 0.5~256 | 8 | 32 | 2.6 | 87.2 |
| 头孢唑啉 | - | - | - | - | - | 1~128 | 87.8 | 12.2 | - | - | - | - | - |
| 头孢呋辛 | - | - | - | - | - | 1~64 | 48.9 | 47.9 | - | - | - | - | - |
| 头孢曲松 | 0.125~64 | 0.125 | 64 | 28.2 | 71.8 | 0.125~64 | 55.6 | 43.3 | 0.125~64 | 0.125 | 0.5 | 9.5 | 90.5 |
| 头孢他啶 | 0.125~64 | 0.25 | 4 | 8.2 | 89.4 | 0.125~64 | 44.4 | 50.0 | 0.125~64 | 0.25 | 1 | 9.0 | 91.0 |
| 头孢他啶/阿维巴坦b | 0.06~4 | 0.125 | 0.25 | 0 | 100 | 0.125~32 | 16.9 | 83.1 | 0.125~8 | 0.5 | 0.5 | 0 | 100 |
| 头孢哌酮/舒巴坦 | 0.25~128 | 1 | 64 | - | - | 0.25~128 | - | - | 0.25~128 | 4 | 8 | - | - |
| 头孢吡肟 | 0.03~64 | 0.125 | 16 | 21.2 | 74.1 | 0.03~64 | 21.1 | 68.9 | 0.03~64 | 0.125 | 0.5 | 5.0 | 93.5 |
| 头孢西丁 | - | - | - | - | - | 0.25~128 | 82.2 | 16.7 | - | - | - | - | - |
| 拉氧头孢 | 0.25~128 | 0.5 | 2 | 1.8 | 96.5 | 0.25~128 | 17.8 | 75.6 | 0.25~128 | 0.25 | 0.5 | 1.0 | 98.0 |
| 氨曲南 | 0.125~64 | 0.125 | 16 | 11.8 | 71.8 | 0.125~64 | 35.6 | 55.6 | 0.125~64 | 0.125 | 1 | 9.0 | 90.5 |
| 厄他培南 | 0.007~32 | 0.016 | 0.064 | 5.3 | 93.5 | 0.007~32 | 13.3 | 83.3 | 0.007~32 | 0.008 | 0.016 | 0.5 | 99.5 |
| 亚胺培南 | 0.25~32 | 0.5 | 2 | 5.3 | 89.4 | 0.03~32 | 11.1 | 84.4 | 0.06~32 | 0.064 | 0.5 | 0.5 | 99.5 |
| 美罗培南 | 0.015~32 | 0.064 | 0.125 | 5.3 | 94.7 | 0.015~32 | 12.2 | 86.7 | 0.015~32 | 0.016 | 0.032 | 0.5 | 99.5 |
| 阿米卡星 | 0.25~64 | 2 | 4 | 0.6 | 99.4 | 0.25~128 | 11.1 | 88.9 | 0.25~128 | 2 | 4 | 1.0 | 98.5 |
| 庆大霉素 | 0.25~128 | 1 | 64 | 18.2 | 81.8 | 0.25~128 | 22.2 | 76.7 | 0.25~128 | 1 | 2 | 8.0 | 92.0 |
| 环丙沙星 | 0.015~32 | 0.5 | 16 | 29.4 | 48.8 | 0.007~32 | 34.4 | 53.3 | 0.007~32 | 0.5 | 1 | 14.9 | 33.3 |
| 左氧氟沙星 | 0.015~32 | 0.25 | 16 | 24.7 | 67.1 | 0.015~32 | 30.0 | 58.9 | 0.015~32 | 0.25 | 2 | 12.4 | 26.4 |
| 复方磺胺甲噁唑 | 0.015~8 | 0.125 | 0.125 | 0.6 | 99.4 | 0.015~8 | 27.8 | 72.2 | 0.015~8 | 0.125 | 8 | 14.9 | 85.1 |
| 磷霉素 | 0.5~256 | 4 | 8 | 1.2 | 98.8 | 0.5~256 | 6.7 | 88.9 | 0.5~256 | 0.5 | 4 | 1.0 | 98.5 |
| 多黏菌素Bc | - | - | - | - | - | 0.5~32 | 0 | 94.4 | 0.5~32 | 2 | 8 | 46.8 | 53.2 |
| 替加环素d | 0.06~4 | 0.5 | 1 | 0.6 | 99.4 | 0.06~4 | 1.1 | 98.9 | 0.03~2 | 0.25 | 0.25 | 0 | 100 |
注:"-".无相关数据;a沙雷菌属细菌、枸橼酸杆菌属细菌和沙门菌属细菌对哌拉西林/舒巴坦检测数分别为83、65和117株,哌拉西林/舒巴坦折点参考哌拉西林折点;b沙雷菌属细菌、枸橼酸杆菌属细菌和沙门菌属细菌对头孢他啶/阿维巴坦检测数为83、65和117株;c折点参考欧洲抗菌药物敏感性试验委员会标准(敏感≤2 mg/L,耐药>2 mg/L);d折点参考美国食品和药品监督管理局标准(敏感≤2 mg/L,中敏4 mg/L,耐药>4 mg/L);MIC.最低抑菌浓度;R.耐药;S.敏感
501株鲍曼不动杆菌中,耐碳青霉烯鲍曼不动杆菌菌株占62.5%(313/501)。鲍曼不动杆除对多黏菌素B和替加环素耐药率<10%,对哌拉西林/舒巴坦、阿米卡星的耐药率分别为44.2%和49.9%外,对其他抗菌药物耐药率均在50%以上。耐碳青霉烯鲍曼不动杆菌仅显示对多黏菌素B和替加环素具有较好的敏感性(表10)。
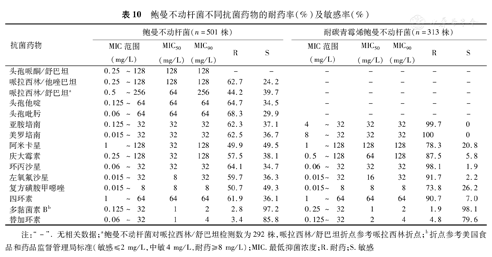
鲍曼不动杆菌不同抗菌药物的耐药率(%)及敏感率(%)
鲍曼不动杆菌不同抗菌药物的耐药率(%)及敏感率(%)
| 抗菌药物 | 鲍曼不动杆菌(n=501株) | 耐碳青霉烯鲍曼不动杆菌(n=313株) | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| MIC范围(mg/L) | MIC50(mg/L) | MIC90(mg/L) | R | S | MIC范围(mg/L) | MIC50(mg/L) | MIC90(mg/L) | R | S | |
| 头孢哌酮/舒巴坦 | 0.25~128 | 128 | 128 | - | - | - | - | - | - | - |
| 哌拉西林/他唑巴坦 | 0.25~128 | 128 | 128 | 62.7 | 24.2 | - | - | - | - | - |
| 哌拉西林/舒巴坦a | 0.5~256 | 64 | 256 | 44.2 | 39.7 | - | - | - | - | - |
| 头孢他啶 | 0.125~64 | 64 | 64 | 64.7 | 34.5 | - | - | - | - | - |
| 头孢吡肟 | 0.06~64 | 64 | 64 | 68.3 | 29.9 | - | - | - | - | - |
| 亚胺培南 | 0.125~32 | 32 | 32 | 62.3 | 37.1 | 4~32 | 32 | 32 | 99.7 | 0 |
| 美罗培南 | 0.015~32 | 32 | 32 | 62.5 | 36.7 | 8~32 | 32 | 32 | 100 | 0 |
| 阿米卡星 | 1~128 | 32 | 128 | 49.9 | 49.5 | 1~128 | 128 | 128 | 78.3 | 20.8 |
| 庆大霉素 | 0.25~128 | 32 | 128 | 57.5 | 38.1 | 0.5~128 | 64 | 128 | 87.5 | 5.8 |
| 环丙沙星 | 0.06~32 | 32 | 32 | 64.1 | 34.7 | 0.06~32 | 32 | 32 | 98.1 | 1.9 |
| 左氧氟沙星 | 0.015~32 | 8 | 32 | 59.7 | 36.3 | 0.015~32 | 16 | 32 | 91.7 | 2.2 |
| 复方磺胺甲噁唑 | 0.015~8 | 8 | 8 | 50.7 | 49.3 | 0.015~8 | 8 | 8 | 73.8 | 26.2 |
| 四环素 | 1~64 | 64 | 64 | 61.9 | 36.1 | 1~64 | 64 | 64 | 90.7 | 7.0 |
| 多黏菌素Bb | 0.125~32 | 1 | 2 | 2.8 | 97.2 | 0.25~32 | 1 | 2 | 1.9 | 98.1 |
| 替加环素 | 0.06~32 | 1 | 4 | 3.4 | 85.8 | 0.125~32 | 2 | 4 | 4.8 | 79.6 |
注:"-".无相关数据;a鲍曼不动杆菌对哌拉西林/舒巴坦检测数为292株,哌拉西林/舒巴坦折点参考哌拉西林折点;b折点参考美国食品和药品监督管理局标准(敏感≤2 mg/L,中敏4 mg/L,耐药≥8 mg/L);MIC.最低抑菌浓度;R.耐药;S.敏感
546株铜绿假单胞菌仅对氟喹诺酮类耐药率均超过20%,对其他抗菌药物的耐药率均在20%以下。对哌拉西林/他唑巴坦的耐药率为12.5% ,对头孢他啶/阿维巴坦的耐药率为2.8%;铜绿假单胞菌对美罗培南(79.5%)和亚胺培南(61.5%)的耐药率接近,但对前者的敏感性高于后者。耐碳青霉烯类铜绿假单胞菌的检出率为18.9%(103/546),阿米卡星和多黏菌素B对耐碳青霉烯铜绿假单胞菌和不耐碳青霉烯铜绿假单胞菌均有较好的体外抗菌活性(表11)。有17.4%(95/546)铜绿假单胞菌对至少3类抗菌药物耐药。
铜绿假单胞菌对不同抗菌药物的耐药率(%)及敏感率(%)
铜绿假单胞菌对不同抗菌药物的耐药率(%)及敏感率(%)
| 抗菌药物 | 铜绿假单胞菌(n=546株) | 耐碳青霉烯铜绿假单胞菌(n=103株) | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| MIC范围(mg/L) | MIC50(mg/L) | MIC90(mg/L) | R | S | MIC范围(mg/L) | MIC50(mg/L) | MIC90(mg/L) | R | S | |
| 头孢哌酮/舒巴坦 | 0.25~128 | 4 | 64 | - | - | - | - | - | - | - |
| 哌拉西林/他唑巴坦 | 0.25~128 | 2 | 128 | 12.5 | 84.1 | - | - | - | - | - |
| 哌拉西林/舒巴坦a | 0.5~256 | 4 | 64 | 8.6 | 84.5 | - | - | - | - | - |
| 头孢他啶 | 0.125~64 | 2 | 32 | 12.1 | 84.2 | - | - | - | - | - |
| 头孢他啶/阿维巴坦 | 2~64 | 4 | 8 | 2.8 | 97.2 | 2~64 | 4 | 16 | 11.6 | 88.4 |
| 头孢吡肟b | 0.125~64 | 1 | 16 | 8.8 | 87.5 | - | - | - | - | - |
| 氨曲南 | 0.125~64 | 4 | 64 | 16.3 | 75.1 | - | - | - | - | - |
| 亚胺培南 | 0.125~32 | 2 | 32 | 18.9 | 61.5 | 8~32 | 32 | 32 | 100 | 0 |
| 美罗培南 | 0.06~32 | 0.5 | 32 | 16.5 | 79.5 | 0.5~32 | 32 | 32 | 87.4 | 5.8 |
| 阿米卡星 | 0.25~128 | 1 | 4 | 0.9 | 98.7 | 1~128 | 2 | 8 | 3.9 | 95.1 |
| 庆大霉素 | 0.25~128 | 2 | 8 | 4.4 | 89.0 | 0.5~128 | 4 | 16 | 13.6 | 68.0 |
| 环丙沙星 | 0.125~32 | 0.5 | 16 | 24.2 | 66.8 | 0.125~32 | 16 | 32 | 73.8 | 20.4 |
| 左氧氟沙星 | 0.5~128 | 1 | 16 | 22.0 | 64.3 | 0.5~128 | 16 | 32 | 70.9 | 18.4 |
| 磷霉素 | 0.5~256 | 32 | 128 | 6.0 | 89.0 | 8~256 | 64 | 256 | 32.0 | 56.3 |
| 多黏菌素B | 0.03~4 | 2 | 2 | 0 | 94.3 | 0.5~2 | 1 | 2 | 0 | 100 |
注:"-".无相关数据;a铜绿假单胞菌对哌拉西林/舒巴坦检测数为362株,哌拉西林/舒巴坦折点参考哌拉西林折点;b折点参考美国临床和实验室标准化研究所标准(敏感≤8 mg/L,中敏16 mg/L,耐药≥32 mg/L);MIC.最低抑菌浓度;R.耐药;S.敏感
107株嗜麦芽窄食单胞菌对头孢他啶和左氧氟沙星的耐药率均低于10%,但对复方磺胺甲噁唑的耐药率为29.9%(表12)。
107株嗜麦芽寡养单胞菌对不同抗菌药物的耐药率(%)及敏感率(%)
107株嗜麦芽寡养单胞菌对不同抗菌药物的耐药率(%)及敏感率(%)
| 抗菌药物 | 嗜麦芽寡养单胞菌 | ||||
|---|---|---|---|---|---|
| MIC范围(mg/L) | MIC50(mg/L) | MIC90(mg/L) | R | S | |
| 头孢哌酮/舒巴坦 | 0.25~64 | 2 | 8 | - | - |
| 头孢他啶 | 1~64 | 4 | 16 | 6.5 | 82.2 |
| 左氧氟沙星 | 0.06~64 | 0.5 | 2 | 6.5 | 90.7 |
| 复方磺胺甲噁唑 | 0.015~16 | 0.25 | 4 | 29.9 | 70.1 |
注:"-".无相关数据;MIC.最低抑菌浓度;R.耐药;S.敏感
77株伯克霍尔德菌属细菌以洋葱伯克霍尔德菌为主(97.5%),对头孢他啶和复方磺胺甲噁唑的敏感率均在75%以上,对其他抗菌药物的敏感率均较低(表13)。
77株伯克霍尔德菌属对不同抗菌药物的耐药率(%)及敏感率(%)
77株伯克霍尔德菌属对不同抗菌药物的耐药率(%)及敏感率(%)
| 抗菌药物 | 伯克霍尔德菌属 | ||||||
|---|---|---|---|---|---|---|---|
| MIC范围(mg/L) | MIC50(mg/L) | MIC90(mg/L) | R | S | |||
| 头孢哌酮/舒巴坦 | 8~128 | 64 | 128 | - | - | ||
| 头孢他啶 | 1~64 | 8 | 32 | 11 | 75.3 | ||
| 美罗培南 | 0.5~64 | 8 | 16 | 16.9 | 15.6 | ||
| 左氧氟沙星 | 0.5~64 | 2 | 32 | 36.4 | 51.9 | ||
| 复方磺胺甲噁唑 | 0.125~8 | 0.25 | 4 | 11.7 | 88.3 | ||
注:"-".无相关数据;MIC.最低抑菌浓度;R.耐药;S.敏感
2018年1月至2019年12月来源于全国18个省市区的50家BRICS成员单位共获得14 778株血流感染病原菌,其中革兰阴性菌所占比例超过72.1%,与BRICS 2014至2017年监测数据相比进一步增加,其中肺炎克雷伯菌增加较为明显(从11.9%增加到17.0%),与泰国的大型血流感染调查结果相类似[8],与欧美国家血流感染病原菌的构成有一定的差异[9]。美国和欧洲革兰阳性菌在血流感染病原菌中分别占50.1%和40.6%,同时,在欧美国家凝固酶阴性葡萄球菌所占比例低于10%[9]。SENTRY监测结果表明,在过去的20年里,大肠埃希菌引起的血流感染比金黄色葡萄球菌更加突出[10],这一变化趋势可能与碳青霉烯类耐药菌株增加有关。
金黄色葡萄球菌是引起血流感染的主要革兰阳性菌[11]。2018至2019年的监测结果与前两期结果相比,MRSA在金黄色葡萄球菌中的分离率(2014至2015年度为33.9%,2016至2017年度为34.2%)呈逐渐下降趋势[12,13],接近欧洲的分离率(25.6%),而低于北美国家(45.6%)[14]。在美国,2005至2016年期间MRSA引起的血流感染也呈下降趋势[15]。MRSA通常对不同种类的抗生素具有多重耐药性,仅对糖肽类、达托霉素和利奈唑胺高度敏感;本监测发现葡萄球菌(包括MRSA)对利福平、复方磺胺甲噁唑和阿米卡星敏感性均在90%左右,同时发现9.2%的金黄色葡萄球菌对青霉素敏感。这种变化趋势与国内近年来MRSA分子型别的变化一致,但导致这种分子演变的原因尚不清楚,考虑与加强院内MRSA防控措施有关,如手消毒液的广泛应用等。凝固酶阴性葡萄球菌为常见血培养的污染菌,但其亦可引起导管相关性血流感染和感染性心内膜炎,通过严格质量控制,BRICS分离凝固酶阴性葡萄球菌占比均低于10%,与其他监测结果不同[16]。MRCNS保持较高的流行率。
本研究中,肠球菌属以屎肠球菌为主,耐药性也明显较粪肠球菌突出,耐万古霉素肠球菌的分离率较低,且均为屎肠球菌,这种现象在既往监测中已有发现,值得关注。链球菌对大环内酯类和克林霉素耐药仍然是我国的突出问题,近90%肺炎链球菌对大环内酯(红霉素)和克拉霉素具有耐药性;本研究发现31.7%的β-溶血链球菌对左氧氟沙星耐药,其主要菌种为无乳链球菌。Hirai等[17]对日本侵袭性感染的无乳链球菌研究发现,对左氧氟沙星耐药的无乳链球菌主要是血清Ib型,同时存在耐药基因gyrA和parC的突变。尽管按非脑膜炎青霉素折点,肺炎链球菌对青霉素耐药率未发现明显增加,但根据BRICS连续的监测发现,肺炎链球菌对脑膜炎折点判断的青霉素耐药率呈上升趋势(从42.9%上升至77.3%),这需要加以关注,是否存在逐渐发生的敏感性降低值得研究,临床用药需要注意。
近10年来,我国耐碳青霉烯类肠杆菌目细菌日益成为临床威胁。2014至2019年BRICS监测结果显示,CRKP从7.2%上升至20.6%,虽然替加环素和多黏菌素B均具有较高的敏感性,但临床用药方法与治疗效果尚未确立。值得庆幸的是,CRE监测期间(2014至2019年)发生率均处于较低水平(低于2%)。新药头孢他啶/阿维巴坦对碳青霉烯类耐药肠杆菌具有较强的抗菌活性,但CRE则仅有40%的菌株敏感,对其他肠杆菌目细菌抗菌活性也不尽人意,这与我国不同类别肠杆菌目细菌对碳青霉烯类耐药机制存在差异有关,CRKP主要耐药机制为产肺炎克雷伯菌耐碳青霉烯酶(KPC型碳青霉烯酶),而CRE则以新德里金属-β-内酰胺酶为主,临床用药中需加以关注。BRICS连续监测结果发现,产ESBLs的大肠埃希菌和肺炎克雷伯菌呈小幅度下降趋势。哌拉西林/他唑巴坦和哌拉西林/舒巴坦(2∶1)对肠杆菌目细菌和铜绿假单胞菌具有相似抗菌活性。
连续BRICS研究显示,鲍曼不动杆菌对碳青霉烯类耐药长期处于极高水平,并未出现下降趋势,这类细菌还对β-内酰胺类、氨基糖苷类和氟喹诺酮类均有超过50%的耐药率,仅多黏菌素B和替加环素具有较好的抗菌活性,但本研究中已有2.8%和3.4%的鲍曼不动杆菌对多黏菌素B和替加环素产生耐药。在国外也有报道,临床分离的鲍曼不动杆菌中存在多黏菌素耐药[18]。耐碳青霉烯铜绿假单胞菌呈缓慢上升趋势,2014至2015年亚胺培南耐药为10.4%,2018至2019年为18.9%,这类细菌除对头孢他啶/阿维巴坦、阿米卡星和多黏菌素敏感性高于88%外,对其他抗菌药物耐药率均较高。
监测还发现,阿米卡星、磷霉素、替加环素、多黏菌素B和利福平等对各自目标细菌具有较高敏感性,但这些药物长期缺乏临床研究,有关药物使用方法和适应症等都没有具体证据,有必要开展相关临床研究,为耐药菌感染治疗提供新的路径。
综上所述,血流感染病原体以革兰阴性菌为主,并呈不断上升态势,其中肺炎克雷伯菌所占比例上升较为突出;细菌整体耐药性也呈现为革兰阴性菌耐药不断恶化,革兰阳性球菌耐药有缓解趋势,MRSA检出率已经低于30%,且对多种药物敏感;CRKP检出率快速上升,耐碳青霉烯类鲍曼不动杆菌检出率维持高位水平,碳青霉烯类铜绿假单胞菌检出率也成缓慢上升趋势。个别药物体外敏感率较高,需要临床研究确定其治疗价值。
所有作者均声明不存在利益冲突



























