
评估奥马环素治疗肺部感染患者的疗效和安全性。
回顾性分析2021年12月至2022年5月浙江大学医学院附属第一医院、杭州红十字会医院和建德市第一人民医院收治的58例肺部感染患者的临床资料,根据用药情况分为奥马环素治疗组(n=29)和美罗培南联合利奈唑胺治疗组(联合治疗组,n=29),奥马环素治疗组采用静脉注射奥马环素200 mg或100 mg,1次/d,联合治疗组静脉注射美罗培南(1 000 mg/次,3次/d)和利奈唑胺(600 mg/次,2次/d);观察2组患者的临床疗效和药物相关不良反应。采用SPSS 22.0统计软件对数据进行处理。
奥马环素组治愈、好转、恶化例数分别为8例(27.6%,8/29)、19例(65.5%,19/29)和2例(6.9%,2/29),联合治疗组治愈1例(3.4%,1/29),好转26例(89.7%,26/29),死亡2例(6.9%,2/29),奥马环素组的临床疗效优于联合治疗组(χ2=6.533,P=0.038)。奥马环素组3例(10.3%,3/29)发生呼吸衰竭,联合治疗组5例(17.2%,5/29)发生呼吸衰竭,2组差异无统计学意义(χ2=0.580,P=0.446)。在治愈或好转的患者中,奥马环素组从治疗开始到疾病缓解的中位时间为3.0(2.0,5.5) d;联合治疗组疾病缓解的中位时间为5.0(4.0,6.0) d。奥马环素组相较于联合治疗组,从治疗开始到疾病缓解的时间间隔更短(Z=-2.122,P=0.034)。两组不良反应发生率差异无统计学意义[6.9%(2/29)比13.8%(4/29), χ2=0.744,P=0.389]。
奥马环素治疗肺部感染患者疗效好,安全性佳,可优先用于治疗肺部感染。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
肺部感染是一种常见的呼吸系统疾病,抗菌药物不合理使用以及耐药菌株增加等因素使得肺部感染的发生率以及病死率正逐年升高[1,2]。肺部感染患者常用的治疗方式包括支持治疗、物理治疗,以及联合抗感染治疗等[3]。目前指南推荐使用以多西环素和米诺环素为代表的二代四环素类药物联合或不联合头孢菌素、β-内酰胺类药物等方案用于肺部感染患者的抗感染治疗[4,5]。但由于细菌的外排泵蛋白可将四环素泵出胞外,以及细胞质中存在核糖体保护蛋白使细菌免受四环素影响等机制,第二代四环素类药物的耐药情况日益严峻[6],例如肺炎克雷伯菌对四环素类药物的耐药率高达60%[7,8]。因此急须寻找新的、有效的抗菌药物用于肺部感染患者的治疗。奥马环素作为第三代四环素类药物,其D环上C9位置由氨甲基环素取代,可克服核糖体保护的耐药机制,且具有抗菌谱广、组织分布广、血药浓度高等优势[9,10,11,12,13]。多项研究已表明奥马环素在治疗各类感染患者中的有效性和安全性[13,14,15],但在肺部感染患者中的应用报道尚少。本研究旨在评估奥马环素治疗肺部感染患者的疗效和安全性。
收集2021年12月2日至2022年5月21日浙江大学医学院附属第一医院、杭州红十字会医院和建德市第一人民医院收治的58例肺部感染患者的临床资料,并进行回顾性分析。肺部感染的诊断标准参照《医院感染诊断标准(试行)》[16],其中29例接受奥马环素治疗(奥马环素组),29例接受美罗培南联合利奈唑胺治疗(联合治疗组),奥马环素组年龄43~91岁,平均(66.0±12.6)岁,其中男性23例,女性6例;联合治疗组年龄41~90岁,平均(69.1±12.5)岁,其中男性21例,女性8例,两组患者性别和年龄差异均无统计学意义(t=-0.941,χ2=0.377,P=0.351和0.539)。
入选标准:(1)年龄≥18周岁;(2)肺部感染严重程度[17]为Ⅰ~Ⅴ级患者,依据肺炎严重指数(Pneumonia severity index,PSI)将肺炎分为Ⅰ、Ⅱ、Ⅲ、Ⅳ和Ⅴ级。Ⅰ级为年龄<50岁,无伴随疾病,无生命体征异常;Ⅱ级为PSI ≤70;Ⅲ级为PSI 71~90;Ⅳ级为PSI 91~130;Ⅴ级为PSI>130;(3)在治疗期间育龄期妇女采取了充分避孕措施。排除标准:(1)有严重的肝肾功能不全,严重败血症或感染性休克;(2)在入组前30 d内参加过其他临床试验。该研究符合《赫尔辛基宣言》要求。
奥马环素组中,24例首日静脉注射奥马环素(浙江海正药业股份有限公司)200 mg,1次/d,之后100 mg,1次/d;4例静脉注射100 mg,1次/d;1例静脉注射200 mg,1次/d;疗程1~21 d,平均疗程为(7.2±4.2) d。联合治疗组中美罗培南(海口市制药厂有限公司)静脉注射1 000 mg/次,3次/d,利奈唑胺( Fresenius Kabi Norge As)静脉注射600 mg,2次/d;疗程3~16 d,平均疗程为(7.5±3.3) d。
患者于治疗结束(疗程<14 d)或启动治疗后的第14天(疗程>14 d)进行疗效评估[17],分为:(1)治愈:治疗前存在的临床症状和体征消失,无需进一步进行抗菌治疗;(2)好转:部分临床症状和体征消失,需继续抗菌治疗;(3)恶化:对当前治疗无应答,有加重或新发临床体征和症状,需改变抗菌药物治疗;(4)死亡:患者于治疗期间死亡。临床体征和症状包括发热、咳嗽、咳痰、胸膜炎性胸痛、呼吸困难等。同时,观察是否发生呼吸衰竭。呼吸衰竭定义为吸入空气状态下,动脉血气分析示PaO2≤60 mmHg(1 mmHg=0.133 kPa)或SpO2≤0.90,伴或不伴PaCO2≥50 mmHg,在应用常规氧疗(鼻导管、简单面罩、非重复呼吸面罩、文丘里面罩)后,100 mmHg≤氧合指数(PaO2/FiO2)<300 mmHg[18]。在治愈或好转的患者中,收集从治疗开始到疾病缓解(治愈或好转)的时间间隔。此外,观察药物治疗后的不良反应,并且由研究者评估这些不良反应是否与治疗药物相关。
采用SPSS 22.0统计软件对数据进行处理。正态分布的计量资料采用 ±s表示,采用t检验。偏态分布的计量资料采用中位数(M)和上下四分位数(Q1,Q3)表示,采用Wilcoxon秩和检验。计数资料以例(百分数)表示,采用χ2检验,以P<0.05为差异具有统计学意义。本研究中疗效和安全性均基于意向治疗(ITT)分析集分析。
±s表示,采用t检验。偏态分布的计量资料采用中位数(M)和上下四分位数(Q1,Q3)表示,采用Wilcoxon秩和检验。计数资料以例(百分数)表示,采用χ2检验,以P<0.05为差异具有统计学意义。本研究中疗效和安全性均基于意向治疗(ITT)分析集分析。
奥马环素组有2例(6.9%,2/29)重症肺炎,联合治疗组无重症肺炎,两组患者在合并疾病、肺炎类型,以及肺炎严重程度上差异均无统计学意义(P>0.05)。
奥马环素组29例患者中,治愈、好转、恶化例数分别为8例(27.6%)、19例(65.5%)和2例(6.9%)。联合治疗组29例患者治愈1例(3.4%),好转26例(89.7%),死亡2例(6.9%),2组疗效差异有统计学意义(χ2=6.533,P=0.038)。奥马环素组共3例(10.3%)患者发生呼吸衰竭,联合治疗组5例(17.2%)发生呼吸衰竭,2组患者发生呼吸衰竭的比例差异无统计学意义(χ2=0.580,P=0.446)。
奥马环素组27例患者从治疗开始到疾病缓解的中位时间为3.0(2.0,5.5) d;联合治疗组27例患者疾病缓解的中位时间为5.0(4.0,6.0) d。2组患者疾病缓解的中位时间差异具有统计学意义(Z=-2.122,P=0.034)。
奥马环素组2例(6.9%,2/29)发生不良反应,其中恶心呕吐和高血压各1例(3.4%);联合治疗组4例(13.8%,4/29)发生不良反应,其中出现恶心呕吐、血小板减少、贫血和皮疹各1例(3.4%)(表2)。两组患者总体药物相关不良反应发生率差异无统计学意义(χ2=0.744,P=0.389)。
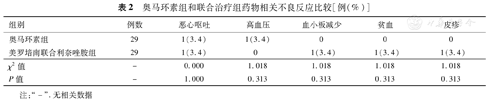
奥马环素组和联合治疗组药物相关不良反应比较[例(%)]
奥马环素组和联合治疗组药物相关不良反应比较[例(%)]
| 组别 | 例数 | 恶心呕吐 | 高血压 | 血小板减少 | 贫血 | 皮疹 |
|---|---|---|---|---|---|---|
| 奥马环素组 | 29 | 1(3.4) | 1(3.4) | 0 | 0 | 0 |
| 美罗培南联合利奈唑胺组 | 29 | 1(3.4) | 0 | 1(3.4) | 1(3.4) | 1(3.4) |
| χ2值 | - | 0.000 | 1.018 | 1.018 | 1.018 | 1.018 |
| P值 | - | 1.000 | 0.313 | 0.313 | 0.313 | 0.313 |
注:"-".无相关数据
肺部感染是临床上常见的感染性疾病之一,其感染的病因较为复杂,包括细菌、病毒、真菌,以及其他病原体等,因此在肺部感染患者的经验性治疗过程中,使用广谱抗菌药物是有必要的[19,20]。临床常用的抗感染药物包括四环素类(多西环素等)、碳青霉烯类(美罗培南等)、噁唑烷酮类(利奈唑胺等)和大环内酯类(阿奇霉素等)等[4,5]。对于传统的二代四环素类抗生素,例如多西环素和米诺环素等,尽管用于治疗肺部感染具有良好的抗菌效果,但由于四环素类药物的广泛使用,耐药率逐年升高[6,7,8]。美罗培南尽管也有广谱抗菌作用,但耐甲氧西林金黄色葡萄球菌对其不敏感;利奈唑胺则不能覆盖革兰阴性菌。因此寻找新的抗菌药物用于肺部感染的治疗是有必要且紧迫的。
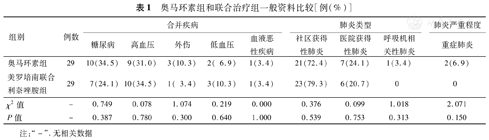
奥马环素组和联合治疗组一般资料比较[例(%)]
奥马环素组和联合治疗组一般资料比较[例(%)]
| 组别 | 例数 | 合并疾病 | 肺炎类型 | 肺炎严重程度 | ||||||
|---|---|---|---|---|---|---|---|---|---|---|
| 糖尿病 | 高血压 | 外伤 | 低血压 | 血液恶性疾病 | 社区获得性肺炎 | 医院获得性肺炎 | 呼吸机相关性肺炎 | 重症肺炎 | ||
| 奥马环素组 | 29 | 10(34.5) | 9(31.0) | 3(10.3) | 2( 6.9) | 1(3.4) | 21(72.4) | 7(24.1) | 1(3.4) | 2(6.9) |
| 美罗培南联合利奈唑胺组 | 29 | 7(24.1) | 10(34.5) | 1( 3.4) | 3(10.3) | 1(3.4) | 23(79.3) | 6(20.7) | 0 | 0 |
| χ2值 | - | 0.749 | 0.078 | 1.074 | 0.219 | 0.000 | 0.376 | 0.099 | 1.018 | 2.071 |
| P值 | - | 0.387 | 0.780 | 0.300 | 0.640 | 1.000 | 0.539 | 0.753 | 0.313 | 0.150 |
注:"-".无相关数据
奥马环素是在米诺环素结构的基础上,对于C9位的氨甲基进行修饰,得到9-烷基氨基甲基二甲胺四环素类似物。奥马环素克服耐药的机制主要包括以下两点:(1)对于C9位置修饰,克服核糖体保护的耐药机制,从而克服耐药;(2)C7位置修饰提高电子基团(二甲氨基)的活性,克服细菌外排的耐药机制,从而克服细菌耐药[9,10,11,12,13]。因此,奥马环素对于常见的革兰阳性菌和阴性菌均具有较好的抗菌活性。前期临床研究也显示奥马环素具有良好的疗效和安全性[13,14,15],然而其应用于治疗肺部感染患者的研究目前仍然少见。
在以往临床研究中,美罗培南联合利奈唑胺作为经验性治疗耐甲氧西林金黄色葡萄球菌肺部感染的常用方案,已经显示了较好的疗效[20,21],因此本研究选取了美罗培南联合利奈唑胺作为对照组。研究结果显示,奥马环素组的整体疗效优于联合治疗组(χ2=6.533,P=0.038),进一步验证了奥马环素在治疗肺部感染患者中具有良好疗效。但由于样本量较少,因此该结果尚需更大样本量研究验证。另外研究结果也显示奥马环素组仅3例(10.3%)患者发生呼吸衰竭,在治愈以及好转的病例中,从治疗开始到疾病缓解的中位时间为3.0(2.0,5.5) d,表明经奥马环素治疗的肺部感染患者进展为重症患者的风险较低,同时也表明奥马环素起效迅速。此外,本研究需要注意的是:对于疗程<14 d的患者,选择治疗结束作为疗效评估时间点;对于疗程>14 d的患者,选择14 d作为疗效评估时间点。临床上,奥马环素治疗后一般14 d可观察到疗效,因此在进行研究设计时选择14 d作为疗效评估时间点,这样的研究设计也与其他奥玛环素的临床试验相同[22,23]。
既往研究发现,奥马环素治疗其他部位感染患者的常见不良反应包括胃肠道反应、肝肾功能异常和注射部位反应等[13,24]。本研究发现,奥马环素治疗肺部感染患者的整体不良反应与美罗培南联合利奈唑胺组无统计学差异,提示了奥马环素治疗肺部感染患者的安全性良好,但仍需要更大样本量的研究来评估奥马环素治疗肺部感染患者的整体安全性。
尽管本研究是对比奥马环素和美罗培南联合利奈唑胺治疗的多中心研究,但仍然存在一些不足之处:(1)样本量较小,导致统计效能较低;(2)本研究为一项真实世界队列研究,因此患者的基线信息存在一定偏倚,未来需要开展随机对照临床试验来消除这些偏倚,并进一步验证该结果;(3)本研究纳入患者的平均年龄>60岁,因此奥马环素在年轻患者中的疗效仍然需要进一步探索;(4)本研究系回顾性研究,患者的筛选可能存在一定偏倚。
综上所述,奥马环素治疗肺部感染患者疗效好,安全性佳,可作为肺部感染患者的治疗方案。
史海燕,胡英,黄建荣,等.奥马环素对比美罗培南联合利奈唑胺治疗肺部感染:一项真实世界队列研究[J].中华临床感染病杂志,2023,16(3):210-214.DOI:10.3760/cma.j.issn.1674-2397.2023.03.008.
杭州红十字会医院和建德市第一人民医院在病例资料收集中给予了大量帮助,在此表示感谢
所有作者均声明不存在利益冲突



























