
版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
患儿,男,14岁,因"乏力、食欲减退半月,发现白细胞高2 d"于2015年11月1日入院。患者于半月前无明显诱因出现全身乏力、食欲减退,呈进行性加重,余无不适。2 d前于当地医院查血常规:白细胞计数(WBC)214.11×109/L,中性粒细胞计数(N)2.49×109/L,淋巴细胞计数(L)181.12×109/L,单核细胞计数(M)30.26×109/L,血红蛋白(HGB)67 g/L,血小板(PLT)25×109/L。未治疗。为求进一步诊治以"白细胞升高"收住本科。入院查体:生命体征平稳。神志清楚,精神尚可。发育正常,营养良好。自主体位,查体合作。贫血貌,全身皮肤黏膜无出血,浅表淋巴结无肿大,咽部无充血,胸骨无压痛。心肺腹未见异常。四肢无水肿。辅助检查,血常规:WBC 193.49×109/L,HGB 54 g/L,PLT 38×109/L。外周血细胞形态:原始淋巴60%,幼稚淋巴20%。生化:乳酸脱氢酶1 377 IU/L、钾6.08 mmol/L、磷2.15 mmol/L、尿酸584.0 μmol/L、β2微球蛋白3.07 mg/L。胸苷激酶-1:2.43 pM(参考值<2.00)。骨髓细胞学检查:原淋+幼淋占96.8%,以大细胞为主,提示ALL-L2。流式细胞仪检测结果(图1):异常细胞群占有核细胞95%;CD2、CD3、CD4、CD5、CD7、CD8、CD10、CD38、cCD3、TdT阳性,其中CD3+CD4+CD8+细胞约占63%,提示急性T淋巴细胞白血病。融合基因均阴性。胸片、心电图、腹部彩超未见明显异常。诊断为"急性T淋巴细胞白血病CD4+/CD8+双阳性BCR/ABL(-)"。入院后予VDLP4周方案诱导缓解治疗,辅以止吐、保肝、水化、碱化、利尿、间断成分输血等对症支持治疗。化疗2周后复查骨穿:淋巴细胞增生受抑,形态正常,提示ALL-CR。化疗期间间断行腰椎穿刺及鞘注治疗。化疗结束后复查血常规:WBC 2×109/L,Neu 1.72×109/L,HGB 67 g/L,PLT 109×109/L,病情稳定后回家休养。此后患者于本科持续治疗,分别给予CAM方案2疗程、大剂量甲氨蝶呤+6MP方案强化4疗程、VDLDex方案、CAM方案、VDLDex方案、CAM方案、EA方案、COADex方案、VDLDex方案、大剂量甲氨蝶呤各1疗程联合化疗共2年余。治疗期间骨髓持续缓解。末次随访时间为2018年5月10日。因经济原因未行骨髓移植术。现患者仍在后续治疗随访中。
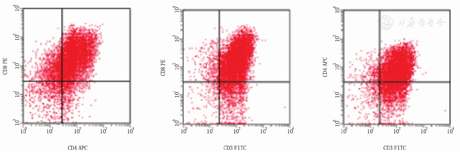

急性淋巴细胞白血病的免疫表型通常为CD4+/CD8-,其他免疫表型如CD4-/CD8+、CD4+/CD8+、CD4-/CD8-均较少见[1]。
T细胞分化、发育过程T淋巴细胞(T lymphocyte)简称T细胞,是淋巴细胞中数量最多、功能最复杂的一类,主要参与适应性免疫反应。T细胞的分化、发育是一个复杂的过程。由多能造血干细胞转变为前胸腺淋巴细胞(Pre-T)迁移至胸腺,在胸腺素的诱导下,经历两个阶段后逐渐发育为识别各种抗原的成熟T细胞。第一阶段为早期T细胞发育阶段,即Pre-T细胞从皮质外层逐渐进入皮质深层,发育为CD4-/CD8-双阴性T细胞(double negative cell,DN),进一步分化为CD4+/CD8+双阳性T细胞(double positive cell,DP);第二阶段为DP T细胞在胸腺中经历阳性选择和阴性选择,否则会发生细胞程序性凋亡。主要组织相容性复合体(major histocompatibility complex,MHC)抗原在这两种选择中起着关键的作用。阳性选择过程中,MHC-Ⅰ类分子选择性结合CD8受体,而使同一双阳性细胞表面CD4受体减少,发育为CD8+/CD4-T细胞;同理,MHC-Ⅱ类分子选择性结合CD4受体,发育为CD8-/CD4+ T细胞。经阳性选择后的T细胞还必须经过阴性选择过程,才能成为成熟的、具有识别外来抗原的T细胞。位于皮质与髓质交界处的树突状细胞(dendritic cells,DC)和巨噬细胞表达高水平的MHC-Ⅰ类抗原和MHC-Ⅱ类抗原,自身抗体成分与其形成复合物。经过阳性选择后的胸腺细胞如能识别DC或巨噬细胞表面自身抗原与MHC抗原复合物,即发生自身耐受而停止发育,而不发生结合的胸腺细胞才能继续发育为CD4+/CD8-或CD4-/CD8+单阳性T细胞(single positive cell,SP),离开胸腺迁移至外周血液[2]。
CD4+/CD8+DP T细胞。多数外周T淋巴细胞免疫表型为CD4+或CD8+单阳性,CD4+/CD8+DP T细胞占人体循环T淋巴细胞1%~2%[3],且可能与自身免疫性疾病及恶性皮肤病有关,如HIV、肝炎、黑色素瘤、乳腺癌、类风湿性关节炎和Chagas巨食管病等。CD4+/CD8+DP T细胞与白血病相关的报道相对较少[4,5,6]。
CD4+/CD8+DP T细胞在胸腺内是T细胞的发育阶段,其表型和功能是有缺陷的,分化发育为CD4+或CD8+SP T细胞后是相对稳定的。外周成熟CD4+/CD8+DP T细胞可在不同物种的外周组织中检测到,最早在猪胸腺外发现[7]。其后在小鼠、豚鼠、人类等物种中都发现。
目前对于CD4+/CD8+DP T细胞的来源尚不统一。一方面,Mucida等[8]支持CD4+/CD8+DP T细胞起源于CD4+/CD8-SP T细胞的假设。CD4和CD8的表达由转录因子严格调控,主要涉及Runx3和ThPOK,从而成熟外周T细胞只表达CD4或CD8[9]。Mucida等[8]认为成熟CD4+/CD8-SP T细胞的结局是不稳定的,CD8a在ThPOK下调后出现再表达。实验结果发现ThPOK-GFP小鼠小肠中发现CD8+T细胞表达GFP-,同时CD4+T细胞也表达GFP-,证实ThPOK表达缺乏。换言之,CD8+的再表达是ThPOK缺失的结果,这种下调表达由ThPOK基因位点上游的沉默子激活引起。CD4+T细胞中GFP表达的缺失与CD8+的重新表达相关,从而将表型转化为CD4+/CD8+DP T细胞。另一项研究也认为CD8a的表达是Runx3上调和ThPOK下调的结果[10]。综上,这些研究一致认为小肠成熟CD4+/CD8+DP T细胞来源于CD4+T细胞。但需注意,这两项研究均为肠道环境,CD4+/CD8+DP T细胞的来源是否会受到组织位置的影响目前尚不清楚。再者,Reimann与Rudolphi[11]将CD4+T细胞转导至SCID小鼠,可在小肠中形成CD4+/CD8+DP T细胞,但肠系膜淋巴结中未发现CD4+/CD8+DP T细胞。另一方面,CD4-/CD8+SP T细胞作为CD4+/CD8+DP T细胞来源的证据也存在[12]。
Overgaard等[13]研究证实CD4+/CD8+T细胞可代表CD4+和CD8+SP T细胞之间的聚集。Clénet等[3]发现CD4+/CD8+T细胞表现出与记忆T细胞相似的特征,包括趋化因子受体的表达(如CCR7、CXCR3、CCR6)和可激活标记物(如CD57、CD95)。与SP T细胞相比,DP T细胞可促进细胞因子(IFN-γ、TNF-α、IL-4、IL-17A)和裂解酶(穿孔素、颗粒酶B)的产生。此外,文献报道Notch1诱导的小鼠T-ALL模型中CD4+/CD8+和CD4-/CD8+T细胞两个亚群的药物敏感性不同,CD4+/CD8+T-ALL对雷帕霉素的治疗较CD4-/CD8+T-ALL敏感,但对环磷酰胺治疗的反应性较差[14]。
Raza等[5]报道1例CD4+/CD8+DP成人急性T细胞白血病/淋巴瘤合并复杂核型及难治性高钙血症中年患者,经强化治疗、自体移植和BEAM治疗后存活2.5年,认为此表型通常为侵袭性病程,预后较差。王建宁等[6]报道1例CD4+/CD8+/NKa+T-大颗粒淋巴细胞白血病老年患者,以乏力、偶有关节疼痛伴腕指关节轻度肿胀7年余就诊,未发现其他肿瘤和自身免疫性疾病如类风湿性关节炎存在的依据,临床进展缓慢。CD4+/CD8+DP T细胞存在异质性,尽管许多疾病与之相关,但其功能仍然存在争议,总的来说,CD4+/CD8+DP T细胞似乎在外周发挥了重要作用,具有细胞毒性作用和免疫抑制作用为一体的矛盾体[8]。
该患儿对治疗敏感,化疗期间骨髓持续缓解,一般状况良好,预后尚可。通过对本例患者的学习,旨在提高对CD4+/CD8+双阳性急性T淋巴细胞白血病的认识。因此,对此疾病的深入研究迫在眉睫,让患者得以及时诊断与治疗。
所有作者均声明不存在利益冲突






























