
中年男性患者。主因“发现血糖升高5年,血糖控制不佳半年”入院。既往有冠心病、陈旧性心肌梗死病史4年,高血压病史4年,有吸烟、饮酒史。入院诊断为2型糖尿病合并视网膜病变,下肢动脉硬化闭塞症,冠状动脉性心脏病,陈旧性心肌梗死,冠状动脉支架植入后状态,心功能Ⅰ级(NYHA分级),高血压3级(很高危),肥胖症,脂肪肝。给予生活方式干预、降糖、降压、调脂、抗血小板聚集、改善循环、营养神经等综合治疗。予二甲双胍缓释片1.0 g(2次/d)、司美格鲁肽0.5 mg(1次/周)、达格列净10 mg(1次/d)联合降糖治疗,空腹血糖控制在6 mmol/L左右,餐后2 h血糖为7~8 mmol/L。3个月后复查糖化血红蛋白6.5%,体重减轻7 kg。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
患者 男,48岁,公司职员。主因“发现血糖升高5年,血糖控制不佳半年”就诊。患者于5年前体检时发现血糖升高,空腹血糖8 mmol/L,无明显“三多一少”症状,于外院诊断为2型糖尿病(type 2 mellitus diabetes,T2DM),给予门冬胰岛素30(具体剂量不详)降糖治疗。2年前因急性心肌梗死于泰达国际心血管病医院住院,行冠状动脉支架植入术。出院后降糖方案为门冬胰岛素30早晚餐前各20 U皮下注射,患者饮食控制不佳,运动量少,半年前出现血糖控制不佳,偶测空腹血糖7~8 mmol/L,餐后2 h血糖18 mmol/L,平素无胸闷、憋气、心悸,无胸痛,为系统诊治收入院。患者自发病以来,饮食、睡眠可,大小便无异常,近期体重无明显变化。
既往有冠心病、陈旧性心肌梗死病史4年,高血压病史4年,血压最高达180/100 mmHg(1 mmHg=0.133 kPa),服用厄贝沙坦氢氯噻嗪降压,血压未监测。吸烟30年,20支/d,未戒烟;饮酒30年,白酒4两/d,未戒酒;否认药物过敏史。否认家族遗传性疾病史。适龄结婚,育1子1女。
体格检查:身高170 cm,体重85 kg,体重指数29.41 kg/m2,腰围106 cm,臀围103 cm,腰臀比1.02,体温36.2 ℃,脉搏84 次/min,呼吸16 次/min,血压130/90 mmHg。发育正常,营养过度。甲状腺未触及肿大,双肺呼吸音清,未闻及干湿性啰音。心音有力,心律齐,心率84 次/min,各瓣膜听诊区未闻及病理性杂音。腹软,肝脾未触及,双肾区无叩击痛,双下肢无水肿,双足背动脉搏动可,四肢肌力Ⅴ级,肌张力正常。病理性反射未引出。
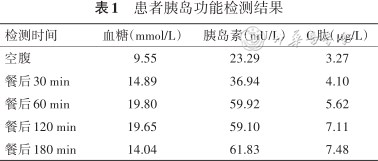
实验室检查:血常规、凝血功能、甲状腺功能未见异常。糖化血红蛋白8.0%,糖尿病三联抗体均阴性。总胆固醇4.10 mmol/L,低密度脂蛋白胆固醇2.27 mmol/L,高密度脂蛋白胆固醇1.45 mmol/L,甘油三酯1.02 mmol/L。γ-谷氨酰转肽酶318.7 U/L,其余肝功能指标未见异常。肌酐43.1 μmol/L,尿素氮4.38 mmol/L,尿酸255.70 μmol/L,估算的肾小球滤过率112.56 ml·min⁻¹·(1.73 m²)⁻¹。尿常规血糖4+,尿蛋白和尿酮体阴性。24 h尿蛋白定量0.07 g/24 h,尿微量白蛋白11.50 mg/24 h。胰岛功能检测结果见表1。
患者胰岛功能检测结果
患者胰岛功能检测结果
| 检测时间 | 血糖(mmol/L) | 胰岛素(mU/L) | C肽(μg/L) |
|---|---|---|---|
| 空腹 | 9.55 | 23.29 | 3.27 |
| 餐后30 min | 14.89 | 36.94 | 4.10 |
| 餐后60 min | 19.80 | 59.92 | 5.62 |
| 餐后120 min | 19.65 | 59.10 | 7.11 |
| 餐后180 min | 14.04 | 61.83 | 7.48 |
辅助检查:眼底镜示左眼中度非增殖性糖尿病视网膜病变。心电图示陈旧性前间壁心肌梗死。超声心动图示左心房、左心室增大,左室顺应性下降,左室射血分数38%。腹部彩色超声多普勒示脂肪肝(轻~中度)。甲状腺超声示双叶弥漫性肿大。双下肢动脉超声示下肢动脉硬化闭塞症(最大狭窄率46%)。
入院诊断:T2DM合并视网膜病变、下肢动脉硬化闭塞症;冠状动脉性心脏病、陈旧性心肌梗死、冠状动脉支架植入后状态、心功能Ⅰ级(NYHA分级);高血压3级(很高危);肥胖症;脂肪肝。
病例特点:中年男性,糖尿病病史5年,体型肥胖,生活作息不规律,不能坚持饮食控制,运动量少,长期大量吸烟、饮酒。血糖控制不达标,糖化血红蛋白8.0%,合并冠心病(陈旧性心肌梗死)、脂肪肝、高血压。
治疗经过:给予生活方式干预、降糖、降压、调脂,抗血小板聚集、改善循环、营养神经等综合治疗。鉴于该患者T2DM合并动脉粥样硬化性心血管疾病(atherosclerotic cardiovascular disease,ASCVD),根据指南建议,合并ASCVD的T2DM患者,无论糖化血红蛋白是否达标,只要没有禁忌证都应该在二甲双胍的基础上加用具有ASCVD获益证据的胰高糖素样肽-1受体激动剂(glucagon-like peptide-1 receptor agonist,GLP-1RA)或钠-葡萄糖共转运蛋白2抑制剂(sodium-glucose cotransporter 2 inhibitor,SGLT2i)。予司美格鲁肽0.5 mg皮下注射(1次/周),二甲双胍缓释片1.0 g(2次/d)、达格列净10 mg(1次/d)口服联合降糖治疗,空腹血糖控制在6 mmol/L左右,餐后2 h血糖7~8 mmol/L左右。3个月后复查糖化血红蛋白6.5%,体重78 kg,减轻7 kg。
近年来,我国心血管疾病的发病率和死亡率呈逐年上升趋势,疾病负担沉重,防治形势严峻[1]。心血管疾病是我国首要的死亡原因,并且我国心血管疾病死亡率位居全球首位[2, 3]。糖尿病患病率逐年增加,中国已经成为糖尿病第一大国[4]。心血管疾病也是糖尿病患者死亡的主要原因[5],心血管疾病风险已经成为T2DM管理中的重要问题[6],降糖药物的心血管安全性对糖尿病治疗策略产生了重大影响。2016年,利拉鲁肽和司美格鲁肽的心血管结局试验相继证实了其心血管获益[7, 8]。心血管结局试验新证据推动了T2DM的治疗革新,除了降糖,T2DM的治疗目标还包括降低心血管并发症及死亡风险。随着对糖尿病认识的深入,糖尿病的治疗理念不断更新,管理策略从“降糖为主”向“关注长期结局管理”转变[9],各大指南糖尿病管理路径导向也开始由“降糖”向“个体化治疗”转变[10]。
GLP-1RA及SGLT2i通过不同机制产生不同方面的心血管保护作用。GLP-1RA可能通过抑制炎症、抑制氧化应激、改善内皮功能等从而抑制动脉硬化进程,进一步减少ASCVD所致终末心脑血管事件发生,减少心血管死亡。SGLT2i可能通过利尿减轻心脏前后负荷,转换心肌代谢底物,从而改善心脏舒张、收缩功能,进一步减少心力衰竭入院,减少心血管死亡[11]。美国心脏病学学会/美国心脏协会与欧洲心脏学会/欧洲糖尿病学会指南共同指出,GLP-1RA的获益来自于ASCVD的降低,而SGLT2i的获益来自于降低心力衰竭风险[12]。
本例患者为中年男性,生活习惯差,血糖控制不佳,合并ASCVD,治疗的目标包括安全平稳降糖,降低心血管病风险,控制和改善并发症。GLP-1RA队伍不断扩大,证据不断积累,使其在国内外指南中的地位不断提升,各大指南均推荐,无论糖化血红蛋白水平如何,确诊ASCVD的T2DM患者优先选择已被证实有心血管获益的GLP-1RA,以最大限度降低患者心血管事件及死亡风险。
所有作者声明无利益冲突































