
肝细胞癌(hepatocellular carcinoma, HCC)早期复发患者往往较晚期复发患者有更差的预后,且该疾病的早期症状大多是非特异性的。随着人工智能(artificial intelligence, AI)日益发展,影像组学与其核心分支机器学习结合,打破了人眼识别的局限性,深度挖掘医学影像图像中隐藏着的纹理、形态等反映细胞一定生物学特征的信息,处理并筛选高维特征进行定量数据分析,构建HCC早期复发预测模型,可以使更多的患者尽早受益于临床诊疗,从而提高生存率,在疾病诊断及预后方面显示出巨大潜力。本文对比分析文献中基于CT及MRI预测HCC早期复发的影像组学模型,并综述其研究进展。

本刊刊出的所有论文不代表本刊编委会的观点,除非特别声明
肝细胞癌(hepatocellular carcinoma, HCC)是全球第六大常见恶性肿瘤,是世界范围内癌症相关的第三大死因[1]。最近的肝癌临床实践指南将HCC根治性切除或消融术后复发分为早期复发(≤2年)和晚期复发(>2年),复发时间是一个独立的生存因素,早期复发患者的总体生存率往往低于晚期复发患者[2, 3, 4, 5]。预测早期复发对肝癌后续进一步监测及治疗意义重大。近年来的一些研究提出了几个HCC早期复发的危险因素,包括微血管侵犯(microvascular invasion, MVI)、肿瘤大小、基因序列、白蛋白-胆红素(albumin-bilirubin, ALBI)评分和甲胎蛋白(alpha fetoprotein, AFP)水平[6, 7, 8, 9, 10]。但由于肿瘤在空间和时间上的异质性,上述哪一种或哪几种因素对复发更重要仍存在争议,仍需要一种能够非侵入性、准确识别预后因素的方法来优化临床预测能力,更好地对肝癌患者进行分层与治疗。
2012年,荷兰学者Lambin等[11]首次提出影像组学的概念,即提取大量医学图像的定量特征分析其与临床及基因数据的关系,以建立预测模型。随着肝脏成像数据的不断扩展和积累以及人工智能技术的飞跃发展,影像组学与机器学习算法结合的新兴影像诊断技术广泛用于从大量图像中提取高通量和高维特征来识别肝脏病变的异质性[12],在肝脏疾病的诊疗及复发预测方面显示了良好的前景。本文对基于CT和MRI影像组学的机器学习模型在预测肝细胞癌根治性治疗后早期复发的研究进展予以综述,并讨论相关模型的前景和面临的挑战。
影像组学分析涉及图像预处理、分割、特征提取及量化、分类与预测等多个过程[13]。传统的统计方法在处理高维影像组学特征时存在一定的局限性,即数据量过大可能导致的模型冗余和过高的假阳性率,因此,许多机器学习算法被用于特征选择和分类,如岭回归、最小绝对收缩和选择算子(least absolute shrinkage and selection operator, LASSO)以及弹性网络正则化[14]。其他用于最佳权重特征选择的常用算法包括K近邻(K-nearest neighbor, KNN)、支持向量机(support vector machine, SVM)、决策树、随机森林和深度学习等[15]。机器学习技术稳健的性能为影像组学提供了良好的应用前景,提高了图像特征的泛化能力,减少了潜在的偏倚,使其成为精准诊断的辅助工具。
深度学习是机器学习的一个子集,为一种特殊的人工神经网络,其功能类似于人类的多层次认知系统[16, 17],可以与影像组学技术结合从而实现病变的自动检测和定量特征分析。已有研究[18]建立并验证了基于人工神经网络(artificial neural network, ANN)的临床预后指标(如乙肝病毒脱氧核糖核酸载量、γ-谷氨酰转肽酶水平、AFP水平等8个相关因素)模型来预测无大血管侵犯的HCC患者早期复发(AUC=0.753)。与临床预测模型相比,影像组学与深度学习结合获得了更令人惊喜的结果,Wang等[19]通过在不同特征提取阶段增加全连接层的方法建立了A、B、C三种联合模型,将多期CT图像数据与临床相关信息结合并输入到深度卷积网络中,以尽可能达到更准确的预测结果,最终联合模型C在对影像及临床数据进行平衡和过滤后AUC值最高(0.825)。Song等[20]纳入601例HCC患者进行回顾性分析,使用常规腹部多参数MRI序列建立深度学习联合临床参数模型预测MVI,该模型使用八个独立的卷积神经网络(conventional neural network, CNN)分别从对应的感兴趣体积(volumes of interest, VOI)中提取特征再进行融合,通过多输入网络提高了HCC患者早期复发和预后不良的预测性能的准确性(测试集AUC=0.931)。然而目前基于深度学习的影像组学预测肝癌早期复发相关研究较少,且现有的结果有待得到更充分的验证以真正投入临床使用。
由于人眼识别的局限性,传统CT和MRI图像中仍可能有大量能预示疾病预后和转归的信息未被正确解读,医学的发展趋势正从定性的、形态描述向定量的、精准预测领域转变。医学影像技术和人工智能的同时进步促进了影像组学的发展。研究结果表明,影像组学特征构建的以临床目标为导向的影像生物标记物在推进精准医学和提高肿瘤复发预测方面具有巨大的潜力[21, 22]。作者查阅近三年文献,分析基于CT及MRI不同影像学手段预测HCC早期复发的影像组学模型,表1展示了不同条件下构建出的最优模型及其预测性能。
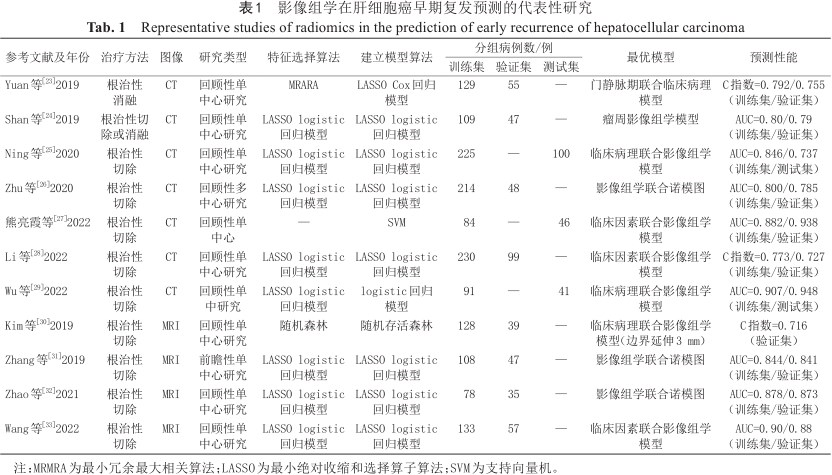
影像组学在肝细胞癌早期复发预测的代表性研究
Representative studies of radiomics in the prediction of early recurrence of hepatocellular carcinoma
影像组学在肝细胞癌早期复发预测的代表性研究
Representative studies of radiomics in the prediction of early recurrence of hepatocellular carcinoma
| 参考文献及年份 | 治疗方法 | 图像 | 研究类型 | 特征选择算法 | 建立模型算法 | 分组病例数/例 | 最优模型 | 预测性能 | ||
|---|---|---|---|---|---|---|---|---|---|---|
| 训练集 | 验证集 | 测试集 | ||||||||
| Yuan等[23]2019 | 根治性消融 | CT | 回顾性单中心研究 | MRARA | LASSO Cox回归模型 | 129 | 55 | — | 门静脉期联合临床病理模型 | C指数=0.792/0.755(训练集/验证集) |
| Shan等[24]2019 | 根治性切除或消融 | CT | 回顾性单中心研究 | LASSO logistic回归模型 | LASSO logistic回归模型 | 109 | 47 | — | 瘤周影像组学模型 | AUC=0.80/0.79(训练集/验证集) |
| Ning等[25]2020 | 根治性切除 | CT | 回顾性单中心研究 | LASSO logistic回归模型 | LASSO logistic回归模型 | 225 | — | 100 | 临床病理联合影像组学模型 | AUC=0.846/0.737(训练集/测试集) |
| Zhu等[26]2020 | 根治性切除 | CT | 回顾性多中心研究 | LASSO logistic回归模型 | LASSO logistic回归模型 | 214 | 48 | — | 影像组学联合诺模图 | AUC=0.800/0.785(训练集/验证集) |
| 熊亮霞等[27]2022 | 根治性切除 | CT | 回顾性单中心 | — | SVM | 84 | — | 46 | 临床因素联合影像组学模型 | AUC=0.882/0.938(训练集/验证集) |
| Li等[28]2022 | 根治性切除 | CT | 回顾性单中心研究 | LASSO logistic回归模型 | LASSO logistic回归模型 | 230 | 99 | — | 临床因素联合影像组学模型 | C指数=0.773/0.727(训练集/验证集) |
| Wu等[29]2022 | 根治性切除 | CT | 回顾性单中研究 | LASSO logistic回归模型 | logistic回归模型 | 91 | — | 41 | 临床病理联合影像组学模型 | AUC=0.907/0.948(训练集/测试集) |
| Kim等[30]2019 | 根治性切除 | MRI | 回顾性单中心研究 | 随机森林 | 随机存活森林 | 128 | 39 | — | 临床病理联合影像组学模型(边界延伸3 mm) | C指数=0.716(验证集) |
| Zhang等[31]2019 | 根治性切除 | MRI | 前瞻性单中心研究 | LASSO logistic回归模型 | LASSO logistic回归模型 | 108 | 47 | — | 影像组学联合诺模图 | AUC=0.844/0.841(训练集/验证集) |
| Zhao等[32]2021 | 根治性切除 | MRI | 回顾性单中心研究 | LASSO logistic回归模型 | LASSO logistic回归模型 | 78 | 35 | — | 影像组学联合诺模图 | AUC=0.878/0.873(训练集/验证集) |
| Wang等[33]2022 | 根治性切除 | MRI | 回顾性单中心研究 | LASSO logistic回归模型 | LASSO logistic回归模型 | 133 | 57 | — | 临床因素联合影像组学模型 | AUC=0.90/0.88(训练集/验证集) |
注:MRMRA为最小冗余最大相关算法;LASSO为最小绝对收缩和选择算子算法;SVM为支持向量机。
CT由于其高敏感性及通用性是检测HCC复发最常用的检查方法[34, 35],且是对不可切除的中晚期HCC患者行肝动脉化疗栓塞术(transcatheter arterial chemoembolization)的重要辅助工具,对肝动脉解剖、瘤体及瘤周边缘的显示具有指导意义[36],在肝癌诊疗及复发预测中发挥重要作用。基于CT的影像组学模型应用相对较早,在HCC患者早期复发中的预测性能日渐成熟。2007年,Segal等[37]通过组合28个CT形态学特征证明其可以实现全球78%的HCC基因表达谱的重建,揭示细胞增殖、肝脏合成功能及患者预后,证明人类肝癌的基因组活性可以通过非侵入性成像进行解码。Zhou等[38]使用机器学习算法构建LASSO回归模型筛选HCC患者影像组学特征,将其结合到传统的临床预测早期复发因素中比单独使用临床变量评估的效果更好,提供了一种全新的思路。Yuan等[23]回顾性分析184例接受根治性射频消融治疗的HCC患者的临床资料,从原始图像和非抽取滤波变换后的滤波后图像中提取了647个影像组学特征,建立和验证了基于增强CT影像组学的HCC早期复发风险模型,结果显示:门静脉期影像组学特征联合临床病理因素模型在训练亚组和验证亚组的预测效果最好,提示联合模型较单纯临床模型有更好的预测能力(P<0.0001)。而在熊亮霞等[27]的研究中,使用t检验和Wilcoxon秩和检验对特征进行降维后,采用SVM对筛选出的4个动脉期、2个静脉期特征进行建模,结果显示基于CT动脉期组学模型预测性能优于静脉期和临床模型,他们认为肿瘤动脉期明显强化且周围微小癌栓造成的“代偿性动脉灌注”是导致动脉期图像能更好地反映肿瘤异质性的原因。
Shan等[24]首次基于HCC切除边缘标准,将研究的感兴趣区(region of interest, ROI)向病变外周扩展2 cm,探索HCC切除或消融术后的瘤周影像组学(peritumoral radiomics, PT-RO)预测早期复发的价值,结果表明PT-RO特征是HCC早期复发的一个强有力的术前预测因子,校准曲线还显示PT-RO模型更符合有效队列中的实际HCC复发情况,优于瘤内影像组学(intratumoral radiomics, T-RO)模型和瘤周强化(peritumoral enhancement, PT-E)模型,但是这项研究提取的是肿瘤最大横截面积而不是三维体积的特征,可能会对模型的准确性以及临床应用的普适性产生一定的影响。Li等[28]也注意到HCC肿瘤边缘对复发率的影响,提取巴塞罗那分期(Barcelona Clinic Liver Cancer, BCLC)0~B期接受根治性切除术前2周患者的肿瘤及肿瘤周围CT图像影像组学特征,在与临床预测指标(年龄、性别、Child-Pugh肝功能等)结合时提高了早期和晚期复发的预测性能。
Ning等[25]研究发现肿瘤包膜、肿瘤大小、γ谷氨酰转移酶水平是HCC患者早期复发的临床危险因素,而基于增强CT图像的影像组学特征可以捕获重要的肿瘤内异质性表型信息,作为肿瘤生物学的粗略替代物在联合预测模型中与肿瘤大小及GGT水平成为HCC早期复发的独立预测因素(P<0.05)。Zhu等[26]将假定的预测成像特征输入LASSO logistic回归模型,再通过十倍交叉验证,将过滤后的非过拟合影像组学特征和临床危险因素(AFP、肿瘤数量和肿瘤大小)合并到诺模图中,在训练队列和验证队列方面都显示出显著的区分性。
差异不仅存在于不同模型之间,使用不同的机器学习算法也可以对结果的准确性产生影响,Wu等[29]分别应用了logistic回归模型、Bayes、SVM和KNN四种算法构建HCC早期复发的预测模型,使用受试者工作特征曲线评估模型的诊断准确性,再经过DeLong测试选择最佳机器学习方法,最终结果表明logistic回归构建的影像与临床联合模型预测性能最佳(AUC:0.907)。
以上研究均强调影像组学特征与肿瘤复发和转移存在潜在的病理生理学联系,从CT图像中提取的特征不仅仅是单纯的图像像素值,还可以反映一定的分子生物学功能,因此联合临床潜在复发因素为后续预测模型构建开拓了新的方向。
已有多项研究表明,MRI对HCC复发的诊断显示出比CT更高的准确性和敏感性,是诊断慢性肝病患者HCC的首选成像方式[39, 40]。Hui等[41]首次提出选择合适的术前MRI单一纹理分析参数预测HCC早期复发的准确率高达84%,但这些发现需要通过进一步的研究来验证。Kim等[30]在随机生存森林中使用了对数秩方法和最大选择检验两种分裂方法来评估预测结果的一致性,并进行超参数优化以提高模型的泛化能力,通过研究HCC术前边缘延伸0、3、5 mm的影像组学模型的预后价值,证明术前瘤周边缘延伸3 mm的增强MRI可以预测可切除HCC患者早期复发的术后无病生存期(disease-free survival, DFS),具有与术后临床病理模型相当的预后价值,提示基于机器学习的影像组学模型更加精细和个性化,可能会改善每个肝癌患者的预测性能。
Zhang等[31]通过一项前瞻性研究建立了一个影像组学诺模图,该图由血清AFP水平、血管侵犯总量以及非光滑肿瘤边缘构建,将多特征纹理以及潜在肿瘤异质性信息集成在一个影像组学评分中用于预测小于1年的HCC术后早期复发,在训练和验证队列中都显示出良好的辨别和校准能力。Zhao等[32]开发并验证了一种基于多参数MRI(multiparametric MRI, mpMRI)的影像组学模型用于预测肝部分切除后HCC患者的早期复发,筛选出的特征描述了图像内体素强度的分布与局部像素的空间关系,提供更完整的形态学及更全面的肿瘤异质性信息,研究证明结合影像组学评分和三个临床病理危险因素(MVI、Edmondson病理分级和肿瘤大小)的联合诺模图更具有竞争力。Wang等[33]同样采用多序列MRI图像提取单个结节直径≤5 cm的HCC影像组学特征,进一步证实了上述结果,他们还提到,在影像组学最终筛选出构建模型的特征中,2个来自T2WI序列,10个来自动态对比增强MRI序列,表明后者图像中隐藏的信息对HCC患者早期复发鉴别诊断有着更大的影响。
这些研究只考察了根治性切除术后HCC的早期复发,而射频消融由于其微创性、并发症少及住院时间短等优点,是小型及早期HCC的主要适应证[42, 43]。Wen等[44]根据两年的随访结果,将单个肿瘤直径≤3 mm且接受手术切除或射频消融术后的小肝癌患者分为早期复发组(n=53)和非早期复发组(n=58),使用互信息(mutual information, MI)、Fisher系数、分类误码概率与平均相关系数相结合三种特征选择方法自动识别出150个纹理特征,再通过LASSO对特征进行降维及十倍交叉验证和100次重复筛选出最优预测因素,经多变量logistic回归分析后,确定影像组学评分和术前血小板计数是小肝癌早期复发的最终独立预测因素,进而建立了基于术前MRI的影像组学诺模图来预测小肝癌的早期复发(AUC:0.981,95% CI:0.957~1.00),其优越的预测性能有助于临床医生简单地使用术前因素进行临床决策,进而为有早期复发风险的小肝癌患者提供更密切的随访或建立更积极的诊疗方案。
总体来说,基于MRI构建影像组学特征及与临床病理因素结合的诺模图具有预测HCC根治术后早期复发的潜力,可以作为一种无创性的有效工具进一步研究,选择最佳的治疗策略并设计更有效的个体化监测方案,以改善临床结果。
基于CT的影像组学研究表明,图像采集参数(如层厚、重建算法、图像分辨率,对比剂的种类、剂量、注射速率及扫描仪型号)的变化对纹理量化的影响最为显著[45, 46]。而通常与基于MRI的影像组学特征有关的影响因素是回波时间(echo time, TE)、重复时间(repetition time, TR)、采样带宽(sampling bandwidth, SBW)、空间分辨率、信噪比(signal-noise ratio, SNR)、场强、扫描仪型号、重建算法和并行成像加速因子的变化[47, 48]。MRI较CT具有更好的软组织分辨力,无辐射和硬化伪影,且可提供多种有助于HCC诊断的序列参数,如扩散加权成像、肝胆特异性对比剂增强序列等,以更可靠多元的纹理特征评估肿瘤的异质性;然而在HCC患者的诊断中,MRI图像获取有着更高的技术复杂性、伪影敏感性以及图像质量不均一性,在屏气困难或大量腹水的患者中,MRI图像将受到较CT更为明显的影响[49],这些因素都会影响影像组学模型为HCC早期复发预测提供准确的相关影像生物标志物信息。
近年来,随着影像组学的理论体系和技术框架在HCC早期复发研究中的应用越来越多,预测性能也趋于稳定。与较早基于语义图像特征带有一定主观性的预测模型相比,影像组学模型通过计算定量图像特征从而具有高度可重复性及客观性。然而将其应用于临床之前仍然存在一些挑战:第一,未将肝癌的类型(如早期肝癌及进展期肝癌)明确区分,且获取图像的影像设备以及图像采集参数不统一,使得用于影像组学分析的图像难以标准化而存在非生物因素差异,这可能对模型的实用性及可行性产生影响。第二,采用机器学习方法与影像组学模型结合仍可能出现研究设计不佳和数据拟合过高的情况。第三,大多数已发表的研究都是回顾性的,可能受主观性影响导致选择偏倚,且许多研究样本量相对较小,缺乏独立的验证队列来评估结果的普遍性和可重复性。
为使预测模型得到充分训练和多重验证,最大程度上模拟真实状态以减少非生物学差异,建立HCC影像数据库和实现数据共享的需求日益迫切。与二维断层图像最大横截面积相比,整个肿瘤的熵和均匀性更能代表肿瘤的异质性,如果在分割ROI时采用三维体积作为统一标准,则可以使整个结果更加精准化[50]。在精准医疗的大背景下,不同手术方式(如根治性切除或消融术)及分期标准的长期总生存率和无病生存期可能会存在一定差异,今后在影像组学模型实际应用中应将术式选择作为纳入标准。另外,使用统计学方法,并借鉴转录组学等其他组学去除批间差异的方式对数据进行校正可能提高模型的准确率。最后,整合多中心回顾性研究对数据进行随机分割,进而对模型进行迭代和多重验证,或者使用荟萃分析的方式整合模型在多个数据集中的结果,也可能对模型的普适性和可重复性提供更可靠的证据。
综上所述,未来使用CT和MRI两种成像方式提取特征并联合建模,或将成为影像组学在肝癌早期复发预测方面的新突破。
全体作者均声明无利益冲突。



























