
孕产妇死亡率(MMR)是衡量一个国家或地区妇女健康状况和社会经济发展的重要指标之一。随着社会经济的发展与孕产妇健康水平的提高,孕产妇死亡已成为极低概率事件,尤其是在发达国家,仅仅使用孕产妇死亡及MMR作为终末指标,已无法全面评价和反映孕产妇医疗保健过程的质量和妇幼健康事业的发展现状,难以为改善孕产妇医疗保健政策及策略的制订,提供有效参考信息。对于将危重孕产妇的临床管理作为导致孕产妇死亡的动态过程和前期指标,这对强化危重孕产妇管理,进而降低MMR,具有重要临床意义。笔者拟就全球近年危重孕产妇管理、救治现状及其最新研究进展进行阐述,旨在为促进我国危重孕产妇应急管理及救治体系的建设和完善提供参考,从而有效提高危重孕产妇急救效率和质量,切实降低MMR。

版权所有,未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别申明,本刊刊出的所有文章不代表中华医学会和本刊编辑委员会的观点。
本刊为电子杂志,以光盘形式出版。本册应读者需求按需印刷,随光盘免费赠阅。光盘如有质量问题,请向编辑部调换。
孕产妇死亡率(maternal mortality ratio,MMR)不仅是评价医疗机构产科质量的重要指标,更是衡量一个国家或地区妇女健康状况和社会经济发展的重要指标。根据新华网报道,2016年中国MMR已经下降至19.9/105[1]。世界卫生组织(World Health Organization,WHO)发布2015年《孕产妇死亡率》报告显示,发展中国家的MMR为239/105,而发达国家则为12/105[2]。由此可见,中国MMR已经处于发展中国家前列,并且接近发达国家水平。
《"健康中国2030"规划纲要》主要指标要求,至2030年,中国MMR应下降至12.0/105[3]。"全面二孩"政策实施以来,高龄孕产妇、瘢痕子宫再次妊娠、经产妇比例呈上升趋势,妊娠期高血压疾病、妊娠期糖尿病、多胎、早产、巨大儿、产后出血等发生率显著增高[4,5]。子痫前期发生风险随着孕产妇年龄增长呈指数增高,尤其是在年龄>40岁孕妇中,该风险为<35岁孕妇的1.5倍[6]。高龄和多次孕产史,是孕产妇发生妊娠期糖尿病的危险因素。妊娠期糖尿病发生率与孕妇年龄呈正相关关系,在40岁孕妇中达到高峰[7]。剖宫产分娩可增加再次妊娠时前置胎盘发生风险,前置胎盘发生率在无剖宫产分娩史和经历过1、2、3次剖宫产分娩的孕妇中,分别为0.33%、1.86%、5.49%及14.28%[8]。在无剖宫产分娩史和经历过1、2、3、4次剖宫产分娩的前置胎盘孕妇中,胎盘植入发生率分别为4%、14%、23%、35%及50%[9]。凶险型前置胎盘是引起产科急性大量出血,进而导致孕产妇死亡(maternal deaths)的主要原因[10]。我国"全面二孩"政策的实施,增加了MMR下降的难度,为孕产妇死亡防控带来新的挑战。
2016年9月,WHO通过全球卫生观察站(Global Health Observatory,GHO)发布报告[11],2015年,每天约830例妇女死于妊娠和分娩相关疾病,99%发生于发展中国家[2],而且多数是可以避免的。妊娠与分娩并发症导致的孕产妇直接死因,主要包括严重出血(severe bleeding),妊娠期高血压疾病(子痫前期、子痫)和感染;而主要间接死因是妊娠前已存在疾病与妊娠交互作用的结果(interaction between pre-existing medical conditions and pregnancy)。发展中国家妇女一生中死于妊娠相关疾病的风险是发达国家妇女的33倍,MMR存在贫富悬殊和巨大城乡差距。在已知的孕产妇死因中,超过80%是可以避免的[12,13]。我国各地区经济发展、预防保健和医疗保障水平极不平衡,东部发达地区的MMR已达到发达国家先进水平,而西部地区则仍处于发展中国家先进水平。总体而言,目前我国妇幼健康服务能力明显不足,难以满足妇女儿童日益增长的多样化健康服务需求,尤其是"全面二孩"政策实施后,累积生育需求集中释放,高龄的高危产妇比例增加,妇幼健康工作仍然面临众多问题和挑战[1]。孕产妇死亡仍然是我国目前面临的严峻卫生经济问题,也是中等收入国家重要的公共卫生问题。
随着经济文化与社会发展的进步,医疗保健系统的可及性与可利用性持续改善,促进MMR下降接近期望水平、孕产妇死亡绝对数不断下降,特别是在高收入国家,孕产妇死亡已成为极低概率事件,MMR远低于10/105,在很多发达国家的医疗机构中,MMR几乎为0。因此,准确获得MMR的难度巨大,这使得MMR的稳定性和代表性受到限制和挑战。同时,进一步降低MMR的进程也十分缓慢。因此,仅仅使用孕产妇死亡及MMR作为终末指标,已无法全面评价和反映孕产妇医疗保健过程质量和妇女卫生事业发展现状,难以为改善孕产妇保健政策及措施的制定,提供充分有效信息[14]。
近20年,很多学者已致力于寻找评价孕产妇健康水平与生存质量、评价医疗机构产科质量的新指标,研究重点集中于可能导致孕产妇死亡的严重致死性疾病,包括孕产妇致死性疾病种类、病因、发生率、有效防控措施等。不同学者针对孕产妇致死性疾病的研究中,使用的术语、相关定义和判断标准不尽一致,其使用的术语包括:严重孕产妇疾病(severe maternal morbidity)[15,16],孕产妇疾病(morbidity)[17],危急孕产妇疾病(severe acute maternal morbidity)[18,19],严重产科疾病(severe obstetrical morbidity)[20],危重孕产妇(maternal near misses)[18]等。
随着对孕产妇致死性疾病研究的深入,对描述罹患严重致死性疾病孕产妇群体的术语逐渐统一为"危重孕产妇"。危重孕产妇这一作为反映孕产妇死亡的动态过程和前期指标,主要针对和强调的是对孕产妇死亡过程的管理[21]。
2009年,WHO专家对危重孕产妇的定义和判断标准进行了统一。危重孕产妇是指罹患严重疾病的孕产妇,即妊娠期、分娩期或产后42 d濒临死亡,但是被成功抢救或由于偶然因素而继续存活的孕产妇[22]。危重孕产妇的病情变化是一个动态过程,即经历从正常孕产妇→高危孕产妇→危重孕产妇→孕产妇死亡。孕产妇分类,见图1[21]。在孕产妇病情动态变化过程中,具有潜在危及生命状况(potentially life-threatening conditions)的孕产妇,病情继续发展至危及生命状况(life-threatening conditions)时,将最终成为危重孕产妇或发生孕产妇死亡。
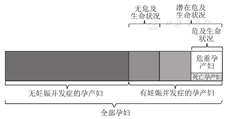

由图1所示的孕产妇分类可见,危重孕产妇数量远多于死亡孕产妇数量,临床对于危重孕产妇的积极救治,是避免孕产妇死亡前的最后一道重要防线。在危重孕产妇管理与孕产妇死亡防控中,应用危重孕产妇这一概念可获得以下益处:①因为危重孕产妇数量远多于死亡孕产妇数量,所以调查和总结危重孕产妇人群的病例资料,可挖掘孕产妇严重疾病发生过程中更有用的信息,从而降低其严重病率和预防孕产妇死亡。②因为多数危重孕产妇最终结局是存活的,所以对参与救治该人群的管理人员和医疗人员展开调查,可能获得更可靠的关于危重孕产妇→孕产妇死亡救治过程的信息,可更为客观地反映该救治过程情况。③针对危重孕产妇数据的分析结果,可为降低孕产妇死亡及孕产妇病率的各项政策和规范的制定及更新提供参考依据[21]。同时,重视孕产妇管理,加强对高危孕产妇的预测、识别与管理,减少妊娠并发症的发生,降低危重孕产妇发生率,加强危重孕产妇与孕产妇死亡的监测和评估,提高危重孕产妇管理与临床救治水平,前移孕产妇死亡防控关口,可再次促进MMR的显著下降进程,有效推进妇女健康水平再上新台阶。
关于危重孕产妇的诊断标准较多,大致可归纳为以下3大类。①临床标准:包括孕产妇临床症状、体征或相关疾病,如子痫或产科出血;②实验室标准:包括孕产妇器官功能紊乱或失代偿,如休克、呼吸窘迫等;③基于救治措施的标准:包括针对孕产妇的特殊干预,如转入重症监护病房(intensive care unit,ICU),子宫切除或者大量输血等。为了便于统计和分析,WHO制定的危重孕产妇的诊断标准中,仅识别孕产妇发生的极其严重事件,如主要涉及生命体征及器官功能紊乱的事件。WHO制定的危重孕产妇诊断标准,见表1[21]。

世界卫生组织制定的危重孕产妇诊断标准
世界卫生组织制定的危重孕产妇诊断标准
| 危重孕产妇诊断标准 | 危重孕产妇诊断标准 | ||
|---|---|---|---|
| 临床标准 | 实验室标准 | ||
| 急性发绀 | 血清肌酐浓度≥300 μmol/L(3.5 mg/dL) | ||
| 喘息 | 血清胆红素浓度>10.0 μmol/L(6.0 mg/dL) | ||
| 呼吸频率>40次/min,或<6次/min | 全血液pH值<7.1 | ||
| 休克 | 全血液乳酸浓度>5 mmol/L | ||
| 采取补液措施或使用利尿剂无效的少尿 | 急性血小板计数降低<50×109/L(50 000/mm3) | ||
| 凝血功能障碍 | 意识丧失伴尿糖或者尿酮呈阳性 | ||
| 意识丧失持续时间≥12 h | 基于救治措施的标准 | ||
| 意识丧失伴脉搏或(和)心跳停止 | 持续使用血管活性物质 | ||
| 脑卒中 | 感染或者产科出血导致的子宫切除 | ||
| 无法控制的痉挛或全身瘫痪 | 静脉输注红细胞≥5 U | ||
| 子痫前期伴黄疸症状 | 与麻醉无关的气管插管及通气时间≥60 min | ||
| 实验室标准 | 因急性肾功能衰竭而采取血液透析治疗 | ||
| 动脉血氧饱和度<90%的持续时间>60 min | 采取心肺复苏治疗 | ||
| 动脉血氧分压与吸入氧气分数的比值<26.7 kPa(200 mmHg) | |||
WHO制定的危重孕产妇诊断标准中,关于危重孕产妇的识别多为实时指标,对危重孕产妇实时与事后判断分析具有重要指导意义。但是,根据WHO制定的统一标准诊断的危重孕产妇与孕产妇死亡只有一步之遥,对临床实践过程中预测、识别和处理危重孕产妇的指导意义不大。因此,开展危重孕产妇高危因素研究,对预测、识别、规范诊治和管理危重孕产妇更为重要。
临床对危重孕产妇的诊断,应该涵盖以下3个方面[21]。①是否合并严重孕产妇相关疾病,包括重度子痫前期、子痫、严重产后出血、羊水栓塞等。②是否对孕产妇采取紧急治疗干预措施,包括转入ICU、紧急子宫切除术、输血治疗等。第2条较好地弥补了第1条的不足,排除了病情较轻的孕产妇相关疾病。但是,不同地区、不同级别医院所采用的孕产妇紧急治疗干预标准可能不同,若仅以上述2条标准作为危重孕产妇的诊断标准,则尚缺乏同质性。③各器官系统是否发生功能障碍,如心功能衰竭、急性肾功能不全,以及弥散性血管内凝血(disseminated intravascular coagulation,DIC)等。
目前,WHO推荐"各器官、系统功能障碍"为危重孕产妇诊断标准中最容易明确判断的标准。各器官、系统功能障碍可通过以下任一一项临床症状、实验室指标及治疗措施进行综合评价[23,24]。①心血管与呼吸系统功能障碍:包括心肌缺血、肺水肿、大量胸腔积液、需接受强心治疗、需高浓度吸氧时间>1 h、非剖宫产术麻醉的气管插管治疗等情况;②中枢神经系统功能障碍:包括发生子痫、昏迷、脑卒中等;③肝功能异常:肝功能生化指标大于正常参考值的3倍;④急性肾功能不全:包括有肾病史者且血清肌酐浓度>200 μmol/L,无肾病史者但是血清肌酐浓度>150 μmol/L;⑤血液系统功能障碍:包括血小板计数<50×109/L 、凝血功能异常、DIC等;⑥严重产科并发症:包括溶血、肝酶升高和溶血、产后大量出血、胎盘早剥及肝酶升高及溶血、肝酶升高和低血小板计数(hemolysis,elevated liver enzymes and low platelet count,HELLP)综合征等。
为了优化危重孕产妇的监测与管理工作,早期识别可能发展为危重孕产妇的孕产妇至关重要。2009年,Say等[21]列举了部分可危及孕产妇生命的临床指标,但是所列举的临床指标并不能全面覆盖这类患者,临床上还存在很多其他异常情况可危及孕产妇生命。此外还应强调的是,孕产妇入院当时或入院后3~6 h出现的危及生命的异常状况,与住院期间出现的危及生命的异常状况不同,后者更能反映医院医疗质量,以其作为识别危重孕产妇病例的临床指标,更有助于完善危重孕产妇的管理和救治。早期识别潜在危重孕产妇的临床指标,见表2[21]。由此可见,早期识别潜在危重孕产妇的指标,至少包括产后大量出血、重度子痫前期、子痫、HELLP综合征、羊水栓塞、子宫破裂、DIC、妊娠合并心功能衰竭、急性脂肪肝、重症感染等。

早期识别潜在危重孕产妇的临床指标
早期识别潜在危重孕产妇的临床指标
| 临床指标 | 临床指标 | ||
|---|---|---|---|
| 出血性疾病 | 其他系统疾病 | ||
| 胎盘早剥 | 抽搐 | ||
| 胎盘植入 | 脓毒血症 | ||
| 异位妊娠 | 休克 | ||
| 产后出血 | 血小板计数<100×109/L | ||
| 子宫破裂 | 甲状腺危象 | ||
| 妊娠期高血压疾病 | 以严重的处理措施为识别的指标 | ||
| 重度子痫前期 | 输血 | ||
| 子痫 | 中心静脉置管 | ||
| 严重原发性或妊娠期高血压 | 子宫切除术 | ||
| 高血压性脑病 | 入住ICU | ||
| HELLP综合征 | 住院时间长(产后>7 d) | ||
| 其他系统疾病 | 非麻醉的气管插管 | ||
| 子宫内膜炎 | 重返手术室 | ||
| 肺水肿 | 手术干预 | ||
| 呼吸衰竭 | |||
注:血小板计数<100×109/L,即<100 000/mm3。HELLP综合征为溶血、肝酶升高和低血小板计数综合征,ICU为重症监护病房
2009年,Ronsmans[25]回顾分析来自24个低收入国家的37篇危重孕产妇相关研究文献指出,危重孕产妇还包括因绝对指征,如严重产前出血,胎儿绝对头盆不称、横位、面先露等,而需进行急诊手术的孕产妇及转诊医学中心的孕产妇等。其中,急诊手术包括剖腹探查术、毁胎术、胎儿内倒转术等。另外,这37篇危重孕产妇相关研究文献中,部分文献对于危重孕产妇的研究,未纳入严重影响孕产妇心、肺、肝、肾、脑等重要脏器功能的疾病,以及栓塞性疾病等非产科疾病导致的危重孕产妇。同年,van Roosmalen与Zwart[26]分析高收入国家危重孕产妇管理情况的结果显示,高收入国家危重孕产妇发生率为0.38%~1.20%,导致危重孕产妇发生的前3大原因是产科出血、子痫前期及子痫。
近年国外学者先后对医院或地区的危重孕产妇病例进行分析,调查危重孕产妇发生率,并研究其相关高危因素,寻找更科学、合理的危重孕产妇管理措施,进行降低MMR的技能培训,以探讨对危重孕产妇的医疗保健与防控重点。危重孕产妇发生率与危重孕产妇高危因素及其所占比例,见表3。
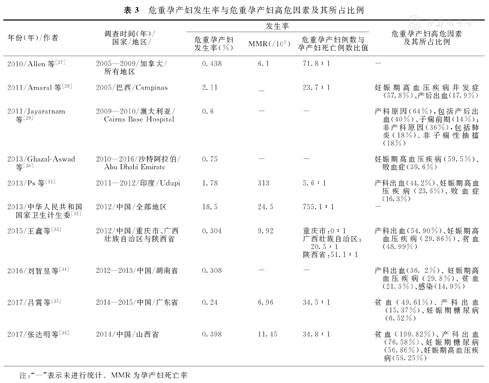
危重孕产妇发生率与危重孕产妇高危因素及其所占比例
危重孕产妇发生率与危重孕产妇高危因素及其所占比例
| 年份(年)/作者 | 调查时间(年)/国家/地区/ | 发生率 | 危重孕产妇高危因素及其所占比例 | ||
|---|---|---|---|---|---|
| 危重孕产妇发生率(%) | MMR(/105) | 危重孕产妇例数与孕产妇死亡例数比值 | |||
| 2010/Allen等[27] | 2005—2009/加拿大/所有地区 | 0.438 | 6.1 | 71.8∶1 | - |
| 2011/Amaral等[28] | 2005/巴西/Campinas | 2.11 | - | 23.7∶1 | 妊娠期高血压疾病并发症(57.8%)、产后出血(17.9%) |
| 2011/Jayaratnam等[29] | 2009—2010/澳大利亚/ Cairns Base Hospital | 0.6 | - | - | 产科原因(64%),包括产后出血(40%)、子痫前期(14%);非产科原因(36%),包括肺炎(18%)、非子痫性抽搐(18%) |
| 2013/Ghazal-Aswad等[30] | 2010—2016/沙特阿拉伯/ Abu Dhabi Emirate | 0.75 | - | - | 妊娠期高血压疾病(59.5%)、败血症(39.6%) |
| 2013/Ps等[31] | 2011—2012/印度/Udupi | 1.78 | 313 | 5.6∶1 | 产科出血(44.2%)、妊娠期高血压疾病(23.6%)、败血症(16.3%) |
| 2013/中华人民共和国国家卫生计生委[32] | 2012/中国/全部地区 | 18.5 | 24.5 | 755.1∶1 | - |
| 2015/王鑫等[33] | 2012/中国/重庆市、广西壮族自治区与陕西省 | 0.304 | 9.92 | 重庆市:0∶1广西壮族自治区:20.5∶1陕西省:51.1∶1 | 产科出血(54.90%)、妊娠期高血压疾病(29.86%)、贫血(48.99%) |
| 2016/刘智昱等[34] | 2012—2013/中国/湖南省 | 0.308 | - | - | 产科出血(36. 2%)、妊娠期高血压疾病(29.8%)、贫血(21.3%)、感染(14.9%) |
| 2017/吕霄等[35] | 2014—2015/中国/广东省 | 0.24 | 6.96 | 34.5∶1 | 贫血(49.61%)、产科出血(15.37%)、妊娠期糖尿病(6.52%) |
| 2017/张达明等[36] | 2014/中国/山西省 | 0.398 | 11.45 | 34.8∶1 | 贫血(199.82%)、产科出血(76.58%)、妊娠期糖尿病(56.86%)、妊娠期高血压疾病(56.25%) |
注:"—"表示未进行统计。MMR为孕产妇死亡率
由此可见,不同发展水平国家与地区的危重孕产妇发生率差异很大,危重孕产妇与孕产妇死亡的比例波动也较大。加强危重孕产妇管理,改善医疗保健机构孕前及产前保健的可及性和可利用性,降低危重孕产妇发生率,动态预测、识别危重孕产妇,合理转诊、规范诊治危重孕产妇,前移孕产妇死亡防控关口,可进一步促进MMR显著下降进程。
WHO在统一危重孕产妇的定义和判断标准的同时,制定了一套产科质量评价指标体系。其主要指标包括以下5个方面。①严重孕产结局发生率(severe maternal outcome ratio,SMOR):是指每1 000例活产孕产妇中,具有危及生命状况的孕产妇例数,即SMOR=(危重孕产妇例数+死亡孕产妇例数)/活产孕产妇例数×(1 000/1 000)。SMOR可同时用于评估一个地区或医疗机构所需要的产科医疗护理和资源的数量。②危重孕产妇发生率:是指每1 000例活产孕产妇中,危重孕产妇例数,即危重孕产妇发生率=(危重孕产妇例数/活产孕产妇例数)×(1 000/1 000)。危重孕产妇发生率与SMOR一样,亦可同时用于评估一个地区或医疗机构所需要的产科医疗护理和资源的数量。③危重孕产妇死亡比(maternal near-miss mortality ratio)=危重孕产妇例数/死亡孕产妇例数,该比值越高,则反映产科质量越高。④孕产妇死亡指数(maternal mortality index,MMI)=死亡孕产妇例数/(危重孕产妇例数+死亡孕产妇例数)×100%。MMI越高,则具有生命危险的孕产妇死亡比例越高;反之,MMI越低,死亡则越低。MMI越低,则反映产科质量越高。⑤围生儿结局指标:包括围生儿死亡率、新生儿死亡率或胎儿死产率。在危重孕产妇监测中,危重孕产妇围生儿结局指标,可以作为产科质量评价的补充指标[21,37]。
临床实践中,需要围绕产科质量评价指标体系,加强危重孕产妇管理。危重孕产妇是孕产妇死亡的前期过程,是一个动态过程指标,即危重孕产妇的病情变化具有双向性:康复←好转←危重孕产妇→孕产妇死亡。临床实践中前瞻性地加强对危重孕产妇病情变化动态过程的预测、识别、规范诊治和管理,加强高危孕产妇的预测与识别,避免具有妊娠并发症孕产妇发生潜在危及生命的状况,阻断具有潜在危及生命状况的孕产妇转变为危重孕产妇,防治危重孕产妇发生死亡,改善这一动态过程的恶化进程,是危重孕产妇和孕产妇死亡防控的关键环节,对改善危重孕产妇结局具有重要意义。
危重孕产妇救治要求以产科为中心的多学科团队(multi-disciplinary team,MDT),以临床指南、专家共识(clinical expert consensus documents)等为依据,随时做好应对突发事件的准备,建立产科安全保障体系。产科安全保障体系的建设,包括高危产科门诊、妇产科急诊、主诊医疗单元和值班医疗单元、应急快速反应医疗单元等医疗团队,危重孕产妇早期预警系统,MDT医疗应急快速反应培训和演练,重症监护,以及不良事件报告、总结及原因剖析、处理方案改进等。有效的交流和团队协作、以产科为中心的MDT医疗急救技术等,对危重孕产妇救治具有重要意义。
危重孕产妇在疾病及病情的动态发展过程中具有其特殊性,但是对患者的应急管理和救治并无明显特异性,完善的危重孕产妇管理救治体系可在全病患人群中推广。一项关于危重孕产妇的研究结果发现,超过30%产后大量出血可导致不良结局,其中13%产后大量出血是由于"可避免的诊断和治疗的延误"所致,11%是由于"未能按照规范救治方案或计划执行救治"所致,5%是由于"不充分的训练和监督管理"所致。同时,规范、统一的危重孕产妇管理救治方案,对提高危重孕产妇救治成功率亦至关重要[38]。另一项针对危重儿童的研究指出,在危重儿童救治过程中,50%应急管理措施,至少有一项影响危重儿童预后的主要因素需要改进[39]。这些需要改进的关键因素包括保健资源的获取(access to care)、危重症识别(identification of the critically ill)、病情严重性评估(assessment of severity)、不恰当复苏(inadequate resuscitation)、决策(decision making)和转诊(referral or transfer)延误。文献报道,从危重儿童的危重症首发表现(first presentation)被识别至转入ICU的中位时间为12.3 h,在转入ICU前,74%危重儿童可避免病情发展为危重症,56.7%危重儿童死亡是可以避免的[37]。综上所述,不论是孕产妇还是儿童,影响危重患者预后的因素具有相似性,并且是可控的,而要对这些因素进行规范化控制,就需要一套完善的管理救治体系,并且该体系应做到病患群体适用性最大化,以便于临床推广。
英国孕产妇和儿童健康调查报告(Confidential Enquiry into Maternal and Child Health)推荐,孕产妇管理应常规使用改进的产科早期预警系统(modified early obstetric warning system,MEOWS)[40],该系统包括以下2个方面。①MEOWS黄色预警:孕产妇体温为35~36 ℃;收缩压为20.0~21.3 kPa(150~160 mmHg);舒张压为12.0~13.3 kPa(90~100 mmHg);心率为100~120次/min或40~50次/min;呼吸频率为21~30次/min;疼痛评分为2~3分,对声音等刺激有应答。②MEOWS红色预警:孕产妇体温<35 ℃或>38 ℃;收缩压<12.0 kPa(90 mmHg)或>21.3 kPa(160 mmHg);舒张压>13.3 kPa(100 mmHg);心率<40次/min或>120次/min;呼吸频率<10次/min或>30次/min;动脉血氧饱和度<95%;除了疼痛,神经系统对声音等其他刺激无应答。MEOWS启动应急团队(rapid response teams)的具体情况还包括:孕产妇急性大量出血、严重腹痛、胎儿窘迫、子痫等。产科急救应结合学科特征,明确危重孕产妇抢救的响应标准,制定专用抢救路线图,并确保其畅通,规范医护人员抢救报告流程,为抢救成功提供保障。我国目前尚无规范、统一的MEOWS及MEOWS启动应急团队的标准。
应急团队于2005年首次被提出,现已广泛应用于临床,也称为医疗急救团队(medical emergency teams)[41]。参照MEOWS,监护人员发现患者出现任一"扳机"临床表现,均应启动应急团队,无需事先通知主诊医师。这与传统的逐级汇报模式差异较大[40]。立即启动应急团队可为抢救争取更多时间,使临床尽快实施干预措施,以避免不良事件发生,如减少患者术后不良结局、降低术后死亡率、缩短住院时间、降低ICU入住率[42]。应急团队的目标是收到启动信号后5 min内到达患者床旁,为患者提供气管插管、无创机械通气、动脉血气分析、中心静脉通道、静脉补液、补充血液制品等干预措施。
在危重孕产妇临床应急管理过程中,可合理借鉴"Ferrari车队进站维修"经验,设立总指挥,明确各级分工,促进抢救方案有条不紊地执行[43]。参与抢救的产科主任医师及主诊医疗单元或值班医疗单元医护人员中,由最高职称医师作为抢救总指挥,对各级医护人员的职责进行明确分工,医院行政职能部门组织多学科会诊,调配抢救资源。各级医护人员严格执行各自岗位职责,可避免不必要的人力、物力资源浪费,为抢救争取更多时间,优化临床抢救效率和效果,提高危重孕产妇抢救成功率。
一个专业、完整的应急团队应包括以下4个部分:启动者、响应者、质量控制和行政管理[41]。启动者包括临床医护人员、患者家属,或者任何一个觉得患者病情异常人员,均可以呼叫、启动应急团队。对于医疗机构,应定期组织医务人员进行临床应急救治培训和演习,而对于患者及其家属,应在患者入院后,对其进行相应宣传教育,确保他们熟知启动应急团队的标准。应急团队启动后,床旁护士应争取时间立即实施供氧等初步抢救措施。响应者是第一时间到达患者床旁并稳定患者病情、决定下一步诊疗的临床医师;当响应者到达患者床旁,启动者应立即简明扼要地向响应者汇报患者病史及当前病情,类似于情况-背景-评估-建议(situation-background-assessment-recommendation,SBAR)汇报模式,以便于启动者简明汇报患者信息,有利于响应者快速准确判断患者病情,为患者提供恰当的医疗服务。响应者将组建应急团队,开展现场急救、决定是否转诊、修正当前诊疗计划等。此时,启动者应转换为响应者帮助稳定患者病情。
加强产科质量控制体系建设,建立危重孕产妇及应急团队评价机制,提出持续改进计划和行动建议,具有重要临床意义。分析危重孕产妇疾病发生、发展过程,相比于单独分析孕产妇死因,更有利于医疗干预措施的制定和实施[44]。及时识别可避免的孕产妇死亡或临近死亡的状况,对于降低孕产妇病死率极为重要[45]。
除了临床诊疗、医疗技术,行政管理对危重孕产妇救治,亦具有重要支撑作用。加强应急转运与物流系统建设、优化救治流程、调配急救资源、讨论危重孕产妇病例、评价不良事件、制定改进方案和行动计划等行政管理措施,均是改善危重孕产妇预后、促进医疗安全质量持续改进的重要举措[46]。
ICU已从初期的综合性危重患者监护向更现代化、更专业化、更深层次的专科ICU(special ICU)方向发展,如新生儿ICU(neonatal ICU,NICU),产科ICU(obstetrics ICU)或孕产妇ICU(maternal ICU,MICU)等。孕产妇具有特殊的心理、生理和病理变化,建立MICU,识别危重孕产妇与非妊娠人群危重症在监护及救治上的不同,具有重要作用。对于危重孕产妇,建议在MICU进行监护和救治[23]。
紧急剖宫产术是为抢救母儿生命而进行的紧急抢救手术,决定紧急剖宫产术至胎儿娩出的时间(decision to delivery interval,DDI),是国际上评估产科质量及鉴定医疗纠纷的重要指标。对于DDI的最佳时限,迄今尚缺乏统一标准,目前比较统一的观点建议DDI在30 min内,并且DDI越短越好[47,48,49]。早在1957年Halsey与Dougl率先针对紧急剖宫产术的DDI进行了研究,然而时至今日,DDI的最佳时限及其对围生结局的影响,仍存在争议。美国妇产科医师学会(American College of Obstetricians and Gynecologists,ACOG)在《妇产科标准(6版)》中,将紧急剖宫产术的DDI建议调整为30 min[50]。但是,英国皇家妇产科医师学院(Royal College of Obstetricians and Gynaecologists,RCOG)和英国国立健康与临床优化研究所(National Institute for Health and Care Excellent,NICE)制定的剖宫产术相关临床指南,将Ⅱ类剖宫产术的DDI更改为≤75 min[51]。Kotarski与Bobiński[52]提出,DDI与产科医师的决策能力、手术技能、应急转运与物流系统、术前准备、麻醉技能,以及训练有素的团队合作密切相关。为缩短DDI,Kotarski与Bobiński[52]建议县级孕产妇急救中心、区域医疗中心、围生医学中心等助产机构,在产房内设置手术室,应急布置急救手术室也可以满足现场紧急救治需要。
美国联合委员会(Joint Commission)研究结果发现,超过50%产科不良事件是由于无效交流和不能进行团队协作造成的。资源缺乏、观念传统,以及忽视医院及其地区具体情况、不能变通执行标准和方案,也是阻碍产科急救成功的重要因素[53]。基于医院及其地区实际情况、急救案例具体状况,持续改进危重孕产妇抢救方案与行动计划,定期组织和设计危重孕产妇救治培训与演练,反复强化应急团队急救意识和团队精神,不断优化急救环节、流程和循证模板,持续提高危重孕产妇救治系统应答能力和应急团队急救能力,可有效降低危重孕产妇不良结局的发生。
仅了解孕产妇死亡水平是不够的,死亡数字不能告诉我们为什么在防止孕产妇死亡所需的知识和资源均可触手可及的当今世界,孕产妇死亡事件仍然在持续发生,而必须要了解导致孕产妇死亡的根本原因,前移孕产妇死亡防控关口。因为很多临床实践证明,即使在医疗资源短缺的国家,孕产妇死亡也是可以避免的,但是需要准确的信息,作为孕产妇死亡干预基础。为了解孕产妇死亡的真正原因,探索孕产妇死亡的可避免因素,WHO编写了《数字背后——回顾孕产妇死亡和并发症,使妊娠更安全》[54]。这是目前被公认的较为全面的孕产妇死亡监测、评审指导手册。
随着孕产妇死因顺位的变化,危重孕产妇的常见病因也应该持续调整。因此,必须在孕产妇死亡评价基础上,持续调整危重孕产妇监测和评价重点,预测危重孕产妇防控方向。2016年,中国MMR为19.9/105,孕产妇死因顺位为产科出血、羊水栓塞、心脏疾病、静脉血栓及肺栓塞、妊娠期高血压疾病。子宫收缩乏力、胎盘因素、异位妊娠和子宫破裂,仍然是致死性产科出血的重要原因,胎盘因素导致难治性产后出血孕产妇死亡的比例呈逐年上升趋势。因此,目前危重孕产妇的关键病因仍然是产科出血、栓塞性疾病、心脏疾病及妊娠期高血压疾病等,并应更多关注胎盘因素导致难治性产后出血发生风险,以及子宫破裂发生风险。
就理论而言,危重孕产妇的调查应该是回顾性研究,需要追踪至孕产妇产后42 d,但是实际工作中更需要前瞻性管理。任何具有危及生命状况的孕产妇,在研究截止期内可以被分为2类:危重孕产妇及孕产妇死亡。危重孕产妇的病情变化是一个动态过程,即前述的康复←好转←危重孕产妇→孕产妇死亡,因此,临床实践中前瞻性地加强对危重孕产妇病情变化动态过程的预测、识别、规范诊治和管理,对改善危重孕产妇结局具有重要意义。
危重孕产妇作为孕产妇死亡前期过程的动态指标,其监测和评价已成为该领域研究的焦点,以期通过对危重孕产妇监测和评价反馈信息,促进和有效改善危重孕产妇管理。对危重孕产妇监测,已成为实时了解一个医疗机构、地区或国家所有孕产妇的生存状况和产科质量的重要工具,以及妇幼卫生决策、干预的重要依据。为连续、动态获取危重孕产妇发生的基线水平,了解其发生特征、产科质量及其影响因素、评估干预和产科质量改善效果,部分国家或地区先后开展了对危重孕产妇的调查研究,不断提高医疗机构识别孕产妇相关严重疾病的能力。采取前瞻性干预措施,可持续改善产科服务质量。巴西[55,56]、尼泊尔[57]和中国建立了国家级的以医院为基础的全国危重孕产妇监测网络。加拿大[58]和新西兰[59]建立了以人群为基础的危重孕产妇监测网络。目前危重孕产妇的概念及诊断标准,均采用WHO相关标准,保证了各国、各地区危重孕产妇调查结果既可纵向比较,又具有横向可比性。
危重孕产妇评审是对发生在一个医疗机构的危重孕产妇病例进行评审。其评审内容包括对危重孕产妇从孕产期医疗保健、入院至出院的全过程进行回顾性分析,尽可能获得完整的孕产期医疗保健服务信息,分析发现孕产期医疗保健服务和管理中存在的问题,提出改进措施,并评估其改进效果。危重孕产妇评审需要循环往复地进行,以总结经验、吸取教训,规范孕产期医疗保健和产科服务流程,提高医务人员对危重孕产妇预测、早期识别、干预和救治能力,改善产科服务质量。危重孕产妇评审已被公认为是分析产科服务标准的工具,但是制定产科服务标准,一直是个难题。
2011年,WHO出版了Evaluating the Quality of Care for Severe Pregnancy Complications: the WHO Near-Miss Approach for Maternal Health[38]。该书详细介绍了危重孕产妇诊断标准、评价方法及其干预措施执行情况、监测方法,提出了危重孕产妇相关的产科质量评价指标体系。危重孕产妇诊断标准、评价方法主要包括以下4个步骤。①基线评估:基于临床危重孕产妇诊断标准,对危重孕产妇、服务提供者和管理人员进行调查;②现状分析:通过危重孕产妇评价,识别和改善医疗保健及服务的关键点和缺陷;③多方面制定和实施改善危重孕产妇医疗服务质量的干预措施;④再次评价:对实施干预措施后的医疗保健服务持续改进现状进行再评价分析,调整、制定并实施新的干预措施及远期行动计划,以持续改进医疗保健服务。
开展危重孕产妇评审,应注意以下问题。①监测与评价互为一体,评价是监测的一个重要环节,评价与监测相结合,才能有效促进产科服务质量持续改进;②危重孕产妇是存活下来的"幸运者",访谈危重孕产妇"幸存者"十分重要,可获得常被临床忽略的医疗保健服务信息;③危重孕产妇的诊断依据,应均来自于医疗机构,不能以社区提供资料为依据;④可以建立医疗机构、地区或国家级危重孕产妇评审专家库。
危重孕产妇或孕产妇死亡监测与评价,目的均为提高产科服务质量,改进孕产妇保健水平,是一个循环往复和螺旋式上升过程,包括病例确定、数据收集、信息分析,根据分析结果提出行动建议和效果评估。监测与评价的最终目的,绝不是简单统计危重孕产妇或孕产妇死亡病例数或计算发生率,而是提出改进措施和计划,并制定行动纲领,不断完善孕产妇医疗保健服务,提高产科质量。产科医务人员需要更新产科服务理念,强化"每一次妊娠都可能发展成为高危妊娠""每一次分娩可能都面临产科出血危险"的意识;改善孕产期医疗保健的可及性和可利用性,预防和降低高危妊娠发生,及时识别、规范管理高危妊娠,降低危重孕产妇发生率,改善针对孕产妇的公共卫生服务,不断提高医务人员现场急救与转诊服务能力;规范管理危重孕产妇,加强县级医院医疗急救能力和围生医学中心服务能力建设,不断提高危重孕产妇救治水平,提高危重孕产妇死亡比,降低MMI,防控孕产妇死亡。规范填报危重孕产妇及孕产妇死亡病例情况报告,及时开展危重孕产妇及孕产妇死亡评价,提出危重孕产妇救治持续改进计划和行动建议。
MMR是衡量一个国家和地区社会、经济、文化发展的重要指标。加强危重孕产妇管理和救治体系建设,动态监测危重孕产妇发生率、危重孕产妇死亡比,执行危重孕产妇监测与评价制度,分析孕产妇医疗保健及产科服务薄弱环节,制定持续改进方案和行动计划,前移孕产妇死亡防控关口,可再次促进MMR显著下降。期待我国早日制定危重孕产妇应急管理指南,不断建设和完善危重孕产妇应急管理及救治体系,有效提高危重孕产妇急救工作效率和质量,为切实降低MMR、践行《"健康中国2030"规划纲要》打下坚实基础。



























