
探讨葡萄糖激酶调节蛋白(GCKR)基因rs780094(C>T)多态性与妊娠期糖尿病(GDM)发病风险的相关性。
选择2013年2月至2016年7月,于西北妇女儿童医院妇产科就诊的252例孕妇为研究对象。其中127例为GDM孕妇,纳入GDM组;125例为健康孕妇,纳入对照组。收集2组孕妇的相关临床资料及实验室检测结果。GCKR基因rs780094(C>T)多态性基因型频率,采用实时荧光定量PCR法进行检测。采用成组t检验,对2组孕妇人体质量指数(BMI),总胆固醇(TC)、高密度脂蛋白胆固醇(HDL-C)、低密度脂蛋白胆固醇(LDL-C)、尿素浓度,以及总蛋白、白蛋白水平进行比较。采用Mann-Whitney U检验,对2组孕妇空腹血糖、75 g口服葡萄糖耐量试验(OGTT) 2 h血糖、三酰甘油、肌酐、尿酸浓度进行比较。采用χ2检验,对2组孕妇的妊娠期高血压疾病发生率、有糖尿病家族史所占比例,以及GCKR基因rs780094(C>T)多态性基因型、等位基因频率进行比较。本研究遵循的程序符合2013年修订的《世界医学协会赫尔辛基宣言》的要求,并与所有孕妇签署临床研究知情同意书。2组孕妇年龄等一般临床资料比较,差异均无统计学意义(P>0.05)。
①与对照组孕妇相比较,GDM组孕妇BMI、妊娠期高血压疾病发生率、有糖尿病家族史所占比例及空腹血糖、75 g OGTT 2 h血糖、三酰甘油、尿酸浓度均显著升高,而总蛋白、白蛋白水平及肌酐、尿素浓度均显著降低,并且差异均有统计学意义(t=-8.087,χ2=7.280、135.428,Z=-2.752、-3.764、-4.657、-2.631,t=5.957、11.810,Z=2.389,t=6.528;P<0.05)。②GDM组和对照组孕妇GCKR基因rs780094(C>T)多态性基因型频率分布,均符合Hardy-Weinberg平衡定律(χ2=0.758、P=0.685, χ2=1.440、P=0.487)。在共显性模型下,GDM组孕妇GCKR基因rs780094(C>T)多态性CC、CT、TT基因型频率分别为50.4%(64/127)、37.8%(48/127)、11.8%(15/127),对照组分别为34.4%(43/125)、54.4%(68/125)、11.2%(14/125),2组比较,差异有统计学意义(χ2=7.589、P=0.022);在显性模型下,GDM组孕妇CC、CT+TT基因型频率分别为50.4%(64/127)、49.6%(63/127),对照组分别为65.6%(82/125)、11.2%(14/125),2组比较,差异亦有统计学意义(χ2=6.956、P=0.010)。对照组T等位基因频率为38.4%(96/250)。
携带GCKR基因rs780094(C>T)多态性C等位基因的孕妇发生GDM的风险升高。因本研究纳入样本量相对较小,GCKR基因rs780094(C>T)多态性与GDM发病风险的相关性,尚需更多大样本、前瞻性随机对照研究结果证实。

版权所有,未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别申明,本刊刊出的所有文章不代表中华医学会和本刊编辑委员会的观点。
本刊为电子杂志,以光盘形式出版。本册应读者需求按需印刷,随光盘免费赠阅。光盘如有质量问题,请向编辑部调换。
妊娠期糖尿病(gestational diabetes mellitus,GDM)是指妊娠期首次发生和发现的不同程度的糖代谢异常[1]。GDM可增加母体、胎儿及新生儿不良结局发生风险。GDM与2型糖尿病(type 2 diabetes mellitus,T2DM)具有相同的病理学和遗传特征[1]。与T2DM相似,GDM亦为多基因综合征,并且一些单核苷酸多态性(single nucleotide polymorphism,SNP)与GDM的发生、发展密切相关[2]。葡萄糖激酶(glucokinase,GCK),己糖激酶(hexokinase,HK)-4、-D,三磷酸腺苷(adenosine triphosphate),以及己糖磷酸激酶(D-hexose 6-phosphotransferase)均为葡萄糖代谢的重要调节酶,可催化胰岛β细胞和哺乳动物肝细胞葡萄糖磷酸化,作为葡萄糖的"传感器",调节胰岛释放胰岛素与合成糖原的功能。在肝细胞中,GCK的催化活性由相对分子质量为68 000的葡萄糖激酶调节蛋白(glucokinase regulatory protein,GCKR)或GCK调节因子HK-4调节[3]。在机体糖代谢正常时,GCK在肝细胞核内与其抑制蛋白GCKR结合,葡萄糖浓度升高,导致GCK-GCKR复合物解离,促使GCK转移至细胞质内,促进肝细胞葡萄糖磷酸化,胰岛β细胞释放胰岛素与合成糖原[4],而GCK则转变为无活性的GCKR。
GCKR最初表达于肝细胞,由位于染色体2p23的GCKR基因编码[5]。GCK基因突变可影响GCKR表达,进而导致机体葡萄糖代谢异常。由于GCK参与糖尿病发生,GCKR与GCK关系密切,因此GCKR基因多态性亦为糖尿病相关候选基因之一。GCKR基因rs780094(C>T)多态性与机体三酰甘油浓度增高、代谢综合征具有显著相关性[6]。文献报道,GCKR基因rs780094(C>T)多态性T等位基因与特定人群的T2DM易感性呈负相关关系[7];而其C等位基因与T2DM发病风险呈正相关关系[8]。本研究对GCKR基因rs780094(C>T)多态性与GDM发病风险的相关性进行评估,旨在探讨GDM可能的发病机制,为临床防治该病提供参考。现将研究结果报道如下。
选择2013年2月至2016年7月,于西北妇女儿童医院妇产科就诊的252例孕妇为研究对象。其中,127例为GDM孕妇,纳入GDM组;125例为健康孕妇,纳入对照组。GDM组孕妇年龄为(31.9±6.4)岁,对照组为(30.6±4.7)岁。本研究遵循的程序符合2013年修订的《世界医学协会赫尔辛基宣言》的要求,并与2组孕妇均签署临床研究知情同意书。2组孕妇年龄等一般临床资料比较,差异均无统计学意义(P>0.05)。
本研究孕妇纳入标准:①孕龄为24~32孕周;②孕前无糖尿病史,GDM诊断均符合美国糖尿病学会推荐的GDM诊断标准[9];③年龄为18~41岁。排除标准:①合并严重妇科疾病、消化系统疾病或内分泌系统疾病;②既往有癌症史或重要脏器疾病史。
本研究252例孕妇均于孕龄为24~28孕周时进行75 g口服葡萄糖耐量试验(oral glucose tolerance test,OGTT)。根据美国糖尿病协会推荐的GDM诊断标准,空腹及OGTT 1 h、2 h血糖临界值分别为5.1 mmol/L(920 mg/L)、10.0 mmol/L(1 800 mg/L)与8.5 mmol/L(1 530 mg/L),若孕妇上述任意一项检测结果达到或超过临界值,即被诊断为GDM[9]。
采集2组孕妇的年龄、妊娠期高血压疾病、糖尿病家族史及人体质量指数(body mass index,BMI)等临床资料。
采集2组孕妇空腹外周静脉血各10 mL,均分别采用乙二胺四乙酸二钾抗凝,置于-20 ℃条件下保存、备用。
取上述备用血液样本3 mL,采用常规试验方法对空腹血糖,总胆固醇(total cholesterol,TC),高密度脂蛋白胆固醇(high density lipoprotein cholesterol,HDL-C),低密度脂蛋白胆固醇(low density lipoprotein cholesterol,LDL-C),三酰甘油,肌酐,尿素,尿酸浓度,以及总蛋白、白蛋白水平等生化指标进行检测。另取备用血液样本2 mL,采用酶联免疫法测定1,5-脱水葡萄糖醇(1,5-anhydro-D-glucitol,1,5-AG)浓度。再另取备用血液样本2 mL,采用免疫比浊法测定GDM组孕妇糖化血红蛋白(glycosylated hemoglobin,HbA1c)水平。
另取备用血液样本3 mL,采用盐析法从全血中提取DNA。将提取的DNA样本含量调节至20 ng/μL,并采用NanoDrop分光光度计(美国Thermo公司)检测DNA纯度,于波长为260 nm和280 nm处,分别测定DNA吸光度值(A),若A260/A280为1.8~2.0,则说明提取的DNA样本纯度较高,可用于后续GCKR基因rs780094(C>T)多态性基因型检测。采用7500 Fast TM Real-Time PCR系统(美国Thermo公司)实时荧光定量PCR法,进行GCKR基因rs780094(C>T)多态性基因型检测。PCR反应体系为:3.0 μL预混合溶液(含DNA聚合酶、Mg2+、缓冲液等),0.1 μL SNP基因分型试剂,1.9 μL超纯水,1.0 μL基因组DNA(20 ng/μL)),共计6.0 μL。PCR反应条件为:60 ℃预变性1 min;95 ℃变性10 min,1个循环,95 ℃预变性15 s,45个循环;60 ℃退火2 min,60 ℃延伸30 s。PCR法基因分型检测结果准确率≥98%。GCKR基因rs780094(C>T)扩增引物序列为:正向引物5′-TCTCTGAGTCCTTCCATATT-AG-3′,反向引物5′-GCAGTGGCACAATCTAGG-3′。
本研究数据采用SPSS 17.0统计学软件包进行处理。采用Ssize软件,估算满足本研究统计检验的最小样本量。首先,采用Kolmogorov-Smirnov检验,对本研究计量资料是否符合正态分布进行检验;采用Levene检验对2组计量资料的方差齐性进行检验。对于呈正态分布且方差齐性的计量资料,如孕妇年龄、BMI,1,5-AG、TC、HDL-C、LDL-C、尿素浓度,以及总蛋白、白蛋白水平等,采用 ±s表示,2组比较,采用成组t检验;对于呈非正态分布的计量资料,如孕妇空腹血糖、75 g OGTT 2 h血糖、三酰甘油、肌酐、尿酸浓度,采用M(P25~P75)表示,2组比较,采用Mann-Whitney U检验。对2组孕妇GCKR基因rs780094(C>T)多态性基因型频率分布进行Hardy-Weinberg平衡检验,评估其是否符合Hardy-Weinberg平衡定律。对于2组孕妇妊娠期高血压疾病发生率、有糖尿病家族史所占比例,以及GCKR基因rs780094(C>T)多态性CC、CT、TT基因型和C、T等位基因频率等计数资料,采用率(%)表示,组间比较,采用χ2检验。所有统计学检验采用双侧检验,以P<0.05表示差异有统计学意义。
±s表示,2组比较,采用成组t检验;对于呈非正态分布的计量资料,如孕妇空腹血糖、75 g OGTT 2 h血糖、三酰甘油、肌酐、尿酸浓度,采用M(P25~P75)表示,2组比较,采用Mann-Whitney U检验。对2组孕妇GCKR基因rs780094(C>T)多态性基因型频率分布进行Hardy-Weinberg平衡检验,评估其是否符合Hardy-Weinberg平衡定律。对于2组孕妇妊娠期高血压疾病发生率、有糖尿病家族史所占比例,以及GCKR基因rs780094(C>T)多态性CC、CT、TT基因型和C、T等位基因频率等计数资料,采用率(%)表示,组间比较,采用χ2检验。所有统计学检验采用双侧检验,以P<0.05表示差异有统计学意义。
与对照组孕妇相比较,GDM组孕妇BMI、妊娠期高血压疾病发生率、有糖尿病家族史所占比例及空腹血糖、75 g OGTT 2 h血糖、三酰甘油、尿酸浓度,均显著升高;而总蛋白、白蛋白水平及肌酐、尿素浓度,均显著降低,并且差异均有统计学意义(P<0.05)。2组孕妇1,5-AG、TC、HDL-C、LDL-C浓度分别比较,差异均无统计学意义(P>0.05)。GDM组孕妇HbA1c值为5.6%(5.3%~5.9%)。2组孕妇相关临床资料及实验室检测结果比较,见表1。
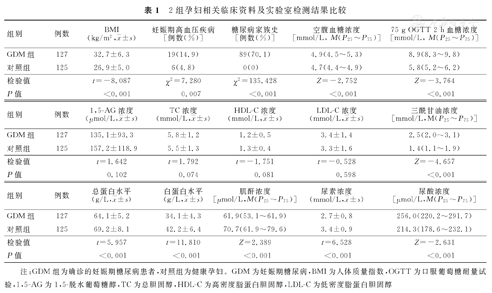
2组孕妇相关临床资料及实验室检测结果比较
2组孕妇相关临床资料及实验室检测结果比较
| 组别 | 例数 | BMI(kg/m2, ±s) ±s) | 妊娠期高血压疾病[例数(%)] | 糖尿病家族史[例数(%)] | 空腹血糖浓度[mmol/L, M(P25~P75)] | 75 g OGTT 2 h血糖浓度[mmol/L, M(P25~P75)] |
|---|---|---|---|---|---|---|
| GDM组 | 127 | 32.7±6.3 | 19(14.9) | 89(70.1) | 4.9(4.5~5.3) | 8.9(8.3~9.8) |
| 对照组 | 125 | 26.9±5.0 | 6(4.8) | 0(0) | 4.7(4.4~4.9) | 5.8(5.2~6.2) |
| 检验值 | t=-8.087 | χ2=7.280 | χ2=135.428 | Z=-2.752 | Z=-3.764 | |
| P值 | <0.001 | 0.007 | <0.001 | <0.001 | <0.001 |
| 组别 | 例数 | 1,5-AG浓度(μmol/L, ±s) ±s) | TC浓度(mmol/L, ±s) ±s) | HDL-C浓度(mmol/L, ±s) ±s) | LDL-C浓度(mmol/L, ±s) ±s) | 三酰甘油浓度[mmol/L,M(P25~P75)] |
|---|---|---|---|---|---|---|
| GDM组 | 127 | 135.1±93.3 | 5.8±1.2 | 1.2±0.5 | 3.4±1.4 | 2.5(2.0~3.1) |
| 对照组 | 125 | 157.2±118.9 | 5.5±1.3 | 1.3±0.4 | 3.3±1.6 | 1.4(1.1~1.9) |
| 检验值 | t=1.642 | t=1.792 | t=-1.751 | t=-0.528 | Z=-4.657 | |
| P值 | 0.102 | 0.074 | 0.081 | 0.598 | <0.001 |
| 组别 | 例数 | 总蛋白水平(g/L, ±s) ±s) | 白蛋白水平(g/L, ±s) ±s) | 肌酐浓度[μmol/L,M(P25~P75)] | 尿素浓度(mmol/L, ±s) ±s) | 尿酸浓度[μmol/L,M(P25~P75)] |
|---|---|---|---|---|---|---|
| GDM组 | 127 | 64.1±5.2 | 34.1±4.3 | 61.9(53.1~61.9) | 2.7±0.8 | 256.0(220.2~291.7) |
| 对照组 | 125 | 69.2±8.1 | 42.2±6.4 | 70.7(61.9~79.6) | 3.4±0.9 | 214.3(178.6~232.1) |
| 检验值 | t=5.957 | t=11.810 | Z=2.389 | t=6.528 | Z=-2.631 | |
| P值 | <0.001 | <0.001 | <0.001 | <0.001 | <0.001 |
注:GDM组为确诊的妊娠期糖尿病患者,对照组为健康孕妇。GDM为妊娠期糖尿病,BMI为人体质量指数,OGTT为口服葡萄糖耐量试验,1,5-AG为1,5-脱水葡萄糖醇,TC为总胆固醇,HDL-C为高密度脂蛋白胆固醇,LDL-C为低密度脂蛋白胆固醇
GDM组和对照组GCKR基因rs780094(C>T)多态性基因型频率分布,经Hardy-Weinberg平衡检验的结果显示,均符合Hardy-Weinberg平衡定律(χ2=0.758,P=0.685;χ2=1.440,P=0.487)。在共显性模型下,2组孕妇GCKR基因rs780094(C>T)多态性CC、CT、TT基因型分布频率比较,差异有统计学意义(P=0.022);在显性模型下,2组孕妇CC、CT+TT基因型频率比较,差异亦有统计学意义(P=0.010);而在隐性模型下,2组孕妇TT、CC+CT基因型频率比较,差异无统计学意义(P=0.879)。2组孕妇T等位基因频率比较,差异无统计学意义(P=0.069)。2组孕妇GCKR基因rs780094(C>T)多态性基因型和等位基因频率比较,见表2。
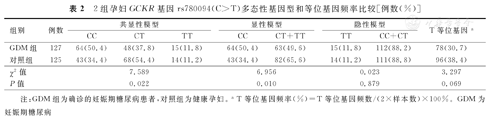
2组孕妇GCKR基因rs780094(C>T)多态性基因型和等位基因频率比较[例数(%)]
2组孕妇GCKR基因rs780094(C>T)多态性基因型和等位基因频率比较[例数(%)]
| 组别 | 例数 | 共显性模型 | 显性模型 | 隐性模型 | T等位基因a | ||||
|---|---|---|---|---|---|---|---|---|---|
| CC | CT | TT | CC | CT+TT | TT | CC+CT | |||
| GDM组 | 127 | 64(50.4) | 48(37.8) | 15(11.8) | 64(50.4) | 63(49.6) | 15(11.8) | 112(88.2) | 78(30.7) |
| 对照组 | 125 | 43(34.4) | 68(54.4) | 14(11.2) | 43(34.4) | 82(65.6) | 14(11.2) | 111(88.8) | 96(38.4) |
| χ2值 | 7.589 | 6.956 | 0.023 | 3.297 | |||||
| P值 | 0.022 | 0.010 | 0.879 | 0.069 | |||||
注:GDM组为确诊的妊娠期糖尿病患者,对照组为健康孕妇。a T等位基因频率(%)=T等位基因频数/(2×样本数)×100%。GDM为妊娠期糖尿病
GDM患者常伴有胰岛素抵抗,可导致胰腺代偿性释放胰岛素,从而导致体重增加。GDM发病风险随着孕妇BMI的增高而增加。肥胖孕妇分娩超重新生儿,选择剖宫产术分娩的几率,均较高正常体重孕妇高。本研究结果显示,GDM组孕妇妊娠期高血压疾病发生率为14.9%(19/127),高于文献报道的5%~10%[10];GDM组孕妇有糖尿病家族史者占70.1%(89/127),显著高于对照组,并且差异有统计学意义(P<0.05)。这提示,有糖尿病家族史的孕妇更容易发生GDM,并且巨大儿娩出率增高。
本研究GDM组孕妇空腹血糖浓度为4.5~5.3 mmol/L(正常参考值为3.89~6.10 mmol/L),HbA1c值为5.3%~5.9%(正常参考值为<6.5%),这2项指标均在正常参考值范围内,说明本研究GDM患者血糖控制较好。1,5-AG作为餐后高血糖标志物,其浓度变化提示机体血糖波动情况。当机体处于高血糖状态下,葡萄糖竞争性抑制肾小管重吸收1,5-AG,导致1,5-AG随着尿液大量排出,而血液中1,5-AG浓度降低,因此1,5-AG浓度可以敏感反映机体葡萄糖排泄及分泌情况[11]。文献报道,GDM孕妇1,5-AG浓度低于健康孕妇,并且GDM孕妇1,5-AG浓度在妊娠期波动较小[12]。本研究中,GDM组孕妇1,5-AG浓度虽然低于对照组,但是2组比较,差异无统计学意义(P>0.05),究其原因,仍需扩大样本量进一步研究、证实。
妊娠期脂类代谢变化,可保证胎儿生长的营养需求。本研究结果显示,GDM组和对照组孕妇TC、HDL-C、LDL-C浓度分别比较,差异均无统计学意义(P>0.05);GDM组三酰甘油浓度,显著高于对照组(2.5 mmol/Lvs 1.4 mmol/L),差异有统计学意义(P<0.001)。GDM可导致机体血脂异常及持续性胰岛素抵抗[13,14,15]。本研究2组孕妇均无肾病临床表现,或血清肌酐值>1.4 mg/dL(1 mg/dL=88.4 μmol/L)。GDM组孕妇肌酐浓度为53.1~61.9 μmol/L(正常参考值为70.7~106.1 μmol/L),尿素浓度为3.7~4.9 mmol/L(正常参考值为2.0~7.1 mmol/L)。相对于对照组,GDM组孕妇总蛋白和白蛋白水平均明显下降,尿酸浓度明显增高,但是无临床意义。
本研究中,GDM组孕妇GCKR基因rs780094(C>T)多态性T等位基因频率为30.7%,对照组为38.4%,分别与日本GDM孕妇、健康孕妇T等位基因频率相似[16],均较美国白种人群中GDM孕妇、健康孕妇T等位基因频率增高[17],而均较芬兰[18]、巴西[19]GDM孕妇、健康孕妇T等位基因频率显著降低,这可能与种族差异有关。芬兰人群中,GCKR基因rs780094(C>T)多态性C等位基因携带者的GDM发生风险,是T等位基因携带者的1.25倍[18]。
一项对GCKR基因rs780094(C>T)多态性的研究结果显示,C等位基因携带者三酰甘油浓度升高,二者具有明显相关性[20]。本研究结果显示,GDM组三酰甘油浓度显著高于对照组,并且差异有统计学意义(P<0.05)。本研究未探讨GCKR基因rs780094(C>T)多态性与三酰甘油的相关性,尚待后续研究、证实。对中国人群GCKR基因rs780094(C>T)多态性T等位基因频率的研究结果显示,肥胖或T2DM与三酰甘油浓度增高相关[21];中国汉族人群C等位基因携带者T2DM发病风险,是T等位基因携带者的1.22倍[22]。
本研究结果显示,在共显性模型下,GDM组孕妇GCKR基因rs780094(C>T)多态性CC、CT、TT基因型频率比较,差异有统计学意义(P<0.05);而在显性模型下,2组孕妇CC、CT+TT基因型频率比较,差异亦有统计学意义(P<0.05),并且GDM组孕妇CC基因型频率均显著高于对照组。这提示,携带GCKR基因rs780094(C>T)多态性C等位基因,可使孕妇发生GDM的风险增加。GCK可使葡萄糖磷酸化,达到控制肝脏清除葡萄糖的目的。GCKR可适应性调节肝脏清除葡萄糖。然而,目前GCKR基因rs780094(C>T)多态性对GCKR表达的作用,尚未确定[22]。Sparsø等[23]研究结果显示,GCKR基因rs780094(C>T)多态性与其他基因连锁不平衡,可影响机体葡萄糖或三酰甘油浓度。因本研究纳入样本量相对较小,GCKR基因rs780094(C>T)多态性与GDM发病风险的相关性,尚需更多大样本、前瞻性随机对照研究结果证实。






























