
类器官是一种可体外培养的简化的三维微型器官,可衍生自干细胞,或者来源于器官成熟细胞,具有自我更新和组织能力,能一定程度再现其来源组织的结构和功能,且可在长期的体外培养中维持结构和基因组的稳定性。以类器官技术为核心,建设生物样本活库,开发高保真的类器官疾病模型,结合基于3D生物影像多参数分析的药物表型筛选,将大大支持临床疾病新靶标发现、新药筛选与先导优化以及作用机制研究等,加速临床精准诊疗进程,缩短新药研发周期。

本刊版权归人民卫生出版社有限公司所有。任何机构或个人欲转发本刊图文,请与本刊联系。凡未经授权而转载、摘编本刊文章者,本刊将保留追究其法律责任的权利。
随着人类疾病谱的不断演化和人民对健康需求的日益提高,尤其是包括医学模式在内的医学科学飞速发展,通过科技创新引领临床医学水平的整体提高将成为未来医学发展的新模式。转化医学研究是将临床与基础研究有机融合的内核。基于数字网络技术的生物大数据应用、基于干细胞与先进制造技术的再生医学研究、基于高通量分析与细胞重编程技术的个性化药物研发、基于基因编辑与细胞治疗技术的基因治疗、基于分子影像智能分析与数字导航的智能手术管理等先进的医学模式越来越依赖于生命科学、材料学、人工智能等交叉学科的融合与发展。全球多个国家已将"推动实验室发现用于临床治疗的转化研究"作为国家医学研究的重要发展战略。通过转化医学,我们希望能从临床获得患者的基因、细胞或组织,经过实验室的研究,提供给患者或者医生精准的诊断和个性化治疗的策略。这构成了临床问题驱动的、从临床来源的问题回归到临床应用的研究范式,即临床问题驱动型研究(clinic driven research,CDR)范式。
CDR范式下多学科融合发展,转化研究团队从临床所面临的痛点问题出发,开展多学科融合的研究。临床医生发现或精准地提出重要临床问题,由科学家、工程学家、社科学家和人文学家等用知识体系与技术对接融合,凝练关键科学或技术问题、发起研究、进行共识立项、沟通协作和应用评价,开展系列策略和方法研究,最终目的是实现患者受益。基于以上理念,从基础研究到临床应用,或者从临床问题到基础研究,再回馈给临床应用,这样的过程被称为健康产品导向型(bedside to bench to clients,BBC)研究模式,见图1。
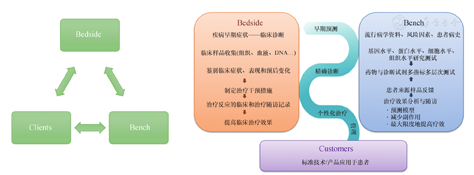

注:Bedside,临床;Clients,患者;Bench,基础;Customers,客户。
肝脏疾病发生发展过程是细胞损伤与再生不断抗衡的过程,当细胞再生修复战胜了损伤,实现有序重构,就可以实现细胞恢复正常功能,如果重构失败,可能发展为肝纤维化,如果再生不足,会发展为肝衰竭,如果过度失控地增殖,有可能发展成肿瘤。从细胞,到局部环境,到系统环境,这些不同层次、尺度、时空维度的再生修复关键细胞与分子事件及其调控网络等,构成了再生修复过程的关键信息,解码这些信息是揭示再生修复机制、寻找有效干预策略的关键瓶颈,也是当前再生修复研究的前沿。健康人群、肝脏疾病患者人群从器官水平到组织、细胞、蛋白、基因水平,多维实时获取组织或基因信息,进行分析、数据融合、模型预测及风险模型建立,最终回归到生物水平和临床水平的验证和应用,形成了当代肝脏转化科学研究的新范式。
利用肝脏的干细胞与类器官培养技术,可以制备成多种肝病模型,用于精准评价药物的安全性、有效性,并针对患者建立个性化诊断和治疗的指导模型。类器官是由干细胞在体外培养时形成的微型自组装的三维组织,可以复制其体内来源器官的许多特异性结构和功能。类器官的这一特性在肿瘤生物学研究领域得到了重大应用,并且被Nature Methods期刊评为2017年生物科技领域"年度技术"。过去肿瘤生物学研究利用的体外模型,如细胞系、小鼠模型都存在着不能完全模拟体内肿瘤特性、研究周期长、成本高昂、无法进行高通量实验等局限性。利用类器官培养技术获取的患者来源的肿瘤类器官(patients derived organoids,PDOs)恰恰在这些方面具有优秀的特性。近年来,利用患者来源的肿瘤类器官进行的肿瘤研究报道逐渐增加,受到了医学界广泛的关注。
2018年2月在Science期刊刊登的研究报道指出,患者来源的肿瘤类器官与患者肿瘤组织具有组学一致性(90%)。利用肿瘤类器官测试出的药物敏感性数据可以非常准确地预测实际临床患者的药物敏感性(敏感性:100%;特异性:93%;阳性预测值:88%;阴性预测值:100%)。2022年6月8日,美国众议院通过修订法案,针对《联邦食品、药品和化妆品法》(21 U.S.C.355)药物开发相关条款进行重要调整,首次将器官芯片和微生理系统作为独立的药物非临床试验评估体系纳入法案,器官芯片和细胞模型、计算机建模以及动物模型等视为同等重要的研究手段。7月15日,美国食品药品监督管理局批准赛诺菲的全球首个基于"器官芯片"研究获得临床前数据的新药(NCT04658472)进入临床试验,该研究利用诱导性多能干细胞分化形成的运动神经元和施万细胞构建两种罕见神经疾病慢性炎症性脱髓鞘性多发性神经病和多灶性运动神经病芯片模型,研究描述的药效数据支持新药临床试验申请。2021年起我国正式从科研和监管层面系统性推进类器官技术发展,2021年1月28日,科技部下发《关于对"十四五"国家重点研发计划"数学和应用研究"等6个重点专项2021年度项目申报指南征求意见的通知》,把"基于类器官的恶性肿瘤疾病模型"列为"十四五"国家重点研发计划中首批启动重点专项任务。2021年11月,国家食品药品监督管理局药品审评中心首次将类器官列入《基因治疗及细胞治疗的验证指南》基因治疗产品非临床药理学研究。今年7月,我国首个类器官指导肿瘤精准药物治疗的专家共识面世。
利用类器官生物模型,在深厚的干细胞生物学和疾病模型建立的背景知识基础上,我们开发了基于类器官多参数细胞影像的高内涵分析标准化流程,已开发多个疾病领域高保真的人源类器官疾病模型,结合基于人工智能+高内涵成像技术的药物表型筛选,能够快速产生海量可靠的实验数据。通过标准化筛选工作流程和生物图像分析以及结合人工智能深度学习的大数据挖掘,支持靶标发现、新药筛选、先导优化和作用机制的研究,大幅节约新药研发全周期费用、时间和降低临床风险,加速先导化合物从早期发现向临床阶段的快速推进。
在清华大学的支持下,北京清华长庚医院建立了临床生物样本资源中心,标准化生物样本库既是基础研究和临床研究的源头,又是实现分子诊断、标志物及药物靶点大样本验证、快速实现转化及个性化精准医疗的关键环节。所承建的临床生物样本资源中心具备以下六方面的特点:①集约化,高标配、自动化、高度安全、信息化的样本储存场地;②标准化,珍惜样本、执行标准、充分应用、维护产权;③特色化,充分考虑地域特色与学科特色,以点带面,拉动医院样本库整体建设与发展;④价值化,共享与充分应用机制;⑤资源化,统一的标准化流程、质量控制体系、安全保障体系,统一标准端口的信息化管理体系;⑥学科化,注重"样本学科"建设与学科、学术、技术带头人的培养。
类器官作为一种特殊的生物样本,可以冻存和复苏,我们着力建设类器官生物样本活库,自主搭建了全流程类器官生物样本智能管理系统,把类器官活库与临床信息对接,整个流程从样本的采集、分发进行全生命周期的追踪,到类器官构建的全过程追踪,再到类器官传代、共存、复苏和出库的追踪,出库交接后全程记录患者个性化的药物敏感性测试以及合作研究,让患者来源的类器官活库,能够得到更高效和科学地应用。从医生诊断到术中拍照、获取标本、获取病理/活组织,到管理病理/活组织水平的整套工作流程,基于生物样本的智能闭环管理系统(图2)为下游转化研究奠定了很好的基础。把基于类器官和测序的药敏实验结果、组织病理学实验结果和分子影像结果的科研数据,和临床患者的基本信息、医嘱系统、病理系统、手术系统、检验系统、诊断系统、影像系统对接,构建全生命周期的类器官生物样本精细化管理,见图3。
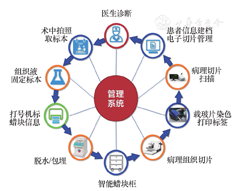

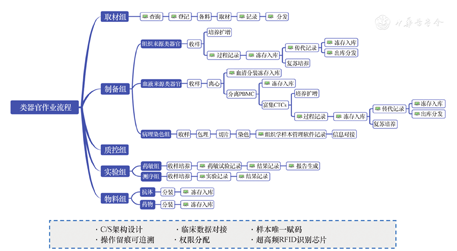

注:PBMC,外周血单个核细胞;CTCs,循环肿瘤细胞;RFID,射频识别。
系统解析肝脏生理病理微环境是批量化、规模化、标准化生产类器官的前提条件。目前常用的基质胶包埋、悬浮培养或气液交接培养成本均非常高昂,改进目前通用的类器官培养方法则可以降低成本,打破技术壁垒和垄断局面。我们拥有具有自主知识产权的脱细胞肝脏生物支架制备技术,可在最短时间内获取具有生物活性的可溶性因子和不溶性支架共存的肝脏微环境支撑材料,其可用于支持肝脏或肝脏肿瘤的类器官的悬浮或包埋培养,提供肝脏组织特异性的微环境。采用定量蛋白质组学对脱细胞生物基质支架进行定量解析和生物信息学分析,进一步优化类器官的培养条件。分析脱细胞肝脏,获取其充分必要条件和更加精简的小分子或细胞外基质成分,构建条件明晰的有利于肝脏或肿瘤的类器官培养的微环境。这样就可以批量化、规模化和标准化地制备肝脏或肝胆肿瘤的类器官。
截至目前,我们已经构建了病毒性肝炎导致的肝损伤、代谢性肝损伤、化学性肝损伤的类器官模型,并且已经用于药物测试及生理情况比对,旨在获得更多有价值的靶点信息。除此之外,把规模化培养起来的类器官放置于96孔板、384孔板里,将不同药物组合,不同药物作用时间之后所致的肝脏损伤进行多参数可视化影像学检测,通过该体系设置可量化的评价指标,系统分析某些药物在特定剂量或特定组合下,发生的肝损伤或者肝毒性的情况及其可能的机制,寻找可能引起肝毒性的分子特定结构,指导进行改构和全新的药物分子的测试和研发。在该思想指导下,研究人员已经成功地找到了1种可以替代肝毒性比较强的用于治疗抑郁症的药物替代分子,目前已进入Ⅱ期临床试验研究。
此外,针对肝胆肿瘤,开展基于多组学大数据与类器官技术相结合的肝胆肿瘤转化研究(图4),目前通过收集胆管癌患者胆汁脱落细胞可成功培养肿瘤类器官,进行药物敏感性、个性化测试。研究人员在临床研究中,采用患者类器官进行多轮药物的筛选、评价以及免疫细胞评价,可以为患者提供精准的治疗指导方案,并在胆管癌患者出现耐药后,提供协同用药方案,我们已经验证拉帕替尼与吉西他滨在人表皮生长因子受体2阳性胆管癌中的协同作用,为实现患者获益提供了新的治疗方案。
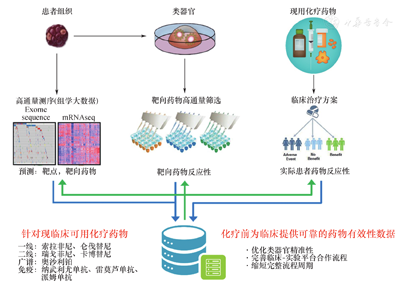

注:Exome sequence,外显子组序列;mRNAseq,mRNA序列;Adverse Event,不良反应;No Benefit,无获益;Benefit,获益。
从临床获得病史、风险因素、临床症状、临床检查、临床影像、临床样品、治疗方案、治疗效果和治疗后随访等资料,在实验室进行多维度的研究,如多组学数据、早期诊断标志物、类器官培养、类器官影像资料、高通量药物筛选、细分患者亚群、验证靶点和药物、血清循环肿瘤细胞DNA监测等,再回归到指导临床,这样的范式将大大推动患者最大化获益的实现。未来我们还可以结合更多学科,具象临床问题,获得更多的可视化、可量化的数据,快速高效地指导患者精准治疗,有效提高肿瘤的早期诊断率、临床治疗效果,构建可推广的合作模式。类器官生物样本活库的建设意义在于帮助研究者理解、诊断、治疗和预防那些可能影响当代甚至后代的疾病,其建设不是一蹴而就、一劳永逸的,我们需要一步一个脚印地打牢基础,加强国内国外相关从业人员之间的经验交流,共同解决发展中的问题,推动标准化智能化建设,助力临床转化。



























