
探讨卡培他滨在标准化辅助治疗后的早期三阴性乳腺癌患者中的临床疗效及安全性。
回顾性收集2015年9月至2022年6月期间于华中科技大学同济医学院附属同济医院就诊的早期三阴性乳腺癌患者资料,根据标准化辅助治疗后是否服用卡培他滨(节拍治疗1年),分为卡培他滨组(78例)及对照组(82例),主要研究终点为无进展生存期(progression-free survival,PFS),随访记录服药期间的安全性数据,包括不良反应及生活质量评分。
共入组160例患者,中位随访46个月,观察到28例复发事件,其中卡培他滨组4例,对照组24例。卡培他滨组PFS生存获益明显高于对照组(HR=0.32,95%CI:0.15~0.70,P=0.029)。卡培他滨相关的常见不良事件是骨髓抑制、手足综合征、肝功能异常。生活质量评分量表结果显示,两组无明显差异(P>0.05)。
在接受标准化辅助治疗的早期三阴性乳腺癌患者中,卡培他滨节拍化疗,与对照组相比,具有较显著的生存获益;不良反应较轻,生活质量未见明显下降。

本刊版权归人民卫生出版社有限公司所有。任何机构或个人欲转发本刊图文,请与本刊联系。凡未经授权而转载、摘编本刊文章者,本刊将保留追究其法律责任的权利。
2020年全球癌症流行病学数据提示,乳腺癌取代肺癌,成为全球第一大癌。三阴性乳腺癌(triple-negative breast cancer,TNBC)是指雌激素受体(estrogen receptor,ER)、孕激素受体(progesterone receptor,PR)以及人表皮生长因子受体2(human epidermal growth factor receptor 2,HER-2)表达缺失的乳腺癌亚型。由于无法从内分泌治疗及传统抗HER-2靶向治疗中获益,放疗和化疗仍是标准的治疗方案。对于早期可手术TNBC,术后化疗多采用以蒽环和紫杉醇类药物的方案,持续6~8个周期。根据术后病理情况给予辅助放疗,后进入临床观察阶段。为进一步提升TNBC的治愈率,研究者们对术后辅助治疗或强化治疗进行了一系列探讨与研究。其中在卡培他滨疗效的探索中,诸如FinXX[1],USO01062[2],GEICAM-COBOMA[3],GEICAM/2003-10[4]等研究均表明,在化疗中加入/序贯卡培他滨,TNBC患者有不同程度的生存受益。在本项研究中,我们观察了在早期乳腺癌标准化辅助治疗后采用卡培他滨节拍化疗的有效性和安全性,以期为未来三阴性乳腺癌的后续治疗提供证据支持。
选取2015年9月至2022年6月于华中科技大学同济医学院附属同济医院就诊的TNBC患者作为研究对象。纳入标准:①女性,术前病理结果为浸润性乳腺导管癌,ER、PR核染色阳性率<1%,HER-2评价采用美国临床肿瘤学会和美国病理学家学会推荐的评分系统判定[5];②根据美国癌症联合委员会(AJCC 2018,第八版)[6]分期标准,患者为T1~3N0~3M0期早期/可手术乳腺癌;③接受标准治疗,包括改良根治性乳房切除术或保乳手术,均行含蒽环[多柔比星(adriamycin,A)、表柔比星(epirubicin,E)等]、烷化剂[环磷酰胺(cyclophosphamide,C)等]、紫杉类[紫杉醇(toxol)、多西他赛(docetaxel)等,简称T]和/或铂类(Pt,简称P)化疗(AC/EC×4周期+T×4周期、AC/EC×4周期+TP×4周期)酌情序贯放疗;④有完整的临床数据。排除标准:①术前接受新辅助治疗的患者;②合并有其他原发性恶性肿瘤;③未完整执行上述标准化疗方案;④在后续随访中失访。研究对象的基线特征通过医院的电子病历系统收集,随访通过门诊复查、住院检查以及电话接收患者反馈来实现。本观察性研究已获得华中科技大学同济医学院附属同济医院伦理委员会批准(TJ-IRB20230386)。
记录每例患者的发病年龄、手术方式、病理类型、放化疗方案;根据是否服用卡培他滨分为卡培他滨组和对照组。其中,卡培他滨给药方案为0.5g(1片),口服,每日3次,持续口服满1年。随后,及时记录患者住院、门诊复诊结果及数据。后期根据乳腺癌随访要求执行定期复查,直到疾病进展。治疗过程中出现手足综合征、骨髓抑制、肝功能损害等不良反应时,根据患者耐受性调整剂量及用药周期,必要时终止用药。
本研究的主要终点为无进展生存期(progression-free survival,PFS),定义为手术起始到疾病进展或死亡的时间。安全性方面:不良反应根据CTCAE 5.0标准执行并记录;同时采用乳腺癌患者生命测定量表采取网络问卷/面谈指导的形式,评估生活质量情况[7]。
所有统计分析和图表均使用SPSS(26.0版)及GraphPad Prism(9.0.0版)进行。符合正态分布的定量资料采用( ±s)来描述,不符合正态分布的定量资料采用M(P25,P75)来描述,定性资料采用例数和构成比来描述。用Kaplan-Meier法绘制生存曲线来分析PFS,采用log-rank法进行单因素分析。对于两组连续性变量采用独立样本t检验,并通过F检验行方差齐性分析。
±s)来描述,不符合正态分布的定量资料采用M(P25,P75)来描述,定性资料采用例数和构成比来描述。用Kaplan-Meier法绘制生存曲线来分析PFS,采用log-rank法进行单因素分析。对于两组连续性变量采用独立样本t检验,并通过F检验行方差齐性分析。
在2015年9月至2022年6月期间,经过筛选排除,共入组患者160例,其中卡培他滨组78例,对照组82例。其中,因不良反应,有3例减量(减量至1片,每日2次),2例停药。两组患者、疾病和治疗的基线特征无明显差别(表1)。大多数患者接受过乳房切除术(80.6%),辅助化疗方案以EC序贯T方案化疗居多(94.4%)。
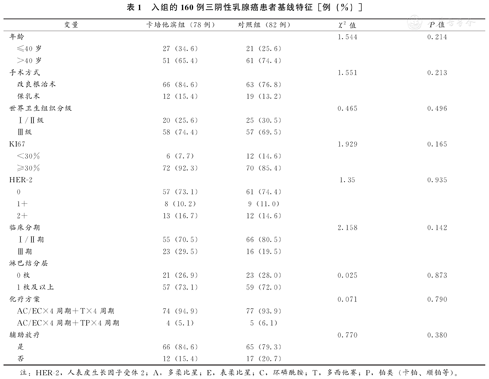
入组的160例三阴性乳腺癌患者基线特征[例(%)]
入组的160例三阴性乳腺癌患者基线特征[例(%)]
| 变量 | 卡培他滨组(78例) | 对照组(82例) | χ2值 | P值 |
|---|---|---|---|---|
| 年龄 | 1.544 | 0.214 | ||
| ≤40岁 | 27(34.6) | 21(25.6) | ||
| >40岁 | 51(65.4) | 61(74.4) | ||
| 手术方式 | 1.551 | 0.213 | ||
| 改良根治术 | 66(84.6) | 63(76.8) | ||
| 保乳术 | 12(15.4) | 19(13.2) | ||
| 世界卫生组织分级 | 0.465 | 0.496 | ||
| Ⅰ/Ⅱ级 | 20(25.6) | 25(30.5) | ||
| Ⅲ级 | 58(74.4) | 57(69.5) | ||
| KI67 | 1.929 | 0.165 | ||
| <30% | 6(7.7) | 12(14.6) | ||
| ≥30% | 72(92.3) | 70(85.4) | ||
| HER-2 | 1.35 | 0.935 | ||
| 0 | 57(73.1) | 61(74.4) | ||
| 1+ | 8(10.2) | 9(11.0) | ||
| 2+ | 13(16.7) | 12(14.6) | ||
| 临床分期 | 2.158 | 0.142 | ||
| Ⅰ/Ⅱ期 | 55(70.5) | 66(80.5) | ||
| Ⅲ期 | 23(29.5) | 16(19.5) | ||
| 淋巴结分层 | ||||
| 0枚 | 21(26.9) | 23(28.0) | 0.025 | 0.873 |
| 1枚及以上 | 57(73.1) | 59(72.0) | ||
| 化疗方案 | 0.071 | 0.790 | ||
| AC/EC×4周期+T×4周期 | 74(94.9) | 77(93.9) | ||
| AC/EC×4周期+TP×4周期 | 4(5.1) | 5(6.1) | ||
| 辅助放疗 | 0.770 | 0.380 | ||
| 是 | 66(84.6) | 65(79.3) | ||
| 否 | 12(15.4) | 17(20.7) |
注:HER-2,人表皮生长因子受体2;A,多柔比星;E,表柔比星;C,环磷酰胺;T,多西他赛;P,铂类(卡铂、顺铂等)。
随访至2022年12月,中位随访46个月,共观察到28例患者病情复发,其中卡培他滨组4例,对照组24例,无死亡病例。卡培他滨组PFS生存获益明显高于对照组(HR=0.32,95%CI:0.15~0.70,P=0.029),如图1所示。
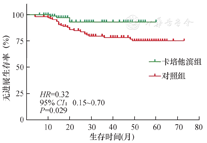

卡培他滨组发生骨髓抑制37例(47.4%),其次为手足综合征(18.0%),3级以上不良事件为骨髓抑制(3.8%)、转氨酶水平升高(1.3%)。卡培他滨组其他常见不良事件为包括胆红素升高(8.9%)、疲劳(6.4%)。对照组所有不良事件的严重程度为1级或2级(表2)。
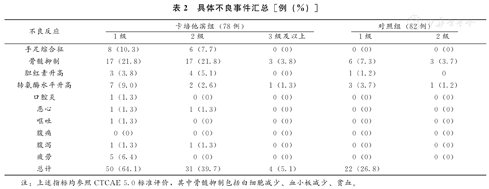
具体不良事件汇总[例(%)]
具体不良事件汇总[例(%)]
| 不良反应 | 卡培他滨组(78例) | 对照组(82例) | |||
|---|---|---|---|---|---|
| 1级 | 2级 | 3级及以上 | 1级 | 2级 | |
| 手足综合征 | 8(10.3) | 6(7.7) | 0(0) | 0(0) | 0(0) |
| 骨髓抑制 | 17(21.8) | 17(21.8) | 3(3.8) | 6(7.3) | 3(3.7) |
| 胆红素升高 | 3(3.8) | 4(5.1) | 0(0) | 1(1.2) | 0 |
| 转氨酶水平升高 | 7(9.0) | 2(2.6) | 1(1.3) | 3(3.7) | 1(1.2) |
| 口腔炎 | 1(1.3) | 0(0) | 0(0) | 0(0) | 0(0) |
| 恶心 | 1(1.3) | 1(1.3) | 0(0) | 0(0) | 0(0) |
| 呕吐 | 1(1.3) | 0(0) | 0(0) | 0(0) | 0(0) |
| 腹痛 | 0(0) | 0(0) | 0(0) | 0(0) | 0(0) |
| 腹泻 | 1(1.3) | 1(1.3) | 0(0) | 0(0) | 0(0) |
| 疲劳 | 5(6.4) | 0(0) | 0(0) | 0(0) | 0(0) |
| 总计 | 50(64.1) | 31(39.7) | 4(5.1) | 22(26.8) | |
注:上述指标均参照CTCAE 5.0标准评价,其中骨髓抑制包括白细胞减少、血小板减少、贫血。
根据乳腺癌患者生命测定量表评分标准,通过网络/面谈指导调查问卷的方式,实际发送调查问卷150份,卡培他滨组回收78份,对照组回收72份。具体分析见表3。可见在所有6个项目方差显著性值均大于0.10,故符合方差齐性,P值均大于0.05,提示两组乳腺癌患者生活质量评分差异无统计学意义。
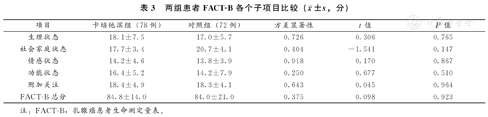
两组患者FACT-B各个子项目比较( ±s,分)
±s,分)
两组患者FACT-B各个子项目比较( ±s,分)
±s,分)
| 项目 | 卡培他滨组(78例) | 对照组(72例) | 方差显著性 | t值 | P值 |
|---|---|---|---|---|---|
| 生理状态 | 18.1±7.5 | 17.0±5.7 | 0.726 | 0.306 | 0.765 |
| 社会家庭状态 | 17.7±3.4 | 20.7±4.1 | 0.404 | -1.541 | 0.147 |
| 情感状态 | 14.2±4.6 | 13.8±3.9 | 0.918 | 0.170 | 0.867 |
| 功能状态 | 16.4±5.2 | 14.2±7.9 | 0.250 | 0.677 | 0.510 |
| 附加关注 | 18.4±4.9 | 18.3±4.1 | 0.643 | 0.045 | 0.964 |
| FACT-B总分 | 84.8±14.0 | 84.0±21.0 | 0.375 | 0.098 | 0.923 |
注:FACT-B,乳腺癌患者生命测定量表。
在这项基于真实世界的观察性研究当中,与安慰剂相比,在标准辅助治疗后采用卡培他滨节拍化疗作为维持治疗1年,显著提高无病生存率。且不良反应随访及生活质量评分情况,初步论证了卡培他滨的安全性。
卡培他滨是一种口服的氟尿嘧啶药物在体内经羧酸酯酶、胞苷脱氨酶和胸苷酸磷酸化酶作用下转变为有细胞毒性的氟尿嘧啶。由于肿瘤组织中胸苷酸磷酸化酶活性比在正常组织中高,故可更具有针对性地杀伤肿瘤细胞。由于卡培他滨的抗肿瘤活性与氟尿嘧啶的静脉持续输注相当,毒副作用低,且口服方便,故常作为维持治疗的选择[8]。节拍化疗作为晚期肿瘤常用的一种维持性治疗方案,不仅能发挥抗肿瘤血管生成,还可通过恢复外周血T细胞增殖,激活免疫效应细胞的细胞杀伤作用[9,10]。研究发现节拍化疗可以通过上调树突状细胞来刺激T淋巴细胞的增殖[11]。已有较多研究提示,节拍化疗在晚期乳腺癌、贲门癌等的治疗中获得肯定的疗效[12,13]。
SYSUCC-001研究[14]作为首个探索卡培他滨节拍治疗用于早期三阴性乳腺癌的随机前瞻性对照研究,具有重要的临床指导价值。该研究结果提示,在56.5个月的中位随访期间,卡培他滨组的5年DFS率明显优于对照组(83% vs.73%,HR=0.63;95%CI:0.42~0.96,P=0.027)[14]。本研究目前的结果和SYSUCC-001的总体一致,均显示了卡培他滨组的生存获益。但本研究与SYSUCC-001在如下方面存在差异。①研究治疗方案的差异:本研究选取了更为关注的特定人群,剔除了术前新辅助化疗的人群,同时辅助化疗方案限定为EC-T或EC-TP方案;另外,在卡培他滨剂量方面,SYSUCC-001研究为650mg/m2,每日两次。本研究考虑到患者耐受性,参考我国女性平均体表面积,借鉴其他卡培他滨节拍化疗文献[12],采用0.5g每日3次。本研究结果初步提示,这一剂量调整显著提升了患者依从性(本研究剂量调整率和停药率分别为3.8%和2.6%;SYSUCC-001研究分别为4.5%和16.7%)。②研究设计差异:SYSUCC-001为多中心大规模的前瞻性的随机对照试验,本研究为基于真实世界的回顾性分析。③研究结果的差异:本研究患者手足综合征、胆红素升高的发生率低于SYSUCC-001研究,可能跟上述研究方案中卡培他滨的剂量调整有关。④本研究新增了两组间的乳腺癌患者生命测定量表评分,通过对比研究,进一步验证了卡培他滨对患者生活质量的影响。
临床实践中,卡培他滨的手足综合征、血液毒性、肝毒性等不良反应较常见,故而限制了长期的维持化疗[15]。而采用低剂量节拍治疗的方案,绝大部分的患者可耐受。安全性研究提示,骨髓抑制、胆红素升高、手足综合征发生率较高,但少有3级以上情况发生;同时,卡培他滨的服用,并没有明显降低患者生命质量。
本研究尚有以下不足之处:①本研究随访时间相对不足,复发及死亡终点事件偏少;需要延长随访,获取更加准确的生存数据。②部分患者在当地医院诊治,难以保证不同医疗机构的临床指标判读的准确性,如胆红素、转氨酶、骨髓抑制等。③本研究为单中心回顾性分析,样本量偏少,可能存在组间信息不匹配,值得在未来开展大规模前瞻性随机对照研究,进一步探寻。
综上所述,在早期可手术三阴性乳腺癌患者标准化辅助治疗结束后,给予卡培他滨节拍治疗1年,本研究结果提示可提高患者无病生存率;且不良反应可耐受,生活质量未见明显下降。



























