
2020年1月到2021年3月采用腹腔镜下零缺血免缝合铥激光肾部分切除术治疗5例肾癌患者,其中男3例,女2例,年龄46~81岁,平均年龄66岁。5例患者均为体检影像学发现肾脏占位,均为单发肿瘤,左侧1例,右侧4例。肿瘤直径1.8~2.8 cm,平均直径2.2 cm。
5例患者均无不适,查体腹软,无压痛及反跳痛,双肾区无叩击痛,神经系统查体无异常。其中1例有开放性阑尾切除手术史,1例有腹腔镜胆囊切除手术史,腹部可见陈旧性手术瘢痕。
结合泌尿系统超声、肾脏血管造影进行临床诊断,最终依据病理免疫组化结果进行确诊。
5例患者均采用腹腔镜下铥激光肾部分切除术,无需进行动脉阻断,创面免缝合,完整切除肿瘤。手术时间90~115 min,平均手术时间103 min。术中切除肿瘤时间45~65 min,平均切除时间55 min,术中出血50~100 ml,平均75 ml,无输血、周围脏器损伤等严重并发症。术后病理提示肿瘤包膜完整,其中4例为透明细胞癌,1例为嫌色细胞癌。
术后恢复良好,术后随访6~18个月未见肿瘤复发。
泌尿外科

版权归中华医学会所有。本文为遵循CC-BY-NC-ND协议的开放获取文章。
随着腹腔镜技术经验的积累和器械的发展,腹腔镜下肾部分切除术得到了广泛应用[1]。对于传统的腹腔镜肾部分切除术,需要进行肾动脉阻断,同时采用肾实质缝合的方式进行创面的闭合和止血。如何减少热缺血时间和术中出血是目前手术面临的主要挑战。我们采用腹腔镜下零缺血免缝合铥激光肾部分切除术治疗5例肾癌患者,取得了满意的效果。
回顾性分析2020年1月到2021年3月我院采用腹腔镜下零缺血免缝合铥激光肾部分切除术治疗的5例肾癌患者临床资料,其中男性3例,女性2例;年龄46~81岁,平均年龄66岁。5例患者均无明显不适主诉,体检影像学发现肾脏占位,均为单发肿瘤,其中左侧1例,右侧4例。3例位于肾上极背侧,1例位于肾中极腹侧,1例位于肾下极腹侧。肿瘤直径1.8~2.8 cm,平均直径2.2 cm。肿瘤均局限于肾皮质,无淋巴结和远处转移,临床分期为T1aN0M0期。
所有患者入院后完善血常规、肾功能、肿瘤指标、心电图等术前检查,术前均行泌尿系统超声、肾脏血管造影或增强MRI检查,明确肿瘤大小、位置、肾血管及腹腔淋巴结情况(图1)。
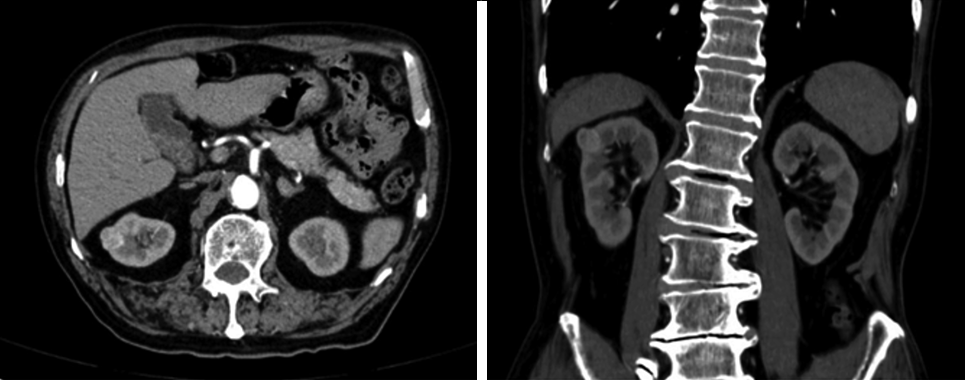

动脉期明显不均匀强化,考虑肾癌可能性大。双肾动脉双支型。周围脂肪间隙清晰,未见明显肿大淋巴结
因早期肾癌患者多无明显的临床表现,主要根据患者泌尿系统超声、肾脏血管造影等影像学表现进行临床诊断,并根据病理免疫组化结果确诊。肾癌常需要与肾血管平滑肌脂肪瘤、肾盂癌、肾囊肿等进行鉴别诊断。肾血管平滑肌脂肪瘤超声表现为高回声,CT表现为密度不均的肿块,含脂肪量较多,CT值为-90~-40 HU。肾盂癌CT表现肾盂肾盏不规则充盈缺损。单纯性肾囊肿超声表现为病变区无回声,囊壁光滑,边界清楚,当囊壁显示不规则回声或有局限性回声增强时,应警惕恶性病变。
患者在全麻下行腹腔镜下零缺血免缝合铥激光肾部分切除术。气管插管全麻,患者取健侧卧位,患侧腰部皮肤消毒铺巾,升高腰桥取折刀位,取十二肋下腋后线、肋缘下腋前线、髂脊上2 cm腋中线交叉点,分别置入直径12 mm、10 mm、10 mm的穿刺器,建立工作通道,注入CO2制备气腹,气腹压力14 mmHg,超声刀清除腹膜外脂肪,暴露肾周筋膜,剪开肾周筋膜及肾脂肪囊,游离肾动脉,肾动脉间隙留置橡胶管备用。使用铥激光(瑞科恩公司锋瑞1940 nm铥激光,
光纤500 μm,能量设置25~37.5 W,从肿瘤边缘5 mm的正常肾组织切开肾被膜,一直暴露至肾肿瘤假包膜,同时另一个操作孔使用吸引器进行钝性分离,寻找肿瘤包膜,然后沿着肿瘤包膜完整切除肿瘤。边切割边进行止血处理,肿瘤切除后仔细观察创面有无活动性出血,使用铥激光彻底止血。沿肋缘下将操作孔打开,将肾脏肿瘤完整取出(图2)。术野放置引流管腋前线伤口引出。
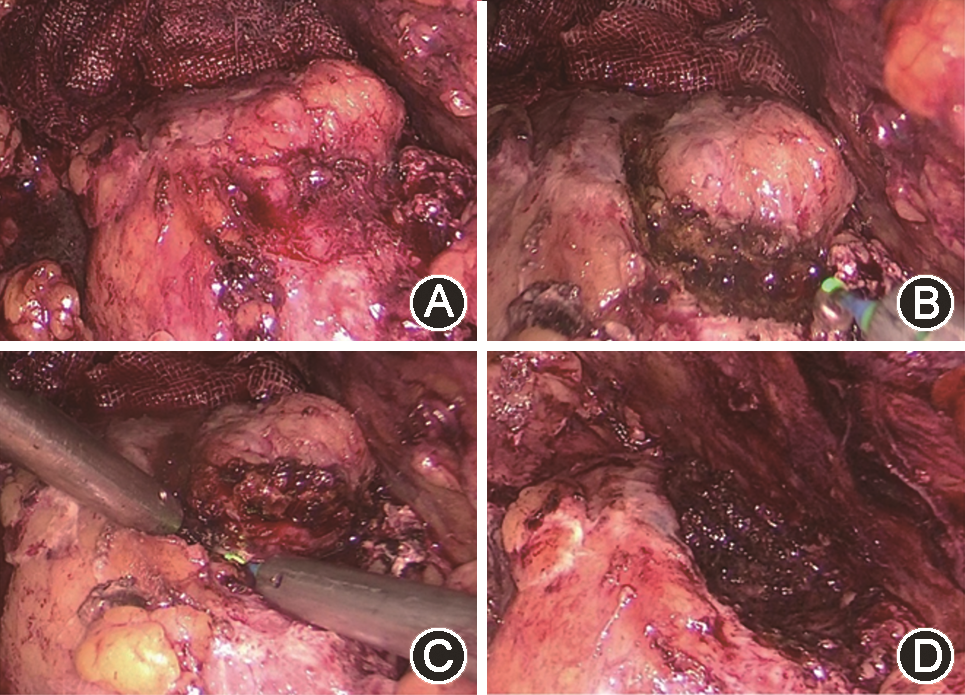

沿着肾被膜充分显露肿瘤;B:沿肿瘤边缘切开正常肾实质至肿瘤包膜;C:钝性分离沿肿瘤包膜完整切除肿瘤;D:切除后创面
5例患者手术均顺利完成,术中均未行肾动脉阻断,无需创面缝合,手术时间90~115 min,平均手术时间103 min。术中切除肿瘤时间45~65 min,平均切除时间55 min,术中出血50~100 ml,平均75 ml,无输血、周围脏器损伤等严重并发症。术后总引流量195~288 ml,平均引流量49~58 ml/d。所有患者术后2 d可缓慢开始床上活动,术后4~5 d拔除腰部引流管,术后7~10 d出院。术前术后血肌酐、尿素氮水平无明显变化。术后病理结果提示4例为透明细胞癌,1例为嫌色细胞癌,肿瘤包膜完整。随访6~18个月未见肿瘤复发,患者恢复良好。
近年来,随着医学影像学的发展以及人们健康意识的提升,早期肾癌的检出率越来越高,对于低分期的肾癌患者,特别是T1a期的患者,建议首先选择保留肾单位手术[2]。腹腔镜下肾部分切除术目前在临床已得到广泛开展[1]。传统的腹腔镜下肾部分切除术为了控制出血、保持清晰的操作视野常需要阻断肾动脉,从而造成肾脏缺血-再灌注损伤。尤其对于慢性肾功能不全的患者,在这些患者中,缺血组织形成低氧自由基在阻断血流5~8 min内就会导致肾实质进一步损坏[3]。传统肾部分切除术的技术关键在于肾脏创面的缝合,缝合时间较长会增加肾脏热缺血时间,缝合对深部肾实质血管切割导致肾部分萎缩,进而对术后肾功能恢复产生不利影响[4]。为了避免传统手术方式的不足,近年来国内外报道了一系列新技术减少热缺血时间、控制术中出血,包括肾动脉选择性分支阻断、控制术中血压、单极电凝免缝合技术、激光辅助免缝合技术,均取得了一定的效果[5, 6]。激光辅助肾部分切除术最早的临床病例可追溯到20世纪80年代[7],尽管初步结果令人鼓舞,但该技术一直未普及,直到近期由于激光广泛应用于泌尿系结石和前列腺增生的治疗,随着泌尿外科医师对激光技术的熟悉和进一步掌握,激光辅助肾部分切除术逐渐开展起来。
铥激光波长1 940 nm,位于水吸收峰值,汽化切割效率高,在组织中穿透深度浅,仅0.1~0.2 mm,组织切割更精准,同时可采用连续波模式,与钬激光相比有着同样的切割和止血能力,既能有效控制术中出血,又可以避免钬激光的爆破特性损伤深部肾脏实质,避免破坏肿瘤包膜[8]。Bui等[9]通过动物实验证实,铥激光浅穿透对剩余的肾实质造成了轻微的缺血性损伤,组织切割边缘组织学结构完全保留。1周后病理可见瘢痕清晰,厚度为0.2~0.6 cm,瘢痕下的组织结构得到很好的保存,没有广泛的组织坏死或炎症。
我们利用铥激光的特性,采用了腹腔镜下铥激光肾部分切除术治疗早期肾癌,临床效果满意。为了防止术中意外出血,我们常规解剖游离肾动脉后,可使用F6红色导尿管或橡胶管控制肾动脉,但未阻断。肾周组织必须完全游离充分,充分暴露肿瘤,便于切割方向调整。我们采用双吸引器自制操作器械,铥激光通过术者右手吸引器通道进行切割操作,左手利用吸引器进行钝性分离和吸引。同时左手吸引器由助手通过三通连接输液皮条,利用针筒进行生理盐水注射。左手吸引器可根据术者需要进行吸引和注水切换。切割时从肿瘤边缘5 mm的正常肾组织切开肾被膜,一直暴露至肾肿瘤假包膜,同时另一个操作孔使用吸引器进行钝性分离,寻找肿瘤包膜,然后沿着肿瘤包膜完整切除肿瘤。铥激光在切割肾组织的同时会形成一定的烟雾和组织碳化,对操作视野和切缘的判断造成影响。在切割的同时由助手沿着激光光纤路径的低压连续盐水灌溉,保证切割同时组织上有冲洗液体存在,可以较好地减少烟雾及组织焦痂形成,分辨切缘。术中应注意保证肿瘤包膜完整,以免术中冲洗液引起肿瘤扩散种植。
相对于传统的腹腔镜下肾部分切除术,该技术真正做到了零阻断、免缝合,减少了对正常肾实质的损伤,最大限度保护了患者的肾功能,术后恢复快,特别是对于高龄患者,可以尽量减少围手术期相关并发症;同时对于术者降低了手术操作难度,缩短了学习曲线。
综上,腹腔镜下零缺血免缝合铥激光肾部分切除术治疗早期局限性肾癌,能够减少肾脏热缺血时间,安全可行。
所有作者均声明本研究不存在利益冲突



























