
患者,女,51岁,家庭主妇。因"记忆力下降、精神行为异常5个月余"入院。入院前5个月余逐渐出现记忆力下降、反应迟钝,夜间入睡困难伴有幻觉、行走不稳。上述症状逐渐加重。期间抗感染、激素及丙球冲击无效。症状进一步加重至卧床,无法交流,伴四肢不自主活动。
嗜睡,反应迟钝,无法沟通,有喘鸣。四肢肌张力高,双上肢可见肌肉抽动,间断有双上肢空中抓取物品动作,静止时可见四肢不自主活动,四肢腱反射(+),双侧巴氏征阳性。
脑脊液及头颅MRI无特殊发现,18F-FDG-PET示全脑代谢减低,视频脑电图示未见典型生理性睡眠波,PRNP基因检测确诊。
对症治疗为主。
出院半年后死亡。
神经科

版权归中华医学会所有。本文为遵循CC-BY-NC-ND协议的开放获取文章。
家族性致死性失眠症(Familial fatal insomnia,FFI)是一种罕见的、致死性的遗传性朊蛋白病。该病为朊蛋白基因(PRNP基因)突变所致的常染色体显性遗传病,主要临床表现为睡眠障碍、自主神经功能异常、认知功能下降,并可伴有共济失调、锥体外系症状以及内分泌异常等表现。该病的临床症状常常为非特异性,异质性较大,因此对其早期临床症状的识别较为困难。我们报道该病1例,旨在提高对本病的认识,减少误诊和漏诊。
患者,女,51岁,家庭主妇。因"记忆力下降、精神行为异常5个月余"于2020年5月4日入院。2019年11月25日患者被人发现呼之不应,当地医院查血糖低,予以高糖推注后意识恢复。此后逐渐出现记忆力下降,反应迟钝,夜间入睡困难、行走不稳。不伴谵妄、激越表现,无抽搐等。当时生活尚能自理。上述症状逐渐加重,2020年1月出现不认识家人,独处情况下诉看到亲戚在房间内,行走需人搀扶。2020年2月下旬出现夜间发热,最高38.5℃,睡眠障碍及幻觉明显加重,并出现饮水呛咳。曾口服"利培酮"治疗,效果不佳。2020年3月下旬至当地医院就诊,考虑"脑炎",给予抗感染、糖皮质激素及丙种球蛋白冲击。病情仍继续进展,间断发热,最高39℃,完全不能行走和交流,出现四肢不自主活动。为进一步诊治至我院,以"认知行为异常待查"收入院。
起病以来,患者精神差,睡眠减少,饮食差,留置胃管,便秘,小便留置尿管,体力体重明显下降。
既往史:高血压病史,2019年10月发现糖尿病,规律服用降糖药物。无类似疾病家族史。
体格检查:嗜睡状态,反应迟钝,无法沟通,有喘鸣,查体欠配合。颅神经未见明显异常。四肢肌张力高,双上肢可见肌肉抽动,间断有双上肢空中抓取物品动作,静止时可见四肢不自主活动,四肢腱反射对称减低,双侧巴氏征阳性。脑膜刺激征阴性。
血常规、生化、甲状腺功能、Torch全套、血尿培养、PCT,免疫全套、IgG4、风湿全套、肿瘤全套等未见明显异常。脑脊液常规、生化、细菌真菌培养等未见异常,脑脊液IgG指数及寡克隆带未见明显异常。血清及脑脊液自身免疫性脑炎抗体谱阴性。血清副肿瘤抗体谱示抗Tr(DNER)抗体IgG(+),脑脊液副肿瘤抗体谱(-)。
胸部CT示肺部感染,全腹CT未见明显异常。头MRI+DWI+增强+MRA:双侧额叶及侧脑室后角点状缺血灶,DWI未见弥散受限,脑萎缩,增强未见明显强化,颅内血管未见狭窄(图1)。18F-FDG-PET示全脑代谢减低,以双侧额叶、颞叶为著(图2)。视频脑电图示未见典型睡眠生理性纺锤、顶尖波及K复合波,双侧半球散在棘波、尖波(图3)。PRNP基因检测示:PRNP基因存在D178N突变,并与129Met连锁,129基因为Met纯合子(图4)。
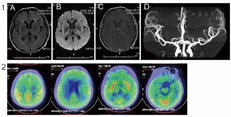

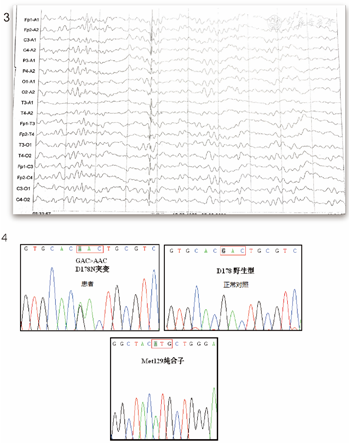

定位诊断:记忆力下降,伴有幻觉、睡眠障碍症状,PET示皮层代谢减低,脑电图显示尖波、棘波发放,提示大脑皮层受累;行走困难并伴有不自主运动,查体显示有不自主运动,四肢肌张力高,双侧巴氏征阳性,考虑定位于锥体系及锥体外系。综上,定位于大脑皮层及皮层下结构(锥体系与锥体外系)。
定性诊断:患者突出表现之一为快速进展性痴呆,因此按照VITAMINS原则进行定性诊断。首先,患者为非卒中样起病,且颅内未见梗死病灶与血管狭窄,排除血管性(V)病变;根据病史,可排除医源性/先天代谢性缺陷(I)以及系统性病变(S)。需考虑的定性包括:1.感染性(I):患者病程中发热,有皮层受累证据,支持感染性病变,但患者脑脊液未发现细胞数异常,MRI也未见病灶,且经历长时间抗病毒及抗生素治疗无效,不支持一般的病毒或细菌感染。2.中毒性和代谢性(T):代谢性疾病,如低血糖可致低血糖脑病,患者可出现意识障碍、认知功能下降等,该患者最初有低血糖病史,但患者整个病程中仅发现一次低血糖,且头MRI未见典型的低血糖脑病改变,不支持低血糖脑病;3.自身免疫性(A):患者亚急性起病,有认知功能下降、不自主运动等症状,血清中存在抗Tr抗体IgG阳性,不能除外自身免疫性脑炎,但患者头MRI未见皮层等处受累病灶,脑脊液该抗体阴性,且对糖皮质激素、丙球等免疫治疗反应差;4.转移瘤/肿瘤性(M):虽患者存在副肿瘤性脑炎可能,但患者经胸腹部CT以及全身PET-CT检查未发现肿瘤证据;5.神经变性(N):常见的神经变性性疾病,如额颞叶痴呆、多系统萎缩等疾病通常为慢性起病,并存在脑相应部位的萎缩,但该患者起病较急,进展快,头MRI未见相应的脑萎缩,不符合常见的神经系统变性病。上述特点提示患者的定性诊断有一定困难。总体而言,患者临床表现为快速进展性痴呆,皮层及锥体束、锥体外系均有受累,经抗感染及强有力免疫治疗病情仍持续进展,提示朊蛋白病可能。最终基因检测证实患者PRNP基因存在D178N突变,并与129Met连锁,129基因为Met纯合子,确诊为FFI。
鉴别诊断:
1.其他朊蛋白病,如家族性CJD、GSS等。朊蛋白病包括以下几种:Creutzfeldt-Jacob病(CJD)、FFI和Gertmann-Straussler-Scheinker综合征(GSS)等。CJD通常可见DWI皮层及尾状核头及丘脑等部位高信号,可呈现"缎带征"及"曲棍球征",典型的EEG表现为特异性周期性同步放电。该患者不具备上述典型表现。FFI的突出表现为睡眠障碍、认知下降、自主神经功能障碍等,与本例患者临床特点部分相符,但患者无明确家族史,自主神经障碍不突出。GSS主要表现为慢性、进行小脑共济失调和构音障碍,通常病程较长,可达2~10年,认知障碍出现较晚。该患者进展较快,且并非以小脑症状为突出表现。家族性CJD、FFI和GSS均为PRNP基因突变所致的常染色体显性遗传病,临床表现上可能存在重叠,但基因突变有所不同。家族性CJD密码子178突变,且密码子129为缬氨酸(Val129);FFI的PRNP基因为密码子178突变,而密码子129为蛋氨酸(Met129)[1];而GSS则主要为密码子102、105、117、145、198或217等的突变。PRNP基因检测可对朊蛋白病进行鉴别。
2.自身免疫性脑炎:自身免疫性脑炎可表现为急性或亚急性发作的认知下降、精神症状以及癫痫等症状,头MRI可显示皮层或相应部位的异常信号或强化等,血清及脑脊液中可检测到相应的自身抗体。一般激素、丙球等免疫治疗有效。该患者亚急性起病,认知功能下降,伴有不自主运动等,血清中存在抗Tr抗体IgG阳性,不能除外自身免疫性脑炎,但患者头MRI未见皮层等处受累病灶,脑脊液该抗体阴性,且对糖皮质激素、丙球等免疫治疗反应差,不支持。
3.神经系统变性病:额颞叶痴呆、路易体痴呆等。通常神经系统变性疾病为慢性起病的认知功能障碍,病程多长达数年,头部影像学表现为相应脑区的萎缩或低代谢等。该患者起病较急,进展迅速、病程短,不符合神经系统变性疾病的特点。
给予抗感染、抗精神症状以及对症治疗。
患者症状未有好转,家属完善检查后要求出院转回当地治疗,半年后患者死亡。
FFI是一种罕见的、致死性的朊蛋白病,绝大多数为遗传性,但亦有散发病例报道。作为一种常染色体显性遗传性朊蛋白病,FFI通常由位于第20号染色体短臂上的、编码朊蛋白的PRNP基因突变所致。PRNP基因的密码子178发生错义突变(GAC>AAC),导致天冬酰胺替换天冬氨酸(D178N),同时伴有密码子129蛋氨酸的多态性改变(Met129)(即D178N-129M)。PRNP基因突变使神经细胞产生异常的且具有蛋白酶K抗性的PrPSC,致使丘脑及大脑皮层神经元变性而致病。FFI的年发病率大约为百万分之一,无性别差异。据报道,我国FFI患者发病年龄为21~68岁,中位年龄46.5岁,病程为6~38个月不等。该疾病突出的临床表现为睡眠障碍,表现包括失眠、睡眠相关不自主运动以及喉部喘鸣等,可同时伴有快速进展性认知功能下降、精神症状、锥体系及锥体外系受累表现以及自主神经功能障碍等[2,3],其中睡眠障碍通常贯穿整个病程。患者除失眠表现外,可伴有睡眠相关呼吸困难。可出现睡眠中的自动行为、幻觉及生动梦境;睡眠相关不自主运动,如入睡抽动、频繁变换体位、四肢不自主运动等。但FFI睡眠相关症状较为多变,部分患者可不表现为失眠。既往的病例总结发现,PRNP基因密码子129的基因多态性与患者临床症状及病程有关。密码子129纯合型(Met/Met)者病程更短,起病症状多为睡眠障碍,且自主神经功能障碍突出;而129杂合型病程较纯合型长,多以共济失调和构音障碍起病,运动障碍和括约肌功能障碍较为明显,且强直性肌阵挛较为常见。多导睡眠监测可显示睡眠结构改变以及睡眠期不自主运动等,对本病有较大的提示意义[4]。本病的头部MRI、脑脊液检查正常,脑电图未见典型睡眠生理性纺锤、顶尖波及K复合波,对诊断有一定提示意义。18F-FDG-PET上丘脑的代谢减低为本病的特征性影像学改变[5],对于该疾病的诊断具有重要作用。而该病的确诊依赖于PRNP基因检测,若结果显示PRNP基因存在D178N突变且伴有129密码子蛋氨酸多态性改变即可确诊为FFI[2,6]。
本病例特点为亚急性起病,快速进展性痴呆,伴有睡眠障碍、精神症状及运动障碍,体格检查显示意识障碍、喘鸣、锥体束征及锥体外系症状,无明确代谢、感染证据,视频脑电图未见典型睡眠纺锤、K复合波,PET显示全脑代谢减低,常规对症、抗感染以及免疫治疗均无效。提示存在朊蛋白病如CJD的可能。然而,该患者的辅助检查如头DWI及脑电图并不符合CJD特征性表现。由于朊蛋白病有数种类型,彼此之间的临床表型可能存在交叉,应考虑除CJD外的朊蛋白病。虽然该患者并无明确的家族史,仍可行PRNP基因检测辅助诊断。该患者PRNP基因检测结果符合FFI基因突变,且129密码子为Met纯合,得以确诊。本例患者睡眠障碍贯穿了全病程,且病程较短(约11个月),但自主神经功能障碍并不突出,提示该疾病的临床异质性。PET的丘脑代谢减低为该病的早期特征性表现,但患者PET显示全脑代谢减低,可能与患者病程有关。
综上所述,以睡眠障碍为突出表现,伴有神经精神症状和自主神经功能障碍的患者,在排除其他疾病后应考虑到FFI的可能,无家族史并不能作为排除诊断的条件。对于考虑朊蛋白病的患者,PRNP基因检测具有重要的诊断和鉴别诊断价值。
所有作者均声明本研究不存在利益冲突



























