
患者,女性,25岁,主因"发现血糖升高1周"入院。患者1周前因肥胖拟行减重手术,术前检查发现糖化血红蛋白为8.7%,无"三多一少"症状。进一步检测空腹血糖8.0 mmol/L、随机血糖、空腹胰岛素、空腹C肽均升高。既往诊断高血压1年,血压最高160/90 mmHg(1 mmHg=0.133 kPa),未用药及监测。发现肝功能异常、高脂血症1年。否认冠心病、脑血管病、慢性肾脏病等。否认吸烟饮酒史。否认手术及输血史。否认食物及药物过敏史。家族中父母均患有T2DM及高血压,否认肥胖及其他家族史。
患者无明显尿中泡沫、视物模糊、手足麻木,无恶心、呕吐,无手套、袜套样改变,无间歇性跛行,无双下肢水肿,患者存在月经紊乱,无明显多毛及痤疮表现,精神、食欲及睡眠可,二便如常,体重无明显变化。
行实验室及辅助检查,肝功能:丙氨酸转氨酶418 U/L、天冬氨酸转氨酶208 U/L、γ-谷氨酰转移酶112 U/L、乳酸脱氢酶364 U/L、空腹胰岛素53.3 mU/L,空腹C肽5.46 μg/L,餐后2 h胰岛素63.50 mU/L,餐后2 h C肽6.55 μg/L;糖化血红蛋白8.7%、空腹血糖10.67 mmol/L,餐后2 h血糖15.45 mmol/L。结合病史及检查结果,考虑诊断为T2DM。
予患者利拉鲁肽每日早餐前1针皮下注射,以0.6 mg起始治疗,逐步增加至1.2 mg。
患者无不适反应,血糖控制明显改善,进食量减少,体重下降,月经恢复正常周期,肝功能和血脂均明显改善。
内分泌科

版权归中华医学会所有。本文为遵循CC-BY-NC-ND协议的开放获取文章。
利拉鲁肽是胰高糖素样肽-1(glucagon-like peptide-1,GLP-1)受体激动剂的代表药物之一,自2005年国际上第一个GLP-1受体激动剂成功上市,随着研发不断深入和循证医学证据的积累,该类药物在2型糖尿病(type 2 diabetes mellitus,T2DM)领域的应用价值逐渐受到重视。GLP-1受体激动剂属于肠促胰素类药物,目前已发现的人体内肠促胰素有两种,包括葡萄糖依赖性胰岛素释放肽和GLP-1,葡萄糖依赖性胰岛素释放肽因刺激胰岛素分泌作用微弱,应用价值有限,而GLP-1主要由回肠和结肠中的L细胞分泌,以葡萄糖浓度依赖性方式促进胰岛素分泌并降低胰高糖素分泌,参与机体血糖稳态调节。另外,GLP-1能减缓胃排空而增加饱腹感,从而导致能量摄入减少而减重。然而,人体内产生的GLP-1很快被二肽基肽酶4降解而失去活性,GLP-1受体激动剂通过结构修饰,保留原有的生物学效应,同时又不易被二肽基肽酶4降解,从而延长作用时间,更有利于血糖控制及降低体重[1]。利拉鲁肽为GLP-1代表药物之一,我们报道1例T2DM合并腹型肥胖的患者使用利拉鲁肽治疗后,血糖控制良好,体重减轻,代谢紊乱改善,期望对后续同类患者的治疗提供参考。
患者,女性,25岁,主因"发现血糖升高1周"入院。患者1周前因肥胖拟行减重手术,术前检查发现糖化血红蛋白为8.7%,无"三多一少"症状。进一步检测空腹血糖8.0 mmol/L(参考值:3.61~6.11 mmol/L),随机血糖11.9 mmol/L,空腹胰岛素49.4 mU/L(参考值:2.6~24.9 mU/L),空腹C肽5.67 μg/L(参考值:1.1~4.4 μg/L)。为进一步诊治收入中如友好医院普外代谢减重门诊。患者无明显尿中泡沫、视物模糊、手足麻木,无恶心、呕吐,无手套、袜套样改变,无间歇性跛行,无双下肢水肿,患者存在月经紊乱,无明显多毛及痤疮表现,精神、食欲及睡眠可,二便如常,体重无明显变化。既往诊断高血压1年,血压最高160/90 mmHg(1 mmHg=0.133 kPa),未用药及监测。发现肝功能异常、高脂血症1年。否认冠心病、脑血管病、慢性肾脏病等。否认吸烟饮酒史。否认手术及输血史。否认食物及药物过敏史。家族中父母均患有T2DM及高血压,否认肥胖及其他家族史。
入院查体:身高173 cm,体重120 kg,体重指数(body mass index,BMI)40.1 kg/m2,腰围113 cm,臀围120 cm。脉搏89次/min,血压150/80 mmHg(左=右)。神清,精神可。腹型肥胖,浅表淋巴结未触及肿大。甲状腺未触及肿大。心脏、肺、腹部查体无明显异常。双下肢无水肿。病理征未引出。双侧足背动脉搏动正常,双下肢痛觉、温度觉、振动觉正常,双侧10 g尼龙丝试验阴性。
实验室及辅助检查:(1)常规化验检查:肝功能:丙氨酸转氨酶418 U/L(参考值:0~40 U/L),天冬氨酸转氨酶208 U/L(参考值:0~42 U/L),γ-谷氨酰转移酶112 U/L(参考值:0~52 U/L),乳酸脱氢酶364 U/L(参考值:100~250 U/L);血脂:总胆固醇5.24 mmol/L(参考值:<5.20 mmol/L),甘油三酯1.44 mmol/L(参考值:<1.70 mmol/L),高密度脂蛋白胆固醇1.14 mmol/L(参考值1.00~2.20 mmol/L),低密度脂蛋白胆固醇3.5 mmol/L(参考值:低中危人群宜<3.50 mmol/L,高危人群宜<2.60 mmol/L,极高危人群宜≤1.80 mmol/L);尿酸539 umol/L(参考值:150~420 μmol/L),血常规、尿常规、粪常规、肾功能、电解质、同型半胱氨酸、心肌酶、甲状腺功能及甲状腺抗体均正常;腹部超声示脂肪肝;(2)糖尿病相关检查:胰岛素自身抗体、胰岛细胞抗体、抗谷氨酰脱羧酶抗体均阴性;空腹胰岛素53.3 mU/L,空腹C肽5.46 μg/L,餐后2 h胰岛素63.50 mU/L,餐后2 h C肽6.55 μg/L;糖化血红蛋白8.7%(参考值:4%~6%),空腹血糖10.67 mmol/L,餐后2 h血糖15.45 mmol/L(参考值:<7.84 mmol/L);尿糖及尿酮体均阴性,尿微量白蛋白135.28 mg/L,尿微量白蛋白/肌酐比值4.75 mg/mmol(参考值:<3.17 mg/mmol),24 h尿蛋白定量0.31 g(参考值:<0.16 g);(3)骨代谢相关指标:血钙磷正常,25-羟维生素D 27.30 ng/ml(参考值:缺乏<25 ng/ml,不足25~74 ng/ml,足够75~250 ng/ml),全片段甲状旁腺素正常;(4)妇科化验检查:血清睾酮2.62 nmol/L(参考值:0.35~2.6 nmol/L),促黄体生成激素/卵泡刺激素比值为2.28,雌二醇、催乳素正常;经阴道妇科B超:双侧卵巢多囊性改变,左右卵巢可见多个大小不等的暗区,每个切面大于10个,最大直径0.8 cm,卵巢实质部分回声稍强,余子宫形态大小、子宫内膜及肌层未见异常。
结合病史及检查结果,考虑诊断为T2DM。
患者为重度肥胖患者,存在高血压、高脂血症等多种心血管危险因素,同时合并脂肪肝、肝功能异常、多囊卵巢综合征等肥胖相关并发症,需积极治疗以延缓疾病损害以改善预后。患者重度肥胖,胰岛素抵抗严重,欲求能降低体重、改善胰岛素抵抗药物,因肝功能异常,口服降糖药物治疗相对受限,因此,新型降糖药物GLP-1受体激动剂可作为优选。予患者利拉鲁肽每日早餐前1针皮下注射,以0.6 mg起始治疗,逐步增加至1.2 mg。
患者无不适反应,血糖控制明显改善,进食量减少,体重下降,月经恢复正常周期,肝功能和血脂均明显改善(患者治疗方案及血糖监测见表1,患者治疗前后指标改善情况见表2),患者满意,遵嘱出院。
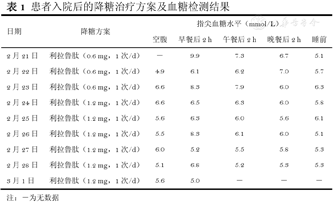
患者入院后的降糖治疗方案及血糖检测结果
患者入院后的降糖治疗方案及血糖检测结果
| 日期 | 降糖方案 | 指尖血糖水平(mmol/L) | ||||
|---|---|---|---|---|---|---|
| 空腹 | 早餐后2 h | 午餐后2 h | 晚餐后2 h | 睡前 | ||
| 2月21日 | 利拉鲁肽(0.6 mg,1次/d) | - | 9.9 | 7.3 | 6.7 | 5.1 |
| 2月22日 | 利拉鲁肽(0.6 mg,1次/d) | 4.9 | 6.1 | 6.2 | 7.0 | 5.7 |
| 2月23日 | 利拉鲁肽(0.6 mg,1次/d) | 6.6 | 8.3 | 7.9 | 6.0 | 6.3 |
| 2月24日 | 利拉鲁肽(1.2 mg,1次/d) | 6.6 | 6.5 | 6.3 | 6.0 | 5.8 |
| 2月25日 | 利拉鲁肽(1.2 mg,1次/d) | 5.6 | 6.3 | 6.0 | 5.6 | 6.1 |
| 2月26日 | 利拉鲁肽(1.2 mg,1次/d) | 5.5 | 8.3 | 6.1 | 6.0 | 5.1 |
| 2月27日 | 利拉鲁肽(1.2 mg,1次/d) | 6.0 | 5.2 | 5.5 | 5.8 | 5.3 |
| 2月28日 | 利拉鲁肽(1.2 mg,1次/d) | 5.1 | 6.8 | 5.2 | 5.3 | 5.3 |
| 3月1日 | 利拉鲁肽(1.2 mg,1次/d) | 5.6 | 5.0 | - | - | - |
注:-为无数据
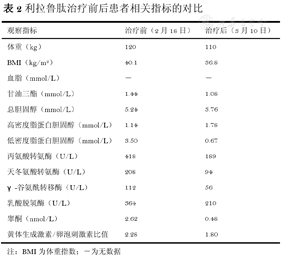
利拉鲁肽治疗前后患者相关指标的对比
利拉鲁肽治疗前后患者相关指标的对比
| 观察指标 | 治疗前(2月18日) | 治疗后(3月10日) |
|---|---|---|
| 体重(kg) | 120 | 110 |
| BMI(kg/m2) | 40.1 | 36.8 |
| 血脂(mmol/L) | - | - |
| 甘油三酯(mmol/L) | 1.44 | 1.08 |
| 总胆固醇(mmol/L) | 5.24 | 3.76 |
| 高密度脂蛋白胆固醇(mmol/L) | 1.14 | 1.78 |
| 低密度脂蛋白胆固醇(mmol/L) | 3.50 | 0.67 |
| 丙氨酸转氨酶(U/L) | 418 | 189 |
| 天冬氨酸转氨酶(U/L) | 208 | 94 |
| γ-谷氨酰转移酶(U/L) | 112 | 56 |
| 乳酸脱氢酶(U/L) | 364 | 210 |
| 睾酮(nmol/L) | 2.62 | 0.48 |
| 黄体生成激素/卵泡刺激素比值 | 2.28 | 1.80 |
注:BMI为体重指数;-为无数据
患者为青年女性,隐匿起病,多次测空腹血糖>7.0 mmol/L,随机血糖>11.1 mmol/L,糖化血红蛋白>6.5%,腹型肥胖,有糖尿病家族史,病程中无"三多一少"症状,无自发酮症酸中毒倾向,存在胰岛素抵抗,胰岛素自身抗体、胰岛细胞抗体、抗谷氨酰脱羧酶抗体均阴性,患者无急慢性胰腺炎、胰腺肿瘤、腹部创伤、胰腺切除、肾上腺疾病、甲状腺疾病等其他内分泌疾病,无特殊用药、病毒感染病史,可排除上述病因导致的特殊类型糖尿病。考虑为T2DM。同时,患者有腹型肥胖。腹型肥胖患者由于内脏脂肪的堆积,免疫细胞种类及数量发生变化,导致促炎和抗炎稳态失衡,大量脂肪因子和炎症因子释放,造成局部和全身炎症反应[2]。在这种炎症状态下,会激活活性氧、核转录因子、应激活化蛋白激酶等多条炎症通路,导致发生摄食异常、体重和内脏脂肪增加、胰岛素抵抗、粥样硬化斑块形成等,进而发生或加重代谢紊乱和心血管疾病[3,4]。因此,腹型肥胖无疑增加了糖尿病患病风险,同时,对于已诊断糖尿病的人群,内脏脂肪也显著增加了血糖控制难度,有数据显示,起始胰岛素治疗用量与内脏脂肪面积呈正相关,而与皮下脂肪无明显相关[5]。值得注意的是,亚洲人群与白种人相比,更容易出现内脏脂肪堆积,在同样腰围下,内脏脂肪更多[6],因此,在亚洲人群中通过腰围间接评估内脏脂肪含量,有可能低估潜在风险。
由上可知,对于2型糖尿病合并腹型肥胖人群,代谢紊乱和心血管疾病风险大大增加,对血糖控制目标需更加严格,GLP-1受体激动剂除降糖作用外,还能减轻体重和减少内脏脂肪含量,有利于更有效地控制血糖。利拉鲁肽作为GLP-1受体激动剂代表药物之一,与人类GLP-1存在97%的同源性,不仅通过促进胰岛素分泌而改善血糖,而且还有减缓胃排空和增加饱腹感的作用,进而减少能量摄入使体重减轻[7]。既往临床研究数据显示,应用利拉鲁肽不仅可显著改善血糖,而且可降低腰围,且基线腰围越大,缩小腰围效果越显著[8,9],最新的荟萃分析结果也提示,利拉鲁肽(3 mg,1次/d)可使体重平均减少4.9 kg,腰围平均减少3.5 cm,BMI平均减轻1.86 kg/m2,在BMI大于35 kg/m2的肥胖人群中,改善程度更加显著[10]。另外,一项随机对照研究发现,在同样减重幅度下,利拉鲁肽治疗与单纯生活方式干预相比,内脏脂肪明显减少,而皮下脂肪无差异[1]。利拉鲁肽LEAD-2研究研究比较了利拉鲁肽和格列美脲分别联合二甲双胍对减少内脏脂肪和皮下脂肪的差异,结果显示,利拉鲁肽在降低内脏脂肪方面更具优势[11]。除此以外,GLP-1受体激动剂的心血管保护作用也逐渐得到重视,2019年美国糖尿病协会指南指出,在合并动脉粥样硬化性心血管疾病或存在多项高危因素人群中,GLP-1受体激动剂因在心血管保护方面的优势,已跃居一线治疗[12]。综上可知,对于腹型肥胖且合并T2DM患者,利拉鲁肽可作为优选方案。
利拉鲁肽在应用过程中也简单方便,不良反应相对少,能更好提高患者依从性。利拉鲁肽为皮下针剂,为增加胃肠道耐受性,推荐起始治疗剂量为0.6 mg,可逐步加量至常规剂量1.2~1.8 mg,可每日1次任意时间皮下注射,无须根据进餐时间给药,但推荐每日固定时间给药,其引起低血糖风险相对低,常见不良反应为胃肠道反应,主要优势在于有明显改善体重和内脏脂肪作用,对心血管高危人群还具有保护作用,对于轻中度肝功能受损及非终末期肾病患者中也同样可以应用。利拉鲁肽可与其他口服降糖药物联合应用,可使血糖控制平稳且达标,引起低血糖风险相对低。对于通过二甲双胍、磺脲类药物和生活方式干预后血糖仍不达标,或动脉粥样硬化性心血管疾病高风险人群,或肥胖人群,建议应用GLP-1受体激动剂[12,13]。利拉鲁肽与二甲双胍联合治疗时,无须调整二甲双胍剂量,与磺脲类药物联用时,则应适当减少磺脲类药物剂量并短期增加自我血糖监测以降低低血糖风险[14]。在GLP-1受体激动剂中,仅利拉鲁肽和索马鲁肽被批准可作为减重药物,索马鲁肽减重效果更突出,平均体重可减轻9~16 kg,超过半数减重比例达10%~15%,利拉鲁肽则可减轻体重4~7 kg,超过半数减重比例达5%以上,而对于改善代谢紊乱及心血管保护作用,则利拉鲁肽更为突出[15]。
新型降糖药物的不断研发上市,为糖尿病诊疗提供了更多灵活便捷的治疗方案,利拉鲁肽作为GLP-1受体激动剂的代表药物之一,其不仅可有效控制血糖,而且也能减轻体重和减少内脏脂肪面积,同时具有心血管保护作用。在应用利拉鲁肽时,我们需要结合患者的年龄、肥胖程度、内脏脂肪含量、胰岛β细胞功能、糖尿病病程、血糖控制目标等具体情况,制定合理的个体化治疗方案。利拉鲁肽因其葡萄糖依赖性降糖作用,低血糖风险低,可以与多种降糖药物联合使用,同时适合肥胖及心血管高风险人群应用,每日1次皮下注射方案,有利于提高依从性,可作为患者居家治疗方案,可有效预防和延缓糖尿病及肥胖相关并发症,降低心血管疾病发生风险。
所有作者均声明本研究不存在利益冲突



























