
患者,男性,65岁,农民,因"胸痛2个月,加重3 d"于2021年10月29日入院。2个月前患者劳动后出现胸痛,为右侧胸胁区隐痛,咳嗽、深呼吸及活动时疼痛诱发,伴咳嗽、咳黄白色黏痰,相继于个体诊所和某民营医院就诊,予口服消炎、止痛药物和静脉注射头孢类抗生素治疗后症状缓解。3 d前患者劳动后上述症状再发并加重,伴畏寒、多汗和喘息,为进一步诊治收入院。
患者主要症状为右侧胸痛,与咳嗽、深呼吸和活动有关。肺部体征为右下肺呼吸音低,可闻及少量湿性啰音,左肺可闻及散在哮鸣音,未闻及胸膜摩擦音。
胸部增强CT示右肺下叶团块状影,考虑肺脓肿,伴脓胸形成;双肺下叶散在感染灶;右侧胸膜增厚,右侧胸腔积液,部分包裹;纵隔淋巴结肿大。右侧胸腔置管引流出脓性胸水约200 ml。
吸氧、抗感染、解痉平喘、止咳祛痰、补液、营养支持、补充白蛋白等对症治疗。行超声引导下胸腔穿刺术、CT引导下脓胸多点穿刺及置管引流术,术后反复用生理盐水和碳酸氢钠冲洗脓腔、尿激酶胸腔内注射。
患者经综合治疗后临床症状逐渐改善,血液炎症指标基本正常,住院26天后好转出院。2022年3月2日患者来院复诊,诉体重增加约5 kg,无明显不适,复查胸部CT示右下肺脓肿已吸收,双肺下叶遗留慢性感染、纤维化灶。
呼吸与危重症医学科;胸外科;全科医学科

版权归中华医学会所有。本文为遵循CC-BY-NC-ND协议的开放获取文章。
包裹性脓胸的处理方式包括抗感染治疗、影像引导置管引流和外科手术等。电视辅助胸腔镜手术对技术和设备要求较高,患者接受度偏低,目前在基层应用受限。本文报道1例支气管哮喘合并肺脓肿、多房包裹性脓胸的重症患者,肺泡灌洗液培养出铜绿假单胞菌,在给予抗感染和营养支持治疗的基础上,相继行超声引导下胸腔穿刺术、CT引导下脓胸多点穿刺及置管引流术,并反复进行脓腔冲洗,最终经内科综合治疗后痊愈。
患者,男性,65岁,农民,因"胸痛2个月,加重3 d"于2021年10月29日入院。
现病史:2个月前患者劳动后出现胸痛,为右侧胸胁区隐痛,咳嗽、深呼吸及活动时疼痛诱发,伴咳嗽、咳黄白色黏痰,无咯血、畏寒、发热,相继于个体诊所和某民营医院就诊,予口服消炎、止痛药物和静脉注射头孢类抗生素治疗后症状有所缓解。3 d前患者劳动后上述症状再发并加重,伴畏寒、多汗和喘息,为进一步诊治收入我科。患病以来精神、食欲、睡眠差,大小便无异常,体重减轻约3 kg。
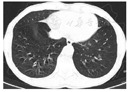
既往史:幼年时因外伤致右眼失明;17年前于重庆某医院诊断为"支气管哮喘",近年喘息、咳嗽症状时有反复,2年前于我科住院,胸部CT(图1)示双肺下叶少许感染、右侧胸膜稍增厚,间断吸入"硫酸沙丁胺醇吸入气雾剂"和"布地奈德福莫特罗粉吸入剂"。无高血压、糖尿病,无免疫系统疾病。

个人史:吸烟40余年,每天约20支;饮酒40余年,100~200 g/d;牙齿卫生差。
体格检查:体温36.6 ℃,脉搏80次/min,呼吸24次/min,血压120/70 mmHg(1 mmHg=0.133 kPa),指氧饱和度92%(吸氧2 L/min),神志清楚,营养中等,全身皮肤黏膜无黄染、出血、皮疹,浅表淋巴结未触及肿大。颈软,气管居中,甲状腺无肿大。右下肺呼吸音低,可闻及少量湿性啰音,左肺可闻及散在哮鸣音,未闻及胸膜摩擦音。心界无扩大,心率80次/min,律齐,各瓣膜区未闻及杂音。腹软,全腹无压痛及反跳痛,双下肢无水肿。四肢肌力、肌张力未见异常,病理征(-)。
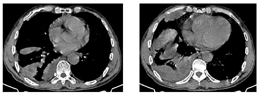
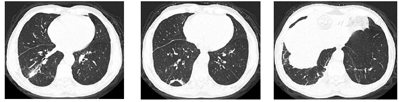
胸部CT(图2、图3):右肺下叶团块状影伴液化坏死,考虑感染(肺脓肿可能),不除外肿瘤;双肺下叶散在感染灶;右侧胸膜增厚,右侧胸腔积液,部分包裹;纵隔淋巴结肿大。床旁心电图:窦性心律,正常心电图。红细胞沉降率82 mm/h;血常规:白细胞计数22.66×109/L,中性粒细胞绝对值19.66×109/L,淋巴细胞绝对值0.72×109/L,嗜酸细胞绝对值0×109/L,血红蛋白121 g/L,中性粒细胞百分率86.8%;C反应蛋白343.78 mg/L;肝功能:谷丙转氨酶19 U/L,谷草转氨酶36 U/L,白蛋白38.7 g/L,前白蛋白93 mg/L,间接胆红素18.6 umol/L,直接胆红素13.7 umol/L,总胆红素32.3 umol/L;肾功能正常;血钠133.3 mmol/L;随机血糖7.87 mmol/L;凝血功能:纤维蛋白原降解产物5.5 μg/ml,血浆纤维蛋白原8.8 g/L,D-二聚体0.97 mg/L;血气分析(吸氧2 L/min):酸碱度7.47,氧分压81 mmHg,二氧化碳分压39.3 mmHg,剩余碱4.1 mmol/L,氧饱和度96.6%;降钙素原2.65 ng/ml;心肌梗死标志物、N-末端脑钠肽前体、肺肿瘤标志物、感染性疾病筛查未见异常;2019新型冠状病毒核酸阴性;常见呼吸道病原体抗体阴性;G试验阴性;痰涂片查结核、真菌阴性;痰、血培养阴性。

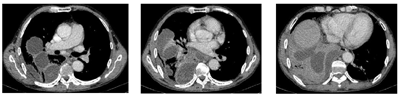
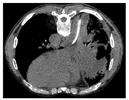
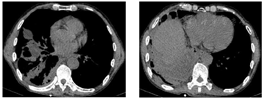
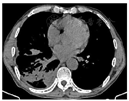
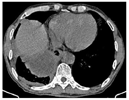
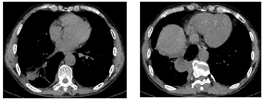
初步诊断:右下肺脓肿,右侧包裹性胸腔积液,支气管哮喘。给予头孢哌酮舒巴坦(3 g,1次/12h)静脉滴注抗感染,同时予吸氧、解痉平喘、止咳祛痰、补液、营养支持等对症治疗。为除外肿瘤和结核,于11月1日行支气管镜检查,见右肺下叶段支气管黏膜充血肿胀,可见散在黄褐色黏痰;在右肺上叶前段、右肺下叶行支气管肺泡灌洗。肺泡灌洗液涂片:上皮细胞≤10/LP、白细胞≥25/LP,G+杆菌1+,G—杆菌1+,查见少量G—双球菌,结核分枝杆菌复合群阴性,未查见抗酸杆菌和真菌。肺泡灌洗液培养:铜绿假单胞菌,对头孢哌酮舒巴坦敏感。复查红细胞沉降率94 mm/h;血常规:白细胞计数22.41×109/L,中性粒细胞绝对值19.07×109/L,淋巴细胞绝对值0.84×109/L,血红蛋白109 g/L,中性粒细胞百分率85.1%;C反应蛋白360.21 mg/L;降钙素原1.25 ng/ml。患者痰量较前增加,呈腥臭味,血液炎症指标仍高,联用克林霉素(0.6g,1次/8h)静脉滴注以覆盖厌氧菌,并再次送检痰培养,仍呈阴性。完善胸部彩超检查示:左侧胸腔肋膈角探及间距约1.3 cm无回声区,右侧胸腔探及范围约5.8 cm×10.8 cm液性暗区反射,其内可见蜂窝状稍强回声分隔,透声差;另于穿刺点处探及范围约6.6 cm×2.9 cm液性暗区反射,进针深度约2.8 cm;右肺组织内探及多处液性暗区反射,其内透声差,可见絮状低回声漂浮,较大范围约7.9 cm×4.9 cm;提示双侧胸腔积液(右侧包裹性),右肺超声所见考虑肺脓肿。因进针深度不够,床旁胸腔穿刺失败。于11月2日在超声引导下行胸腔穿刺术,胸水常规:深黄色、浑浊胸水,无凝块,白细胞总数45660 ×106/L,单个核细胞25%,多个核细胞75%,红细胞30×109/L,李凡他实验+++;胸水生化:白蛋白29.6 g/L,球蛋白25.6 g/L,总蛋白55.2 g/L,淀粉酶30 U/L,葡萄糖0.31 mmol/L,乳酸脱氢酶2427 U/L,腺苷脱氨酶72 U/L;胸水培养(需氧菌+厌氧菌)阴性。胸水检验结果支持脓胸。胸部增强CT(图4,图5,图6):右肺下叶团块状影,考虑肺脓肿,伴脓胸形成,建议治疗后复查除外肿瘤;双肺下叶散在感染灶,较前加重;右侧胸膜增厚,右侧胸腔积液,部分包裹;纵隔淋巴结肿大。

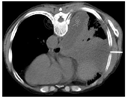
患者肺脓肿并多房包裹性脓胸诊断明确。于11月3日在CT引导下行包裹性脓胸穿刺(图7)及置管引流(图8)术。穿刺处胸水常规:深黄色、微浊胸水,无凝块,白细胞总数29×106/L,单个核细胞31%,多个核细胞69%,红细胞0×109/L,李凡他实验+;胸水生化:白蛋白25.5 g/L,球蛋白17.7 g/L,总蛋白43.2 g/L,淀粉酶40 U/L,葡萄糖7.01 mmol/L,乳酸脱氢酶556 U/L,腺苷脱氨酶17.91 U/L。胸水检验结果支持肺炎旁胸腔积液。置管处胸水常规:黄色、浑浊胸水,无凝块,白细胞总数100803×106/L,单个核细胞15%,多个核细胞85%,红细胞38×109/L,李凡他实验+++;胸水生化:白蛋白26.4 g/L,球蛋白23.6 g/L,总蛋白50 g/L,淀粉酶30 U/L,葡萄糖0.03 mmol/L,乳酸脱氢酶7020 U/L,腺苷脱氨酶130.15 U/L;胸水培养(需氧菌+厌氧菌)阴性;未查见抗酸杆菌。引流出脓性胸水约200ml(图9)。胸水检验结果支持脓胸。复查红细胞沉降率102 mm/h;血常规:白细胞计数11.9×109/L,中性粒细胞绝对值9.15×109/L,血红蛋白103 g/L,中性粒细胞百分率76.9%;C反应蛋白260.45 mg/L;肝功能:白蛋白33.5 g/L,直接胆红素26.2 umol/L,总胆红素32.4 umol/L,总胆汁酸17 umol/L;降钙素原0.69 ng/ml。予生理盐水和碳酸氢钠反复冲洗脓腔、尿激酶(1万U,1次/d)胸腔内注射,同时给予人血白蛋白静脉滴注以纠正低蛋白血症。复查胸部彩超提示右侧胸腔包裹性积液,积液黏稠,周围壁及分隔较厚。复查胸部CT(图10、图11)示:右肺上叶后段、右肺中叶及下叶多发感染并右肺下叶肺脓肿形成,右肺感染较前有所吸收;右侧胸腔引流术后,右侧胸腔积液、积脓较前吸收减少;右侧胸膜增厚。于11月8日再次在CT引导下行包裹性脓胸穿刺术。患者临床症状逐渐改善,11月17日复查红细胞沉降率96 mm/h;血常规:白细胞计数7.89 ×109/L,中性粒细胞绝对值4.53×109/L,血红蛋白104 g/L,中性粒细胞百分率57.4%;C反应蛋白25.75 mg/L;白蛋白40.8 g/L;降钙素原正常。11月22日复查胸部CT(图12,图13):右肺下叶见片状、不规则状密度增高影,部分可见液化坏死,较前片吸收好转;右肺底局限性包裹性积液;双肺下叶、右肺中叶感染;右侧胸膜弥漫性增厚,右侧胸腔包裹性积液;右侧斜裂少许包裹性积液;纵隔淋巴结肿大。11月23日复查红细胞沉降率60 mm/h;血常规:白细胞计数5.57×109/L,中性粒细胞绝对值2.76×109/L,血红蛋白106 g/L,中性粒细胞百分率49.6%;C反应蛋白11.93 mg/L;电解质正常。患者病情好转于11月24日出院,继续口服莫西沙星和甲硝唑抗感染治疗1个月。







诊断:1.右下肺脓肿;2.右侧多房包裹性脓胸;3.肺部重症感染;4.右侧包裹性胸腔积液;5.支气管哮喘;6.低蛋白血症;7.肝功能不全;8.低钠血症;9.凝血功能异常。
鉴别诊断:细菌性肺脓肿需与空洞型肺结核和支气管肺癌并发化脓性感染以及肺囊肿继发感染相鉴别,后者可通过临床症状结合影像学表现、治疗效果、细胞学和病原学检查来进一步明确。脓胸则需与肺脓肿和胸膜肿瘤相鉴别。与脓胸相比,脓肿的壁一般较厚且不规则、与胸壁夹角通常为锐角、多侵蚀而非压迫邻近肺组织;增强CT检查可以用来区分脓胸、肺脓肿和胸膜肿瘤性病变。
12月24日复查胸部CT提示双肺感染、右肺下叶脓肿较前片吸收;右肺底局限性包裹性积液、右侧胸腔包裹性积液和右侧斜裂少许包裹性积液较前片减少(图14、图15)。2022年3月2日患者来院复诊,诉体重增加约5 kg,无明显不适,复查胸部CT(图16,图17,图18)提示右下肺脓肿已吸收,双肺下叶慢性感染、纤维化灶。


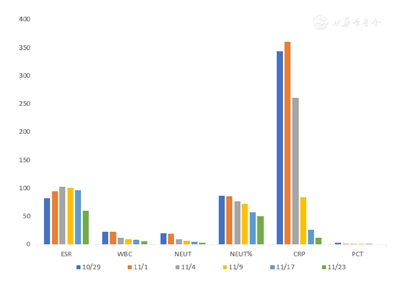

注: ESR:红细胞沉降率, WBC:白细胞, NEUT:中性粒细胞, NEUT%:中性粒细胞百分比; CRP:C-反应蛋白; PCT:降钙素原
脓胸是指胸膜腔受明显的细菌感染而形成脓性渗出液,其发生的常见原因是细菌性肺炎被误诊或治疗被延误而导致感染向胸膜腔蔓延。此外,脓胸也可见于肺脓肿、支气管扩张或肺癌合并感染、结核分枝杆菌感染等[1]。肺脓肿通常由误吸口咽部的分泌物所致,原有肺空洞继发感染、支气管阻塞、脓毒性栓塞或脓胸等局部感染直接蔓延也可引起肺脓肿。故肺脓肿与脓胸之间既可以互为因果,也可以是细菌性肺炎在不同阶段的两种严重并发症。肺脓肿并发脓胸以后,患者住院时间延长,死亡风险增加,治疗难度也相应增加[2]。Cai等[3]的研究表明,经肺裂脓肿、糖尿病、巨大肺脓肿(直径>5 cm)和胸膜炎症状是肺脓肿相关性脓胸的独立危险因素。本例患者有酗酒史、支气管哮喘病史和吸入性糖皮质激素使用史,牙齿卫生不良,前期肺炎治疗不彻底,表现为胸膜炎性胸痛,具备肺脓肿和脓胸发病的高危因素。
化脓性细菌如肺炎链球菌、口腔链球菌、厌氧菌和金黄色葡萄球菌是肺炎旁胸腔积液和脓胸的最常见病原体[4]。误吸相关脓胸常为多种病原体感染,主要包括口腔链球菌和厌氧菌。克雷伯杆菌、大肠埃希菌和铜绿假单胞菌等革兰阴性杆菌引起的脓胸相对较少,但有研究指出糖尿病患者更可能发生肺炎克雷伯杆菌肺脓肿和脓胸[5]。本例患者单次肺泡灌洗液培养出铜绿假单胞菌,可能与患者长期吸入糖皮质激素、入院前曾于外院住院治疗以及使用广谱抗生素等高危因素有关。该患者有酗酒史、口腔卫生不良,存在较高误吸风险,故混合厌氧菌感染的可能性较大,但患者多次痰培养和胸水培养均无阳性结果,可能与厌氧菌难以培养、使用抗生素后取样以及目前的培养方法不够敏感等有关。综上,单次的培养阳性结果尚不足以判定病原体是否为主要致病菌,可能多次、多样本的阳性结果以及结合宏基因组二代测序的方式能够使判定更为准确。
不同阶段的脓胸治疗略有差异,急性脓胸的治疗方案主要包括营养支持治疗、抗感染治疗、胸腔穿刺和置管引流、胸腔内纤溶治疗以及外科手术治疗[6]。目前指南除推荐电视辅助胸腔镜手术(video-assisted thoracic surgery, VATS)作为所有Ⅱ期急性脓胸患者的一线手术方式(Ⅱa类)外,还推荐在早期、小分隔脓胸中行影像引导下的胸腔置管引流术(Ⅰ类)[7]。而对于多房包裹性脓胸的处理,是先行抗感染治疗联合胸腔置管引流术还是直接接受VATS,目前仍缺乏高质量的临床研究数据。该例支气管哮喘合并肺脓肿和多房包裹性脓胸的重症患者,入院后即给予抗感染和营养支持治疗,但患者症状改善不明显,血液炎症指标仍居高不下;随后相继行超声引导下胸腔穿刺术、CT引导下脓胸多点穿刺及置管引流术,患者症状随即改善,血液炎症指标明显下降;再后来反复进行脓腔冲洗和胸腔内纤溶治疗,患者最终经内科综合治疗即获得痊愈。
通过对本例患者诊治经过的回顾和分析,结合有关文献,我们有如下体会:(1)对于肺部感染较严重且合并有胸腔积液或抗感染治疗效果欠佳的患者,要警惕复杂性肺炎旁胸腔积液和脓胸形成可能,及时完善胸部CT或超声检查,必要时行胸腔穿刺抽液送检。(2)当胸腔积液为脓性、革兰染色阳性或培养阳性、pH<7.2[8]或葡萄糖<40 mg/dL(2.2 mmol/L)、乳酸脱氢酶>1000 IU/L或形成明显的包裹性积液[7]时,预示着需要及时行胸腔置管引流术。(3)脓胸的预后较差且死亡率较高,一旦确诊除应尽快启动覆盖厌氧菌的经验性抗感染治疗外,还应尽早置管引流以控制感染源。(4)诊断性胸腔穿刺术应在超声或CT引导下进行,因为包裹性积液位置特殊且容易随体位变动、患侧胸膜增厚致麻醉进针深度不够,从而容易发生气胸、出血和胸膜反应;相比于超声引导,CT引导操作视野更清晰、对并发症判断更准确、患者舒适性更好,但缺点是存在辐射且费用较高。(5)若经内科综合治疗后患者病情无改善,如积液持续或增加、发热反复或再发、血液感染指标升高持续或加重,在调整抗生素覆盖范围、充分引流、给予胸腔内纤溶治疗以及排除其他部位感染和脓肿后,可考虑手术处理。(6)胸腔内纤溶治疗有一定的出血风险,且可能导致发热,需注意与穿刺或置管损伤、疾病本身进展相鉴别。
感谢本院介入中心帅鸿浩主治医师、超声科罗艳主治医师和胸外科何武副主任医师在该例患者诊治过程中给予的帮助和支持
所有作者均声明本研究不存在利益冲突



























