
患者,男性,44岁。主因"多尿、口干、多饮40余天,加重2 d"入院。2021年8月中旬无明显诱因出现多尿、口干、多饮症状,日饮水量约3 000 ml,排尿量>2 500 ml,未重视。2021年9月25日自觉上述症状明显加重,且出现轻度视物模糊及泡沫尿来院就诊,测空腹血糖13.16 mmol/L,为进一步诊治收入院。精神、食欲可,两便如常,体重无明显变化。既往身体健康,否认冠心病、高血压、高脂血症、慢性肾脏病史。否认手术、外伤史。否认食物及药物过敏史。吸烟饮酒近20年。父亲有糖尿病史,否认高血压、冠心病家族史。
身高180.0 cm,体重92 kg,体重指数28.39 kg/m2,腰围94 cm,臀围92 cm。生命体征平稳。神志清楚,精神可。体型肥胖,浅表淋巴结无肿大。甲状腺未触及肿大。心脏、肺、腹无明显异常。双下肢无水肿。病理征未引出。双侧足背动脉搏动正常,双下肢痛觉、温度觉、振动觉正常,双侧10 g弹力丝试验阴性。
尿葡萄糖4+,尿蛋白1+,尿酮体1+。尿酸619.3 μmol/L,空腹血糖12.53 mmol/L,甘油三酯2.84 mmol/L,糖化血红蛋白10.7%,稳态模型评估胰岛素抵抗指数为3.09。胰岛细胞抗体、胰岛素自身抗体及谷氨酸脱羧酶抗体均阴性。腹部超声提示脂肪肝;颈动脉彩色超声提示右侧颈动脉硬化伴斑块形成。诊断为2型糖尿病。
治疗第1阶段,予皮下胰岛素泵强化治疗,患者血糖控制较前改善,逐渐减少泵内胰岛素剂量。治疗第2阶段,调整为皮下注射甘精胰岛素10 U联合皮下注射司美格鲁肽注射液(起始第1、2周剂量为0.25 mg、1次/周,第3周加至0.5 mg、1次/周)降糖治疗,逐步滴定胰岛素剂量。同时强化生活方式干预,饮食方面,进行"5+2"轻断食(1周内非连续2 d热卡≤600 kcal,非断食日正常糖尿病饮食)。运动方面,进行慢跑、游泳、打羽毛球等有氧运动,每次50 min以上,每周≥3次。
血糖达标,控制平稳,体重指数降至正常范围。
内分泌科

版权归中华医学会所有。本文为遵循CC-BY-NC-ND协议的开放获取文章。
目前肥胖患病率在全世界范围内日益严峻,由此引起2型糖尿病(type 2 diabetes mellitus,T2DM)发生率亦快速升高。最新数据显示,中国是成人糖尿病患者最多的国家,据估计,2021年我国成年糖尿病患者人数为1.41亿,预测到2045年患病人数将达到1.744亿[1]。流行病学显示我国T2DM合并腹型肥胖(即"糖胖病")患者占总体T2DM患者的45.4%[2]。2016年世界卫生组织《全球糖尿病报告》[3]明确提出,可通过减重和限制能量摄入实现T2DM缓解。因此,减重在诱导糖胖病患者缓解中发挥了重要作用。司美格鲁肽注射液作为一种新上市降糖药物,归属胰高糖素样肽-1受体激动剂(glucagon-like peptide-1 receptor agonist,GLP-1RA),其在临床药物减重方面有显著优势,同时在T2DM非胰岛素类药物缓解方案选择中也有重要的地位,并且兼具心血管获益效应。本文我们报道1例初发T2DM合并肥胖患者使用司美格鲁肽治疗后达到糖尿病缓解状态的诊治过程,期望为同类患者提供更多治疗经验。
患者,男性,44岁。主因"多尿、口干、多饮40余天,加重2 d"入院。2021年8月中旬无明显诱因出现多尿、口干、多饮症状,日饮水量约3 000 ml,排尿量>2 500 ml,未重视。2021年9月25日自觉上述症状明显加重,且出现轻度视物模糊及泡沫尿来院就诊,测空腹血糖13.16 mmol/L,为进一步诊治收入院。精神、食欲可,两便如常,体重无明显变化。既往身体健康,否认冠心病、高血压、高脂血症、慢性肾脏病史。否认手术、外伤史。否认食物及药物过敏史。吸烟饮酒近20年。父亲有糖尿病史,否认高血压、冠心病家族史。
入院查体:身高180.0 cm,体重92 kg,体重指数28.39 kg/m2,腰围94 cm,臀围92 cm。生命体征平稳。神志清楚,精神可。体型肥胖,浅表淋巴结无肿大。甲状腺未触及肿大。心脏、肺、腹无明显异常。双下肢无水肿。病理征未引出。双侧足背动脉搏动正常,双下肢痛觉、温度觉、振动觉正常,双侧10 g弹力丝试验阴性。实验室及辅助检查如下。(1)常规化验检查:血常规、便常规未见异常;尿常规:尿葡萄糖4+,尿蛋白1+,尿酮体1+;天冬氨酸转氨酶14.1 U/L(参考值15~40 U/L),丙氨酸转氨酶11 U/L(参考值9~50 U/L),血肌酐73.6 μmol/L(参考值64~104 μmol/L),尿酸619.3 μmol/L(参考值208.3-428.4 μmol/L),空腹血糖12.53 mmol/L(参考值3.9~6.1 mmol/L),总胆固醇3.85 mmol/L(参考值3.0~5.7 mmol/L),甘油三酯2.84 mmol/L(参考值0~1.7 mmol/L),高密度脂蛋白胆固醇0.86 mmol/L(参考值1.03~1.55 mmol/L),低密度脂蛋白胆固醇2.95 mmol/L(参考值1.89~4.21 mmol/L)。(2)甲状腺相关检查:甲状腺功能未见异常。(3)糖尿病相关检查:糖化血红蛋白(glycated hemoglobin A1c,HbA1c)10.7%;糖耐量及胰岛素、C肽释放试验见表1;稳态模型评估胰岛素抵抗指数为3.09(参考值>1);胰岛细胞抗体、胰岛素自身抗体及谷氨酸脱羧酶抗体均阴性。(4)影像学检查:腹部超声提示脂肪肝;颈动脉彩色超声提示右侧颈动脉硬化伴斑块形成。
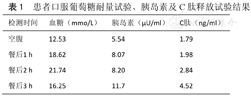
患者口服葡萄糖耐量试验、胰岛素及C肽释放试验结果
患者口服葡萄糖耐量试验、胰岛素及C肽释放试验结果
| 检测时间 | 血糖(mmo/L) | 胰岛素(μU/ml) | C肽(ng/ml) |
|---|---|---|---|
| 空腹 | 12.53 | 5.54 | 1.79 |
| 餐后1 h | 18.62 | 8.07 | 1.98 |
| 餐后2 h | 21.74 | 8.20 | 2.84 |
| 餐后3 h | 16.25 | 11.7 | 4.52 |
患者为中年男性,不同日2次测空腹血糖>7.0 mmol/L,HbA1c>6.5%,体型肥胖,有糖尿病家族史,病程中无自发酮症酸中毒倾向,考虑为T2DM。患者病程较短,血糖水平高,化验基础C肽及胰岛素水平尚可,需除外成年隐匿性自身免疫性糖尿病(latent autoimmune diabetes in adults,LADA),但化验谷氨酸脱羧酶抗体阴性,因此可排除LADA诊断。
治疗第1阶段,尿酮体1+,为避免发生酮症酸中毒,予皮下胰岛素泵强化治疗,患者血糖控制较前改善,逐渐减少泵内胰岛素剂量。治疗第2阶段,调整为皮下注射甘精胰岛素10 U联合皮下注射司美格鲁肽注射液(起始第1、2周剂量为0.25 mg、1次/周,第3周加至0.5 mg、1次/周)降糖治疗,逐步滴定胰岛素剂量。同时强化生活方式干预,饮食方面,进行"5+2"轻断食(1周内非连续2 d热卡≤600 kcal,非断食日正常糖尿病饮食)。运动方面,进行慢跑、游泳、打羽毛球等有氧运动,每次50 min以上,每周≥3次。
治疗第3阶段,院外随访调整用药(表2):2021年12月首次复诊后,调整方案:停用甘精胰岛素,继续司美格鲁肽注射液0.5 mg、1次/周,联合上述饮食、运动干预。2022年2月第2次复诊后,调整降糖方案:司美格鲁肽注射液0.25 mg、1次/周,2周后停药,饮食+运动干预。停降糖药物于2022年5月第3次复诊血糖达标,控制平稳,体重指数降至正常范围。
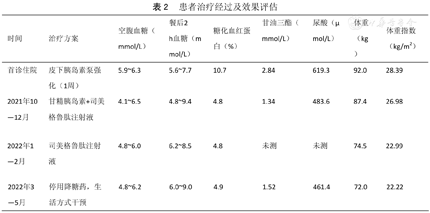
患者治疗经过及效果评估
患者治疗经过及效果评估
| 时间 | 治疗方案 | 空腹血糖(mmol/L) | 餐后2 h血糖(mmol/L) | 糖化血红蛋白(%) | 甘油三酯(mmol/L) | 尿酸(μmol/L) | 体重(kg) | 体重指数(kg/m2) |
|---|---|---|---|---|---|---|---|---|
| 首诊住院 | 皮下胰岛素泵强化(1周) | 5.9~6.3 | 5.6~7.7 | 10.7 | 2.84 | 619.3 | 92.0 | 28.39 |
| 2021年10—12月 | 甘精胰岛素+司美格鲁肽注射液 | 4.1~6.5 | 4.8~9.4 | 4.8 | 1.34 | 483.6 | 87.4 | 26.98 |
| 2022年1—2月 | 司美格鲁肽注射液 | 4.8~6.0 | 6.2~8.5 | 4.8 | 未测 | 未测 | 74.5 | 22.99 |
| 2022年3—5月 | 停用降糖药,生活方式干预 | 4.8~6.2 | 6.0~9.0 | 4.9 | 1.52 | 461.4 | 72.0 | 22.22 |
2021年欧洲糖尿病研究学会/美国糖尿病学会联合发布新版T2DM缓解共识报告[4],修订完善了T2DM缓解定义,继续沿用"缓解(remission)"作为描述糖尿病预后,能更恰当表达血糖改善的动态平衡状态,提示糖尿病并非时时处于进展状态,同时也表明目前尚无任何措施通过阶段性干预,可有效终止T2DM自然病程,T2DM缓解状态的维持需要持续的干预措施。2021年国内亦颁布了首个关于糖尿病缓解共识——《2型糖尿病缓解中国专家共识》(以下称"《共识》")[5]。《共识》指出减重是缓解超重或肥胖T2DM的核心,体重改善幅度是T2DM缓解效果的标志。英国DiRECT研究显示,实施有效的体重管理有望使T2DM达到持续缓解,其结果显示,24个月时,体重管理的干预组糖尿病缓解的患者比例为36%,对照组为3%[6]。
本例患者腹型肥胖,根据《共识》[5]建议:(1)超重或肥胖的T2DM患者,在初诊时血糖水平高并伴有明显高血糖症状或出现糖尿病酮症酸中毒,可给予短期胰岛素强化治疗。(2)待患者高血糖明显改善、糖尿病酮症酸中毒纠正后,重新进行评估,如符合缓解T2DM的基本条件,可采用改善体重的非胰岛素治疗措施,以促进实现T2DM的长期缓解。该患者糖尿病病程短,发病起始空腹血糖>11.1 mmol/L,HbA1c>10%,合并糖尿病酮症,因此治疗初期给予胰岛素强化治疗,血糖平稳后,进行"ABCD"4个维度评估[5]:A抗体阴性,B体重指数28.39 kg/m2(≥25 kg/m2),C1空腹C肽1.790 ng/ml(≥1.1 ng/ml),C2无相关并发症,D病程≤5年。该患者缓解机会较高,治疗第2阶段,制定减重策略,生活方式干预贯穿全疗程(饮食+运动),使用具有减重效果的降糖药物,我们考虑该中年患者白天在外工作,为减少白天用药,一方面短期给予长效胰岛素每晚注射1次改善胰岛β细胞,另一方面皮下注射司美格鲁肽,起始每次0.25 mg、1次/周使患者耐受消化道不良反应,逐渐滴定至靶标剂量0.5 mg、1次/周,此方案提高了患者依从性。该患者经6个月治疗,体重下降达22%,停用降糖药物3个月,血糖达标,HbA1c<6.5%,根据《共识》[5]效果评价,达到临床缓解。
能量代谢是一切生命活动的基础,胰岛素是能量代谢的关键调控者。肥胖患者体内能量代谢异常,细胞内大量脂肪堆积,可能造成细胞内能量应激损伤,会阻断细胞内胰岛素信号传递,造成胰岛素抵抗[7]。当肝脏内脂肪过多,造成胰岛素抑制生糖作用不敏感,肝细胞过度生糖,血糖升高。另一方面胰腺内脂肪过度堆积,脂毒性引起胰岛β细胞去分化或转分化,抑制胰岛细胞分泌胰岛素[8]。因此强调T2DM缓解与纠正肥胖或显著改善体质量、改善脂肪肝和脂肪胰、改善胰岛素抵抗和高胰岛素血症、纠正高糖毒性和胰岛β细胞去分化及转分化密切相关[5]。
GLP-1RA作为非胰岛素类药物作为糖尿病缓解的药物之一[5,9],主要通过改善胰岛β细胞功能、延缓胃排空、抑制下丘脑摄食中枢、促进白色脂肪褐色重塑和脂肪细胞褐变活化等机制,兼具降糖、减重作用。全球多中心大型临床试验研究SUSTAIN(Semaglutide Unabated Sustainability in Treatment of Type 2 Diabetes)系列临床研究共纳入11 000余例T2DM患者,其中纳入中国T2DM患者605例,证实司美格鲁肽具有良好的降糖、减重疗效以及安全性和心血管代谢获益。SUSTAIN China研究[10]显示,在超重或肥胖的中国T2DM患者中使用司美格鲁肽,HbA1c降低达1.8%,体重下降4.2 kg。此外,该系列研究显示,司美格鲁肽还能够改善主要心血管不良事件发生风险,在标准药物治疗基础上,相较安慰剂组,司美格鲁肽组主要心血管不良事件发生风险下降达26%,非致死性卒中发生风险下降达39%[11,12]。在另一项临床系列研究STEP项目中,纳入4 500例以上超重或肥胖患者,研究显示,与接受安慰剂的患者相比,接受每周一次司美格鲁肽注射制剂,体重下降具有统计学意义,且安全性和耐受性良好[13]。其中STEP 4试验中,每周1次注射司美格鲁肽注射制剂2.4 mg并结合生活方式干预,20周可降低肥胖患者体重10.6%[14]。研究显示,司美格鲁肽通过减少能量摄入,从源头抑制能量过剩,一项随机、双盲、安慰剂对照的交叉试验纳入30例肥胖患者,随机接受司美格鲁肽1.0 mg或安慰剂每周一次皮下注射治疗12周后及交叉治疗12周后分别评估进食早餐后食欲抑制情况和全天能量摄入情况,结果显示,司美格鲁肽相比于安慰剂组显著提高空腹整体食欲抑制评分(P=0.002 3),并在之后的5 h内持续高于安慰剂组,同时显著减少能量摄入[15]。
研究显示,司美格鲁肽注射液在改善胰岛β细胞功能方面也具有显著效果。德国一项单中心、双盲、安慰剂对照、平行组试验[16]中纳入75例成人T2DM参与者,司美鲁肽1.0 mg或安慰剂治疗12周。共同主要终点为通过静脉葡萄糖耐量试验测量第一(0~10 min)和第二(10~120 min)相胰岛素分泌变化,并进行了精氨酸刺激试验和24 h膳食刺激试验,使用分级葡萄糖输注试验评估了治疗参与者和健康参与者的胰岛素分泌率。其结果显示,静脉葡萄糖耐量试验后,司美鲁肽组的曲线下面积(area under the curve,AUC)0~10 min和AUC10~120 min均显著增加。进一步24 h膳食试验显示,司美鲁肽组的空腹、餐后和整体血糖水平以及胰高糖素反应均降低。精氨酸刺激试验显示,司美鲁肽治疗后最大胰岛素容量增加。另外在分级葡萄糖输注试验期间,司美鲁肽显著增加胰岛素分泌率至与健康参与者相似的水平。因此,在T2DM患者中,每周1次使用司美鲁肽治疗12周可显著改善β细胞功能和控制血糖。
综上,目前,对于糖胖病患者,随着多种新型降糖药物的研发,实现糖尿病缓解的方案越来越多,其中减重治疗和体重管理是多种缓解方案的核心,也是维持更长缓解时间的关键。多项研究支持司美格鲁肽注射具有显著的减重效果,并且可以改善胰岛β细胞功能,维持血糖平稳。同时因其较长的半衰期,且小剂量滴定的优势,患者依从性好,更容易实现个体化管理。虽然不可能使所有糖胖病均达到停药缓解,但通过缓解T2DM治疗方案的实施有益于血糖控制、延缓并发症进展,改善心血管临床结局,提高T2DM患者生活质量,建立健康的生活方式,并且终身获益。
所有作者均声明本研究无利益冲突



























