
患者,男性,64岁。反复活动后胸闷、气促5年,加重1周入院。既往有高血压病3年。心电图提示窦性心律,完全性左束支传导阻滞。冠脉CTA未见明显狭窄。
BP 126/75 mmHg(1 mmHg=0.133 kPa),神志清楚,呼吸增快,口唇、指端无青紫,颈静脉充盈,肝颈静脉回流征阳性,双肺可闻及湿啰音,心率90次/min,律齐,各瓣膜区未闻及杂音,腹部平坦,软,无压痛,双下肢水肿。
心衰及其病因诊断:既往冠脉CTA、心脏超声,生化检查以及影像学检查明确病因诊断,且排除其他缺血、内分泌、自身免疫等病因导致的心衰。
药物治疗+CRTD治疗,CRTD治疗中左室电极采用希浦系统起搏技术植入。
患者目前心衰症状明显缓解,心超评估心脏明显缩小且收缩功能得到明显提升。
心血管内科;急诊内科;心外科

版权归中华医学会所有。本文为遵循CC-BY-NC-ND协议的开放获取文章。
心脏收缩失同步是慢性心衰患者心功能恶化、病情加重的重要因素之一。据研究统计,超过1/3慢性心衰患者存在心脏收缩失同步[1]。心脏再同步化治疗(cardiac resynchroni-zation therapy,CRT)是在传统起搏基础上增加左心室起搏,以恢复左、右心室间和左室内收缩同步性,提高心脏排血效率,长期应用可逆转心肌重构、降低心衰住院率和死亡率。BLOCK HF研究[2]显示,对起搏依赖且心功能受损的患者,CRT较右心室起搏可以降低死亡及心衰发生率,改善生活质量。尽管传统CRT技术在一定程度上恢复了心室电学同步性,但左室心外膜电极产生的电激动仍沿普通心肌传导,心室整体激动时间长于生理情况下沿希浦系统传导的时间,并不能在真正意义上恢复生理性电学同步。近年来新兴的希浦系统起搏技术(包括希氏束起搏和左束支起搏),能够使心室电活动沿希氏束-浦肯野系统下传,恢复心室生理性传导,并可以纠正近端左束支传导阻滞(left bundle branch block,LBBB),改善左室电活动的同步性。现报道1例采用希浦系统起搏技术的CRT治疗病例,该例呈现超反应状态,明显改善心功能和临床症状,体现了希浦系统起搏在CRT技术方面的有效性。
患者,男性,64岁。2017年开始出现反复活动后胸闷、气促,休息后可逐渐缓解。后症状逐渐加重,未规范就诊及治疗。2019年因感冒后突发胸闷、气促加重,无胸痛、晕厥,于我院就诊。行心超检查提示左房、左室增大,左室壁收缩活动普遍减弱且欠协调,左室收缩功能中重度减退,LVEF 30%。冠脉CTA提示冠状动脉未见明显狭窄。诊断为扩张性心肌病。予以心衰标准化药物治疗并规范随访,逐步将药物调整至"培哚普利2 mg/d,比索洛尔2.5 mg/d,托拉塞米10 mg/d,螺内酯20 mg/d",自觉胸闷、气促症状好转,坚持服药。2021年4月患者受凉后出现咳嗽、咳痰,活动后胸闷、气促,活动耐力明显下降,伴夜间阵发性呼吸困难,少尿,双下肢水肿。无胸痛,晕厥,无体重减轻,大便次数增多,心电图提示窦性心律,完全性左束支传导阻滞。阳性体征包括:神志清楚,呼吸增快,口唇、指端无青紫,颈静脉充盈,肝颈静脉回流征阳性,双肺可闻及湿啰音,心率90次/min,律齐,各瓣膜区未闻及杂音,腹部平坦,软,无压痛,双下肢水肿。
既往史:患者既往有高血压病史3年,最高血压150/90 mmHg(1 mmHg=0.133 kPa),口服培哚普利4 mg/d,比索洛尔2.5 mg/d,血压波动于110~130/60~80 mmHg。无关节红、肿、热、痛,无甲状腺疾病病史。否认其他慢性病史。
个人史:否认烟酒等不良嗜好。职业会计,已退休4年。否认毒物接触史。
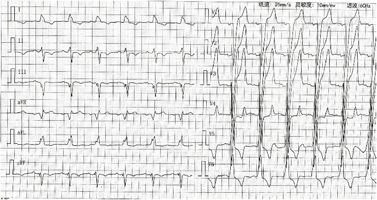
血常规:血红蛋白147 g/L,白细胞计数9.37×109/L,血小板计数227×109/L;血肌酐98 μmol/L,血清尿素氮6.4 mmol/L,尿酸321 μmol/L;NT-proBNP 3335 pg/ml。肝功能:总胆红素17.7 U/L,丙氨酸氨基转移酶16 U/L,天冬氨酸氨基转移酶18 U/L。甲状腺功能:未见异常。自身免疫抗体:均阴性。心电图:窦性心律,完全性左束支传导阻滞,QRS波时程160 ms(图1)。

胸片:两肺纹理增多,心影增大,主动脉硬化。
心超:左房(54 mm)、左室(60 mm)增大,左室壁收缩活动普遍减弱且欠协调,左室收缩功能重度减退,左室射血分数(left ventricular ejection fraction,LVEF)29%。中重度二尖瓣反流,右房(48 mm)增大,轻度三尖瓣反流,中度肺动脉高压;左室舒张功能减退,微量心包积液。
初步诊断:1.扩张型心肌病心律失常-完全性左束支传导阻滞心功能Ⅲ级(NYHA);2.高血压病1级。
本患者以胸闷、气促、双下肢水肿的心衰症状为主要表现,需对引起患者心衰的病因进行鉴别。患者高血压病史3年,最高血压150/90 mmHg,既往口服培哚普利4 mg/d,比索洛尔2.5 mg/d,托拉塞米10 mg/d,螺内酯20 mg/d控制血压并改善心肌重构、抗心衰治疗。血压波动于110~130/60~80 mmHg。患者无心绞痛或心肌梗死,既往冠脉CTA未见明显冠脉狭窄,不考虑缺血性心肌病。患者否认既往有内分泌代谢疾病,否认烟、酒嗜好及毒物接触史,无关节红、肿、热、痛,无贫血,甲状腺功能正常,自身免疫性疾病可能性不大。
该患者治疗原则:有效控制心衰和心律失常,预防猝死和栓塞,提高患者生活质量及生存率。患者入院时有明显胸闷、气促、双下肢水肿,治疗方案在沙库巴曲缬沙坦、醛固酮拮抗剂的基础上利尿剂加量以纠正心衰;同时控制摄入量,并监测体重,每天减轻0.5~1.0 kg。当患者呼吸困难、肺淤血症状好转后加用β受体阻滞剂。同时,患者既往接受过指南推荐的优化药物治疗,但LVEF仍≤35%,心电图提示窦性心律,左束支传导阻滞,QRS时限160 ms,推荐植入CRTD(I类推荐)。患者心电图符合Strauss标准的真性完全性左束支传导阻滞(QRS时限,男性140 ms,女性130 ms以上;V1、V2导联的QRS波呈QS或rS型,且R波<0.1 mV,avL导联的Q波<0.1 mV;在I、avL、V1、V2、V5、V6导联中至少2个导联存在QRS波切迹或顿挫)特征,可能为近端左束支阻滞。希浦系统起搏可以纠正近端左束支阻滞,提示患者可能从希浦系统起搏中获益。2021年4月16日对患者行CRTD治疗,并采用希浦系统起搏中的左束支起搏(LBBP)技术植入左室电极。
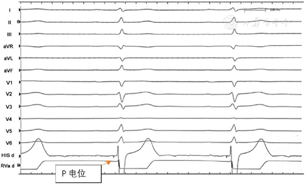
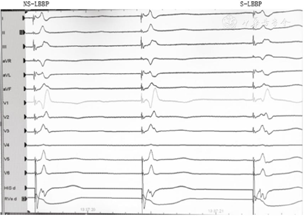
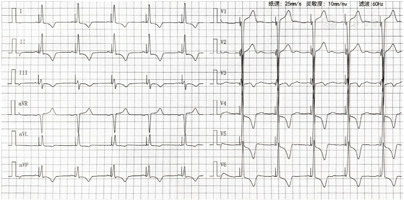
手术过程:常规采用左侧腋静脉入路,J型导丝引导下送入C315鞘(美国美敦力公司)至右心房,经鞘管送入美敦力3830导线至房室沟和三尖瓣环处希氏束的位置,先进行希氏束标测,确定希氏束位置,在右前斜位30°,将远端希氏束部位与心尖连线方向的1~1.5 cm处的右心室面作为初始部位,逆时针旋转鞘管,保持导线头端垂直于室间隔,寻找起搏时V1导联呈"W"形,顿挫在QRS底部的右心室间隔位点。定位后快速旋转导线拧入电极。起搏图形由左束支阻滞形态逐渐变为右束支阻滞形态。旋入过程中动态监测3830导线单极阻抗、单极起搏图形以及测量高电压(5V)、低电压(阈值电压)起搏状态下的左心室达峰时间。左束支夺获的判断标准如下:(1)起搏形态为右束支传导阻滞(right bundle branch block,RBBB)形态,起始陡峭;(2)记录左束支电位(P电位)(图2);(3)观察到选择性左束支起搏图形(S-LBBP)(图3)。本病例表现为:当输出电压为5V@0.4ms时,腔内心电图呈现非选择性左束支起搏图形(NS-LBBP)。即起搏信号与QRS波之间无等电位线,心电图V1导联呈QR型;当输出电压降低为1V@0.4ms时,腔内心电图呈现S-LBBP。即起搏信号与QRS波之间存在等电位线或间隙,心电图V1导联呈M型,R波宽且有切迹;(4)随着电压增高,左室达峰时间骤然缩短,且输出继续增高时,达峰时间保持不变;(5)起搏纠正阻滞,恢复前传电位顺序,证实直接传导束夺获。记录左室达峰时间(stimulus to peak LV activation time,Sti-LVAT)为75 ms;R波幅度:12 mV,阈值:1.0 V,阻抗:580欧姆。撤去C315鞘后再测试参数,满意后连接DTBA2D1脉冲发生器。术后复查心电图:QRS波时限明显缩短(120 ms)(图4)。



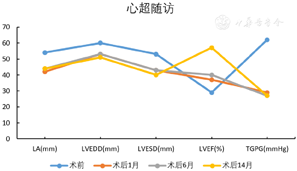
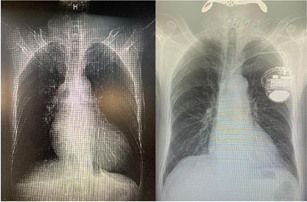
术后患者长期服用阿司匹林100 mg/d,沙库巴曲缬沙坦100 mg/d,比索洛尔2.5 mg/d,螺内酯20 mg/d治疗,同时坚持低盐饮食(2~3 g/d),每日晨起监测体重,体重维持在68~70 kg。1个月后复查心超提示:左室壁收缩活动普遍减弱,左室收缩功能中度减退,LVEF:0.37.左房增大(42 mm)。6个月后复查心超:左室壁收缩活动普遍减弱,左室收缩功能中度减退,LVEF 0.40,左房增大(44 mm)。14个月后复查心超:左房增大(44 mm),LVEF 0.57(图5)。同时复查胸片:心影明显缩小(图6)。患者心衰症状明显好转。


传统CRT方法已经有大量研究证实其在改善心衰、减少心衰再住院及死亡率方面的疗效[2]。但传统方法仍存在左室电极植入失败,左室电极位置不理想等问题。传统CRT无应答者甚至心衰恶化比例占20%~30%。近年来,希浦系统起搏的兴起为慢性心衰合并左束支传导阻滞患者提供了另一有效的再同步化治疗方式。本例患者通过左束支起搏的CRT治疗纠正真性完全性左束支传导阻滞,术后随访14个月,EF值明显上升,临床结果满意。
多个临床研究已经证实,希浦系统起搏可以获得满意的心室电-机械同步性。QRS波时限是心脏电同步性的重要指标,窄QRS波常提示良好的电同步性[3]。随着QRS波时限延长,心室间和左室内的电活动呈现失同步状态,会引起心脏增大和心力衰竭。传统右心室起搏呈现明显宽大畸形的QRS波,制造了人为的左室传导延缓,对左室电活动的同步性有很大影响,可以导致起搏诱导的心肌病。可见QRS波时限与左室功能呈负相关的关系[4,5]。而近年来的研究显示左室激动的达峰时间—即起搏钉到R波顶峰的时间(Sti-LVAT)是标志左室内电活动同步性更加重要的指标,它表示的是左室侧壁的最大除极时间。达峰时间越短意味着左室电活动的同步性越好。当起搏电极从右室间隔部的心肌组织逐渐拧至间隔部的左室内膜下,到达左束支传导束时,达峰时间会出现由长到短的跳跃并固定下来。Sti-LVAT保持最短并恒定是夺获左束支的有力证据[6]。希浦系统起搏技术中无论是希氏束起搏还是左束支起搏都可以使电传导沿心脏的高速传导通路—希浦系统下传,与传统右室起搏相比可以得到更短的达峰时间,从而获得更好的左室电同步性。2019年Hou等[7]评估左束支起搏(left bundle branch pacing,LBBP)、希氏束起搏(His bundle pacing,HBP)和右室起搏右心室起搏(right ventricular pacing,RVP)3种起搏模式对左心室电学同步性的影响,结果显示左束支起搏可实现与希氏束起搏相似的左心室电-机械同步性,与右室起搏相比可以得到更短的达峰时间,效果更优。该结论已通过核素检查及超声心动图检查证实[6,7,8]。
本例患者的希浦系统起搏是比较成功的,术中较好地完成了希浦系统起搏理论要求的指标:包括P电位,选择性左束支起搏图形,左室达峰时间的突然缩短,并随电压升高保持不变。该患者经左束支起搏后很好地纠正了LBBB,QRS波时限从160 ms明显缩短至120 ms,左室达峰时间为75 ms,意味着左室电活动的同步性得到了极大改善。电活动的同步性也在机械收缩的同步性上得到了体现。术后心超评估LVEDD、LVEF明显改善。患者为CRT超反应。并且在随访中经程控关闭CRTD后,恢复自身LBBB状态,再次测量左室机械同步性,结果显示较术前明显改善。考虑可能与左室内径缩小,LVEF提高相关,左室自身同步性随左室逆重构、心肌收缩力恢复而得到改善。
所有作者均声明本研究不存在利益冲突































