
患者,男性,19岁,因"头痛5年,伴颈肩部疼痛7个月"来院诊治。
患者5年前无明显诱因下出现头痛,多表现为右侧颞部、枕部疼痛。近2个月头痛加重,每隔1 d头痛发作1次,发作时NRS 5~6分。体格检查:颞部、颈椎椎旁斜方肌、右侧枕部、右侧胸锁乳突肌、右侧颈椎横突出口有局部压痛,呈酸胀痛,NRS 1分,无恶心呕吐、畏光畏声、流泪流涕等。
患者头痛部位,疼痛发作次数、持续时间、疼痛程度等临床表现符合国际头痛分类第三版关于无先兆性偏头痛的诊断标准,确诊偏头痛。
查血清同型半胱氨酸水平显著偏高,亚甲基四氢叶酸还原酶(5,10-methylenetetrahydrofolate reductase, MTHFR)基因检测结果示患者基因型为T/T,属于慢代谢型。予叶酸、甲钴胺等降同型半胱氨酸治疗。
治疗后患者同型半胱氨酸水平恢复正常,未再发头痛。
疼痛科;神经内科;药剂科

版权归中华医学会所有。本文为遵循CC-BY-NC-ND协议的开放获取文章。
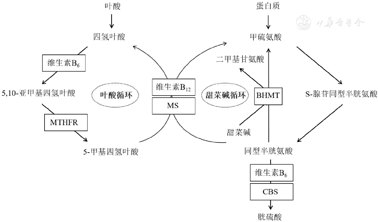
偏头痛是一种常见的慢性神经血管性疾病,多表现为偏侧头部反复发作的中重度搏动性疼痛。近年来MTHFR基因多态性对偏头痛的影响备受关注。MTHFR是叶酸-同型半胱氨酸代谢的关键酶(图1),研究发现MTHFR C677T位点发生突变,使得Ala222→Val,导致MTHFR酶活性降低,造成同型半胱氨酸(homocysteine,Hcy)水平偏高,引起神经元过度兴奋,促进神经末梢释放大量头痛介质及炎症因子,最终诱发偏头痛[1,2,3]。本文报道1例基于MTHFR基因检测治疗偏头痛的案例,结合文献复习,探索偏头痛诊疗新思路。

患者,男性,19岁,因"头痛5年,伴颈肩部疼痛7个月"于2021年7月18日来院诊治。患者自诉5年前无明显诱因下出现头痛,多表现为右侧颞部、枕部疼痛,疼痛与体位无关,睡眠后能有所缓解,曾服用对乙酰氨基酚、氟桂利嗪等,治疗效果不佳。近2个月头痛加重,每隔1日头痛发作1次,呈搏动性疼痛,发作时NRS 5~6分,持续7~10 h。否认头痛家族史。入院体格检查:患者颞部、颈椎椎旁斜方肌、右侧枕部、右侧胸锁乳突肌、右侧颈椎横突出口有局部压痛,呈酸胀痛,NRS 1分,无恶心呕吐、畏光畏声、流泪流涕等。
Hcy 55.4μmol/L ↑,血清维生素B12 136.0pg/ml↓,血清叶酸4.5 ng/ml,CRP 3.1 mg/L,ESR 3 mm/h。MTHFR基因检测结果示患者基因型为T/T,属于慢代谢型。
患者MTHFR基因型为T/T,提示患者叶酸代谢风险高,较易发生高同型半胱氨酸血症,目前临床上根据Hcy水平不同将高同型半胱氨酸血症分为轻度(10~15 μmol/L)、中度(15~30 μmol/L)及重度(>30 μmol/L)[4]。本例患者Hcy 55.4 μmol/L,属于重度高同型半胱氨酸血症,同时患者血清维生素B12 、叶酸水平较低,提示其存在叶酸-同型半胱氨酸代谢障碍。考虑到Hcy水平升高与偏头痛的发生相关,初始治疗予叶酸片5 mg tid po,甲钴胺片0.5 mg tid po降Hcy处理,交代患者饮食上增加黄豆、菠菜、腐竹、苋菜等富含叶酸食物的摄入。
2021年9月10日复诊,患者主诉疼痛明显好转,头痛发作频率减为1~2周发作1次,发作时NRS 3分,疼痛持续时间4~6 h。检验结果示Hcy 23.2 μmol/L (↑),血清维生素B12 252.0 pg/ml,血清叶酸40.0 ng/ml (↑),可见Hcy水平较前明显下降,血清维生素B12已恢复至正常水平,而血清叶酸水平显著偏高。一般认为叶酸水平升高对人体无毒性,但长期大剂量(>1 mg/d)补充叶酸,可能增加癌症发生风险,加重神经系统退行性病变等[5]。故调整患者叶酸剂量为0.4 mg qd po,并交代患者均衡饮食,规律作息,定期复诊。
2022年1月12日复诊,患者主诉头痛较前进一步好转,发作频率由1~2周发作1次减为1个月发作1次,头痛发作可能与近期准备考试致情绪紧张、睡眠不佳相关,呈搏动性疼痛,发作时NRS 2~3分,疼痛持续时间较前无明显变化。辅助检查结果为:Hcy 29.5 μmol/L ↑,叶酸17.8 ng/ml,提示小剂量叶酸对降低Hcy水平疗效差。由图1知Hcy通过叶酸循环和甜菜碱循环2条途径完成代谢,2条途径互相补充,但不能相互替代。研究表明,甜菜碱是高效的甲基供体,能同时提供3个甲基参与Hcy甲基化代谢,是治疗因MTHFR基因突变或叶酸缺乏所致高同型半胱氨酸血症的常用药物[6]。临床上常使用天然甜菜碱、叶酸、维生素B6、维生素B12组成的复合营养素降Hcy[7]。基于以上证据,建议患者换用膳食补充剂类活性同型半胱氨酸继续降Hcy治疗,其具体成分表如表1所示:

活性同型半胱氨酸营养成分表
活性同型半胱氨酸营养成分表
| 主要营养成分 | 含量/粒 |
|---|---|
| 维生素B6 | 50 mg |
| 叶酸 | 800 mcg DFE |
| 维生素B12 | 500 mcg |
| 甜菜碱 | 500 mcg |
2022年2月18日复诊,患者主诉近期无头痛发作,辅助检查结果为:Hcy 7.6 μmol/L,叶酸15.4 ng/ml。目前患者头痛控制可,Hcy、叶酸均已恢复至正常水平,治疗有效。患者诊疗过程中的检验指标、疼痛情况及用药变化见表2。
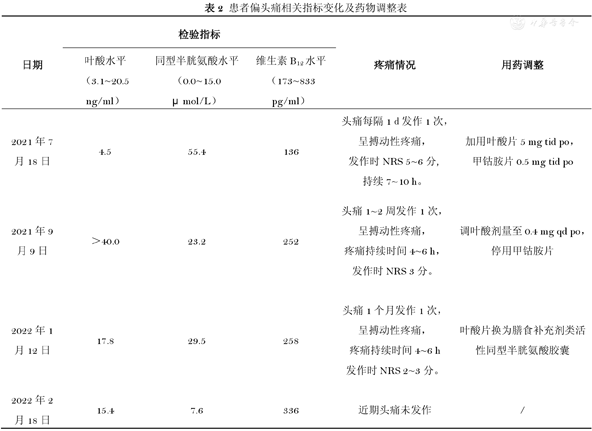
患者偏头痛相关指标变化及药物调整表
患者偏头痛相关指标变化及药物调整表
| 日期 | 检验指标 | 疼痛情况 | 用药调整 | ||
|---|---|---|---|---|---|
| 叶酸水平(3.1~20.5 ng/ml) | 同型半胱氨酸水平(0.0~15.0 μmol/L) | 维生素B12水平(173~833 pg/ml) | |||
| 2021年7月18日 | 4.5 | 55.4 | 136 | 头痛每隔1 d发作1次,呈搏动性疼痛,发作时NRS 5~6分,持续7~10 h。 | 加用叶酸片5 mg tid po,甲钴胺片0.5 mg tid po |
| 2021年9月9日 | >40.0 | 23.2 | 252 | 头痛1~2周发作1次,呈搏动性疼痛,疼痛持续时间4~6 h,发作时NRS 3分。 | 调叶酸剂量至0.4 mg qd po,停用甲钴胺片 |
| 2022年1月12日 | 17.8 | 29.5 | 258 | 头痛1个月发作1次,呈搏动性疼痛,疼痛持续时间4~6 h发作时NRS 2~3分。 | 叶酸片换为膳食补充剂类活性同型半胱氨酸胶囊 |
| 2022年2月18日 | 15.4 | 7.6 | 336 | 近期头痛未发作 | / |
现有证据表明,引起偏头痛发生发展的因素较多,包括神经和脑脊液周围炎症因子的产生,线粒体功能障碍,降钙素基因相关肽(calcitonin gene related peptide,CGRP)增加、血清Hcy水平上调、一氧化氮(Nitric oxide,NO)含量升高等[8,9]。其中,Hcy水平升高是导致偏头痛发生的一个重要因素,Hcy通过下调体内甲基化反应诱导氧化应激的产生,促使5-HT、IL-6及TNF-α等释放入血,同时高Hcy能够刺激血管内皮细胞,增加血管通透性,致使血液中炎性介质含量进一步增多,从而不断刺激三叉神经,引起偏头痛发作[10]。有研究表明,当Hcy>15μmol/L时,患者发生先兆性偏头痛的风险增加了6倍[11]。而MTHFR作为Hcy代谢过程中的关键酶,其基因多态性在偏头痛的发生中同样扮演着重要角色,目前研究较多的是MTHFR C677T位点突变与偏头痛发生的相关性。数据显示,MTHFR C677T位点发生突变,其酶活性显著降低,CT杂合突变基因型的酶活性是CC野生型的65%,TT纯合突变型的酶活性是CC型的30%[12],这将导致Hcy代谢紊乱,使得体内Hcy大量堆积,进而诱导偏头痛的发生,目前已有大量研究证实偏头痛患者MTFHR C677T基因突变率较正常人显著升高[13,14,15]。另外,MTFHR C677T基因突变也可影响偏头痛的临床表现症状,相较于CC型,TT纯合突变型患者多表现为单侧偏头痛,畏光症状更为明显[16,17];而CT杂合突变型患者主要表现为压力性偏头痛、活动性偏头痛,头痛发作时常伴有恶心、疲劳、失眠、恐嗅症等[18]。对于该患者,其MTHFR基因型为TT纯合突变型,引起患者体内叶酸-同型半胱氨酸代谢障碍,造成Hcy水平升高;同时,叶酸代谢产生的5-甲基四氢叶酸作为Hcy代谢中的重要甲基供体,维生素B12作为辅助因子均参与了Hcy的甲基化,患者初诊时其叶酸水平、维生素B12水平均偏低,这也进一步加重了Hcy代谢循环障碍,上述因素协同作用导致患者重度高Hcy,这是引起患者发生偏头痛的主要原因。
另外,NO是神经递质中的气体信使分子,也是诱导头痛发生的一系列级联反应的起始因子。NO可通过环磷酸鸟苷信号通路促进CGRP的释放,介导谷氨酸等兴奋性氨基酸细胞毒性作用,引起脑血管扩张并生成大量炎症因子,从而导致偏头痛的发生[19,20]。而维生素B12具有清除NO的作用,能有效预防偏头痛[21]。该患者维生素B12水平低下,使得NO清除受阻,这可能是其发生偏头痛的另一原因。
基于以上分析,在本例患者初诊时加用叶酸、甲钴胺治疗偏头痛,后根据血清叶酸、维生素B12及Hcy水平及时调整用药方案直至上述指标恢复正常范围,同时交代患者饮食上注意多食富含叶酸的食物,规律作息并保持心情愉悦,治疗后患者头痛明显缓解,提示MTHFR基因多态性在指导偏头痛的个体化治疗中具有一定的临床价值,偏头痛诊疗中应根据基因检测结果优化偏头痛治疗方案并做好随访工作,实现精准治疗。
所有作者均声明本研究不否存在利益冲突



























