
患者,男性,52岁。诊断为慢性淋巴细胞白血病5年余。经利妥昔单抗+氟达拉滨+环磷酰胺方案治疗后缓解,并在第4年复发。在伊布替尼单药治疗期间,患者出现突发性头痛。颅脑影像学检查发现明确的右侧枕顶叶肿块并广泛水肿。采用宏基因组二代测序快速诊断毛霉病感染。采用两性霉素B胆固醇硫酸酯复合物、泊沙康唑及介入手术治疗,治疗成功。同时,考虑到泊沙康唑对复发患者病情进展的控制,以及与泊沙康唑的药物相互作用。选择Bruton酪氨酸激酶抑制剂泽布替尼作为后续控制慢性淋巴细胞白血病的治疗方案。患者已随访近1年,病情稳定。
头晕、头胀、行动迟缓。
头颅磁共振、宏基因组二代测序、活检。
两性霉素B胆固醇硫酸酯复合物、泊沙康唑及介入手术治疗。
慢性淋巴细胞白血病处于完全缓解状态,毛霉菌控制稳定。
神经科;感染科;血液科

版权归中华医学会所有。本文为遵循CC-BY-NC-ND协议的开放获取文章。
毛霉病年发病率约每10万人次3.3例[1]。中枢神经系统毛霉感染的发病率在免疫功能低下的中枢感染患者中占比小于0.04%,极为罕见,致死率高达80%[2,3,4]。中枢神经系统毛霉病的发病率近年来呈逐年上升趋势[5]。毛霉病的诊断依赖于组织病理学和组织培养微生物的鉴定[6]。倘若延迟诊断和治疗,死亡的风险在1周内翻倍[3]。本文报道1例成功救治的复发慢性淋巴细胞白血病患者的中枢毛霉感染。旨在提高对隐匿性真菌感染的警惕,减少误诊和漏诊。
患者,男性,52岁。2015年因淋巴结进行性增大、乏力起病,左侧淋巴结活检病理确诊为慢性淋巴细胞白血病/小淋巴细胞白血病(chronic lymphocytic leukemia/small lymophocytic leukemia,CLL/SLL),FISH:ATM(-)、RB1(-)、CSP12(-)、D13S25(-)、TP53(-);NGS基因:IGHV(+)、SF3B1(+)、MYC(+)。脾脏超声:80 mm×211 mm×91 mm。评估疾病分期为RAI Ⅱb期、BINET B期,CLL IPI 3分,中危。当时予以标准剂量RFC方案(美罗华500 mg/m2 d0+氟达拉滨25 mg/m2 d1~d3+CTX 250 mg/m2 d1~d3)治疗,总共6次。治疗结束后评估病情为CR,定期门诊随访,疾病维持稳定长达4年。2020年9月因淋巴结再次出现进行性增大考虑复发,病理活检确认为慢性淋巴细胞白血病,重复予以RFC方案(美罗华500 mg/m2 d0+氟达拉滨25 mg/m2 d1~d3+CTX 250 mg/m2 d1~d3)。由于治疗期间患者出现溶血性贫血,考虑氟达拉滨药物作用,故于2020年10月将治疗方案更换为IR方案(伊布替尼420 mg、每日1次+美罗华700 mg×1 d、每28天/cycle)。4次IR方案治疗后,因"间质性肺炎"中断美罗华治疗,应用泼尼松+SMZ治疗维持2个月左右后好转。期间持续伊布替尼单药控制慢性淋巴细胞白血病,疾病持续缓解状态。2021年7月中旬,患者无明显诱因出现步态不稳,无发热,不伴意识障碍,不伴头痛、头晕,不伴有脓性鼻涕,不伴恶心、呕吐,不伴关节肿痛,不伴口角歪斜、流涎,未在意,未行诊治。7月下旬患者出现头痛,呈胀痛,位于枕部,伴发热,体温最高达38°C,无恶心、呕吐,无咽痛、流涕、鼻塞,无皮疹、寒战,无腹痛、腹泻,无尿频、尿急、尿痛。
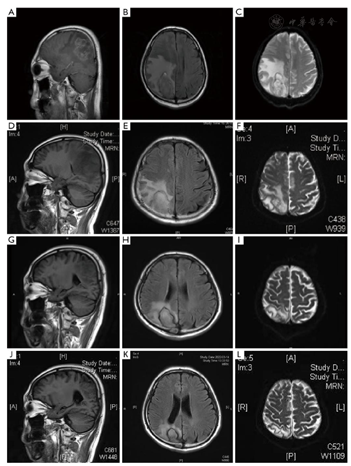
入院后检查血常规示:白细胞计数5.92×109/L(3.97×109~9.15×109/L)正常:中性粒细胞计数4.76×109/L(正常:2.00×109/L~7.00×109/L),(1,3)-beta-d-葡聚糖试验、半乳甘露聚糖试验均正常,降钙素原<0.02 ng/ml。患者淋巴细胞亚群显示T细胞以及自然杀伤细胞下降,CD4/CD8:0.2(正常:1.0~2.5),CD4计数:90/μl(正常:384~1346/μl),CD4/CD45RA:0.6%(正常:15.0%~25.0%),同时患者合并低丙种球蛋白血症,免疫球蛋白G(immunoglobulin G,IgG):7.62 g/L(正常:8.6~17.4 g/L)。头颅磁共振影像(平扫):右侧枕顶叶占位伴大片水肿,建议颅脑MR增强检查,左侧额叶、两侧半卵圆区缺血灶。2021年8月3日头颅磁共振影像增强:右侧枕顶叶占位伴大片水肿,考虑恶性,结合病史,转移性肿瘤可能(图1)。给予"甘露醇、甘油果糖、速尿脱水降颅压处理"。患者症状进一步加重,出现步态不稳加重,左侧肢体无力且感觉迟钝。2021年8月6日腰椎穿刺:测颅压大于300 cmH2O(80~180 cmH2O,1 cmH2O=0.098 kPa),脑脊液常规:透明度清,潘氏试验(+),红细胞1×106/L,白细胞<1×106/L;脑脊液生化:脑脊液糖4.0 mmol/L(2.2~3.9 mmol/L),脑脊液氯(干式法)108 mmol/L(118~132 mmol/L),脑脊液蛋白(干式法)1733 mg/L(<500 mg/L)。真菌荧光染色检查:阴,真菌染色荧光涂片:直接涂片未发现细菌,抗酸染色涂片:未找到抗酸杆菌。脑脊液PMseq病原微生物高通量基因检测报告(该病原体基因组上的位置分布)提示:根毛霉属(Rhizomucor,检出序列数3842)、微小根毛霉(Rhizomucor pusillus,检出序列数3771)。样本测序数据及病原理论灵敏度:检出总序列数43 797 028;真菌(100 MB)理论灵灵敏度(copies/ml):1.00E+00(图2)。期间患者症状持续加重,出现嗜睡、左侧肢体肌力减退,肌力1级。

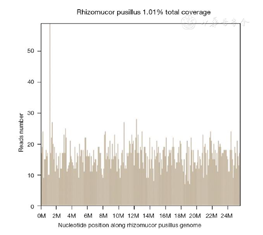

结合头颅磁共振、宏基因组二代测序、活检诊断。
于2021年8月11日起应用两性霉素B胆固醇硫酸酯复合物联合泊沙康唑治疗(两性霉素B胆固醇硫酸酯复合物逐渐增加剂量至150 mg,泊沙康唑首剂负荷剂量600 mg后300 mg,每日1次)。
应用治疗第2天患者意识恢复清醒,体温正常,且左侧肌力也逐日好转。用药1周左右肌力恢复至4级。2周左右肌力完全恢复正常水平。8月31日复查头颅MR病灶均较前好转(图1)。后患者症状恢复,精神状态好,肌力完全恢复正常。考虑进一步治疗患者中枢毛霉感染,于2021年10月14日在静脉全身麻醉下行颅内脓肿引流术及活检。病理结论:(右顶)染色结果,符合毛霉菌感染。免疫组化:CD2(部分+)、CD20(-)、CD68(组织+)、GFAP(组织+)、Olig2(-),特殊染色PAS(+),银染(+)。2021年11月15日复查头颅MRI增强提示病灶较前缩小(图1)。目前选择应用泊沙康唑口服降阶梯治疗。2022年3月复查头部MRI显示感染病灶改善(图1)。
患者为中危慢性淋巴细胞白血病合并溶血性贫血。泽布替尼对BTK的抑制具有更强的选择性,其安全性和有效性已得到证实。因此,选择泽布替尼控制原发性血液肿瘤,考虑与三唑类药物联合应用,泽布替尼的口服剂量调整为80 mg、每日2次。患者血液肿瘤状态是稳定的。11月18日对CLL进行评估;血液学提示外周血可测残余病灶为阴性,目前疾病完全缓解。
根毛霉菌是毛霉目的一种嗜热真菌[1],属于人类罕见的感染,包括根霉属、犁头霉属(重新分类为伞状毛菌属、瓶霉属和鳞质霉属)等[6,7,8,9]。毛霉病感染致死率较高,总死亡率约为62%[1],其中中枢神经系统的毛霉病感染是极为少见并致命性的[11]。在国内,对毛霉菌感染的认识还比较有限,尤其是中枢毛霉菌感染,其相关死亡率尚未见报道。2010年1月—2017年1月的一项国际流行病学调查显示,除糖尿病外,血液肿瘤是毛霉病感染的第二大常见因素,占32%。特别是当患者接受肿瘤化疗和免疫治疗时,免疫抑制的发生率会更高[11]。我们的患者是用伊布替尼治疗的难治性CLL。患者感染时的外周血细胞分析显示,他们没有中性粒细胞减少症。患者的淋巴细胞亚群显示T细胞、NK细胞减少,同时存在低丙种球蛋白血症,提示毛霉病感染高危因素。在毛霉病感染控制期间,给予免疫球蛋白(IVIG)1 g/(kg·月)(持续1周)静脉注射,以纠正体液免疫。
侵袭性真菌病的宿主因素有很多,其中BTK抑制剂伊布替尼治疗也被列为主要宿主因素之一[3]。使用BTK抑制剂期间的毛霉病感染可涉及多个部位,常见的感染部位是肺部和皮肤[12,13,14,15,16,17,18]。本例是一种罕见的中枢神经系统感染,其发病通常是非常隐匿的。然而一旦出现相关感染症状,该疾病侵袭性极高并危及生命。早期诊断对改善预后起着关键性作用。一直以来真菌培养和组织活检是毛霉病诊断的金标准。欧洲医学真菌学联合会(ECMM)于2019年发布的全球毛霉病诊断指南描述了使用组织培养、分子技术和原位杂交以及物种鉴定和药敏试验相结合的毛霉病诊断[19]。推荐的属和种鉴定方法为ITS测序法和基质辅助激光解吸电离飞行时间法(MALDI-TOF)。这两种属和种的鉴定都有一定的局限性。特别是对于临床高危患者,这些方法诊断率低且耗时[20,21]。Fehr等[12]报道了1例71岁的CLL患者,在伊鲁替尼治疗期间发生中枢神经系统毛霉病并迅速死亡。尸检后经聚合酶链反应(PCR)鉴定为毛霉病,延误了医疗。PCR是一种分子检测方法,可以对特定的目标生物进行许多单独的检测,但仍可能漏掉罕见的病原体,或使用与所涉及的微生物菌株不匹配的引物,从而降低了检测的敏感性。然而,mNGS是一种无偏倚的诊断方法,具有检测几乎任何生物体的潜力,可能成为微生物诊断测试的巨大转变[22]。我们将该患者的脑脊液应用PMseq方法检测,48 h内获得报告提示根毛霉菌感染。这为早期用药提供了依据。从临床实际操作来说,CSF mNGS检测方法比传统的金标准方法如活检等方法更容易获得。同时,它在脑膜炎病原体鉴定,尤其是在种鉴定方面具有优势,推荐用于感染性中枢神经系统疾病的诊断[23]。本例疾病表现为中枢神经系统感染。开始时很隐匿,然而进展非常快。因此,需要快速诊断和治疗以改善预后。虽然通过直接定位组织中感染区域的DNA测序是一种很有前途的方法,但该方法对实验室设备的要求很高[24]。在临床实践中,有时很难获得组织病理学组织。此时推荐CSF mNGS作为二线检测方法。
目前关于NGS在中枢神经系统感染中的应用报道主要以病例报道的形式,很少有大规模的研究可参考。在以往对脑脊液病原体二代测序的研究中,诊断率不高,部分原因是在脑脊液上清中只能检测到脱细胞病毒或脱细胞微生物核酸,检出率较低[25,26,27,28,29]。因此,临床上应正确使用CSF作为测序标本,以提高检出率[30]。Miller等[31]的研究表明,与传统的临床实验室结果相比,二代测序的敏感性为73%,特异性为99%,阳性预测值为81%,阴性预测值为99%。在目前的国内国外报道中,毛霉菌中枢感染经二代测序获得成功诊治的病例较少,其疗效和临床价值有待进一步探索。二代测序对中枢神经系统真菌感染的疗效尚需更大样本量的临床试验验证,并应密切结合患者临床表现和实验室检测结果进行解读和验证。通过结合NGS等方法,可以加快真菌感染的病因诊断,使尽早开始有效的全身抗真菌治疗成为可能,同时控制基础疾病发展。早期有效的疾病控制可改善预后。在治疗过程中,我们可以通过脑脊液中发现的序列数量来监测疾病控制的情况。滴度降低也能在一定程度上反映病情。由于宏基因组的高敏感性,宏基因组检测结果可以显示疾病控制情况,并可在患者临床症状改善、影像学结果阴性后指导停药。如果患者需要长期应用免疫抑制剂或病情进展需要进一步治疗,如细胞介导免疫,亦可应用宏基因组学监测毛霉病活性。
所有作者均声明本研究不存在利益冲突
张佼佼,糜坚青.早期诊治复发慢性淋巴细胞白血病伴中枢毛霉感染1例[DB/OL].中国临床案例成果数据库,2023(2023-01-08).http://journal.yiigle.com/LinkIn.do?linkin_type=cma&DOI=10.3760/cma.j.cmcr.2023.e00166.































