
版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
血栓性血小板减少性紫癜(TTP)是一组以微血管病性溶血、血小板减少为主要特征的临床综合征,表现为广泛微血栓形成、组织灌注不足而引发多器官功能障碍,是一种严重威胁生命的血液科急症。特发性TTP是指在无明确基础疾病或诱发因素时患者体内因产生针对血管性血友病因子(VWF)裂解蛋白酶ADAMTS13的自身抗体(抑制物),进而导致ADAMTS13活性降低或缺乏,从而引起相应临床表现[1]。在血浆置换采用前,TTP患者的早期死亡率达90%以上,而采用血浆置换作为标准一线治疗方案后,TTP患者的早期存活率已达80%[2],但仍有部分患者出现疾病进展或复发。近年来,我们采用糖皮质激素+血浆置换+利妥昔单抗的联合方案治疗10例难治/复发TTP患者并获得良好疗效,报告如下。
2010年10月至2016年5月北京协和医院收治的10例难治/复发特发性TTP患者纳入研究。诊断标准符合文献[3]:存在微血管病性溶血性贫血及血小板减少(PLT<100×109/L),ADAMST13活性<10%且ADAMST13抑制物阳性,无明确相关基础疾病或诱发因素(结缔组织病、感染性疾病、肿瘤、骨髓移植或药物相关)。难治性TTP:足量血浆置换5次后,血小板计数无回升或<50×109/L伴LDH持续升高。复发性TTP:停止血浆置换等治疗30 d后再次出现临床症状、血小板计数下降及乳酸脱氢酶(LDH)升高[4]。
统计患者发病的临床信息,包括出血表现、精神症状、发热、腹部症状等。同时记录患者治疗期间各种血液生化指标情况及变化,主要包括血红蛋白、血小板计数、LDH、血肌酐等。
①所有患者均接受泼尼松1 mg·kg-1·d-1或等效剂量甲泼尼龙治疗;对于伴严重精神症状的患者予以甲泼尼龙1.0 g/d×3 d冲击治疗,之后序贯常规剂量泼尼松或甲泼尼龙,1个月后逐渐减量。②急性发作期患者给予单膜血浆置换治疗,每日1次,每次2 000 ml;当血浆供应不足时,采用双膜血浆置换联合白蛋白及新鲜血浆输注。③利妥昔单抗:375 mg/m2静脉滴注,每周1次,连用4次。利妥昔单抗用药前,予对乙酰氨基酚、苯海拉明、地塞米松预防输液反应,同时进行心电监护。若使用利妥昔单抗期间进行血浆置换,则在血浆置换结束后立即给药,并距离下次血浆置换间隔至少20 h。
临床反应:停止血浆置换后,血小板计数恢复正常(PLT>100×109/L),LDH降至参考值上限的1.5倍以下;临床缓解:停止血浆置换后,临床反应持续30 d以上。恶化:停止血浆置换后30 d内,已获得临床反应的患者再次出现症状及血小板减少、LDH升高[4]。
通过门诊随访或电话的方式,随访患者的生存状况及不良事件。随访期自确诊之日截止到2017年2月或患者死亡。
采用SPSS 20.0统计软件处理数据,正态分布的计量结果以 ±s表示,非正态分布的计量资料以中位数(范围)表示。
±s表示,非正态分布的计量资料以中位数(范围)表示。
本研究共入组患者10例,男、女各5例,中位年龄40.5(17~65)岁。10例患者中,首次发病的难治性患者9例,复发患者1例。所有患者均有微血管病性溶血性贫血及血小板计数下降(100%),均有皮肤瘀点、紫癜、鼻出血、黑便等出血表现。其中9例出现神经精神症状(意识障碍、癫痫发作、谵妄、运动性失语、肢体运动障碍、头痛等),6例出现肾脏损害(尿量减少、肉眼血尿等),6例出现发热(均为高热),4例患者出现消化系统症状(呕吐、腹痛),未发生消化道出血。10例患者临床表现见表1。
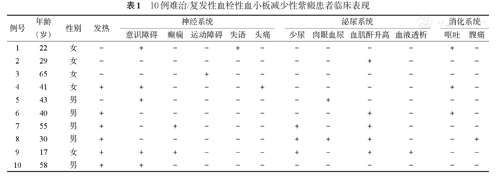
10例难治/复发性血栓性血小板减少性紫癜患者临床表现
10例难治/复发性血栓性血小板减少性紫癜患者临床表现
| 例号 | 年龄(岁) | 性别 | 发热 | 神经系统 | 泌尿系统 | 消化系统 | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 意识障碍 | 癫痫 | 运动障碍 | 失语 | 头痛 | 少尿 | 肉眼血尿 | 血肌酐升高 | 血液透析 | 呕吐 | 腹痛 | ||||
| 1 | 22 | 女 | - | + | - | - | + | - | - | - | - | - | + | - |
| 2 | 29 | 女 | - | - | - | - | - | - | - | - | + | - | - | - |
| 3 | 65 | 女 | - | - | - | + | - | - | - | - | - | - | - | - |
| 4 | 41 | 女 | + | + | - | - | - | + | - | - | - | - | + | - |
| 5 | 43 | 男 | - | + | - | - | - | - | - | + | - | - | - | - |
| 6 | 40 | 男 | + | - | - | - | - | - | - | - | + | - | + | - |
| 7 | 55 | 男 | + | - | + | - | - | - | + | - | + | - | - | - |
| 8 | 30 | 男 | + | - | - | - | - | - | + | + | + | - | - | + |
| 9 | 17 | 女 | + | + | + | - | - | - | + | - | + | + | - | - |
| 10 | 58 | 男 | + | + | - | - | - | - | - | - | - | - | - | - |
①血常规及溶血指标:患者起病时血常规(中位数):HGB 62(45~96)g/L,PLT 11(6~79)×109/L。所有患者血涂片破碎红细胞均>1%。网织红细胞比例中位数为10.0%(2.3%~27.2%)。Coombs试验均为阴性。6例患者测定游离血红蛋白含量,其中4例升高。②肾脏损伤指标:9例患者存在尿潜血阳性,4例患者尿蛋白升高,5例患者出现血肌酐升高。③凝血指标:全部10例患者中位纤维蛋白原为2.16(1.13~3.48)g/L(参考区间1.80~3.50 g/L),5例患者纤维蛋白原低于正常;PT、APTT大致正常。④其他:全部10例患者LDH中位数为1 129(344~3 790)U/L。9例患者检测肌钙蛋白(cTnI),7例升高,但无相关症状及心电图动态改变。6例患者行外周血补体检测,3例补体C3下降,5例补体C4下降。⑤ADAMTS13活性及抑制物:9例患者ADAMTS13活性为0,1例为7.2%;ADAMTS13抑制物检测均为阳性。
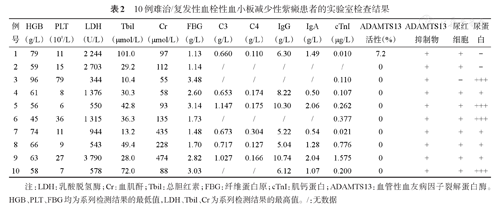
10例难治/复发性血栓性血小板减少性紫癜患者的实验室检查结果
10例难治/复发性血栓性血小板减少性紫癜患者的实验室检查结果
| 例号 | HGB(g/L) | PLT(109/L) | LDH(U/L) | Tbil(μmol/L) | Cr(μmol/L) | FBG(g/L) | C3(g/L) | C4(g/L) | IgG(g/L) | IgA(g/L) | cTnI(μg/L) | ADAMTS13活性(%) | ADAMTS13抑制物 | 尿红细胞 | 尿蛋白 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 79 | 11 | 2 244 | 101.0 | 97 | 1.13 | 0.660 | 0.110 | 6.30 | 1.49 | 0.010 | 7.2 | + | + | - |
| 2 | 59 | 15 | 2 703 | 29.2 | 112 | 1.14 | / | / | / | / | / | 0 | + | + | - |
| 3 | 96 | 79 | 344 | 10.4 | 55 | 3.48 | / | / | / | / | 0.110 | 0 | + | - | +++ |
| 4 | 61 | 8 | 1 376 | 30.3 | 58 | 2.60 | 0.653 | 0.174 | 8.22 | 0.50 | 0.107 | 0 | + | + | + |
| 5 | 56 | 6 | 550 | 42.8 | 93 | 3.14 | 1.147 | 0.175 | 10.30 | 2.06 | 0.262 | 0 | + | + | +++ |
| 6 | 45 | 36 | 1 315 | 36.3 | 135 | 1.73 | / | / | / | / | 0.377 | 0 | + | + | +++ |
| 7 | 74 | 11 | 944 | 13.2 | 435 | 1.48 | 0.673 | 0.304 | 5.22 | 0.54 | 0.021 | 0 | + | + | + |
| 8 | 66 | 9 | 543 | 49.4 | 228 | 1.70 | 0.717 | 0.127 | 5.04 | 1.28 | 0.776 | 0 | + | + | + |
| 9 | 63 | 27 | 3 790 | 28.0 | 474 | 2.82 | 1.027 | 0.166 | 10.74 | 2.04 | 1.575 | 0 | + | + | + |
| 10 | 58 | 7 | 578 | 72.0 | 88 | 3.03 | / | / | 6.12 | 1.07 | 0.200 | 0 | + | + | +++ |
注:LDH:乳酸脱氢酶;Cr:血肌酐;Tbil:总胆红素;FBG:纤维蛋白原;cTnI:肌钙蛋白;ADAMTS13:血管性血友病因子裂解蛋白酶。HGB、PLT、FBG均为系列检测结果的最低值,LDH、Tbil、Cr为系列检测结果的最高值。/:无数据
10例TTP患者均在入院后24 h内开始糖皮质激素联合血浆置换治疗,血浆置换的中位次数为10(4~11)次,置换血浆量中位数为12 500(4 000~15 000)ml。首剂利妥昔单抗用药的中位时间为入院后10.5(6~17)d,5例患者首剂利妥昔单抗治疗后继续接受血浆置换,持续时间中位数为2(1~11)d。10例患者中,8例完成4次利妥昔单抗治疗,另2例在首剂利妥昔单抗治疗后1周出现严重感染而停用后续利妥昔单抗治疗,并分别于入院第17天和第23天死亡。完成4次利妥昔单抗治疗的8例患者均获得临床缓解,获得临床缓解的中位时间为首剂利妥昔单抗治疗后15(6~45)d,其中血小板恢复的中位时间为10(4~24)d,LDH恢复的中位时间为9.5(0~45)d。9例伴神经精神症状的患者中,7例在利妥昔单抗治疗前神经精神症状已消退,其余2例患者分别在用药后第2、18天消退。3例患者接受大剂量甲泼尼龙冲击治疗,2例患者使用环磷酰胺。
所有患者在利妥昔单抗治疗后半年内停用糖皮质激素及免疫抑制剂。8例获得临床反应患者的中位随访时间为14(4~69)个月,均为临床缓解状态,未见复发。随访过程中,2例患者监测ADAMTS13酶活性剂抑制物水平,首剂利妥昔单抗治疗1个月后至末次随访,ADAMTS13活性均为100%,抑制物检测持续阴性。
10例患者共计输注利妥昔单抗34次,发生2级以上输液反应(皮疹、胸闷、头痛)3次(8.9%),未发生3级以上输液反应及过敏反应。治疗期间2例患者死亡:1例患者于入院第12天,行血浆置换及糖皮质激素治疗期间中即出现革兰阳性菌血流感染,曾一度控制,之后于第17天使用利妥昔单抗治疗,第20天再次出现发热、大量血性痰、呼吸衰竭并最终死亡。另1例患者入院后第7天使用利妥昔单抗治疗,次日出现高热、寒战,胸部CT显示双肺多发斑片影,经过积极抗感染治疗仍有高热,后出现感染性休克、弥散性血管内凝血、消化道大出血,最终因脑出血、脑疝死亡。
本组3例患者监测IgG水平,无低丙种球蛋白血症出现,较基线亦无明显下降。感染方面,除急性期外,整个随访过程,无2级以上感染事件发生。除急性期外,整个随访过程中未发生2级以上感染事件。
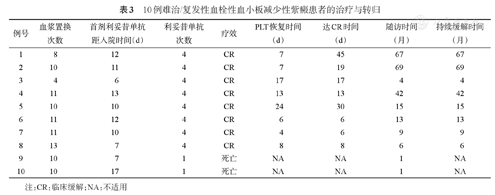
10例难治/复发性血栓性血小板减少性紫癜患者的治疗与转归
10例难治/复发性血栓性血小板减少性紫癜患者的治疗与转归
| 例号 | 血浆置换次数 | 首剂利妥昔单抗距入院时间(d) | 利妥昔单抗次数 | 疗效 | PLT恢复时间(d) | 达CR时间(d) | 随访时间(月) | 持续缓解时间(月) |
|---|---|---|---|---|---|---|---|---|
| 1 | 8 | 12 | 4 | CR | 7 | 45 | 67 | 67 |
| 2 | 10 | 11 | 4 | CR | 7 | 19 | 69 | 69 |
| 3 | 4 | 6 | 4 | CR | 17 | 17 | 4 | 4 |
| 4 | 11 | 13 | 4 | CR | 13 | 13 | 42 | 42 |
| 5 | 10 | 10 | 4 | CR | 24 | 30 | 15 | 15 |
| 6 | 11 | 12 | 4 | CR | 6 | 6 | 13 | 13 |
| 7 | 11 | 10 | 4 | CR | 4 | 6 | 9 | 9 |
| 8 | 13 | 7 | 4 | CR | 8 | 8 | 6 | 6 |
| 9 | 10 | 7 | 1 | 死亡 | NA | NA | 1 | NA |
| 10 | 10 | 17 | 1 | 死亡 | NA | NA | 1 | NA |
注:CR:临床缓解;NA:不适用
TTP是血液科急症,典型临床表现为"五联征",包括发热、溶血性贫血、血小板下降、精神症状、肾脏损伤。目前认为,获得性TTP患者的发病是由于不同原因导致ADAMTS13抑制物产生,导致ADAMTS13酶活性下降,无法有效剪切VWF多聚体,从而引起微血栓发生[5,6]。虽然血浆置换联合糖皮质激素治疗的有效率可达到80%~90%,但仍有部分患者难以缓解。
利妥昔单抗是CD20单克隆嵌合型抗体,通过补体依赖的细胞毒作用、抗体依赖的细胞毒作用和直接效应快速清除循环的CD20阳性B淋巴细胞,从而减少抗体的产生,已经用于多种自身免疫性疾病的治疗。利妥昔单抗目前是原发免疫性血小板减少症、自身免疫性溶血性贫血的二线治疗方案,在抗中性粒细胞抗体(ANCA)相关系统性血管炎、类风湿关节炎、获得性血友病、冷凝集素病中也有较多应用经验[7,8,9]。自2002年起,已有研究报道利妥昔单抗可以用来治疗难治性TTP。在2007年,Scully等[10]报道25例难治/复发TTP患者接受利妥昔单抗联合血浆置换治疗,所有患者均达到临床缓解,平均起效时间为11 d,其中21例患者的ADAMTS13抑制物转阴。2012年一项来自法国前瞻性Ⅱ期研究显示,21例难治性TTP患者使用利妥昔单抗治疗,30 d反应率达到100%,其PLT恢复时间、30 d缓解率、远期复发率均优于历史数据[11]。2016年另一项法国研究(NCT009000751)也得到了相似结论[12]。另有多个研究得到类似结果,其总有效率为80%~100%,平均起效时间为11~14 d[13,14,15,16]。本组病例的总反应率为80%,中位随访14个月,与以往研究结果相近。利妥昔单抗的起效中位时间为15 d,与既往的研究报道类似。这可能与病例数少,病例选择偏倚以及LDH监测不规律有关。长期疗效方面,利妥昔单抗也显示出良好效果。历史文献显示,TTP的复发率为40%,复发多出现在治疗后1年之内[17];接受利妥昔单抗治疗患者的复发率为0~30%,且短期复发率较低[10,16]。本研究中位随访14个月,未出现复发病例。
2011年,Scully等[18]将利妥昔单抗联合血浆置换作为TTP的初始治疗,可以减少血浆置换的次数,并缩短住院日。2015年王静等[19]将17例患者分为两组,比较了血浆置换+糖皮质激素是否联合利妥昔单抗治疗的区别,发现两组间早期疗效无差异,但联合利妥昔单抗组的复发率显著降低。
联合利妥昔单抗治疗与单纯血浆置换对于ADAMTS13抑制物持续阳性的无症状TTP患者,是否可以预防性使用利妥昔单抗,目前仍有争议。2014年,Hie等[20]对30例临床缓解但ADAMTS13活性持续<10%的患者给予预防性应用利妥昔单抗(375 mg/m2每周1次,共4次),中位随访36个月后,无复发生存率高于非利妥昔单抗预防组(P=0.049),但因入组病例少等原因,该研究的结论并未获得广泛认同。Pequeño-Luévano等[21]以小剂量利妥昔单抗(100 mg每周1次,共4次)治疗6例TTP患者,所有患者均取得临床反应,ADAMTS13活性恢复正常,随访8~24个月无复发。
本组病例共输注利妥昔单抗34次,发生2级以上输液反应3次(8.9%),与以往研究类似。2例患者在治疗早期死亡,这两例患者病情加重的时间为利妥昔单抗使用后1~3天,最终死亡原因是感染。利妥昔单抗影响体液免疫功能,导致低球蛋白血症,可增加乙肝病毒再激活风险,少与急性感染相关[22,23]。因此以上2例急性感染为糖皮质激素及血浆置换相关,而非利妥昔单抗所致。本研究中3例患者监测了免疫球蛋白水平,未发现明显低球蛋白血症出现。这与以往研究中利妥昔单抗增加低丙种球蛋白血症比例、但感染风险不增加[24]的结果相似。
本组病例结果初步显示,对于常规血浆置换联合糖皮质激素的治疗方案治疗无效的难治/复发TTP,利妥昔单抗可以作为安全有效的治疗选择,其起效迅速,安全性好,缓解率高达80%,1年内复发率亦低于传统治疗方案,须警惕早期感染。但目前利妥昔单抗给药的最佳时机、最适剂量等问题仍未解决,需更多前瞻性临床数据。


























