
探讨二甲双胍对大鼠脑缺血再灌注损伤后炎性细胞因子的影响及机制。
应用线栓法建立大鼠大脑中动脉闭塞(MCAO)模型;采用改良的神经功能评分法评价大鼠神经行为功能;原位末端标记(TUNEL)法检测细胞凋亡;酶联免疫吸附测定(ELISA)法检测血清中白细胞介素-6(IL-6)、白细胞介素-8(IL-8)和肿瘤坏死因子α(TNF-α)的含量;蛋白质印迹法(Western Blot)检测脑组织缺氧诱导因子-1α(HIF-1α)、BAX及BCL-2蛋白的表达水平。
与对照组相比,脑缺血损伤大鼠神经功能评分明显升高,组织细胞凋亡明显增多(均P<0.01)。与模型组相比,二甲双胍可减轻大鼠脑缺血再灌注后的神经功能损伤,并使血清中IL-6、IL-8和TNF-α的表达水平显著降低(均P<0.01)。二甲双胍可显著下调大鼠脑组织中HIF-1α和BAX蛋白的表达水平,上调BCL-2蛋白的表达水平,进而调控凋亡相关蛋白的表达,减少脑组织细胞凋亡。
二甲双胍可能通过降低炎性细胞因子表达,抑制脑缺血再灌注后细胞凋亡,对脑缺血再灌注损伤起保护作用,其机制可能与调控凋亡相关蛋白的表达,抑制HIF-1α表达,并抑制相关炎症因子TNF-α、IL-6和IL-8的释放有关。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
缺血性脑血管病(ischemic cerebral vesscular disease,ICVD)致残率极高,是威胁人类健康与生存的主要疾病之一。脑缺血后,缺血脑组织局部离子浓度失衡及细胞产物的堆积会刺激脑内细胞(如胶质细胞、神经元和上皮细胞等)产生细胞因子[如白细胞介素1(interleukin 1, IL-1)、IL-6、IL-8、肿瘤坏死因子(tumor necrosis factor,TNF)等],引起缺血区微血管阻塞,导致小胶质细胞和白细胞被激活,从而发生水肿并产生炎症反应[1,2]。脑缺血再灌注损伤时,氧自由基等信使激活炎性细胞因子使白细胞和血管内皮细胞表面的黏附分子表达上调,中性粒细胞向微血管内皮细胞移动和黏附,致使中性粒细胞在缺血脑组织中浸润,引起损伤[3,4]。脑缺血再灌注可激活机体免疫系统,导致IL-1、IL-6和肿瘤坏死因子α(TNF-α)等炎性细胞因子分泌增多,引起神经元损伤并增加其凋亡。因此,抑制炎症反应和减少细胞凋亡对于减轻脑缺血再灌注损伤具有重要作用[5]。二甲双胍(metformin)是治疗2型糖尿病起始、基础和全程的一线药物。随着临床的广泛应用,发现二甲双胍在治疗肥胖症、保护心血管、治疗多囊卵巢综合征、抗肿瘤、降低由空气污染引发的心血管疾病风险等多领域具有重要的应用价值[6,7,8,9]。本研究中,旨在探讨二甲双胍对脑缺血再灌注损伤后炎性细胞因子的影响及机制,验证其对脑缺血损伤后大鼠的神经功能保护作用,为缺血性脑血管病的合理治疗提供理论依据。
SPF级成年健康雄性Wistar大鼠(n=55),8~9周龄,体质量为220~250 g,购于北京维通利华实验动物技术有限公司,许可证号为SCXK(京)2012-0001。二甲双胍(纯度>98%、相对分子质量512,美国Sigma-Aldrich公司),4%多聚甲醛(北京索莱宝科技有限公司),TUNEL检测试剂盒(KGA7025-50 assays,南京凯基生物科技发展有限公司),酶联免疫吸附测定(enzyme linked immunosorbent assay,ELISA)试剂盒(上海江莱生物科技有限公司),兔源缺氧诱导因子-1α(hypoxia-inducible factor-1α,HIF-1α)、IL-6、IL-8、TNF-α、BCL-2和BAX抗体(美国Abcam公司),兔抗鼠β-肌动蛋白(β-actin)抗体、辣根过氧化物酶(horseradish peroxidase,HRP)标记的山羊抗兔二抗(美国Cell Signaling Technology公司)。
高速离心机(美国Thermo Scientific公司),电泳仪(美国Bio-Rad公司),石蜡包埋机和石蜡连续切片机(德国Leica公司),光学显微镜及显微镜成像分析系统(日本Olympus公司),Gel-Pro analyzer分析系统(美国Media Cybernetics公司)。
所有大鼠均饲养于室温25 ℃环境,给予标准饲料喂养,自由饮水。实验过程中大鼠处置严格遵守动物伦理准则和指南的相关规定。随机选择40只大鼠应用线栓法建立大脑中动脉阻塞(middle cerebral artery occlusion,MCAO)模型。具体方法如下:大鼠术前24 h禁食,自由饮水,10%水合氯醛(3.5 ml/kg)腹腔注射进行麻醉并仰卧固定于手术台上;无菌条件下,经左侧颈外-颈内动脉插线,行中动脉阻塞;缺血2 h后,将尼龙线栓抽出,恢复左侧大脑中动脉供血;将麻醉苏醒后的大鼠放回鼠笼进行单笼饲养,自由进食。术后2 h应用改良神经功能评分标准(modifiedneurological severity score, mNSS)对大鼠神经功能进行评价[10],剔除术后死亡和不符合标准的大鼠,共获得30只MCAO大鼠模型。
将成功造模的30只MCAO模型大鼠按简单随机抽样法分为模型组和二甲双胍组,每组各15只。另随机选择15只健康大鼠为对照组。二甲双胍组在缺血再灌注前30 min根据大鼠体质量按200 mg/kg给予二甲双胍生理盐水溶液灌胃。模型组在缺血再灌注前30 min,根据大鼠体质量按200 mg/kg给予生理盐水灌胃。对照组大鼠除不插线进入颅内外,其余操作同实验组并根据其体质量按200 mg/kg给予生理盐水灌胃。
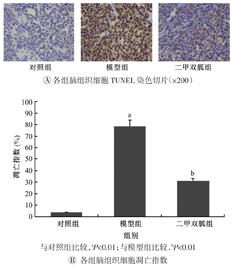
缺血再灌注24 h后,快速断头处死大鼠取脑组织,10%甲醛固定24 h,梯度乙醇脱水,二甲苯透明后进行石蜡包埋,制成石蜡切片。将石蜡切片进行TUNEL染色,方法步骤按照其检测试剂盒说明书进行。TUNEL染色后,阳性(凋亡)细胞核染成棕黄色,而非凋亡细胞核呈蓝色。在光学显微镜下观察视野内凋亡细胞个数,计算凋亡细胞占所有细胞总数的百分比,即凋亡指数(apoptosis index, AI)。每个样本取5个视野的凋亡细胞取平均值,作为其凋亡细胞数。凋亡指数AI(%)=凋亡细胞数/细胞总数×100%。
缺血再灌注24 h后,于大鼠腹主动脉取血6 ml,静置4 h后,4 ℃、3 000 r/min离心5 min,取上清液按照ELISA试剂盒说明书检测血清中IL-6、IL-8和TNF-α。加入100 μl标准品和100 μl血清于反应板孔中,混匀,封住板孔,37 ℃温育60 min;洗板,反复洗涤5次后每孔加入100 μl 1×Biotin,封住板孔,37 ℃温育60 min;再洗板,每孔加入100 μl 1×HRP,封住板孔,37 ℃温育30 min;洗板后每孔加入100 μl TMB显色液,混匀,37 ℃暗处温育15 min;每孔加入100 μl终止液混匀;30 min内在450 nm处读吸光度(A)值。以A值为纵坐标,以标准品质量浓度为横坐标,绘制标准曲线。根据血清样品的A值可在标准曲线上计算其质量浓度。
采用Western Blot法检测HIF-1α及凋亡相关蛋白的表达。取各组大鼠脑组织样品,用裂解液提取组织蛋白,采用二喹啉甲酸法检测总蛋白并制备蛋白样品。取蛋白样品50 μg,经10%SDS-PAGE电泳后,转膜,5%脱脂奶粉室温封闭膜1 h,加入HIF-1α抗体(1∶1 000)、BCL-2和BAX抗体(1∶1 000),4 ℃过夜,TBST缓冲液洗3次,加入辣根过氧化物酶标记的山羊抗兔二抗(1∶2 000),于37 ℃孵育1 h,洗膜,电化学发光法显影。β-actin检测作为内对照,进行细胞间蛋白表达的比较。
采用SPSS19.0统计学软件处理数据,各组数值以均值±标准差( ±s)表示,组间比较采用单因素方差(One-way ANOVA)分析,组间多重比较采用SNK-q检验,以P<0.05为差异具有统计学意义。
±s)表示,组间比较采用单因素方差(One-way ANOVA)分析,组间多重比较采用SNK-q检验,以P<0.05为差异具有统计学意义。
应用mNSS法评定各组大鼠的神经行为功能,分数范围0~18分,评分越高说明大鼠神经行为功能损伤越重,反之则较轻。评估结果显示,对照组大鼠未出现脑组织梗死及神经功能损伤症状,实验组(模型组和二甲双胍组)大鼠均有不同程度的神经功能损伤症状和脑组织梗死。与对照组相比,模型组脑组织梗死体积增加,神经功能评分升高,其差异有统计学意义(P<0.01)。与模型组相比,二甲双胍组大鼠脑缺血再灌注后的神经功能损伤得到减轻,脑梗死体积明显减小,其差异有统计学意义(P<0.01)。(表1)

各组大鼠神经功能评分及脑梗死体积比较( ±s)
±s)
各组大鼠神经功能评分及脑梗死体积比较( ±s)
±s)
| 组别 | n | 神经功能评分(分) | 脑梗死体积(%) |
|---|---|---|---|
| 对照组 | 15 | 0 | 0 |
| 模型组 | 15 | 15.35±1.24a | 45.39±3.65a |
| 二甲双胍组 | 15 | 7.68±0.62b | 24.84±2.31b |
注:与对照组比较,aP<0.01;与模型组比较,bP<0.01
TUNEL染色结果显示,大鼠缺血再灌注24 h后,对照组无明显的凋亡细胞(细胞核呈蓝色),而模型组和二甲双胍组均可见凋亡细胞(细胞核呈棕黄色),且模型组凋亡细胞明显多于二甲双胍组(图1)。结果表明,对照组、模型组和二甲双胍组AI分别为(3.8±0.34)%、(78.6±4.58)%和(31.2±2.14)%。与对照组相比,模型组脑组织凋亡率明显增加(P<0.01);与模型组相比,二甲双胍组的凋亡率明显减少(P<0.01),表明二甲双胍可以降低脑缺血再灌注后组织细胞凋亡的发生。

ELISA检测结果表明,缺血再灌注24 h后,模型组大鼠血清中IL-6、IL-8和TNF-α表达水平明显升高(均P<0.01);与模型组相比,二甲双胍组大鼠血清中IL-6、IL-8和TNF-α的表达水平显著降低(均P<0.01)。以上结果表明,二甲双胍能抑制脑缺血再灌注损伤大鼠的炎性细胞因子。(表2)
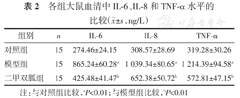
各组大鼠血清中IL-6、IL-8和TNF-α水平的比较( ±s,ng/L)
±s,ng/L)
各组大鼠血清中IL-6、IL-8和TNF-α水平的比较( ±s,ng/L)
±s,ng/L)
| 组别 | n | IL⁃6 | IL⁃8 | TNF⁃α |
|---|---|---|---|---|
| 对照组 | 15 | 274.46±24.15 | 308.57±28.69 | 319.28±30.26 |
| 模型组 | 15 | 865.24±60.28a | 1 039.34±80.65a | 1 214.39±94.58a |
| 二甲双胍组 | 15 | 425.48±41.47b | 652.38±50.72b | 572.81±47.15b |
注:与对照组比较,aP<0.01;与模型组比较,bP<0.01
Western Blot检测结果显示,与对照组相比,缺血再灌注24 h后,模型组大鼠脑组织中HIF-1α和BAX蛋白的表达水平明显上调,而BCL-2蛋白的表达水平明显下调,其差异均具有统计学意义(均P<0.01);与模型组相比,二甲双胍组大鼠脑组织中HIF-1α和BAX蛋白的表达水平下调,而BCL-2蛋白的表达水平上调,其差异均有统计学意义(均P<0.01)。上述结果表明,二甲双胍能抑制局灶性脑缺血再灌注24 h所诱导的HIF-1α蛋白的表达,并调控凋亡相关蛋白的表达,减少脑组织细胞凋亡,二甲双胍对脑缺血再灌注损伤的保护作用与其调控细胞凋亡密切相关。(图2)
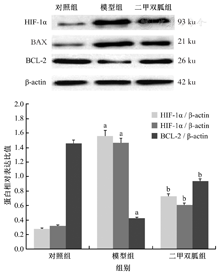

HIF-1α—缺氧诱导因子-1α;BAX—免抗人单克隆抗体;BCL-2—B淋巴细胞瘤基因;β-actin—肌动蛋白。与对照组比较,aP<0.01;与模型组比较,bP<0.01
炎性反应是脑梗死重要的病理生理过程,脑梗死患者脑缺血受损部位有白细胞浸润和炎性细胞因子存在,表明炎性过程参与了脑缺血的神经细胞损伤[11]。目前,无论是动物模型研究还是临床试验均支持炎性反应参与缺血性脑损伤。抗炎治疗可加宽脑梗死的治疗时间窗,但炎性反应自身及其对缺血性脑损伤的影响相当复杂,且因缺血程度与缺血再灌注时间的不同而存在差异[12]。脑组织局部产生过度炎症反应及细胞凋亡增加在脑缺血再灌注损伤中起重要作用[13]。因此,针对脑缺血再灌注损伤炎性因子及细胞凋亡的研究显得相当重要。本研究中,采用线栓法构建大鼠大脑MCAO模型,探讨二甲双胍对脑缺血再灌注损伤大鼠炎性因子和细胞凋亡的影响。结果表明,脑缺血再灌注损伤大鼠出现神经功能损伤症状,其脑组织出现脑梗死病灶与细胞凋亡增加,脑组织中凋亡相关蛋白表达失调,血清中炎性因子表达增加。而给予二甲双胍治疗的脑缺血再灌注损伤大鼠,其血清中炎性因子的表达显著降低,表明二甲双胍对该损伤具有显著疗效。
TNF-α是参与炎症反应的重要因子之一,脑缺血损伤发生后,TNF-α表达水平快速升高可加剧血管炎症反应,增加兴奋性神经递质的释放,诱导细胞坏死并加重脑组织损伤[14]。IL-6是炎症急性反应期重要的细胞因子之一,其表达失调与缺血再灌注损伤密切相关,在脑缺血急性期的表达水平显著增高,并与其预后不良有密切联系[15]。IL-8是一种强力的中性粒细胞趋化和活化因子,可趋化并激活中性粒细胞,促进中性粒细胞的溶酶体酶活性和吞噬作用[16]。本研究结果表明,二甲双胍能显著降低脑缺血再灌注损伤大鼠血清中IL-6、IL-8和TNF-α的表达,抑制其炎性细胞因子与炎性反应,发挥其对脑损伤的保护作用。
HIF-1α是缺血、缺氧环境中的重要信号分子。在低氧条件下,HIF-1α被上调,并和芳香烃受体核转运子(aryl hydrocarbon receptor nuclear translocator 1,ARNT-1)形成HIF-1复合物,随后结合到缺氧反应元件(hypoxia responsive element,HRE)上,从而激活相应基因包括GLUT-1、p53、p21、BCL-2等[17]。此外,HIF-1α对缺血缺氧环境中细胞的能量代谢、血管收缩控制、血管生成及细胞凋亡等方面均具有重要作用[18,19]。在改善炎症方面,HIF-1α不仅可以调节参与炎症反应的重要分子如血管内皮生长因子(vascularendothelial growth factor,VEGF)和一氧化氮,同时也在影响炎症细胞因子释放及调节免疫应答方面发挥重要作用[20]。本研究结果表明,二甲双胍能显著降低大鼠脑组织中HIF-1α和BAX蛋白的表达水平,升高BCL-2蛋白的表达水平,进而调控凋亡相关蛋白的表达,减少脑组织细胞凋亡。
二甲双胍可明显减轻脑缺血再灌注大鼠神经功能损伤,减少脑组织细胞凋亡,并对脑缺血再灌注损伤起保护作用。其作用机制可能与调控凋亡相关蛋白的表达、抑制HIF-1α表达、抑制相关炎症因子(TNF-α、IL-6和IL-8)释放有关,但其确切的调控信号通路和作用机制还需进一步研究证实。本研究中,验证了二甲双胍对脑缺血损伤后大鼠的神经功能的保护作用,为二甲双胍在缺血性脑血管病的应用提供理论依据。
无



























