
探讨超声引导病理穿刺取材在新型冠状病毒肺炎死亡病例尸检中的初步应用价值。
选择2020年2月20日至3月28日于华中科技大学同济医学院确诊新型冠状病毒肺炎死亡患者24例,男性17例,女性7例,年龄39~91(66.6±10.6)岁。超声引导行心脏、双肺、肝脏、双肾及脾脏组织穿刺取材,记录每例取材所需时间,并测量各器官取材组织标本的大小。以满足病理组织学、免疫组化及遗传学分析样本需求量为取材成功标准,计算超声引导下尸检病理穿刺取材技术对各器官组织的取材成功率。
超声图像可清晰显示穿刺针的行进路径,并准确定位心脏、肺、肝脏、肾脏及脾脏等脏器穿刺部位。每例尸检穿刺取材所需时间32~54(39.8±5.7)min。心脏、双肺、肝脏、双肾、脾脏取材标本长度分别为10(8,14)mm、13(12,15)mm、14(13,15)mm、13(11,15)mm、14(13,15)mm。超声引导病理组织穿刺取材成功率为心脏87.5%(21/24)、双肺91.7%(44/48)、肝脏100%(24/24)、双肾89.6%(43/48)、脾脏83.3%(20/24)。
超声引导穿刺病理取材能快速获取新型冠状病毒肺炎死亡患者组织标本,为尸检病理取材提供了一种实用方法。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
新型冠状病毒肺炎(COVID-19)已成为全球重大的突发公共卫生事件。截至2020年5月10日,全球确诊COVID-19患者已超过3 925 818例,死亡274 488例,其中中国确诊患者84 450例,死亡4 643例[1,2]。目前,有关COVID-19的致病机制及致死原因尚不完全明确,诸多病理过程与临床诊断尚缺乏充足的病理学证据[3,4,5]。尸检是研究和诊断重大疫情疾病的重要科学手段,特别是对一个危害严重的新发疾病尤其如此。基于尸检取材的病理学研究对提高临床救治水平和防控效果具有重大意义[4,5,6]。传统解剖尸检受多种因素的影响,国内开展十分有限。高传染性疾病传统解剖尸检对解剖场所防护条件要求高,操作人员暴露感染风险大,在重大疫情流行期间开展受限因素多[4,7,8,9]。超声影像设备具有实时显像、便于移动、高图像分辨力等特点,在日常临床工作中超声引导活体器官组织穿刺取材已得到广泛应用。国内王福生院士及卞修武院士等团队报道了数例COVID-19死亡患者微创穿刺取材的病理结果[10,11],但有关超声引导穿刺取材的文献尚少。本研究介绍24例COVID-19死亡患者超声引导穿刺病理取材的实践体会,初步探讨超声引导下尸体组织穿刺病理取材的应用价值与前景。
选择2020年2月20日至3月28日于华中科技大学同济医学院附属协和医院诊治的24例COVID-19死亡患者尸体,其中男性17例,女性7例,年龄39~91(66.6±10.6)岁。纳入标准:①死者年龄>18岁;②确诊为COVID-19;③尸体组织取材距死亡时间<2 h。
本研究经华中科技大学同济医学院附属协和医院伦理委员会批准通过([2020]伦审字[0139]号),超声引导取材前由死亡患者直系亲属签署知情同意书。
①M9型便携式彩色多普勒超声诊断仪(深圳迈瑞生物医疗电子股份有限公司),配备C5-1s凸阵探头、SP5-1s相控阵探头、L12-4s高频线阵探头;②一次性无菌探头保护套(经方精密医疗深圳有限公司);③JSM-022、JSM-011、JSM-007超声探头穿刺架(经方精密医疗深圳有限公司);④Max-Core 1416一次性活检针(Bard Peripheral Vascular,Inc)。
超声引导微创取材团队由2名中高年资超声介入医师、2名病理科医师组成。2名超声医师各操作一台超声仪,对不同器官进行分工取材。病理科医师辅助超声医师操作超声仪主机,并进行取材标本现场质控、测量、分装及密封。
超声引导下微创尸检流程如下:
(1)所有参与人员穿戴三级防护后进入隔离病区内终末处理间。
(2)取材前所有人员对逝者遗体行集体默哀。
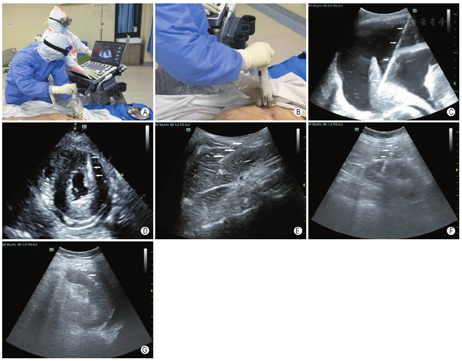
(3)尸体平卧位,充分暴露胸腹腔。1名超声介入医师于尸体左侧操作,负责左肺、心脏、脾脏、左肾取材,另1名超声介入医师位于尸体右侧操作,负责右肺、肝脏、右肾取材。超声介入医师先快速行胸腔、腹腔超声检查,检查各取材脏器的解剖位置与形态结构,存储超声图像。依据病理取材部位需求,在超声引导下,14G活检针行徒手或穿刺架导向下穿刺取材(图1A,图1B),各部位包括基于脏器解剖分布的基础取材和局灶性病变的附加取材。①肺取材:分别于左锁骨中线3、6肋间,腋中线4、7肋间及右锁骨中线3、4、6肋间、腋中线4、5、7肋间进行双肺基础穿刺点取材,各穿刺点至少取材2次。含气肺组织紧邻胸膜下者,第1次于超声图像显示针尖达胸膜表面时取材,第2次当针尖达胸膜表面后继续进针2 cm进行取材;胸腔积液或实变肺者,超声图像引导穿刺针尖到达肺组织表面时穿刺取材第1次,第2次在针尖达肺表面后继续进针2 cm取材(图1C)。实际操作中为最大程度保证准确取材,对超声图像显示为局灶性异常声像图区域需增加穿刺取材。②心脏取材:心脏左室、室间隔及右室各行基础取材3次。胸骨旁或剑突下短轴切面图像引导左室壁心肌取材(图1D),胸骨旁短轴、心尖或胸骨旁四腔切面图像引导室间隔心肌取材。超声图像引导穿刺针尖达心外膜后,微调进针方向,尽量使穿刺针行进方向与心室壁或室间隔组织平行,再继续进针0.5 cm取材。右室壁心肌取材可选择胸骨旁长轴或短轴切面引导,可徒手或穿刺架导向下操作穿刺针,超声图像显示针尖达心外膜后直接穿刺取材。剑突下切面引导取材时推荐使用穿刺架。对于超声图像上显示心肌厚度及回声异常区域需增加穿刺取材。③肝脏取材:肝右叶经过右侧第6~8肋间斜切面引导进针,肝左叶及尾状叶于剑突下纵切面引导自足侧向头侧进针(图1E),超声引导下显示针尖进入肝包膜下1~2 cm后取材,肝右前叶、右后叶、左内叶、左外叶及尾状叶各取材2次,对于超声显示局灶性占位区域需增加穿刺取材。④肾脏取材:双肾于侧腰部纵切面或横切面穿刺架导向或徒手穿刺进针(图1F),超声图像显示针尖达肾上、中、下部包膜处直接取材,各部位取材2次,取材组织应包括肾实质和肾窦组织,超声发现局灶性异常回声区域需增加穿刺取材。⑤脾脏取材:于腋中线第10肋间水平引导进针,分别穿刺脾脏上、中、下部实质,超声图像引导下显示针尖进入相应实质后取材(图1G)。各部位取材2次,对于超声显示局灶性回声异常区域需增加穿刺取材。上述器官取材完成后,记录从开始超声检查至完成穿刺取材的总时间。

(4)病理科医师肉眼观察、判断取材组织条质量,测量、记录取材标本长度,并行分装及密封处理。
(5)各器官取材完成后,对遗体体表进行清洁。取材后穿刺点有体液渗出者,予以纱布及敷贴密封。通知民政部门相关人员按感控流程进行遗体处理。
(6)所用活检针毁形后置入锐器盒,与其他一次性使用物品及操作污染物分别用双层医疗废物黄色垃圾袋密闭封装,并行清晰COVID-19标识,按疫期感染性医疗废物处理。穿刺架用2 000 mg/L有效含氯消毒溶液浸泡30 min后清洗,集中送消毒供应中心消毒。术后操作间及超声仪器按终末消毒流程处理。
(7)按医院感控流程,由专人转运标本至病理科指定区域,进行后续处理及检验。
服从正态分布的计量资料以均数±标准差表示,不服从正态分布的计量资料以M(P25,P75)表示。
尸检取材病例年龄39~91(66.6±10.6)岁,男性17例,女性7例。7例有恶性肿瘤病史,14例合并高血压、糖尿病、冠心病、慢性肾病、支气管哮喘等慢性基础疾病。尸体肝脏、双肾、脾脏二维超声图像与活体器官超声图像类似。含气肺组织呈无滑动的气体反射表现,22例肺可见实变或压缩肺组织,呈胸腔内固定实性低回声,15例可见静态空气支气管征,16例伴不同程度胸腔积液(图2A)。心腔及大血管内可见实性血凝块组织回声(图2B)。肠管无蠕动,部分可呈类实性组织回声。1例可见胸腹壁软组织内大量气体反射(图2C)。


所有死亡患者均进行心脏、双肺、肝脏、双肾和脾脏超声检查与取材,耗时32~54(39.8±5.7)min。心脏、肺、肝脏、肾、脾脏标本长度分别为10(8,14)mm、13(12,15)mm、14(13,15)mm、13(11,15)mm、14(13,15)mm(图3)。以满足临床病理组织学、免疫组化及遗传学分析需求样本量为取材成功标准,心脏、双肺、肝脏、双肾和脾脏取材成功率分别为87.5%、91.7%、100%、89.6%、83.3%。各器官具体取材次数及相应取材失败原因详见表1。
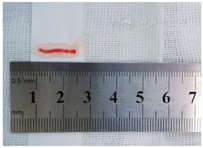


24例COVID-19死亡患者尸体组织超声引导下取材情况
24例COVID-19死亡患者尸体组织超声引导下取材情况
| 取材器官 | 穿刺次数 | 取材成功率 | 取材失败原因 |
|---|---|---|---|
| 双肺 | 483 | 91.7%(44/48) | 3例左肺:1例左侧胸腔充满积液与带状回声、1例左侧胸壁大量积气、1例左侧胸腔广泛积气1例右肺:胸腔大量积液,肺组织取材标本量少 |
| 心脏 | 198 | 87.5%(21/24) | 3例心脏:胸腔气体干扰且剑下切面无法显示心脏 |
| 肝脏 | 240 | 100%(24/24) | 无 |
| 双肾 | 264 | 89.6%(43/48) | 4例左肾:1例重度积水,肾实质菲薄,取材标本量少;1例腹壁大量积气无法显示;2例未测及左肾1例右肾:腹壁大量积气无法显示 |
| 脾脏 | 127 | 83.3%(20/24) | 4例脾脏:1例腹壁大量积气无法显示,3例未测及 |
目前,全球COVID-19疫情流行趋势依然严峻,死亡病例不断增加,降低危重症患者病死率是当前抗疫临床实践工作面临的重要挑战。通过尸检取材进行病理组织学、免疫组化及遗传学分析等研究是探究COVID-19危重症患者致死原因及临床病理改变的重要手段。由于国内生物安全保护3级(BSL-3)尸体解剖实验室严重配置不足及国人对解剖尸检认同率低等原因,COVID-19相关尸检取材工作及时开展十分受限。自Terry于1955年提出微创穿刺尸检的理念以来,伴随医学影像学技术的不断发展,基于CT、MRI、超声、腔镜等多种影像引导的微创尸体取材技术已成为获取尸体组织标本的重要手段[8,9,10,11,12,13,14,15]。近年来,国内外已有基于超声引导的HIV、MERS、黄热病、COVID-19等传染性疾病尸体组织取材的应用报道[10,11,13,14,15],但相关研究未对超声引导微创穿刺取材的具体技术方法进行介绍。本研究介绍24例COVID-19患者超声引导微创尸体组织穿刺取材的实践经验,初步探讨COVID-19死亡患者超声引导尸体组织微创穿刺取材的应用价值及前景。
国内外临床研究显示危重型COVID-19患者除肺部弥漫性损伤外,还常常伴随肝脏、心脏、肾脏和免疫系统等多器官组织的功能异常[3,16,17,18]。与活体组织病理穿刺取材不同,尸体穿刺取材无需考虑出血、气胸、周围脏器损伤等并发症[19],穿刺次数也无明确限制。本研究针对肺、心脏、肝脏、肾脏、脾脏采用14G活检针行多点多次穿刺取材,以提高获得的组织标本量。其中肺组织是COVID-19攻击的最主要靶器官,危重症患者肺组织常表现为渗出、实变、纤维化等多种病理改变共存,为提高肺组织穿刺取材组织病理改变的代表性,依据人体肺解剖定位于左锁骨中线3、5肋间,腋中线4、7肋间及右锁骨中线3~5肋间,腋中线4、5、7肋间进行至少双肺20个穿刺点常规取材,同时针对肺组织不同病变的超声图像改变,采取补充穿刺进一步提高病理取材的标本量。其他部位同样也采取基础穿刺点取材及局灶性病变的附加取材策略。
本研究在超声图像引导下,对不同组织病理取材的成功率分别为肺91.7%、心脏87.5%、肝脏100%、肾脏89.6%、脾脏83.3%。1例尸体因胸腹壁广泛积气影响心脏、左肺、脾脏、双肾超声图像显示,相应组织取材未成功,该例为ICU持续有创机械通气患者,胸腹壁积气不排除呼吸机相关肺损伤继发气胸后气体破入胸腹壁所致。另2例患者左侧胸腔大量气体干扰心脏显示,未完成相应组织取材。心脏组织取材成功率高于Cox等[13]报道的72%,可能与采取剑突下、左侧胸骨旁及心尖多路径多切面多点取材有关,也与穿刺架使用及超声介入医师操作经验有关。Fariña等[9]报道超声引导下尸体左肺组织取材成功率达100%,高于本研究,可能与两者纳入研究对象的肺部病变不同有关。本研究初期1例患者左侧胸腔见大量气体反射回声表现,多次穿刺无肺组织,考虑可能为大量气胸所致,活体气胸与正常肺气超声较易区别,后者多存在典型的肺滑动征[20],而尸体中此种差异消失,后期实践发现正常含气肺组织穿刺针进入脏层胸膜时可见脏层胸膜内移征象,可帮助鉴别。1例左侧胸腔充满积液并带状回声者超声未测及肺组织而未完成取材,考虑可能为压缩肺组织移位影响超声显示;1例右侧胸腔大量积液,超声显示压缩肺组织菲薄,取材时穿刺针与肺组织存在明显错动,局部肺组织取材量较少。对于大量胸腔积液影响肺组织取材者,可考虑先行胸腔积液穿刺引流后再行穿刺取材以提高肺组织显示和取材成功率。本研究肝组织取材成功率达100%,与既往报道一致[9,13,15]。肾脏组织取材成功率显著高于无影像引导下取材成功率[13]。本研究中脾脏取材成功率最低,除1例因腹壁广泛积气干扰显示外,余取材失败者有可能与患者左肺病变引起膈肌及脾脏位置移位、脾脏萎缩及尸体的体位影响超声显示有关。今后结合尸体影像学容积数据的融合成像导航技术,有望克服非目标气体干扰及器官组织位置改变对超声引导穿刺取材的影响。
高致病性传染病解剖尸检的诸多防护条件要求较高,超声引导尸体穿刺取材可于隔离病区内进行,亦可减低尸体转运过程中存在的潜在疾病传播风险。本研究平均每具尸体完成多种器官组织的超声引导取材耗时约40 min,明显短于传统解剖尸检的2~4 h。本研究所有尸体组织取材均在死亡后2 h内开始进行,明显低于解剖尸检的等待时间,有效减轻尸体组织自溶对器官组织结构的破坏,更有利于标本固定与进行微生物、免疫组化、电镜、RNA等检查[8,9,13,21]。此外,Kang等[22]报道,穿刺尸检取材较传统解剖尸检取材,死亡者家属可接受度提高18%。
超声引导穿刺病理取材是近年发展起来的一种尸检取材方法,与传统的大体解剖尸检相比,在诸多方面值得进一步研究与探讨:如针对不同的器官,选择何种切面去引导穿刺,以最大限度保证穿刺取材的准确性与全面性;针对不同病变,如何识别尸体脏器的超声图像特征,准确引导穿刺部位以获取高质量取材样本。随着研究的深入,尚需探讨超声引导穿刺尸检病理取材的标准与规范,并与传统大体解剖尸检进行比较,探讨其优点与局限性,以及特殊情况下该项技术应用的优势。随着该技术在日常临床工作中的不断成熟与规范应用,将有助于推动我国医学事业的发展。
所有作者均声明不存在利益冲突



























