本文综述了2015年美国心脏病学会和2016年欧洲儿童肺血管疾病协作网制定的儿童肺动脉高压诊治指南,强调了对肺动脉高压危象的早期识别及规范治疗,同时介绍了常用肺动脉高压治疗药物的使用方法和注意事项,以指导儿童肺动脉高压的诊治。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
肺动脉高压(pulmonary hypertension,PH)以肺动脉阻力进行性升高、最终引起右心功能衰竭为主要特征,因其起病隐匿、病因复杂、诊治困难,且严重者可因PH危象危及生命,越来越引起人们的关注。近年来,随着研究的进展及循证医学指南的更新,成人PH的预后有了极大的改善。然而,儿童PH与成人有着截然不同的病理生理特点,成人PH指南并不适用于儿童患者,因此,迫切需要针对PH患儿建立诊断标准及治疗流程。2015年美国心脏病学会[1,2]和2016年欧洲儿童肺血管疾病协作网[3,4]对儿童PH进行了详细的阐述,对其定义、评估和治疗进行了重点分析。本文将对上述指南内容进行阐述,以期对儿童PH有更深入的了解,更好的指导儿童PH的诊治。
儿童PH定义为足月儿出生3个月以后,在海平面水平静息状态下,肺动脉平均压≥25 mmHg(1 mmHg=0.133 kPa)[5]。胎儿肺动脉压力与体循环压力相似,出生后迅速下降,在两到三个月时达到成人水平。在某些情况下,肺动脉压力的升高不能排除PH性血管病(pulmonary hypertensive vascular disease,PHVD),比如先天性心脏病导致的肺动脉压力升高,其诊断和处理有着不同的临床特点。
成人和儿童的PH在血管功能和结构、遗传、病程、对右心室的影响和对PH治疗的反应方面都有很大差异,最主要的是因为儿童PH与肺的生长发育密切相关。正常肺血管床对维持肺的结构、代谢及气体交换非常必要,也具有对运动后负荷增加的耐受能力。新生儿和婴幼儿PH常常与出生后由胎儿循环向生后循环转化的功能和结构适应性改变有关[6],发育中的肺组织对不良刺激,包括高氧血症、低氧血症、血流动力学改变以及炎症所造成的肺血管损伤具有时限性,早期识别PH的易感因素,同时采取干预措施,存在一个重要的时间窗[7]。围生期婴儿PH的高危因素可能增加成年后发展为PH的风险[8]。此外,肺血管床发育的血流动力学影响、肺循环的成熟也在肺远端的肺泡发育和器官形成中发挥重要作用。儿童PH的发病机制与成人具有很大的差异[9],成人PH的治疗策略和最佳剂量在儿童身上还未得到充分研究时可能存在潜在不利,因此,儿童和成人PH的诊疗指南应该有所不同。
(1)在最初诊断PH时,需要综合病史和体格检查,到有经验的临床中心进行PH病理生理/分类和心脏功能的诊断性检查。(2)在诊断时,要进行影像学检查,排除包括肺动脉血栓栓塞性疾病、肺动脉周围狭窄、肺静脉狭窄、肺静脉闭塞病及肺实质性疾病[10]。(3)经过全面的初步评估后,进行系列的超声心动图检查,在处理不断变化的临床情况下,建议经常进行超声心动图检查。(4)推荐开始靶向治疗前,进行心导管检查,除非患儿处在危重情况下,需要立即进行经验性治疗[11]。(5)除非有特殊的禁忌证,心导管检查应包括急性血管反应试验(acute vasoreactive testing,AVT)[11,12]。(6)儿童AVT阳性的判断是肺动脉压(pulmonary artery pressure,PAP)和肺血管阻力(pulmonary vascular resisitance,PVR)/全身血管阻力(systemicvascularpressure,SVR)至少降低大于20%,而没有心输出量的减少。(7)在初始治疗后3~12个月,推荐重复心导管检查,以评估治疗反应或临床情况是否加重。(8)在评估预后和治疗后潜在反应时,应该做连续系列心导管检查。(9)磁共振成像用于随访评估心室功能和心室的大小变化。(10)脑钠肽(BNP)或脑钠肽前体(pro-BNP)作为诊断和随访期间临床决策补充手段。(11)6 min步行距以测试不同年龄的PH患者运动能力。(12)推荐将睡眠研究作为PH患者睡眠呼吸紊乱风险诊断评估的一部分,也可以作为评估患者对治疗反应的方法。
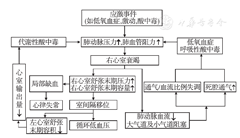
肺动脉压的急剧升高是威胁生命的紧急状态,可能很快导致心肺功能的衰竭。慢性PH引起右心室负荷增加,血管适应性改变和重塑,在代偿机制失败,右心收缩功能失代偿、左室前负荷急剧下降导致心输出量和冠状动脉灌注减少时,称为PH危象[13]。此时,没有"准备好"的右心室不能耐受后负荷急剧升高(即肺动脉压力),健康成人肺动脉压力急剧升高>40 mmHg,右心室将不能很好地工作,当右心室后负荷剧烈升高,超微结构和功能不能产生适应性改变,心律失常、心肌缺血和(或)肺部疾病,都可能触发肺血管阻力升高,肺动脉压力急剧升高,右心室扩张,收缩功能受损,右心室衰竭[14];右心室舒张末期容积增加,导致室间隔左移,左心室舒张末期容量减少,左心输出量减少,引起体循环动脉低血压、左心室和右心室舒张末期压力增加;右心室舒张末期压力及容积增高,降低了冠状动脉的灌注,引起心肌缺血、组织缺氧和酸中毒,进一步升高肺血管阻力和肺动脉压力;右心室衰竭引起肺血流减少,肺小动脉扩张和肺水肿,导致气道阻塞,肺通气死腔增加和通气血流比例失调,加重低氧血症和呼吸性酸中毒,使肺动脉压力和肺血管阻力进一步增高,形成恶性循环(图1)[1]。
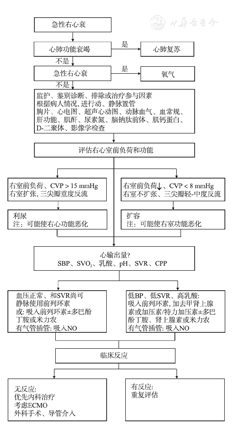
欧洲心脏协会和美国心脏协会基于儿童PH的诊治,提出如表1中的推荐。ICU里急性PH的治疗如下:

儿童重症监护病房急性肺动脉高压的治疗建议[1]
儿童重症监护病房急性肺动脉高压的治疗建议[1]
| 推荐 | COR推荐级别 | LOE证据级别 |
|---|---|---|
| 在有肺动脉高压和心脏解剖正常的患儿血氧饱和度<95%时给氧 | Ⅰ | C |
| 有严重肺动脉高压的患儿静脉使用前列环素 | Ⅱa | B |
| 在术后有肺动脉高压需要进行机械通气的患儿,为了改善氧合,建议使用吸入NO,以减少肺动脉高压危象 | Ⅱb | B |
| 为了防止肺动脉高压反弹,在撤除吸入NO的过程中,建议合并使用西地那非;在逐步撤除吸入NO过程中,也可以再次开始NO吸入 | Ⅰ | B |
| 建议在危重症患者有肺动脉高压时,静脉使用西地那非,特别是对吸入NO治疗效果欠佳的患者 | Ⅱb | B |
| 在儿童术后肺动脉高压的患者,吸入伊洛前列素效果与吸入NO效果相当 | Ⅱb | B |
| 在最佳的内科治疗后,仍然有心输出量降低、严重呼吸衰竭症状的患儿,可以考虑使用体外生命支持 | Ⅱb | C |
氧气是潜在的肺血管扩张剂和弱的体循环血管收缩剂,在动脉血氧饱和度<95%时需要进行氧疗,以保证周围器官足够的能量代谢。存在体-肺循环分流的儿童,氧疗会增加肺循环血量使心脏功能和肺功能恶化,这部分患者动脉血氧饱和度在75%~85%时才需要氧疗。
在PH危象时,碱化是即刻有效的治疗手段,酸中毒会提高肺动脉压力,降低正性肌力药物和血管活性药物的作用,pH值达到7.44可明显降低肺动脉压力。应注意新生儿长时间低碳酸性碱化可能导致神经系统损害。
焦虑和躁动会增加肺动脉压力和氧耗,应该尽量避免。
对有严重PH合并明显紫绀,初始治疗无效的呼吸性酸中毒和代谢性酸中毒患儿,应该采用机械通气,而对内科治疗有效的患儿则应避免机械通气。对PH患儿进行麻醉时,应有经验丰富的麻醉师在场。气管插管时麻醉诱导可能引起外周血管阻力的明显下降,从而引起循环衰竭,可以使用血管加压剂。避免可能引起PH危象的处理,如镇静不足、PCO2升高或导管内吸引。推荐采用正常的机械通气(维持PCO2水平在35~40 mmHg之间)和较长的呼气时间,换气过度会减少心输出量,增加外周血管阻力,引起肺损伤。
在新生儿及显著PH患者,右心室功能与前负荷密切相关,他们对容量丢失的耐受性差,在急性PH危象患儿,容量控制可能有用,但必须进行血流动力学监测。另一方面,慢性右心衰竭常常伴有液体过负荷和体循环的充血。当不得不使用利尿剂或者血液滤过时,要注意降低右室负荷的时候,也会降低心输出量。
肺动脉高压的靶向治疗能够改善肺血流和降低右心室后负荷,在排除了通气血流比例失调的情况下,危重PH患者可以考虑静脉使用前列腺素类药物(依前列醇、伊洛前列素、曲前列环素),由于前列腺素类药物会降低外周血管阻力,故应同时使用全身性的缩血管药物。由于吸入性的前列腺素类药物和吸入一氧化氮对外周血管阻力影响较小,故早期应考虑使用,特别是在全身血压较低的时候。此外,吸入或雾化治疗不会加重通气血流比例失调,而静脉途径可能产生不良影响。
吸入一氧化氮是机械通气患者的首选治疗方案。在体外循环治疗后,吸入一氧化氮可以降低肺动脉压力、降低PH危象的风险和缩短术后过程。然而,最近先天性心脏病患者吸入一氧化氮的Meta分析研究显示,主要结果治疗后的生存率和次要结果严重的血流动力学方面受到质疑,作为替代方案,有研究发现吸入伊洛前列素对降低肺动脉压力有一定疗效,但目前尚缺乏设计良好的前瞻性的临床研究。
口服西地那非有利于吸入一氧化氮的撤除,然而,在ICU口服药物常有无法预知的吸收问题,先天性心脏病术前预防性地使用西地那非对PH有一定疗效,也有静脉使用西地那非的报道,但其作用尚未完全肯定,其不良反应包括低血压和对氧合的影响[21]。
在PH合并有严重右心衰竭的情况下,有必要使用正性肌力药物。米力农和左西孟旦可作为正性肌力药物的首选,其能够降低肺动脉压力,而对心率没有或很少影响。左西孟旦也是血管扩张剂,单中心研究显示左西孟旦在心脏外科手术后降低肺动脉阻力方面产生了积极的影响,其主要作用是改善了心肌收缩力。多巴酚丁胺和肾上腺素可以改善右心的收缩功能,但也可能诱发心动过速,降低舒张期充盈和冠状动脉灌注,降低心输出量。
去甲肾上腺素、垂体后叶素或特利加压素,可以用于促进逆转室间隔缺损导致的左向右分流,改善低血压患者的组织灌注,治疗由于PH靶向治疗引起的全身性低血压。病例系列研究显示,垂体后叶素和特利加压素在降低肺动脉阻力同时又提高了体循环阻力。
根据成人的治疗经验,应避免在急性心功能失代偿期和终末期的右心衰患者实施心房球囊扩张术(中心静脉压力>20 mmHg)。然而,在某些特定的患者,采用心房球囊扩张术,降低右心房和右心室的压力,可能可以挽救患者的生命[22]。
作为肺移植的替代治疗,有采用肺动脉分流术(Potts分流术)治疗特发性PH的少量病例研究,虽然通过手术有希望获得长期生存的结果,但由于病例有限,尚不能推荐使用[23]。
依赖右心功能的静脉-静脉或者静脉-动脉ECMO是通向恢复和移植的桥梁[24]。心脏手术后PH危象导致循环衰竭常常需要CPR,常规CPR不能恢复自主循环时,ECMO是很好的支持选择。
目前尚无证据支持心室辅助装置在PH引起右心室衰竭儿童中的治疗。
对于最大程度的联合治疗都无效果的PH患儿,PVP仍然处于Ⅲ到Ⅳ级,可以考虑双肺移植,肺移植的中位生存时间是5.6~6.1年[25]。
急性PH是儿童的严重并发症,包括先天性心脏病术后的PH患者,在PICU的治疗应该基于潜在的病理生理学,着眼于降低右心室后负荷、增加右心室前负荷和心肌收缩力的基本目标。此外,维持足够的冠状动脉灌注压和血流量,保证心肌的氧气和能量供应,从而保证左右心室的收缩功能和氧气供应。早期识别患者的特殊风险,及时建立有效的治疗措施,可以防止发生严重的心功能不全、低心排血量。
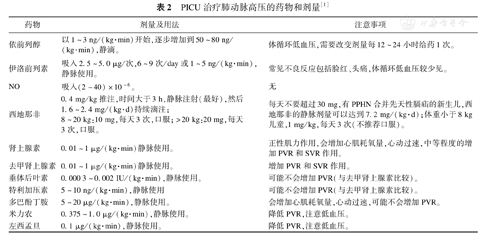
PICU治疗肺动脉高压的药物和剂量[1]
PICU治疗肺动脉高压的药物和剂量[1]
| 药物 | 剂量及用法 | 注意事项 |
|---|---|---|
| 依前列醇 | 以1~3 ng /( kg·min )开始,逐步增加到50~80 ng /( kg·min ),静滴。 | 体循环低血压,需要改变剂量每12~24小时给药1次。 |
| 伊洛前列素 | 吸入2.5~5.0 μg /次,6~9次/day或1~5 ng /( kg·min ),静脉使用。 | 常见不良反应包括脸红、头痛,体循环低血压较少见。 |
| NO | 吸入(2~40)×10-6。 | 无 |
| 西地那非 | 0.4 mg/kg推注,时间大于3 h,静脉注射(最好),然后1.6~2.4 mg/( kg·d )持续滴注;8~20 kg:10 mg,每天3次,口服;>20 kg:20 mg,每天3次,口服。 | 每天不要超过30 mg,有PPHN合并先天性膈疝的新生儿,西地那非的静脉剂量可以达到7.2 mg/( kg·d );体重小于8 kg儿童,1 mg/kg,每天3次(不推荐口服)。 |
| 肾上腺素 | 0.01~1 μg /( kg·min )静脉使用。 | 正性肌力作用,会增加心肌耗氧量,心动过速,中等程度的增加PVR和SVR作用。 |
| 去甲肾上腺素 | 0.01~1 μg /( kg·min )静脉使用。 | 增加PVR和SVR作用。 |
| 垂体后叶素 | 0.000 3~0.002 IU/( kg·min ),静脉使用。 | 可能不会增加PVR(与去甲肾上腺素比较)。 |
| 特利加压素 | 5~10 ng /( kg·min ),静脉使用 | 可能不会增加PVR(与去甲肾上腺素比较)。 |
| 多巴酚丁胺 | 5~20 μg /( kg·min ),静脉使用。 | 会增加心肌耗氧量,心动过速,可能不会增加PVR。 |
| 米力农 | 0.375~1.0 μg /( kg·min ),静脉使用。 | 降低PVR,注意低血压。 |
| 左西孟旦 | 0.1 μg /( kg·min ),静脉使用。 | 降低PVR,注意低血压。 |