肺通气/灌注(V/Q)平面显像常用于肺栓塞检查,但存在局限性,SPECT显像通过生成的三维显像数据可克服诸多局限。肺V/Q SPECT显像较平面显像有更高的灵敏度、特异性和准确性,且诊断不明确率低。SPECT显像可采用V/Q比值参数图显示和分析数据。较之CT肺血管造影,SPECT显像灵敏度高、辐射剂量低,且无造影剂相关的不良反应。任何配置有现代多模态显像设备的核医学科都可进行肺V/Q SPECT与CT(低剂量程序)融合显像,以提高诊断准确性。肺V/Q SPECT显像(有或无CT融合)也可应用于其他肺疾病诊断及研究。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
自Wagner等[1]于1964年首次报道以来,肺平面显像一直是核医学中常用的显像方法之一,但这项检查有明显的局限性[2,3],尤其存在解剖部位的重叠,难以把放射性缺损定位到具体肺段,且不同患者间肺段的大小和形状差异使其难以准确判断单个肺段栓塞的程度[2],栓塞处放射性缺损若与正常灌注的肺段重叠则难以被探测到,致使肺灌注减低的程度被低估[4]。此外,平面显像通常不能观察到右肺下叶基底段[2,5]。受这些因素影响,此法达不到报告标准,再加上其相对高的诊断不明确率,因此不能满足临床需求[6,7],而增强CT肺动脉造影(CT pulmonary angiography, CTPA)采用二元的报告方式(阳性或阴性),在临床上尤其在美国已成为评估肺栓塞的首选影像检查方法[8,9]。
SPECT具有三维显像的能力,已常规用于核医学的很多方面,但很多单位肺显像仍采用二维显像技术。肺SPECT显像可避免肺段重叠及受邻近肺组织影响,能更准确地确定单个肺段灌注缺损大小和位置已是不争的事实[2]。
平面和SPECT肺显像的对比研究一致认为SPECT优于平面显像。对狗[10]、猪[11]及蒙特卡罗(Monte Carlo)模拟方法(亦称统计学模拟法)[5]的研究均显示SPECT对肺栓塞的探测较平面显像灵敏度更高。在人体研究中,Bajc等[12]发现SPECT探测肺栓塞的灵敏度较平面显像高(100%与85%)。在此研究中,SPECT较之平面显像,阅片人间的差异少,且能更好地显示不匹配缺损。Collart等[13]也证实SPECT比平面显像特异性好(96%与78%),且在阅片人自身(94%与91%)和不同阅片人间(88%与79%)都有更好的重复性。Reinartz等[14]对1组83例患者的研究表明,较之平面显像,SPECT有更高的灵敏度(97%与76%)、特异性(91%与85%)和准确性(94%与81%)。在此研究中,SPECT对肺段的缺损探测可提高约13%,对肺亚段的缺损可提高80%以上。综合来看,SPECT的灵敏度为80%~100%,特异性为93%~100%[8]。肺通气/灌注(ventilation/perfusion, V/Q) SPECT显像被一致认为其诊断不明确率比平面显像低得多,常不到5%[8,15,16,17,18,19]。Leblanc等[20]指出SPECT对肺栓塞的诊断有很高的阴性预测值,达98.5%。在对108例患者的研究中,仅3%的病例肺栓塞诊断不能明确。因此,SPECT较平面肺显像有更好的灵敏度和特异性,可重复性高,且诊断不明确率低。
1.技术要求。如平面显像一样,SPECT显像通常先行肺通气显像,再行肺灌注显像。肺通气显像有多种显像剂选择。惰性放射性气体如81Krm和133Xe反映局部通气最准确,但由于采集图像时需持续给药,且成本贵,81Krm发生器的寿命短,只有少数单位能使用[21]。尽管133Xe有半衰期更长的优势,但因其再循环和低γ光子能量导致空间分辨率低,故并不是最理想的选择[21]。由于这些局限性,99Tcm-二乙烯三胺亚乙酸(diethylene-triamine pentaacetic acid, DTPA)或超细碳纳米颗粒99Tcm-Technegas(Cyclomedica)等锝标记的微粒子气溶胶因其易获得、成本低、成像质量好,得到了更广泛的应用[19]。Technegas是肺通气SPECT显像的理想显像剂,其颗粒直径为30~60 nm,可更多抵达肺泡,而不像99Tcm-DTPA等雾化生成的水性放射性气溶胶易在中央部位沉积[22]。但美国Technegas未商业化提供,因而不能向SPECT显像转化[23],只能选择99Tcm-DTPA或99Tcm-硫胶体等。虽然99Tcm-DTPA的显像质量在许多患者中已能满足要求,但Technegas能更好地到达肺末梢部位,更适于阻塞性肺病的患者[24]。99Tcm标记的肺通气显像剂给药剂量通常为30~50 MBq,与平面显像的剂量相当[14,17,20]。
肺血流灌注评估常用99Tcm-大颗粒聚合白蛋白[17]。99Tcm-大颗粒聚合白蛋白的给药剂量取决于肺通气显像剂的种类和剂量,但若肺通气显像剂是锝标药物,则一般约为100~250 MBq。欧洲核医学协会肺V/Q SPECT显像指南的推荐剂量为该范围的低值,但最终给药剂量应由每个单位依据图像质量和当地辐射防护标准决定[25]。图像质量受准直器、γ相机的灵敏度和处理参数等因素的影响。
对孕妇而言,肺通气和肺灌注显像的给药剂量通常减半[25],因此需要延长图像采集时间以保证图像质量。一些单位提倡省去肺通气显像,但此举降低的辐射量很小,且可能影响诊断准确性[26]。
2.图像采集、处理、显示和报告。多探头γ相机更适合肺V/Q SPECT显像[19]。一般而言,完成肺通气和肺灌注显像需要20~30 min,比传统的采集6或8个平面体位图像所需时间少[14,20]。常规的图像采集和处理参数见表1。在装有专用图像显示软件包的工作站上呈现图像可得到最好的阅片效果。这种软件包能自动或手动融合肺通气和肺灌注的图像数据,且可在各垂直切面上审阅图像[27]。

肺V/Q SPECT显像的常规图像采集和处理参数a
肺V/Q SPECT显像的常规图像采集和处理参数a
| 参 数 | 描 述 |
|---|---|
| SPECT图像采集方法 | 每帧3°,共360° |
| 每个投射采集时间 | 肺通气显像12 s,肺灌注显像8 s |
| 准直器 | 低能高分辨 |
| 矩阵大小 | 128×128(64×64也可) |
| 重建方法 | 有序子集最大期望值法(8次迭代,4个子集) |
| 重建后滤波 | 三维Butterworth滤波,cutoff值0.8周期/cm,序列9 |
注:a本法来自Royal North Shore Hospital, Sydney
对于熟悉平面影像图的报告专家,SPECT显像数据可采用多种方法生成平面图像。Bailey等[28]提出了1种重投影(reprojection)的方法,但很多商用软件提供的是更简单的角度求和方法。这种方法通过对SPECT图像的多个连续投影求和生成图像,在一定弧度上获得数据,因此会使小的放射性缺损变模糊,但能生成近乎真实的平面显像图[29]。这些平面显像图为快速评估提供了熟悉而快捷的肺视野图,对平面显像向SPECT图像转化有着特殊的价值。
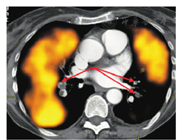
SPECT显像数据可进行更高级的数据处理。首先,通过扣除之前肺通气显像中残留的本底放射性,以进一步增强肺灌注SPECT显像中的放射性缺损对比度[12,30]。其次,通过测定基于像素的V/Q比值可从SPECT数据中生成比值图。这些图像有助于撰写诊断报告,且能改善放射性缺损的定位和程度的显示(图1)[30]。另一项图像处理技术是V/Q比值的客观定量,已证实其能增加诊断准确性,减少诊断不明确数量[31,32]。

肺V/Q显像常依照欧洲核医学协会的指南发诊断报告。该指南建议,如果肺V/Q显像出现至少1个或2个亚段与肺血管解剖相符的不匹配,则可报告为肺栓塞阳性[17]。不建议肺V/Q SPECT显像采用平面显像中使用概率的报告方法[14,33]。
3.与CTPA的比较。多探头CTPA已发展成潜在肺栓塞患者常用的首要影像检查方法[34]。美国许多医疗单位已将其作为评估肺栓塞的首选影像检查。这种倾向有多种原因:易行(尤其在非工作时间),图像采集速度快,能诊断除肺栓塞外导致患者症状的其他病情,以及相关医师更偏好二元论的报告[8,9]。
但CTPA用于肺栓塞的诊断有明显的局限性。首先,一些研究[18,35]表明CTPA的灵敏度不足。在1项大样本肺栓塞诊断Ⅱ期的前瞻性研究中,CTPA灵敏度为83%(当把技术不达标的病例纳入后则为78%)[35]。当显影结果与临床的预计不一致时,诊断准确性尤其不佳,这与初期肺栓塞诊断中平面肺V/Q显像的结果相似[36]。其次,技术上的伪影会影响图像质量,这主要与肺动脉对比度较差、运动伪影和某些患者体质相关的图像噪声有关[37]。技术因素导致的诊断不明确率估计为5%~11%[38,39]。孕妇患者的诊断不明确率更高,30%以上的CTPA诊断不明确,甚至采用64排CT时也存在较高的诊断不明确[40,41],这被认为是孕期下腔静脉压力增大所致。第三,静脉注射造影剂可产生不良反应。在肺栓塞诊断研究中,22%的患者由于造影剂过敏和肾功能不全被剔除在外[35]。有研究报道[42]行CTPA后3%的患者会出现某种即时的造影剂反应等并发症,1%~3%的患者会出现造影剂引发的肾病[42]。第四,CT辐射量高,CTPA对乳腺的辐射剂量估计为10~70 mSv,对于年轻女性应特别注意[44,45]。与之相比,肺V/Q显像对乳腺的辐射剂量约为0.3~1 mSv[46]。CTPA的总辐射剂量约为8~20 mSv,而肺V/Q SPECT显像则约为2.5 mSv[26],因此不适合用CTPA来随访监测肺栓塞治疗。最后,一些次要病变或不相关病变的发现会引起人们的担心,虽然CTPA在很多患者中能诊断其他病变,但这些病变可能并非患者出现症状的原因[47]。对这些偶然发现的次要病变进一步检查花费昂贵,还会造成额外的辐射和造影等侵入性检查,但回报并不确定[48]。研究[49]发现,在前期检查有低或中度可能性而常规胸部X线片无明显证据的患者中,行CTPA检查后仅3.2%的病例改变了诊断。
总之,直接对比肺V/Q SPECT显像和CTPA的研究相对较少。Reinartz等[14]发现SPECT比4排的CTPA检查灵敏度高(97%与86%),但特异性低(91%与98%)。Miles等[50]在1项含100例患者的研究(使用16排CTPA)中也发现两者准确性相当。研究指出SPECT检查的禁忌证更少,患者辐射剂量也更低,且对非诊断性的病变发现较少。Gutte等[18]在对81例患者的研究中发现,肺V/Q SPECT显像较16排的CTPA灵敏度高(97%与68%),但特异性低(88%与100%)。
上述对比研究一致表明,SPECT检查灵敏度高,CTPA特异性高,而总的准确性两者相当。每种显像模式都有其优势和不足(表2),因此任何患者在选择检查方式时都应考虑包括年龄、性别、肾功能情况、糖尿病、合并的肺疾病及医院本身等因素(如检查的易获得性及专业知识情况)。
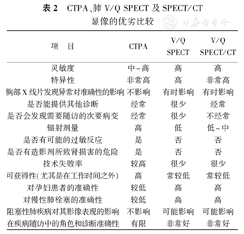
CTPA、 肺V/Q SPECT及SPECT/CT显像的优劣比较
CTPA、 肺V/Q SPECT及SPECT/CT显像的优劣比较
| 项 目 | CTPA | V/QSPECT | V/QSPECT/CT |
|---|---|---|---|
| 灵敏度 | 中~高 | 高 | 高 |
| 特异性 | 非常高 | 高 | 非常高 |
| 胸部X线片发现异常对准确性的影响 | 不影响 | 有时影响 | 有时影响 |
| 是否能提供其他诊断 | 经常 | 很少 | 经常 |
| 是否会发现需要随访的次要病变 | 经常 | 很少 | 不经常 |
| 辐射剂量 | 高 | 低 | 低~中 |
| 是否有可能的过敏反应 | 是 | 否 | 否 |
| 是否有造影剂所致肾损害的危险 | 是 | 否 | 否 |
| 技术失败率 | 较高 | 很少 | 很少 |
| 可获得性(尤其是在工作时间之外) | 高 | 常较低 | 常较低 |
| 对孕妇患者的准确性 | 较低 | 高 | 高 |
| 对慢性肺栓塞的准确性 | 较低 | 高 | 高 |
| 阻塞性肺疾病对其影像表现的影响 | 不影响 | 可能影响 | 可能影响 |
| 在疾病随访中的角色和诊断准确性 | 有限 | 非常好 | 非常好 |
尽管V/Q不匹配是肺栓塞的标志,但其他病变也可导致这种表现[17]。此外,并非所有的肺栓塞患者都有典型的V/Q不匹配表现,因为有些患者发展成肺梗死而表现为匹配的缺损[17]。为此,多数认为胸部X线片表现有助于解释肺V/Q显像,胸部X线片所见病变常用于提高肺V/Q显像报告的准确性和特异性[17,36,51]。
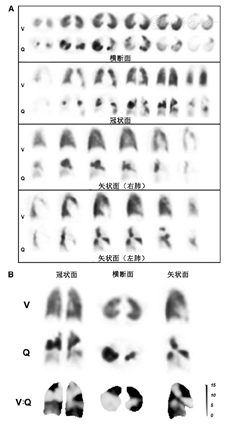
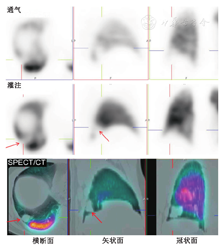
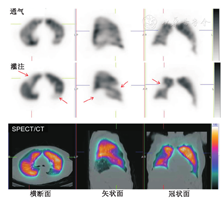
随着SPECT/CT的发展,将CT扫描的解剖信息与SPECT显像的功能信息进行融合已成为可能。肺V/Q SPECT显像联合CT扫描,甚至可以采用低剂量CT扫描来降低患者辐射剂量,以充分发挥每种显像模式的优势。肺栓塞以外的病变(如放疗后改变、肺气肿、肿瘤或纵隔淋巴结肿大等病变引起的外周血管受压)造成的V/Q不匹配也可被SPECT/CT显像发现(图2)[17]。另外,SPECT/CT有助于确定非栓塞病因所致的匹配改变,如肺炎、肺脓肿、胸膜或心包积液、肿瘤和肺梗死(图3)[3,9,47]。因此,SPECT/CT融合显像可通过明确引起灌注缺损的原因而提高肺V/Q显像的特异性[18,52]。肺V/Q SPECT/CT显像能通过单次显像过程为肺栓塞探测提供较高灵敏度和特异性的诊断,这也有助于鉴别导致胸痛和呼吸困难的各种其他疾病。


1.操作流程,图像处理,图像显示和报告。双探头SPECT/CT目前已在很多核医学科应用,虽然大多数设备可以使用诊断级CT,但也可使用低剂量参数只做衰减校正和解剖定位[52]。
肺CT扫描常在肺灌注SPECT显像之后即刻进行,不需要静脉造影剂,其管电流降至20~80 mA即可,如此其辐射剂量为1~2 mSv[18,26],与肺V/Q显像自身的辐射剂量2~2.5 mSv相当,远小于诊断性CTPA受到的辐射水平[26,45,53]。CT采集速度快(小于1 min),加上设置时间也只是在肺V/Q SPECT显像基础上增加几分钟。虽然屏气常用于诊断性CT检查,但由于SPECT采集时间长而不能用于肺V/Q SPECT显像。为减少呼吸运动造成的图像重合不良,建议在吸气中量时屏气进行CT扫描,或者扫描时让患者维持浅呼吸状态[54]。
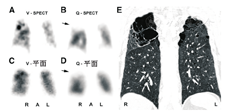
建议肺V/Q SPECT/CT显像与SPECT显像一样按照欧洲核医学协会的指南发报告。尽管这些指南没有专门叙述融合显像,但CT部分的加入可能有助于对肺V/Q SPECT显像进行更恰当的判断。CT可提供患者的解剖信息,包括肺和肺段边界、叶间裂、大血管位置和任何与之相关的实质性病变(图4)。叶间裂位置值得注意,因为在肺灌注SPECT显像上能见到1条与之对应的线形减低,而在肺通气显像上程度低一些。任何V/Q匹配改变的部位都值得注意,因为继发于肺栓塞的实质性改变常发生在缺损外围,而炎性病变所致的病变常见于邻近缺损处[55]。

2.临床价值。许多研究证实,肺SPECT/CT联合显像能改善肺核素显像的特异性和总的诊断准确性。Herald等[56]报道的1组48例患者的研究表明,SPECT显像联合低剂量CT(30~50 mA)可使肺V/Q SPECT显像的假阳性率降低50%。Gutte等[18]的更大样本前瞻性研究表明,肺V/Q SPECT显像联合低剂量CT有很高的诊断准确性。在这81例连续患者的系列研究中,81Krm气体被用作肺通气显像剂,结果显示肺V/Q SPECT/CT显像与SPECT显像有同样的灵敏度(97%)。然而低剂量CT的加入表明,肺灌注显像的不匹配缺损可能归因于叶间裂等解剖结构及诸如肺气肿、肺炎、肺不张、胸腔积液等病理改变,因此核素显像的特异性可从88%提高至100%。肺V/Q SPECT/CT显像的诊断不明确率为0,而单用SPECT显像则为5%。这是目前唯一直接对比16排CTPA和肺V/Q SPECT/CT显像的研究[18]。尽管CTPA特异性高达100%,与所报道的肺V/Q SPECT/CT显像的特异性相同,但其灵敏度比SPECT和SPECT/CT都低得多(68%与97%)。
SPECT/CT显像的另一优势是能将患者的肺灌注缺损精确地定位到肺段。由于个体的解剖会因肺不张和胸腔积液等与肺栓塞并存而发生变形,因而用于指导SPECT报告的肺段参考图可能有误(图5)[52,57]。这一信息有助于引导发报告的放射学医师正确地认识肺段动脉,以明确肺V/Q SPECT显像的发现,而这些肺段动脉本来需要用CTPA来证实。
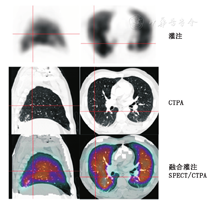

3.肺V/Q SPECT和CTPA联合显像。结构和功能联合显像的另一选择是将肺灌注SPECT显像与诊断性CTPA融合,这可在同一融合显像仪器上完成或在另一CT扫描后通过软件完成(图6)[58]。尽管这种方法需要合适的软件和专业操作者,但其对特定患者有价值,且利用CTPA能更好地引导放射科报告医师,观察到可疑的栓塞部位[59]。
1.肺通气显像是否必要?有了能显示解剖结构异常的SPECT/CT后,肺通气显像的必要性受到质疑。一些研究表明,如果省略肺通气显像则其特异性会明显降低。Gradinscak等[60]指出,13%的肺V/Q SPECT显像不匹配能在CT上看到实质性的异常,这常为肺亚段不张。Gutte等[18]表明仅行肺灌注SPECT/CT显像会有较之肺V/Q SPECT/CT显像有更高的诊断不明确率(17%)和更低的特异性(51%与100%)。尽管在没有合适肺通气显像剂的地方可以考虑只行肺灌注SPECT/CT,但有限的文献表明,肺通气显像可使其特异性最大化并降低假阳性率。
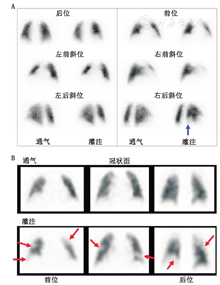
2.SPECT探测到的额外栓塞是否有必要治疗?虽然肺V/Q SPECT和SPECT/CT显像的灵敏度较平面显像高,但有人质疑对这些额外栓塞(通常在肺亚段)的发现究竟对抗凝治疗有多少意义[3,23,53,61]。尽管需要大样本的前瞻性研究来回答这个问题,但SPECT探测到的额外肺栓塞不仅存在于肺亚段水平(图7)[14]。对心肺储备功能不全,并发深静脉血栓或小的肺栓塞复发(有肺动脉高压的危险)的患者,任何肺栓塞,包括小的肺栓塞的诊断都可能特别重要[62]。虽然对于到底是诊断准确性还是临床结局更重要,这一考虑会引发更宽泛的哲学问题,但灵敏度和准确性更高,阅片者信心就更足,发报告更容易,有进行SPECT/CT联合显像的能力是肺栓塞影像检查中SPECT显像替代平面显像令人信服的原因。

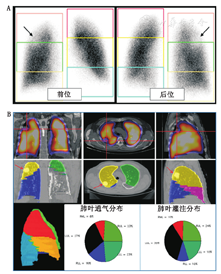
3.肺栓塞以外的应用和未来方向。肺V/Q SPECT和SPECT/CT显像不仅用于肺栓塞检查。对行肺减容术的患者,SPECT/CT可为单个肺段提供比平面显像更准确的相对肺灌注(和肺通气)的评估(图8)。肺V/Q SPECT显像可用于多个方面,如预测肺癌患者肺切除术后肺功能,修订放疗野以使功能肺的辐射暴露最小化,确定哮喘时的局部肺通气和肺灌注改变以及估测间质性肺病患者的局部肺功能[63,64,65]。

SPECT/CT的未来方向会包含肺栓塞放射性标记血栓的显像[66]。联合显像中通过使用患者专一的衰减校正方法将有利于定量SPECT[34]。使用PET放射性药物行肺显像,如68Ga-碳纳米颗粒(Galligas)和68Ga-大颗粒聚合白蛋白可能会加强核医学在肺栓塞和其他肺疾病评估中的作用,促进该领域的发展[49]。