
探讨肝血管周上皮样细胞瘤(PEComa)的临床特征、诊断与治疗方法。
回顾性分析2012年4月至2017年10月中国医科大学附属盛京医院收治的11例肝脏PEComa的临床资料,对其临床特点、影像学特征、诊断、治疗、病理学特性及预后进行总结。
11例患者年龄35~55岁(平均年龄47岁),3例为男性,8例为女性。2例患者就诊主诉为上腹部疼痛,其余患者无自觉症状。1例患者合并丙型肝炎病毒感染。11例患者术前影像学诊断率仅为9.09%(1/11)。患者均接受手术治疗,确诊依赖于术后病理及免疫组织化学结果。免疫组化一抗因病例而异,其中Melan A阳性率达100%(10/10)、黑色素瘤抗体(HMB)45阳性率达90%(9/10)、平滑肌肌动蛋白(SMA)阳性率达77.8%(7/9),S-100阳性率达33.3%(3/9),Ki-67阳性指数为1%~10%。1例患者因术后出血死亡,其余10例患者(随访5~71个月)均未肿瘤转移及复发。
肝脏PEComa是一种罕见的能够表达黑色素细胞和肌细胞标志物的间叶性肿瘤,常见于中年女性,无特异性临床表现,术前难以诊断,确认依赖于病理及免疫组化结果。手术及长期密切随访是目前公认的治疗方法。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
血管周上皮样细胞瘤(PEComa)是近年来发现的一种在组织学和免疫学表型上表现血管周上皮样细胞特征的间叶性肿瘤。PEComa家族包括肝肾血管平滑肌脂肪瘤(AML)、肺及肺外组织透明细胞"糖"瘤(clear cell"sugar"tumor,CCST)、淋巴管平滑肌瘤病(LAM)、肝镰状韧带/圆韧带透明细胞肌色素性细胞肿瘤(CCMMT),以及发生于结肠、胰腺、后腹膜、心脏、肾上腺等其他器官及软组织的非特殊性血管周上皮样细胞瘤(PEComa-NOS)[1]。PEComa常见于子宫、后腹膜、肠系膜、网膜,消化道等部位,而肝脏PEComa罕见,且肝PEComa无典型的临床特征及影像学诊断标准,常被误诊为肝细胞癌,肝局灶性结节增生等其他疾病。本研究总结报道了11例肝PEComa,探讨其临床特点、诊断及治疗,以提高临床对该病的认识。
收集中国医科大学附属盛京医院2012年4月至2017年10月手术病理证实为肝脏PEComa患者11例。所有患者临床资料完整,术前检查包括常规血液生化学检查、肿瘤标志物、肝炎病毒学检查及腹部影像学检查。
所有患者接受手术治疗,术后病理证实组织切缘阴性,均为R0切除,所有患者未接受放化疗等辅助治疗。肿瘤标本均经10%中性甲醛固定,石蜡包埋,常规切片,行HE染色,其中10例完成免疫组化,免疫组化使用Leica BOND全自动免疫组织化学(组化)及原位杂交染色平台,所采用的一抗因病例而异,其中包括黑色素瘤抗体(HMB)45、Melan A、肌间线蛋白(Desmin)、平滑肌肌动蛋白(SMA)、S-100、CD34、CD35、CD23、CD68、Ki-67、波形蛋白(Vimentin)、热休克蛋白(HSP)70、Hepatocyte、CK,所有抗体均购于中国北京中杉金桥生物技术有限公司。
本组11例患者中,1例因术后迟发性出血死亡,其余10例患者采用电话及门诊随访,随访截止时间为2018年4月25日。
11例患者中男3例,女8例(男女比例1∶2.7),年龄分布在35~55岁,平均年龄为47岁。其中1例合并肾AML,1例合并腹膜后AML,其余皆为肝脏单发肿瘤。2例患者就诊主诉为上腹部疼痛,其余患者无自觉症状,为健康体检时偶然发现肝脏占位性病变。所有患者血尿便常规、肝功能、肝胆胰癌肿瘤标志物甲胎蛋白(AFP)、癌胚抗原(CEA)、CA-199等化验检查均未见异常,肝炎病毒学检查中1例合并丙型肝炎病毒感染(表1)。
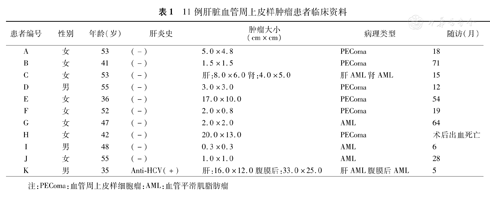
11例肝脏血管周上皮样肿瘤患者临床资料
11例肝脏血管周上皮样肿瘤患者临床资料
| 患者编号 | 性别 | 年龄(岁) | 肝炎史 | 肿瘤大小(cm×cm) | 病理类型 | 随访(月) |
|---|---|---|---|---|---|---|
| A | 女 | 53 | (-) | 5.0×4.8 | PEComa | 18 |
| B | 女 | 41 | (-) | 1.5×1.5 | PEComa | 71 |
| C | 女 | 53 | (-) | 肝:8.0×6.0肾:4.0×5.0 | 肝AML肾AML | 15 |
| D | 男 | 55 | (-) | 3.0×3.0 | PEComa | 12 |
| E | 女 | 36 | (-) | 17.0×10.0 | PEComa | 54 |
| F | 女 | 52 | (-) | 2.0×0.8 | PEComa | 19 |
| G | 女 | 47 | (-) | 2.0×2.0 | AML | 64 |
| H | 女 | 42 | (-) | 20.0×13.0 | PEComa | 术后出血死亡 |
| I | 男 | 48 | (-) | 0.3×0.3 | AML | 6 |
| J | 女 | 55 | (-) | 1.0×1.0 | AML | 28 |
| K | 男 | 35 | Anti-HCV(+) | 肝:16.0×12.0腹膜后:33.0×25.0 | 肝AML腹膜后AML | 5 |
注:PEComa:血管周上皮样细胞瘤:AML:血管平滑肌脂肪瘤
术前只有1例肝肾并发AML患者被影像学明确诊断,其余多被误诊为肝细胞癌。CT平扫中肿瘤密度稍低于周围肝实质,动脉期呈不均匀强化或边缘强化,2例可见异常增生的血管。门静脉期及延迟期强化程度缓慢下降,可呈稍高密度,等密度,甚至稍低密度。在磁共振中,病灶内均见长T1,长T2信号,增强扫描可见点状或线状的血管影及强化的包膜。
肿瘤大多为圆形或类圆形,边界较清晰,直径为0.3~33 cm。肿瘤质软,切面观多呈红色或棕黄色,偶有出血样外观。镜下可见上皮样、梭样肿瘤细胞呈片状、巢状或束状排列,散在薄壁或厚壁血管,5例AML中可见间杂的脂肪组织。所有肿瘤胞质丰富,透亮或呈嗜酸性。此外,1例可见髓外造血。免疫组化所用一抗因病例而异,其中Melan A阳性率达100%(10/10)、HMB45阳性率达90%(9/10)、SMA阳性率达77.8%(7/9),S-100阳性率达33.3%(3/9),Ki-67阳性指数为1%~10%。此外,4例可见血管源性标志物CD34阳性。
本组11例患者中,1例术后因术后迟发性出血死亡,其余10例术后长期随访(5~71个月),均未见肿瘤转移、复发以及患者死亡。
人们对于PEComa的认识源于3种肿瘤:肾和肝AML、肺透明细胞"糖"瘤(CCST)、淋巴管平滑肌瘤病(LAM),1992年Bonetti等[2]最先将这种形态学和免疫表型相似的肿瘤的组成细胞定义为PEC。1996年Zamboni等[3]通过报道1例发生于胰腺的CCST,将这些发生在不同部位、貌似没有关联的肿瘤定义为PEComa,这种观点逐渐被大家接受并沿用至今。2013年世界卫生组织(WHO)[4]在第4次软组织及骨肿瘤分类中将PEComa定义为由和血管壁呈特殊关系,能够特异性表达黑色素细胞和肌细胞标志物的细胞组成的间叶性肿瘤。
肝脏PEComa多无特异性临床症状,常因体检发现,患者血清AFP等肝胆胰肿瘤标志物常呈阴性,肿瘤与肝炎病毒史及肝硬化无明显相关性。肝脏PEComa在任何年龄段都会出现,但多见于中年女性,可能与激素水平差异有关。肝PEComa在CT平扫时常呈不均匀的低密度,动脉期不均匀或边缘强化,门静脉其及延迟期呈现稍高密度,等密度,甚至稍低密度。在MR中,病灶在T1WI常呈稍低信号;T2WI中呈稍高信号。CT联合MR对本病的诊断正确率也只有20%左右[5],无脂肪组织的典型PEComa相对于AML更加难以诊断。
肝脏PEComa主要依靠针吸细胞活检或者术后病理诊断,自从1976年这种疾病被人发现以来,已经有超过200例相关报道,但大多数为典型的AML[6],其特征包括:具有成熟的脂肪细胞、血管以及大小不等的梭形、肌样、上皮样细胞。如果肿瘤无脂肪细胞,则将之定义为"PEComa"更为合适。关于PEComa的恶性诊断标准,目前尚无定论,2005年Folpe等[7]暂时提出了一种恶性PEComa的评价标准:(1)肿瘤最大径>5 cm; (2)浸润性生长;(3)细胞核高度异型性;(4)细胞密集程度;(5)核分裂≥1/50 HPF; (6)凝固性坏死;(7)脉管侵犯。不具有任一上述指标者为良性,≥2个指标者则为恶性,余为不确定恶性者。
在免疫组化中,PEComa中的瘤细胞可同时表达黑色素细胞标志物,如HMB45、Melan A、酪氨酸酶、小眼转录因子(MiTF)等,以及SMA等肌源性标志物。其中,HMB45及Melan A阳性率最高,少量病例中也可见结蛋白及S-100阳性[8]。
目前,对于肝PEComa,尚无明确的诊疗指南,根治性手术切除及长期随访是当前首选的治疗方法,对于暂时无法手术切除的肿瘤,通过立体定向放射治疗(SBRT)为手术创造机会[9]。PEComa的发病机制可能与结节性硬化综合征(TSC)有关,主要表现为TSC2失活和TSC调控的下游因子mTOR的高表达,促使细胞过度增殖,形成肿瘤样变。雷帕霉素作为特效的mTOR抑制剂,已应用于肾脏AML中,并取得一定的疗效[10],但该化疗方法对肝脏PEComa的疗效尚需数据支持。



























