
版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
随着现代医学模式的转换,疼痛管理成为重要的健康问题之一。且在快速康复外科中,多模式镇痛被视为不可或缺的一环[1]。单方药物镇痛不能完全满足临床需要。由对乙酰氨基酚/布洛芬与弱/强阿片类镇痛药按固定比例组成的复方阿片类镇痛药,临床应用日趋广泛,是治疗伤害感受性疼痛、神经病理性疼痛、癌性疼痛等急慢性、中重度疼痛的重要药物。与单方相比,复方阿片类镇痛药具有协同镇痛作用、不良反应少、获取便捷、用药依从性好等优点被国内外专家广泛推荐[2,3,4]。但临床应用中仍有潜在的安全性风险[5],且国内外关于复方阿片类药物临床应用的循证医学证据较少,无法对复方阿片类镇痛药的临床应用进行有效指导。为规范复方阿片类镇痛药的临床应用,中华医学会疼痛学分会组织国内疼痛科专家撰写了本共识。
复方阿片类镇痛药主要由一种阿片类药物(如可待因、氢可酮、羟考酮、曲马多)和一种非甾体类抗炎药(如对乙酰氨基酚、布洛芬)组成。组分不同导致联合作用机制、起效时间、作用时间、代谢途径等亦有所不同,复合使用后可起到协同镇痛、延长作用时间、减少药物不良反应等效果。常用复方阿片类镇痛药组份和药理学性质见表1。
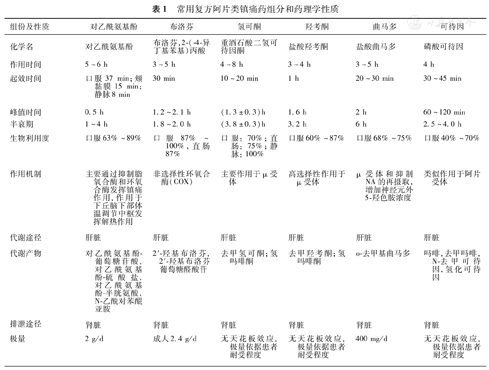
常用复方阿片类镇痛药组分和药理学性质
常用复方阿片类镇痛药组分和药理学性质
| 组份及性质 | 对乙酰氨基酚 | 布洛芬 | 氢可酮 | 羟考酮 | 曲马多 | 可待因 |
|---|---|---|---|---|---|---|
| 化学名 | 对乙酰氨基酚 | 布洛芬,2-(-4-异丁基苯基)丙酸 | 重酒石酸二氢可待因酮 | 盐酸羟考酮 | 盐酸曲马多 | 磷酸可待因 |
| 作用时间 | 5~6 h | 3~5 h | 4~8 h | 3~4 h | 3~5 h | 4 h |
| 起效时间 | 口服37 min;颊黏膜15 min;静脉8 min | 30 min | 10~20 min | 1 h | 20~30 min | 30~45 min |
| 峰值时间 | 0.5 h | 1.2~2.1 h | (1.3±0.3)h | 1.6 h | 2 h | 60~120 min |
| 半衰期 | 1~4 h | 1.8~2.0 h | (3.8±0.3)h | 3.2 h | 6 h | 2.5~4.0 h |
| 生物利用度 | 口服63%~89% | 口服87%~100%,直肠87% | 口服:70%;直肠:75%;静脉:100% | 口服60%~87% | 口服68%~75% | 口服40%~70% |
| 作用机制 | 主要通过抑制脂氧合酶和环氧合酶发挥镇痛作用,作用于下丘脑下部体温调节中枢发挥解热作用 | 非选择性环氧合酶(COX) | 主要作用于μ受体 | 高选择性作用于μ受体 | μ受体和抑制NA的再摄取,增加神经元外5-羟色胺浓度 | 类似作用于阿片受体 |
| 代谢途径 | 肝脏 | 肝脏 | 肝脏 | 肝脏 | 肝脏 | 肝脏 |
| 代谢产物 | 对乙酰氨基酚-葡萄糖苷酸,对乙酰氨基酚-硫酸盐,对乙酰氨基酚-半胱氨酸,N-乙酰对苯醌亚胺 | 2′-羟基布洛芬,2′-羟基布洛芬葡萄糖醛酸苷 | 去甲氢可酮;氢吗啡酮 | 去甲羟考酮;氢吗啡酮 | o-去甲基曲马多 | 吗啡,去甲吗啡,N-去甲可待因,氢化可待因 |
| 排泄途径 | 肾脏 | 肾脏 | 肾脏 | 肾脏 | 肾脏 | 肾脏 |
| 极量 | 2 g/d | 成人2.4 g/d | 无天花板效应,极量依据患者耐受程度 | 无天花板效应,极量依据患者耐受程度 | 400 mg/d | 无天花板效应,极量依据患者耐受程度 |
洛芬待因由布洛芬和磷酸可待因组成。布洛芬为非甾体类抗炎药,通过抑制环氧合酶抑制前列腺素合成,产生抗炎、镇痛和解热作用。可待因是中枢镇痛药,通过作用于中枢神经系统的阿片受体而发挥镇痛作用,其与阿片受体亲和力较低[6],故镇痛效果弱于吗啡[7],其主要代谢产物为可待因-6-葡萄糖醛酸[8],是慢性非癌痛中度疼痛的一线用药[9]。洛芬待因主要有两种剂型:(1)洛芬待因片:每片含布洛芬200 mg和磷酸可待因12.5 mg;(2)洛芬待因缓释片:每片含布洛芬200 mg与磷酸可待因13 mg。其主要适用于急慢性中度疼痛,尤其在骨关节炎、骨质增生、风湿性关节炎、强直性脊柱炎等炎性疼痛治疗中具有优势,也可用于偏头痛和术后疼痛。对轻、中度癌痛治疗也有一定的适应证,较为适宜骨转移疼痛和伴有咳嗽的癌痛患者[10]。洛芬待因临床应用中安全性较高,没有严重不良反应[11,12],尤其是恶心、呕吐等不良反应发生率低,患者满意度较高[13]。
洛芬待因临床应用需注意药物的过量应用及不良反应,如胃肠道的出血和(或)成瘾性等。12岁以下的儿童禁用,12岁以上儿童及老年患者可酌情减少药量。哺乳期妇女禁用。已知为CYP2D6超快代谢者禁用。
氨酚待因是对乙酰氨基酚与磷酸可待因的复方制剂,含对乙酰氨基酚300 mg和磷酸可待因15 mg。对乙酰氨基酚主要通过抑制脂氧合酶和环氧合酶发挥作用,引起下丘脑前列腺素和白细胞介素-1合成减少,从而抑制疼痛信号的传递[14]。临床上主要用来治疗中度疼痛,对创伤性疼痛和兼有发热、咳嗽的疼痛尤为适用,常用于治疗术后痛、骨折、骨关节疼痛、软组织损伤、牙痛、头痛及痛经等[15],也是癌痛治疗二阶梯的常用药物[16]。
7~12岁儿童使用时按体重相应减量,连续使用一般不超过5 d,7岁以下儿童不宜使用。本品所含两种药物成分均可透过胎盘而影响胎儿,可使胎儿成瘾,引起新生儿的戒断症状;同时本品所含两种药物成分均可自乳汁排出,因而孕妇及哺乳期妇女应慎用。老年患者慎用。呼吸抑制及有呼吸道梗阻性疾病,尤其是哮喘发作的患者应禁用。多痰患者禁用,以防因抑制咳嗽反射,使大量痰液阻塞呼吸道。
氨酚氢可酮是对乙酰氨基酚与氢可酮的复方制剂,含对乙酰氨基酚500 mg和氢可酮5 mg。氢可酮在结构上与吗啡类似,为半合成的阿片受体激动剂,选择性作用于μ受体,与G-蛋白复合物偶联并通过腺苷酸环化酶调节突触传递产生镇痛、欣快等作用。氢可酮主要由CYP2D6和CYP3A4分别代谢为氢吗啡酮和甲氢可酮,氢吗啡酮对μ阿片受体的亲和力比母体药物高约30倍,因此CYP2D6表型影响其镇痛效果[17],其变异可使药物镇痛效果不佳或者产生不良反应[18]。氢可酮主要临床优点是起效快、持续时间长、不良反应较少。氨酚氢可酮是中重度慢性非癌痛的一线用药[9],如骨骼肌关节疼痛[19]。也可用于术后和创伤性疼痛[20]、软组织损伤、口腔外科手术疼痛[21]等,在急性肌肉骨骼痛的急诊患者中,其快速镇痛效果优于曲马多[22]。氨酚氢可酮也可作为癌痛治疗第二阶梯的药物。
有报道氨酚氢可酮可用于学龄前儿童(3~5岁)的术后镇痛[23]。孕妇及哺乳期妇女慎用,老年患者应用此药物应密切关注可能出现的呼吸抑制等严重并发症。
氨酚羟考酮是盐酸羟考酮和对乙酰氨基酚的复方制剂,剂型为5 mg/325 mg。羟考酮主要是κ受体激动剂[24],其镇痛作用与其在脊髓和下行抑制系统中的受体激动活性有关[25]。羟吗啡酮是羟考酮的活性代谢物,具有较高的μ-阿片受体亲和力。氨酚羟考酮作用于中枢和周围神经系统发挥协同镇痛。氨酚羟考酮适用于各种原因引起的急慢性中重度疼痛。在治疗骨关节炎和中重度慢性腰背痛方面,氨酚羟考酮片可以提供有效的镇痛效果[26,27,28],显著改善生活质量[29]。也可应用于轻、中度癌痛及爆发痛的控制。
需要注意的是,对于急性腰背痛,在非甾体类抗炎药基础上联合使用氨酚羟考酮不会增加疼痛缓解和功能改善的疗效[30]。同时存在阿片类药物禁忌证如严重呼吸抑制、急性或严重支气管哮喘、高碳酸血症,疑似或已诊断有麻痹性肠梗阻患者禁用。对于年老体弱、肝肾功能不全、甲状腺功能减退、前列腺肥大、尿道狭窄的患者慎用。运动员慎用。不推荐用于孕妇及哺乳期妇女。对儿童的安全性尚未确立。
氨酚曲马多是由对乙酰氨基酚与盐酸曲马多组成的复方制剂。每片含对乙酰氨基酚325 mg,盐酸曲马多37.5 mg。曲马多及其代谢产物O-去甲基曲马多作用于μ阿片受体,同时抑制5-羟色胺及去甲肾上腺素再摄取,同时兼具镇痛和抗焦虑作用。相比其他口服阿片镇痛药,曲马多的镇痛效果弱,且安全性没有明显优势,一般不推荐为一线用药[31]。氨酚曲马多可在较低剂量下达到单方制剂相同的镇痛效果,减少不良反应[32]。适用于各种中、重度的急性、慢性疼痛,如偏头痛、骨性关节炎、慢性腰痛、带状疱疹神经痛、糖尿病周围神经痛、癌性疼痛及外伤后、手术后疼痛的治疗[33]。
癫痫患者或被认为有癫痫发作危险的患者(如:脑部创伤、代谢异常、酒精和药物的戒断、中枢神经系统感染)应慎用[34]。老年患者慎用。肾功能不全患者应慎用,如必须使用,肌酐清除率低于30 ml/min,建议延长服药间隔,且12 h的用量不得超过2片。目前尚无肝功能损害患者的研究资料,不推荐使用。尚无本药物用于16岁以下人群的安全性和有效性的资料。酒精、安眠药、麻醉剂、中枢镇痛药、阿片类或精神药物急性中毒的患者禁用。
复方阿片类镇痛药最常见的不良反应包括便秘、头晕及恶心呕吐[35]。其他不良反应包括皮疹、皮肤瘙痒、嗜睡及尿潴留等[36];氨酚氢可酮有引发呼吸抑制、不规则呼吸或周期性呼吸的可能[37]。
复方阿片类药物与抗癫痫药、抗抑郁药或其他麻醉镇痛药联合使用时会产生叠加的中枢抑制效应,应注意可能会出现过度镇静,如嗜睡,意识障碍等,严重者可发生呼吸抑制。此外,与上述药物合用时,便秘与尿潴留的发生概率也会大大增加。因此,联合用药时应减少其中一种或全部药物的剂量。
阿片类镇痛药使用过程中需进行成瘾性的风险评估,既往有酒精或药物滥用史或依赖史的个体较易出现成瘾性。镇痛药疗效欠佳时盲目增加用量,可能会导致药物成瘾,故医生应对患者临床表现及心理状况进行动态评估和实时干预。如需停药,原则上应在两周内平稳递减药量,以防出现戒断症状。
复方制剂用于治疗神经病理性疼痛时,应联合抗癫痫药或抗抑郁药物。
1.复方阿片类镇痛药物主要是对乙酰氨基酚或布洛芬复合弱阿片/强阿片镇痛药。除氢可酮外均属于非精神类药品,不受处方管制。
2.复方阿片类镇痛药的应用遵循了多模式镇痛原则,具有多重镇痛机制和协同作用,镇痛效果强于单方制剂,起效时间快,不良反应少。
3.复方阿片类镇痛药适应于急慢性、中重度疼痛的治疗。
4.复方阿片类镇痛药应在医生指导下规范应用,避免过量使用,长期应用应注意监控药物不良反应。
5.复方阿片类镇痛药镇痛效果不佳,应在医生指导下更换药物或选用微创介入等其他治疗方法。
执笔者:马柯(上海交通大学医学院附属新华医院疼痛科)
专家组成员名单(按姓氏笔画数排序):马柯(上海交通大学医学院附属新华医院疼痛科);王云霞(湖北省第三人民医院疼痛科;冯艺(北京大学人民医院疼痛科);吕岩(空军军医大学西京医院疼痛科);刘广召(河北医科大学第二医院疼痛科);刘先国(中山大学中山医学院疼痛研究中心);刘延青(首都医科大学附属北京天坛医院疼痛科);刘金锋(哈尔滨医科大学附属第二医院疼痛科);刘慧(四川大学华西医院疼痛科);庄志刚(郑州大学第二附属医院疼痛科);陆丽娟(南京大学医学院附属鼓楼医院疼痛科);宋涛(中国国医科大学附属第一医院疼痛科);严敏(浙江大学医学院附属第二医院疼痛科);杨晓秋(重庆医科大学附属第一医院疼痛科);张小梅(昆明医科大学第一附属医院疼痛科);梁立双(山东大学齐鲁医院疼痛科);熊源长(海军军医大学附属长海医院疼痛科)

























