
版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
儿童Hutchinson-Gilford早老症(HGPS)是一种罕见的人类早老性疾病,最早由Hutchinson于1886年发布病例报道,Gilford于1904年再次描述了这种疾病。其发病率极低,约为1/800万[1]。HGPS患儿的特征性表现为快速衰老,出生后不久即可出现脱发、皮肤衰老等症状。患儿常死于心血管并发症,平均寿命约13岁。迄今文献报道的HGPS患者最长寿命为30岁[1]。现对首都医科大学附属北京儿童医院诊治的1例HGPS患儿的临床资料进行分析,以期提高临床医师对本病的认识。
患儿,男,2岁10个月,因"发现皮肤发硬、生长缓慢2年余"到首都医科大学附属北京儿童医院内分泌科门诊就诊。出生20 d左右家长发现患儿全身皮肤发硬,以双臀为著,且腹部皮肤发紧,四肢无法伸直,以双下肢为著,曾多次到当地医院就诊,未能确诊,患儿上述症状进行性加重。患儿6个月时曾就诊于上海市儿童医院,疑诊"早老症",未予特殊治疗。2年多来,患儿身高和体质量增长缓慢,具体增长速度不详,头发渐脱落。为行进一步诊治,就诊于首都医科大学附属北京儿童医院内分泌科。
患儿系第1胎,第1产,足月顺产,无宫内窘迫史,出生后无窒息。出生体质量3.1 kg,身长48 cm,2个月会抬头,6个月会坐,6个月开始长牙,1岁3个月会走、会叫"爸爸、妈妈",现智力基本正常。出生后人工喂养,现可正常饮食,但喜流食及半流食,不喜肉食。出生时皮肤菲薄、发黑,自幼皮肤磕碰后易青紫,伤口愈合缓慢,经常无明显诱因出现鼻出血。否认糖尿病、低血糖等家族遗传病史,父母非近亲结婚。父亲身高170 cm,母亲身高163 cm。
体格检查:身高78 cm,体质量8.5 kg(均小于中国儿童生长曲线第3百分位),指间距73 cm,坐高44 cm,头围47 cm,胸围43.5 cm,腹围37 cm,皮下脂肪厚度(肱三头肌)6 mm,皮下脂肪厚度(腹壁)2.5 mm。神志清楚,精神反应可,对答切题,声音尖细,下肢呈骑马样姿态。身材瘦小,全身皮肤变薄,皮下脂肪菲薄,颜色偏黑,头皮及四肢浅表静脉显露明显,躯干及四肢可见网状色素沉着斑和老年斑。全身皮肤触感硬,以躯干及双下肢为著。前囟已闭合,老人面容,头发及眉毛稀疏,额头突出,眼球突出,似鸟样外观,牙18颗,排列不整齐,下颌小,耳位不低,未见通贯掌。梨状胸廓,锁骨短小,双侧肋缘外翻,双肺及心脏听诊无异常,腹部触诊无异常,肝脾未触及肿大。四肢关节无法伸直,指、趾屈曲畸形,指甲甲板不平,趾甲甲板菲薄、凹陷、萎缩或缺失。神经系统查体未见异常。正常男童外生殖器,阴毛Tanner Ⅰ期(图1)。
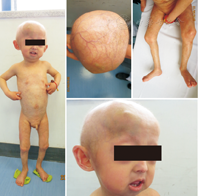

辅助检查:白细胞9.82×109/L,中性粒细胞0.273,淋巴细胞0.563,单核细胞0.132,血红蛋白136 g/L,血小板425×109/L,C反应蛋白(CRP) 0.5 mg/L;钾(K) 4.52 mmol/L,钠(Na) 140 mmol/L,氯(Cl) 100 mmol/L,天冬氨酸氨基转移酶(AST) 27 IU/L,丙氨酸转氨酶(ALT) 12.8 IU/L,总蛋白48.3 g/L,清蛋白34.2 g/L,球蛋白14.1 g/L,尿素氮3.5 mmol/L,肌酐9.5 μmol/L,总胆红素37.4 μmol/L,二氧化碳结合率(CO2CP) 19.5 mmol/L,阴离子间隙(AG) 25.02 mmol/L,三酰甘油(TG) 0.58 mmol/L,胆固醇4.02 mmol/L;甲状腺功能五项:三碘甲状腺原氨酸(T3) 2.86 nmol/L,甲状腺素(T4)125.26 nmol/L,促甲状腺激素(TSH) 10.96 mIU/L,游离三碘甲状腺原氨酸(FT3)7.22 pmol/L,游离甲状腺素(FT4)14.36 pmol/L;促甲状腺素受体抗体(TRAB)、甲状腺球蛋白抗体(TGAb)、甲状腺过氧化物酶(TPO)均阴性;尿便常规未见异常。心脏超声:房间隔小缺损0.2 cm(卵圆孔型);腹部彩超:肝脾、双侧肾上腺未见明显占位性病变,左肾集合系统分离;头颅磁共振成像(MRI)未见异常。心脏增强MRI:左主干(LM)位置起源稍高,位于窦管交界,余未见明显异常;延迟扫描心肌未见活性减低征象;冠状动脉管壁光滑,未见钙化,管腔不窄。胸部及四肢X线片:全身骨质疏松,骨质变细、变短,肋骨变细,末节指、趾骨末端骨质部分吸收变短。本研究已征得患儿监护人知情同意,并获医院医学伦理委员会批准(批准文号:2016-12)。
根据患儿典型临床表现及实验室检查结果,临床考虑为HGPS。留取患儿及其家长外周静脉全血,委托智因东方医学检验中心对患儿及其家长进行LMNA基因检测,结果在患儿发现了1个杂合突变,位于第11外显子的第1 824位碱基由C突变为T(c.1824C>T),导致氨基酸p.G608G变异。该位点突变导致蛋白羧基端50个左右的氨基酸缺失,从而导致疾病发生。患儿父母基因检测均未发现异常(图2)。
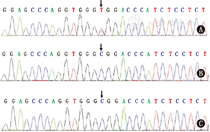

注:A:患儿,可见c.1824C>T杂合突变;B:患儿父亲,未见突变;C:患儿母亲,未见突变 A:the patient,showing the c.1824C>T heterozygous mutation;B:the patient′s father,no mutation was found;C:the patient′s mother,no mutation was found
治疗及随访:因本综合征无特殊治疗方法,入院后未予特殊药物治疗。予高热量、高蛋白质、易消化饮食,补充维生素D。0.5年后随访患儿身高体质量增加不明显,余无明显不适。
HGPS是一种婴儿期出现的过早老化,并累及皮肤、脂肪、心血管、骨骼等多器官系统的罕见遗传病。患者多为儿童,其发病率为1/800万,男女发病率比例为1.21.0,无明显种族差异[2]。根据HGPS的临床表型,可分为典型HGPS和非典型HGPS,其表型均具有同质性。
HGPS患儿的特征表现是出生后极速衰老,主要表现为严重生长迟缓、秃顶、皮下脂肪菲薄、硬皮症、特异性颅骨异常(鸟样脸、小下颌、雕鼻等)。典型HGPS患儿还可出现特征性骨骼改变:骨质疏松症、锁骨重吸收、趾骨末端重吸收、指甲发育不良、肋骨变细及下颌骨发育不良等;患儿大关节僵硬出现关节活动受限,膝关节挛缩呈骑马样姿态等[3]。本病多在2岁左右发病,多在青春期前出现加速的动脉粥样硬化、充血性心力衰竭、心肌梗死等严重症状并导致死亡,平均寿命13岁,最长寿命为30岁[1]。除机体衰老之外,HGPS患者不表现正常衰老的其他特征,如不会发生癌症。据统计,自1886年开始至今,全球约有100余例HGPS患者被报道。我国自1981年首次报道本病,至今报道约20例[4]。辅助检查上,HGPS患者尿透明质酸排泄量增多,是健康人的10~20倍[5]。甲状腺激素、甲状旁腺素、肾上腺素水平正常,部分患儿可能有胰岛素抗性增加。患者生长激素正常,但可能出现生长激素失活或内源性生长激素抵抗[5]。影像学方面常见锁骨重吸收,可被纤维组织取代,肢端骨溶解等[6]。尸体病理检查主要为大动脉粥样硬化,部分可见肾硬化、心肌纤维化、血管钙化、皮肤脂肪缺失、胶原排列紊乱等。本例患儿新生儿期起病,具有皮肤、骨骼等多器官衰老的典型临床表现,考虑典型HGPS可能性大。患儿血TSH水平升高,但甲状腺抗体阴性,无明确甲状腺功能减退症状,暂不考虑相关疾病。患儿目前血脂正常,完善心血管影像学检测并无明显异常,继续予长期随访。
HGPS遗传发病机制多样,典型HGPS为常染色体显性遗传,多为散发,而非典型HGPS常呈现常染色隐性遗传。其分子机制是由于染色体1q上编码A/C型核纤层蛋白的LMNA基因发生点突变而引起[7]。核纤层蛋白是组成细胞核纤层(nuclear lamina)的最主要成分,在维持细胞核形和机械性质、锚定核孔复合体与核膜蛋白、为外周异染色质提供锚定、维持染色体结构、DNA的复制与转录、DNA损伤修复和维持基因组稳定性等方面发挥着重要作用。LMNA基因位于1q21.2-q21.3,全长56.7 kb,包含12个外显子。HGPS疾病突变位点位于第11外显子,进一步研究发现,典型HGPS 90%与LMNA基因杂合突变G608G相关,非典型HGPS可能与LMNA基因的K542N和R527C位点突变相关[1,4,7]。由于LMNA基因突变,产生了被截短的、保留法尼基化结构的不成熟A型核纤层蛋白,对于HGPS发病机制,普遍存在以机械应激和基因表达失控2种假说。
本例患儿LMNA基因检测发现的经典G608G突变虽未导致氨基酸改变,但既往研究表明,此突变在LMNA基因外显子11区域产生了一个潜在的剪切位点,使得lamin A蛋白前体C末端包含ZMPSTE24酶切位点在内的50个氨基酸残基被剪切,产生早老蛋白,早老蛋白无ZMPSTE24酶切位点而保留了法尼半胱氨酸甲酯,永久法尼基化的早老蛋白不能从内核膜释放,最终导致细胞核结构和功能受损[3]。国外研究报道,携带G608G突变的典型HGPS患者皮肤成纤维细胞表达早老蛋白,细胞核变形、核膜出泡改变,并且随细胞老化而加剧,并且携带此突变患者多伴发骨骼异常[8]。本例患儿临床表现与之相符。
HGPS患者的病情严重,发展迅速,目前仍无有效的治疗。随着研究的深入,细胞和动物研究方面取得一定成果。其中普遍认可的是法尼基化的抑制剂(FTI),FTI能抑制A型核纤层蛋白前体的法尼基化,从而避免细胞毒性,改善细胞与组织的表型,但FTI只能改善HGPS小鼠的症状,不能完全根治早老症表型[9]。还有一种RNA干扰技术,可以抑制progerin细胞表达,减少核变形,延缓衰老,长远目标是为了干涉冠状动脉粥样硬化的病变过程[9]。以上治疗仅在动物模型或少量HGPS患者使用,目前国内尚缺乏相应的治疗手段。本例患儿未予特殊治疗,建议予高热量、高蛋白质、易消化配方营养支持,少量多食,定期门诊随访生长发育情况。


























