
尖端赛多孢子菌是一种条件性真菌,普遍存在于土壤、污水、腐物等受污染的环境中,可引起各种类型的感染,特别是在免疫功能低下的患者中极为常见。由于临床和形态学上与其他真菌(如曲霉)相似,很难诊断,加之对多种抗菌药物耐药,病死率高。现报道我院1例免疫功能异常者因尖端赛多孢子菌引起的肺部感染。

版权归中华医学会所有。
未经授权,不得转载、摘编本刊文章,不得使用本刊的版式设计。
除非特别声明,本刊刊出的所有文章不代表中华医学会和本刊编委会的观点。
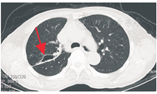
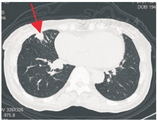
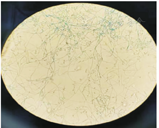
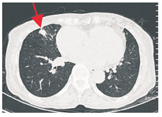
患者女,70岁,因"反复咳嗽、咳痰8年,加重1月"于2019年4月7日入住浙江省人民医院呼吸内科,患者8年来无明显诱因下出现反复咳嗽、咳痰,曾至我院就诊,支气管镜常规病理示:"右上支气管黏膜慢性炎症伴曲霉团",予伊曲康唑(200 mg,1次/d)治疗,2年后因经济原因自行停药,每年复查胸部CT,自诉病灶相仿,曾于2018年5月23日在我院查肺部CT,示双肺感染伴支气管扩张,余病灶同前(图1),予哌拉西林/他唑巴坦(4.5 g,1次/d)抗感染和对症治疗后咳嗽、咳痰等症状好转。2019年3月6日因"类风湿关节炎"在我院风湿免疫科住院,3月8日复查胸部CT示两肺多发结节(图2),病灶较前进展。既往史:陈旧性肺结核11年,规律抗结核治疗半年,后痰培养未找到结核分枝杆菌。类风湿性关节炎病史10年,规律服用羟氯喹(0.2 g,1次/d)和白芍总苷胶囊(0.6 g,3次/d),雷公藤(20 mg,2次/d)等免疫抑制剂对症治疗。入院查体:体温37.3 ℃,呼吸19次/min,脉搏83次/min,血压112/68 mmHg(1 mmHg=0.133 kPa),神志清,精神可,锁骨上淋巴结未及肿大,胸骨无压痛,双肺听诊呼吸音粗,未闻及明显干湿性啰音,心率83次/min,律齐,各瓣膜听诊区未闻及明显病理性杂音,肝脾肋缘下未及,腹平软,无压痛、反跳痛,右手尺侧偏斜,余四肢关节未见明显肿胀畸形。神经系统检查未见明显异常。4月7日查血常规:白细胞计数6.72×109/L、红细胞计数3.60×1012/L、血红蛋白114 g/L、血小板计数239×109/L、超敏C-反应蛋白11.9 mg/L; 4月8日查红细胞沉降率53 mm/1 h,入院时患者咳黄色黏痰,诉多关节疼痛,无发热,予以消炎止痛及免疫抑制剂治疗后稍有好转。建议患者再次复查胸部CT了解病情变化,患者拒绝。鉴于患者之前的胸部CT表现,4月9日完善病原学检查:半乳甘露聚糖(GM试验):0.62 μg/L,1,3-β-D葡聚糖(G试验)165.30 pg/mL(升高);全血结核感染特异性T细胞阴性;支气管镜检查未见明显异常,肺泡灌洗液新型隐球菌检查:阴性;外送肺泡灌洗液GM试验为6.98(阳性),烟曲霉IgG抗体定量92 AU/mL,灌洗液经Vitek-MS方法培养出尖端赛多孢子菌。4月10日镜下菌落特点:菌丝分隔,直径约为2~4 μm,分生孢子梗长短不一,末端着分生孢子,分生孢子呈卵圆形,单细胞,黄色至淡棕色(图3)。根据上述特点,最终鉴定该菌为尖端赛多孢子菌。体外药敏试验:对伏立康唑敏感。考虑到患者类风湿性关节炎诊断明确,结缔组织疾病需要抑制免疫治疗,但真菌病原学指标升高,加用免疫抑制剂可能导致肺部感染加重,因此在抑制免疫治疗的同时进行抗真菌治疗,即口服伏立康唑片(200 mg,2次/d)联合羟氯喹(0.2 g,1次/d)和白芍总苷胶囊(0.6 g,3次/d)治疗3个月。住院3 d后患者自觉症状好转,要求带药出院。嘱患者门诊定期复查,患者于7月5日于我科门诊复查胸部CT(图4),病灶较前吸收好转。




尖端赛多孢子菌是波氏假阿利什菌的无性型,是一种条件致病菌,肺部和上呼吸道是尖端赛多孢子菌最常见的受累部位[1]。本例患者为老年女性,慢性病程,因长年服用抗风湿性药物引起免疫功能异常,从而诱发因尖端赛多孢子菌引起的肺部感染。该患者11余年前有肺结核病史,结核空洞给真菌提供了生长空间。患者8年前病理学诊断为曲霉团,不排除误诊的可能,因为肺部尖端赛多孢子菌感染的影像和组织学检查是非特异性的,与常见的曲霉感染的表现非常相似,其临床特征和组织病理学表现更像侵袭性肺曲霉的征象[1]。尖端赛多孢子菌的肺部影像学常可见多发边缘模糊的结节性球形影,结节病灶周围有毛玻璃样稀薄液渗出,即周围有出血性坏死,向外周扩大形成低透光带即"晕征",可形成空洞和出现新月形气影即"新月征",内附真菌球影[2]。为了准确诊断,建议同时进行细胞学和病理学检查。尖端赛多孢子菌引起的肺部受累可分为几类:暂时性局部定植、支气管肺损伤、真菌球形成和侵袭性感染[3]。当肺部受侵犯时临床表现常为咳嗽、咳痰,黏痰呈白色、含血丝、甚至咯血,呈持续性发热、无寒战盗汗,呼吸困难,胸痛,肺部湿啰音,不具有特异性[2]。而本例患者8年来反复出现咳嗽、咳痰,曾多次在省中医院及我院就诊,给予抗感染、祛痰、对症等治疗后好转,但一直未能明确病因。
尖端赛多子菌感染的危险因素包括免疫抑制疗法、人体免疫缺陷病毒感染、溺水(从废水或受污染的池塘中分离出的病原体)、糖尿病或营养不良等[4],本例患者长期使用免疫抑制剂,支气管扩张,陈旧性肺结核等病史导致肺的结构病变,从而增加了尖端赛多孢子菌引起肺部感染的机会。
临床上对于怀疑真菌感染者,首先进行真菌G联合GM试验,尖端赛多孢子菌感染时G试验呈阳性,GM试验呈阴性,最后通过肺泡灌洗液真菌菌丝培养的方法,最终培养出尖端赛多孢子菌。
关于尖端赛多孢子菌的治疗,由于对两性霉素B及其他抗真菌药的耐药性,使得早期处理尖端赛多孢子菌病非常复杂,病死率为50%~70% [4]。抗真菌药物伏立康唑对尖端赛多孢子菌的体外活性最低抑菌浓度为0.12~0.5 mg/mL[5]。因此,伏立康唑目前被认为是最佳的治疗方法。近年来,抗真菌联合疗法已成为一种常规的方案,因为在较低浓度下可以取得治疗效果并减少不良反应,提高安全性和耐受性,防止治疗失败[6]。推荐的组合是与特比萘芬联合治疗,伏立康唑的血清谷浓度应保持在1~5 mcg/mL [7]。有研究发现,在未发生严重免疫损害的患者中,尖端赛多孢子菌感染容易发展为局部病变。此时如果单用抗真菌药物,疗效通常不佳,部分原因在于其对多种抗真菌药物的内在敏感性降低。此时手术切除是一个行之有效的选择[1]。因尖端赛多孢子菌多发生在免疫抑制的患者中,恢复固有的宿主防御往往是成功治疗感染的关键。粒细胞集落刺激因子(G-CSF)可促进中性粒细胞的恢复,粒细胞输注可稳定感染。IFNγ和粒细胞巨噬细胞集落刺激因子(GM-CSF)增强了对尖端赛多孢子菌的抗真菌活性。这些细胞因子诱导Th1反应,有利于抗真菌病,在转录水平上调节NADPH氧化酶亚基的基因表达,增强巨噬细胞中抗菌肽的合成。G-CSF或GM-CSF联合IFNγ的免疫调节可作为辅助治疗策略,诱导中性粒细胞抗真菌活性增强[6]。结合相关文献及药敏试验结果同时考虑患者经济情况,本例患者尽管只单用伏立康唑抗真菌治疗,但效果较好。
综上所述,对于反复咳嗽咳痰病因不明者,需要警惕真菌感染的可能,尤其免疫功能异常者。尖端赛多孢子菌引起的肺部感染容易和肺曲霉相混淆,对于临床上怀疑该真菌者,需及早进行病原学检查,有助于帮助治疗。
所有作者均声明不存在利益冲突



























